渗出性视网膜脱离是一种不伴有裂孔或牵拉的非孔源性视网膜脱离 ,血-视网膜屏障 (BRB)破坏是其共同病理机制。
体位改变时脱离部位移动的“shifting fluid”是该疾病的特征性临床表现。
病因多种多样,包括炎症性(如VKH病)、血管性(如Coats病 )、肿瘤性、RPE 疾病(如CSC )、药物性和妊娠相关。
治疗原则是确定并治疗原发病,去除病因后视网膜下液 常可自行消退。
MEK抑制剂(如比美替尼)引起的药物性渗出性视网膜脱离在停药后数天内消失。4)
妊娠期双侧浆液性视网膜脱离 与子痫前期密切相关,常在分娩后自行消退。6)
使用免疫检查点抑制剂 (ICI )的患者中,有报道出现VKH样炎症性渗出性视网膜脱离,需注意。12)
诊断时,光学相干断层扫描 (OCT )、荧光素眼底血管造影 、吲哚青绿血管造影(ICGA )和超声检查等多模态成像很有用。
不同病因的视力 预后差异很大。VKH和CSC 早期治疗可望获得良好预后。
渗出性视网膜脱离(exudative retinal detachment; ERD)是非孔源性视网膜脱离 的一种类型。不伴裂孔的视网膜脱离 称为非孔源性视网膜脱离 ,大致分为渗出性和牵拉性两种。渗出性视网膜脱离是指在没有视网膜裂孔 或牵拉的情况下,液体在视网膜 下腔积聚的病理状态,可由炎症性疾病、变性疾病、感染或肿瘤等多种疾病引起。
基本病理是视网膜 血管、视网膜色素上皮 (RPE )或脉络膜 功能障碍导致渗出液积聚在视网膜 下。血-视网膜屏障 (BRB)破坏后,脉络膜 血管、视网膜 血管和RPE 渗出的液体在视网膜 下积聚。有时与“浆液性视网膜脱离 ”几乎同义使用,但本文涵盖广义的渗出性视网膜脱离,包括肿瘤性、炎症性和药物性。
脱离程度低的轻症病例称为浆液性视网膜脱离 ,代表性疾病是中心性浆液性脉络膜视网膜病变 (CSC )。糖尿病视网膜病变 、视网膜静脉阻塞 、年龄相关性黄斑变性 和视网膜 微动脉瘤 也可发生,但伴有视网膜 下出血时则变得难治。
病因多种多样,包括Vogt-小柳-原田病 (VKH)和后巩膜炎 等葡萄膜炎 、CSC 和多发性后极部视网膜色素上皮 病变(MPPE)等视网膜色素上皮 疾病、年龄相关性黄斑变性 等视网膜 下新生血管 、Coats病 等血管疾病、脉络膜 血管瘤和视网膜母细胞瘤 等肿瘤性疾病、葡萄膜渗漏、糖尿病黄斑水肿 等。由于不同疾病的治疗方法根本不同,准确诊断非常重要。
与孔源性视网膜脱离 的区别如下所示。
项目 渗出性 孔源性 视网膜裂孔 无 有 脱离形态 圆顶状、光滑 皱褶状、不规则 移动性液体 有 无至少量 治疗原则 治疗原发病 手术(封闭裂孔)
Q
孔源性视网膜脱离和渗出性视网膜脱离有何不同?
A
孔源性视网膜脱离 是由于视网膜 出现裂孔,玻璃体 液流入所致。渗出性视网膜脱离没有裂孔,而是由于血管或RPE 损伤导致视网膜下液 体积聚。前者原则上通过手术封闭裂孔,后者则以治疗原发病为基础。体位改变时脱离部位移动的“移动性液体”是渗出性视网膜脱离的特征性表现。
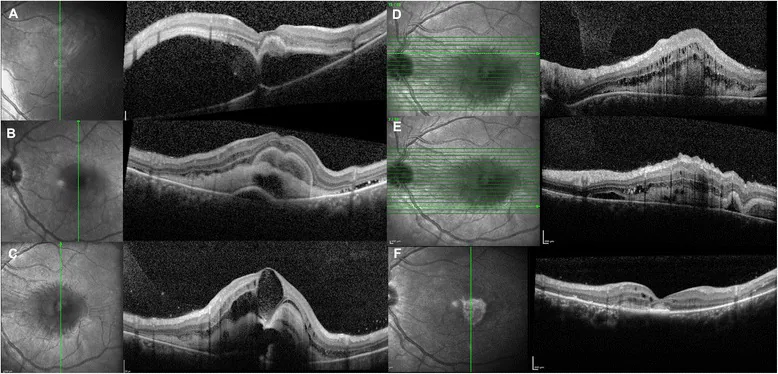
渗出性视网膜脱离的OCT表现 Maggio E, et al. Multimodal imaging findings in a case of severe Central Serous Chorioretinopathy in an uncomplicated pregnancy. BMC Ophthalmol. 2015. Figure 1. PM
CI D: PMC4688919. License: CC BY.
光学相干断层扫描 (OCT )显示黄斑部 神经感觉视网膜 明显浆液性隆起,伴有视网膜 下高反射物质(a),以及随访期间视网膜下液 消失和视网膜 下渗出物积聚(b-c)。这对应于本文“2. 主要症状和临床所见”中讨论的浆液性视网膜脱离 。
视力 下降视网膜下液 侵犯黄斑 时导致明显视力 下降。视物变形 黄斑部 视网膜 隆起导致物体看起来扭曲。视物模糊 视野缺损 视野缺损 。全身症状 :根据原发病(如VKH)可能伴有头痛、耳鸣或感冒样症状。
典型的渗出性视网膜脱离表现为视网膜 呈穹隆状隆起,表面光滑,视网膜下液 随体位改变而移动(shifting fluid)。通常不会出现孔源性脱离中见到的皱褶或不规则隆起。
炎症性(VKH)
双侧浆液性脱离 :双眼出现多个穹隆状隆起。
脉络膜 增厚OCT 显示明显脉络膜 增厚(约600μm)。2)
OCT 特征性表现视网膜脱离 ,脉络膜 管腔结构变窄。
视乳头充血 水肿 :视神经乳头 也伴有炎症性改变。
药物性(MEKAR)
急性发作的双侧SRD :MEK抑制剂给药后迅速发生。4)
症状通常轻微 :有些病例视力 下降轻微,自觉症状不明显。
可逆性 :停药后3天内常消退。4)
妊娠相关
双侧浆液性RD :可能合并子痫前期/HELLP综合征。6)
黄斑部 优势脱离黄斑部 积聚,引起视物变形 和视力 下降。
产后消退 :产后常自然消退,视力 多可恢复。6)
外伤性/医源性
RPE 裂孔后ERDRPE 裂孔后继发渗出性脱离。1)
ROP 激光后ERD早产儿视网膜病变 激光治疗 后可能发生。5)
体位变化时液体移动 :可观察到移动性液体。
Coats病
黄色调视网膜 下渗出物 :来自迂曲的周边异常血管网的大量渗漏。
好发于男童 :不伴遗传性或全身性疾病。成人也可发病。
荧光素眼底血管造影
葡萄膜渗漏(uveal effusion)
高度可移动的浆液性脱离 :随头位变化而容易移动。
合并周边脉络膜 脱离 :常同时出现脉络膜 脱离。
合并表现 :小眼球、高度远视 、涡静脉异常、巩膜 增厚。
血-视网膜屏障 (BRB)破坏是最终共同通路,其原因多种多样。
炎症性/免疫性
Vogt-小柳-原田病 (VKH)2)
交感性眼炎
后巩膜炎 /葡萄膜炎 :巩膜 和脉络膜 炎症引起的继发性渗出。
全身性疾病及其他
妊娠相关(子痫前期) :动脉痉挛→脉络膜 缺血→oBRB破坏。发生率约为子痫前期的1%。6)
CSC (中心性浆液性脉络膜视网膜病变 )RPE 泵功能障碍导致的浆液性脱离。
渗出型年龄相关性黄斑变性 :脉络膜新生血管 的渗出液积聚在视网膜 下。
药物性(MEKAR) :MEK抑制剂(如比美替尼)通过MAPK通路导致RPE 功能障碍。黑色素瘤治疗中发病率为0.6%~27%,结直肠癌治疗中为0.9%。4) 倾斜视 盘综合征(TDS) :巩膜 增厚和脉络膜 变薄导致的局部循环障碍引起黄斑部 浆液性脱离。3) 外伤性RPE 裂孔 :挫伤等外伤后出现RPE 裂孔,可能导致继发性渗出性脱离。1) 医源性(ROP 激光后) :早产儿视网膜病变 激光光凝后可能出现渗出性脱离。胎龄超过40周、低出生体重被认为是危险因素。5) 肿瘤性 :脉络膜 恶性黑色素瘤、转移性脉络膜 肿瘤可引起ERD。Coats病 眼底检查 可见周边部迂曲的异常血管网,荧光血管造影显示该部位有强烈的荧光渗漏。出现黄色视网膜 下渗出物和渗出性视网膜脱离。儿童患者必须与视网膜母细胞瘤 鉴别,后者超声显示实性肿块,头部CT显示钙化。葡萄膜渗漏 :特征为随头位容易移动的高度活动性浆液性视网膜脱离 和周边脉络膜 脱离。常合并小眼球、高度远视 、涡静脉异常、巩膜 增厚。巩膜 减压术是治疗选择之一。免疫检查点抑制剂 (ICI )相关ERDCI 的患者中报告了VKH样炎症性葡萄膜炎 和浆液性视网膜脱离 。12) 是否继续ICI 需与肿瘤科协商。
患有高血压或子痫前期的孕妇,如果出现急剧视力 下降或视物变形 ,请立即就诊眼科。
使用MEK抑制剂(抗癌药)期间如果感到视力 变化,请立即向主治医生报告。
外伤后出现视力 下降或视物变形 ,可能存在RPE 裂孔或继发性视网膜脱离 ,需要眼科就诊。
Q
抗癌药也会引起视网膜脱离吗?
A
包括MEK抑制剂(如比美替尼)在内的一些抗肿瘤药物可通过MAPK通路损害RPE 功能,引起渗出性视网膜脱离(MEKAR)。4) 多数无症状或轻微,停药后数天内消退。是否继续治疗需与主治医生商议。
对于确定病因和评估病情,采用多种检查手段的多模态方法非常重要。在检眼镜检查中,不仅要观察视网膜脱离 的部位和范围,还要仔细检查伴随表现,如视网膜 出血、渗出斑、色素上皮脱离、视网膜 下新生血管 以及有无隆起性病变。还应检查整个眼球,确认前节和中间屈光 间质有无炎症表现。全身检查也很重要,如VKH的脑脊液检查和听力检查,肿瘤性疾病的影像学检查等。
检查 主要所见/用途 OCT 确认视网膜下液 ,测量脉络膜 厚度 荧光眼底造影(FA ) 确定渗漏点和新生血管 ICGA 评估脉络膜 循环不全和低灌注区域 超声检查 鉴别后巩膜炎 和脉络膜 肿瘤
OCT (光学相干断层扫描 )视网膜下液 的有无、量和分布。测量脉络膜 厚度也有助于评估VKH的活动性。VKH急性期,OCT 显示脉络膜 明显增厚,约600 μm。2) 荧光眼底造影(FA ) :VKH的特征性表现为多发性点状强荧光和视盘荧光渗漏。2) CSC 在FA 上可见荧光渗漏点,IA可见脉络膜 血管通透性增高。CSC 需与年轻患者的特发性CNV 和视盘小凹 鉴别,与老年患者的息肉状脉络膜血管病变 (PCV )和厚脉络膜新生血管病变 鉴别,需通过IA和OCTA 确认有无息肉状病灶和CNV 。9) ICGA (吲哚青绿血管造影)2) 对评估脉络膜 循环障碍非常有用。超声检查(B型) :后巩膜炎 可确认巩膜 增厚和T征(Tenon囊积液)。对鉴别肿瘤性病变也很重要。儿童Coats病 必须与视网膜母细胞瘤 鉴别;超声显示实性肿块,头部CT显示钙化,可与视网膜母细胞瘤 区分。
Q
仅凭OCT就能诊断吗?
A
OCT 对于检测和随访视网膜下液 至关重要,但确定病因通常需要结合FA 、ICGA 和超声检查的多模态成像。2) 例如,在VKH中,ICGA 上的多发性低灌注区与FA 表现共同构成诊断依据。
Q
如何鉴别Coats病和视网膜母细胞瘤?
A
Coats病 的特征性表现为黄色调的视网膜 下渗出物和周边部异常血管网,荧光素眼底血管造影 可见明显的荧光渗漏。视网膜母细胞瘤 在超声检查中表现为实性肿块,头部CT检查常显示特征性钙化。这在儿童白瞳症 的鉴别中尤为重要,因为两种疾病的治疗方案根本不同,准确鉴别至关重要。
治疗的基础是确定并治疗原发病。通常不需要直接引流视网膜下液 ,一旦病因消除,液体常可自行消退。
对于VKH,据报道,球筋膜下注射曲安奈德 (20 mg)联合口服泼尼松龙(1 mg/kg/日)和免疫抑制剂(甲氨蝶呤 ;MTX)可在两周内使浆液性视网膜脱离 消退。2)
Peng等人(2025)报告了一例VKH合并单侧脉络膜 脱离的病例,采用球筋膜下TA 20 mg联合泼尼松龙1 mg/kg/日和MTX治疗,两周后视网膜下液 和脉络膜 脱离均消退。2)
停用致病药物是首选治疗。据报道,停药后三天内可迅速消退,多数情况下无需特殊眼科治疗。4)
Sakumura等人(2022)报告了一例由比美替尼(MEK抑制剂)引起的双侧浆液性视网膜脱离 。OCT 显示双眼多发性视网膜下液 ,但停用比美替尼后三天完全消退。4)
血压管理和分娩是最重要的治疗干预。分娩后浆液性脱离可自行消退,视力 通常恢复。6)
Phang等人(2022)报告了一例子痫前期合并HELLP综合征的孕妇出现双侧浆液性视网膜脱离 的病例。紧急剖宫产和降压治疗后,视网膜下液 消退,视力 恢复至发病前水平。6)
阈下微脉冲激光 被认为有效。
Minowa等人(2021)报告了对5只伴有倾斜视 盘综合征的浆液性视网膜脱离 眼进行阈下激光治疗 ,其中4只眼(80%)的视网膜下液 消失。3)
对于外伤后RPE 裂孔继发的渗出性视网膜脱离,采用保守治疗(如泼尼松龙滴眼液)。
Panigrahi等人(2023)报告了一例外伤后出现RPE 裂孔和渗出性视网膜脱离的病例。使用泼尼松龙滴眼液2周后自发消退,视力 恢复。1周后的OCT 显示脱色素细胞填充了RPE 裂孔部位。1)
Zou等人(2022)报告了一例早产儿视网膜病变 激光治疗 后单眼出现渗出性视网膜脱离的病例。增加泼尼松龙滴眼液次数(每日4次增至8次)后,8周后视网膜下液 消退。5)
以下列出每种病因的治疗方法。各疾病的详细信息请参阅专门文章。
病因 一线治疗 备注 VKH 类固醇冲击疗法 →维持疗法早期治疗影响视力 预后7) CSC 观察(3-4个月) 慢性型:PDT 湿性AMD 玻璃体 腔注射抗VEGF药物 需定期随访 Coats病 激光光凝/冷冻凝固 重症:玻璃体 手术 葡萄膜渗漏 巩膜 减压术合并小眼球病例 MEKAR 停用致病药物4) 3天内消退 子痫前期 血压管理和分娩6) 产后自然消退 ICI 相关 局部/全身类固醇 治疗12) 需与肿瘤科协商 肿瘤性 肿瘤治疗(放疗等) 取决于疾病
不同病因的视力 预后差异很大。
VKH :早期治疗视力 预后相对良好。需注意复发和慢性化。7) CSC 视力 预后不良。渗出型AMD :目标是通过抗VEGF治疗 维持稳定。长期病程中需警惕地图状萎缩 。Coats病 视力 。重症及全视网膜脱离 病例预后不良。药物性(MEKAR) :停用致病药物后迅速消退,视力 预后良好。4) 妊娠相关 :分娩后自然消退。视力 通常恢复。6) 肿瘤性 :根据肿瘤的性质和治疗成败而有很大差异。
渗出性视网膜脱离的治疗根据根本原因而完全不同。错误的治疗(例如,作为孔源性视网膜脱离 进行手术)可能会加重病情。
当MEK抑制剂用于抗肿瘤目的时,是否停药需要与肿瘤科协商;仅凭眼科判断需谨慎。
VKH的类固醇 治疗早期开始对预后很重要;如怀疑,应迅速转诊至专科医生。
渗出性视网膜脱离的发病机制中,**血-视网膜屏障 (BRB)**的破坏是共同的病理状态。
BRB有两个组成部分。
BRB类型 解剖部位 破坏示例 内层BRB(iBRB) 视网膜 血管内皮糖尿病视网膜病变 、放射性视网膜病变 外侧BRB(oBRB) RPE 紧密连接VKH、CSC 、药物性
主要病理是CD4阳性T细胞以黑色素细胞(RPE 和葡萄膜的黑色素生成细胞)为靶点的自身免疫反应。已知与HLA-DRB1*0405有强烈的遗传关联,VKH在东亚地区多见。2) 炎症破坏RPE 的紧密连接(oBRB破坏),导致脉络膜 的浆液流入视网膜 下腔。OCT 特征性地观察到多发泡状视网膜脱离 和分隔结构,以及急性期明显的脉络膜 增厚。2)
MEK抑制剂通过抑制MAPK通路改变RPE 中水通道蛋白的表达密度,从而损害RPE 的液体转运功能(oBRB破坏)。4) 这种机制是可逆的,停药后功能迅速恢复。
在子痫前期,胎盘来源的因子(如抗VEGF抗体样物质)引起全身血管痉挛。脉络膜 动脉痉挛导致脉络膜 缺血,RPE 泵功能受损,oBRB破坏。6)
巩膜 增厚和脉络膜 变薄导致局部脉络膜 循环异常。这种异常循环被认为降低了RPE 的液体转运能力,引起慢性浆液性脱离。3)
挫伤等物理外力导致RPE 断裂,局部oBRB急性破坏。RPE 撕裂后一周内,脱色素细胞开始填充和修复撕裂处,有时可自行消退。1)
Q
血-视网膜屏障(BRB)是什么结构?
A
BRB是控制血液和视网膜 组织之间物质交换的屏障机制。它由两层结构组成:视网膜 血管内皮细胞紧密连接形成的内侧BRB(iBRB)和RPE 紧密连接形成的外侧BRB(oBRB)。oBRB的破坏是许多渗出性视网膜脱离的共同病理。
对于倾斜视 盘综合征(TDS)相关的慢性浆液性视网膜脱离 ,已有病例报告显示阈下激光的有效性。3) 提示其可能在不留下光凝瘢痕、保留RPE 功能的同时促进液体吸收,但尚缺乏对照试验的充分验证。
关于MEK抑制剂眼部不良反应(MEKAR)与抗肿瘤效果的相关性,目前尚无足够数据。4) 如何平衡药物持续使用与视功能保护是未来的重要研究课题。
OCT血管成像 (OCTA )与ICGA 的结合可以更详细地评估脉络膜毛细血管层 的血流变化。2) 这有望提高对渗出性视网膜脱离病因疾病病理机制的理解以及治疗效果评估的准确性。
近年来,CSC 被重新归类为以脉络膜 增厚和粗大血管(扩张的大口径脉络膜 血管)为特征的厚脉络膜 谱系疾病的一种类型。9) 厚脉络膜 的概念对于理解息肉状脉络膜血管病变 (PCV )和厚脉络膜新生血管病变 (PNV )等相关疾病也很重要,并正在影响渗出性视网膜脱离的诊断和鉴别诊断体系。
随着免疫检查点抑制剂 (ICI )适应症的扩大,包括VKH样炎症性葡萄膜炎 和浆液性视网膜脱离 在内的眼部不良事件正在增加。12) 眼科专家与肿瘤科之间的协作进行适当管理已成为重要课题。
对于类固醇 抵抗性或类固醇 依赖性的VKH,已有使用英夫利西单抗 、阿达木单抗 等TNF -α抑制剂以及利妥昔单抗 等生物制剂 的报道。8) 虽然尚未成为标准治疗,但作为难治性病例的选择,相关研究仍在继续。
Panigrahi PK, et al. Spontaneous resolution of posttraumatic RPE tear and associated exudative retinal detachment. J Curr Ophthalmol. 2023;35:408-410.
Peng C, et al. Unilateral choroidal detachment in Vogt-Koyanagi-Harada disease. Front Immunol. 2025;16:1514306.
Minowa Y, et al. Subthreshold laser for serous retinal detachment in tilted disc syndrome. Case Rep Ophthalmol. 2021;12:978-986.
Sakumura M, et al. Bilateral serous retinal detachment with MEK inhibitor (binimetinib). Intern Med. 2022;61:1707-1712.
Zou H, Fletcher-Morehouse L. Exudative retinal detachment after retinopathy of prematurity laser treatment. Cureus. 2022;14(8):e27891.
Phang DSK, et al. Bilateral serous retinal detachment in pregnancy. Cureus. 2022;14(10):e30019.
日本眼炎症学会ぶどう膜炎診療ガイドライン作成委員会. ぶどう膜炎診療ガイドライン. 日眼会誌. 2019;123(3):224-318.
Tayal A, Bansal S. Vogt-Koyanagi-Harada disease: a narrative review. Ther Adv Ophthalmol. 2024;16:25158414241244681.
Cheung CMG, Lee WK, Koizumi H, et al. Pachychoroid disease. Eye (Lond). 2019;33(1):14-33.
Daruich A, Matet A, Moulin A, et al. Mechanisms of macular edema: beyond the surface. Prog Retin Eye Res. 2018;63:20-68.
Campbell M, Humphries P. The blood-retina barrier: tight junctions and barrier modulation. Adv Exp Med Biol. 2012;763:70-84.
Dalvin LA, Shields CL, Orloff M, et al. Checkpoint inhibitor immune therapy: systemic indications and ophthalmic side effects. Retina. 2018;38(6):1063-1078.
复制全文后,可以粘贴到你常用的 AI 助手中提问。
打开下面的 AI 助手,并把复制的内容粘贴到聊天框。