滲出性視網膜剝離是一種不伴有裂孔或牽引的非裂孔源性視網膜剝離 ,血液視網膜 屏障(BRB)破壞是其共同病理機制。
體位改變時剝離部位移動的「shifting fluid」是該疾病的特徵性臨床表現。
原因多樣,包括發炎性(如VKH病)、血管性(如Coats病 )、腫瘤性、RPE 疾病(如CSC )、藥物性及妊娠相關。
治療原則是找出並治療原因疾病,去除原因後視網膜下液 常會自然消退。
MEK抑制劑(如比美替尼)引起的藥物性滲出性視網膜剝離,在停用原因藥物後數天內消失。4)
懷孕期間的雙側漿液性視網膜剝離 與子癇前症密切相關,常在分娩後自然消退。6)
使用免疫檢查點抑制劑 (ICI )的患者中,有報告出現VKH樣發炎性滲出性視網膜剝離,需注意。12)
診斷上,光學同調斷層掃描 (OCT )、螢光眼底攝影 、吲哚青綠血管攝影(ICGA )及超音波檢查等多模式影像檢查很有用。
不同原因疾病的視力 預後差異很大。VKH和CSC 早期治療可望有良好預後。
滲出性視網膜剝離(exudative retinal detachment; ERD)是非裂孔源性視網膜剝離 的一種類型。不伴裂孔的視網膜剝離 稱為非裂孔源性視網膜剝離 ,大致分為滲出性和牽引性兩種。滲出性視網膜剝離是指在沒有視網膜裂孔 或牽引力的情況下,液體在視網膜 下腔積聚的病理狀態,可由發炎性疾病、變性疾病、感染或腫瘤等多種疾病引起。
基本病理是視網膜 血管、視網膜色素上皮 (RPE )或脈絡膜 功能障礙導致滲出液積聚在視網膜 下。血-視網膜屏障 (BRB)破壞後,脈絡膜 血管、視網膜 血管和RPE 滲出的液體在視網膜 下積聚。有時與「漿液性視網膜剝離 」幾乎同義使用,但本文涵蓋廣義的滲出性視網膜剝離,包括腫瘤性、發炎性和藥物性。
剝離高度低的輕症病例稱為漿液性視網膜剝離 ,代表性疾病是中心性漿液性脈絡膜 視網膜 病變(CSC )。糖尿病視網膜病變 、視網膜靜脈阻塞 、年齡相關性黃斑 變性和視網膜 微動脈瘤 也可發生,但伴有視網膜 下出血時則變得難治。
原因疾病多樣,包括Vogt-小柳-原田病 (VKH)和後鞏膜炎 等葡萄膜炎 、CSC 和多發性後極部視網膜色素上皮 病變(MPPE)等視網膜色素上皮 疾病、年齡相關性黃斑 變性等視網膜 下新生血管 、Coats病 等血管疾病、脈絡膜 血管瘤和視網膜母細胞瘤 等腫瘤性疾病、葡萄膜滲漏、糖尿病黃斑 水腫等。由於不同疾病的治療方法根本不同,準確診斷非常重要。
與裂孔源性視網膜剝離 的區別如下所示。
項目 滲出性 裂孔源性 視網膜裂孔 無 有 剝離形態 圓頂狀、平滑 皺褶狀、不規則 移動性液體 有 無至少量 治療原則 治療原發疾病 手術(封閉裂孔)
Q
裂孔性視網膜剝離與滲出性視網膜剝離有何不同?
A
裂孔性視網膜剝離 是因視網膜 出現裂孔,玻璃體 液流入所致。滲出性視網膜剝離沒有裂孔,而是因血管或RPE 損傷導致視網膜下液 體積聚。前者原則上以手術封閉裂孔,後者則以治療原發疾病為基礎。改變體位時剝離部位移動的「移動性液體」是滲出性視網膜剝離的特徵性表現。
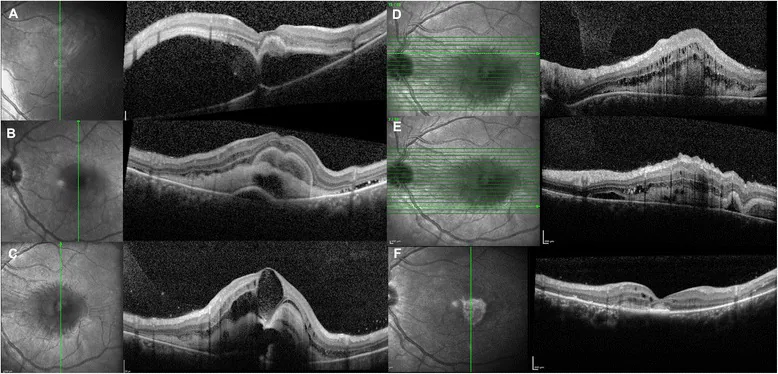
滲出性視網膜剝離的OCT所見 Maggio E, et al. Multimodal imaging findings in a case of severe Central Serous Chorioretinopathy in an uncomplicated pregnancy. BMC Ophthalmol. 2015. Figure 1. PM
CI D: PMC4688919. License: CC BY.
光學同調斷層掃描 (OCT )顯示黃斑部 神經感覺視網膜 明顯漿液性隆起,伴有視網膜 下高反射物質(a),以及追蹤期間視網膜下液 消失和視網膜 下滲出物積聚(b-c)。這對應於本文「2. 主要症狀與臨床所見」中討論的漿液性視網膜剝離 。
視力 下降視網膜下液 侵犯黃斑 時導致明顯視力 下降。變視症 黃斑部 視網膜 隆起導致物體看起來扭曲。霧視 視野缺損 視野缺損 。全身症狀 :根據原發病(如VKH)可能伴有頭痛、耳鳴或感冒樣症狀。
典型的滲出性視網膜剝離表現為視網膜 呈穹窿狀隆起,表面光滑,視網膜下液 隨體位改變而移動(shifting fluid)。通常不會出現裂孔源性剝離中見到的皺褶或不規則隆起。
炎症性(VKH)
雙側漿液性剝離 :雙眼出現多個穹窿狀隆起。
脈絡膜 增厚OCT 顯示明顯脈絡膜 增厚(約600μm)。2)
OCT 特徵性所見視網膜剝離 ,脈絡膜 管腔結構變窄。
視乳頭充血 水腫 :視神經乳頭 也伴有炎症性改變。
藥物性(MEKAR)
急性發作的雙側SRD :MEK抑制劑給藥後迅速發生。4)
症狀通常輕微 :有些病例視力 下降輕微,自覺症狀不明顯。
可逆性 :停藥後3天內常消退。4)
妊娠相關
雙側漿液性RD :可能合併子癇前症/HELLP症候群。6)
黃斑部 優勢剝離黃斑部 積聚,引起視物變形和視力 下降。
產後消退 :產後常自然消退,視力 多可恢復。6)
外傷性/醫源性
RPE 裂孔後ERDRPE 裂孔後繼發滲出性剝離。1)
ROP 雷射後ERD早產兒視網膜病變 雷射治療 後可能發生。5)
體位變化時液體移動 :可觀察到移動性液體。
Coats病
黃色調視網膜 下滲出物 :來自迂曲的周邊異常血管網的大量滲漏。
好發於男童 :不伴遺傳性或全身性疾病。成人也可發病。
螢光眼底血管攝影
葡萄膜滲出(uveal effusion)
高度可移動的漿液性剝離 :隨頭位變化而容易移動。
合併周邊脈絡膜 剝離 :常同時出現脈絡膜 剝離。
合併表現 :小眼球、高度遠視 、渦靜脈異常、鞏膜 增厚。
血-視網膜屏障 (BRB)破壞是最終共同路徑,其原因多種多樣。
發炎性/免疫性
Vogt-小柳-原田病 (VKH)2)
交感性眼炎
後鞏膜炎 /葡萄膜炎 :鞏膜 和脈絡膜 發炎引起的繼發性滲出。
全身性疾病及其他
妊娠相關(子癇前症) :動脈痙攣→脈絡膜 缺血→oBRB破壞。發生率約為子癇前症的1%。6)
CSC (中心性漿液性脈絡膜 視網膜 病變)RPE 幫浦功能障礙導致的漿液性剝離。
滲出型年齡相關性黃斑部 病變 :脈絡膜新生血管 的滲出液積聚在視網膜 下。
藥物性(MEKAR) :MEK抑制劑(如比美替尼)經由MAPK路徑導致RPE 功能障礙。黑色素瘤治療中發生率為0.6%~27%,大腸癌治療中為0.9%。4) 傾斜視 盤症候群(TDS) :鞏膜 增厚和脈絡膜 變薄導致的局部循環障礙引起黃斑部 漿液性剝離。3) 外傷性RPE 裂孔 :挫傷等外傷後出現RPE 裂孔,可能導致續發性滲出性剝離。1) 醫源性(ROP 雷射後) :早產兒視網膜病變 雷射光凝後可能出現滲出性剝離。胎齡超過40週、低出生體重被認為是危險因子。5) 腫瘤性 :脈絡膜 惡性黑色素瘤、轉移性脈絡膜 腫瘤可引起ERD。Coats病 眼底檢查 可見周邊部迂曲的異常血管網,螢光血管造影顯示該部位有強烈的螢光滲漏。出現黃色視網膜 下滲出物和滲出性視網膜剝離。兒童患者必須與視網膜母細胞瘤 鑑別,後者超音波顯示實質性腫塊,頭部CT顯示鈣化。葡萄膜滲漏 :特徵為隨頭位容易移動的高度活動性漿液性視網膜剝離 和周邊脈絡膜 剝離。常合併小眼球、高度遠視 、渦靜脈異常、鞏膜 增厚。鞏膜 減壓術是治療選擇之一。免疫檢查點抑制劑 (ICI )相關ERDCI 的患者中報告了VKH樣炎症性葡萄膜炎 和漿液性視網膜剝離 。12) 是否繼續ICI 需與腫瘤科協商。
患有高血壓或子癇前症的孕婦,如果出現急劇視力 下降或視物變形,請立即就診眼科。
使用MEK抑制劑(抗癌藥)期間如果感到視力 變化,請立即向主治醫師報告。
外傷後出現視力 下降或視物變形,可能存在RPE 裂孔或續發性視網膜剝離 ,需要眼科就診。
Q
抗癌藥也會引起視網膜剝離嗎?
A
包括MEK抑制劑(如比美替尼)在內的一些抗腫瘤藥物可經由MAPK路徑損害RPE 功能,引起滲出性視網膜剝離(MEKAR)。4) 多數無症狀或輕微,停藥後數天內消退。是否繼續治療需與主治醫師商議。
對於確定病因和評估病情,採用多種檢查方式的多模式方法非常重要。在檢眼鏡檢查中,不僅要觀察視網膜剝離 的部位和範圍,還要仔細檢查伴隨表現,如視網膜 出血、滲出斑、色素上皮剝離、視網膜 下新生血管 以及有無隆起性病變。也應檢查整個眼球,確認前房 和中間屈光 介質有無發炎表現。全身檢查也很重要,如VKH的腦脊髓液檢查和聽力檢查,腫瘤性疾病的影像學檢查等。
檢查 主要所見/用途 OCT 確認視網膜下液 ,測量脈絡膜 厚度 螢光眼底攝影 (FA ) 確定滲漏點和新生血管 ICGA 評估脈絡膜 循環不全和低灌注區域 超音波檢查 鑑別後鞏膜炎 和脈絡膜 腫瘤
OCT (光學同調斷層掃描 )視網膜下液 的有無、量和分佈。測量脈絡膜 厚度也有助於評估VKH的活動性。VKH急性期,OCT 顯示脈絡膜 明顯增厚,約600 μm。2) 螢光眼底攝影 (FA ) :VKH的特徵性表現為多發性點狀強螢光和視神經 盤螢光滲漏。2) CSC 在FA 上可見螢光滲漏點,IA可見脈絡膜 血管通透性增加。CSC 需與年輕患者的特發性CNV 和視神經盤小凹 鑑別,與老年患者的息肉狀脈絡膜血管病變 (PCV )和厚脈絡膜新生血管病變 鑑別,需透過IA和OCTA 確認有無息肉狀病灶和CNV 。9) ICGA (靛氰綠血管攝影)2) 對評估脈絡膜 循環障礙非常有用。超音波檢查(B型) :後鞏膜炎 可確認鞏膜 增厚和T徵(Tenon囊積液)。對鑑別腫瘤性病變也很重要。兒童Coats病 必須與視網膜母細胞瘤 鑑別;超音波顯示實質性腫塊,頭部CT顯示鈣化,可與視網膜母細胞瘤 區分。
Q
僅用OCT就能診斷嗎?
A
OCT 對於檢測和追蹤視網膜下液 至關重要,但確定病因通常需要結合FA 、ICGA 和超音波檢查的多模態影像。2) 例如,在VKH中,ICGA 上的多發性低灌注區與FA 表現共同構成診斷依據。
Q
如何鑑別Coats病和視網膜母細胞瘤?
A
Coats病 的特徵性表現為黃色調的視網膜 下滲出物和周邊部異常血管網,螢光眼底血管攝影 可見明顯的螢光滲漏。視網膜母細胞瘤 在超音波檢查中表現為實質性腫塊,頭部CT檢查常顯示特徵性鈣化。這在兒童白瞳症 的鑑別中尤為重要,因為兩種疾病的治療方針根本不同,準確鑑別至關重要。
治療的基礎是確定並治療原發病。通常不需要直接引流視網膜下液 ,一旦病因消除,液體常可自行消退。
對於VKH,據報導,眼球筋膜下注射曲安奈德 (20 mg)聯合口服潑尼松龍(1 mg/kg/日)和免疫抑制劑(甲氨蝶呤 ;MTX)可在兩週內使漿液性視網膜剝離 消退。2)
Peng等人(2025)報告了一例VKH合併單側脈絡膜 剝離的病例,採用眼球筋膜下TA 20 mg聯合潑尼松龍1 mg/kg/日和MTX治療,兩週後視網膜下液 和脈絡膜 剝離均消退。2)
停用致病藥物是首選治療。據報導,停藥後三天內可迅速消退,多數情況下無需特殊眼科治療。4)
Sakumura等人(2022)報告了一例由比美替尼(MEK抑制劑)引起的雙側漿液性視網膜剝離 。OCT 顯示雙眼多發性視網膜下液 ,但停用比美替尼後三天完全消退。4)
血壓管理和分娩是最重要的治療介入。分娩後漿液性剝離可自行消退,視力 通常恢復。6)
Phang等人(2022)報告了一例子癇前症合併HELLP症候群的孕婦出現雙側漿液性視網膜剝離 的病例。緊急剖腹產和降壓治療後,視網膜下液 消退,視力 恢復至發病前水平。6)
閾值下微脈衝雷射 被認為有效。
Minowa等人(2021)報告對5隻伴有傾斜視 盤症候群的漿液性視網膜剝離 眼進行閾值下雷射 治療,其中4隻眼(80%)的視網膜下液 消失。3)
對於外傷後RPE 裂孔繼發的滲出性視網膜剝離,採用保守治療(如潑尼松龍滴眼液)。
Panigrahi等人(2023)報告了一例外傷後出現RPE 裂孔和滲出性視網膜剝離的病例。使用潑尼松龍滴眼液2週後自發消退,視力 恢復。1週後的OCT 顯示脫色素細胞填充了RPE 裂孔部位。1)
Zou等人(2022)報告了一例早產兒視網膜病變 雷射治療 後單眼出現滲出性視網膜剝離的病例。增加潑尼松龍滴眼液次數(每日4次增至8次)後,8週後視網膜下液 消退。5)
以下列出每種病因的治療方法。各疾病的詳細資訊請參閱專門文章。
病因 一線治療 備註 VKH 類固醇脈衝療法 →維持療法早期治療影響視力 預後7) CSC 觀察(3-4個月) 慢性型:PDT 濕性AMD 玻璃體內注射 抗VEGF藥物 需定期追蹤 Coats病 雷射光凝固 /冷凍凝固 重症:玻璃體 手術 葡萄膜滲漏 鞏膜 減壓術合併小眼球病例 MEKAR 停用致病藥物4) 3天內消退 子癇前症 血壓管理與分娩6) 產後自然消退 ICI 相關 局部/全身類固醇 治療12) 需與腫瘤科協商 腫瘤性 腫瘤治療(放射線等) 取決於疾病
不同病因的視力 預後差異很大。
VKH :早期治療視力 預後相對良好。需注意復發與慢性化。7) CSC 視力 預後不良。滲出型AMD :目標是透過抗VEGF治療維持穩定。長期病程中需擔心地圖狀萎縮 。Coats病 視力 。重症及全視網膜剝離 病例預後不良。藥物性(MEKAR) :停用致病藥物後迅速消退,視力 預後良好。4) 妊娠相關 :分娩後自然消退。視力 通常恢復。6) 腫瘤性 :根據腫瘤的性質和治療成敗而有很大差異。
滲出性視網膜剝離的治療根據根本原因而完全不同。錯誤的治療(例如,作為裂孔源性視網膜剝離 進行手術)可能會加重病情。
當MEK抑制劑用於抗腫瘤目的時,是否停藥需要與腫瘤科協商;僅憑眼科判斷需謹慎。
VKH的類固醇 治療早期開始對預後很重要;如懷疑,應迅速轉診至專科醫生。
滲出性視網膜剝離的發病機制中,**血-視網膜屏障 (BRB)**的破壞是共同的病理狀態。
BRB有兩個組成部分。
BRB類型 解剖部位 破壞示例 內層BRB(iBRB) 視網膜 血管內皮糖尿病視網膜病變 、放射性視網膜病變 外側BRB(oBRB) RPE 緊密連接VKH、CSC 、藥物性
主要病理是CD4陽性T細胞以黑色素細胞(RPE 和葡萄膜的黑色素生成細胞)為標的的自體免疫反應。已知與HLA-DRB1*0405有強烈的遺傳關聯,VKH在東亞地區多見。2) 發炎破壞RPE 的緊密連接(oBRB破壞),導致脈絡膜 的漿液流入視網膜 下腔。OCT 特徵性地觀察到多發泡狀視網膜剝離 和分隔結構,以及急性期明顯的脈絡膜 增厚。2)
MEK抑制劑通過抑制MAPK路徑改變RPE 中水通道蛋白的表現密度,從而損害RPE 的液體轉運功能(oBRB破壞)。4) 這種機轉是可逆的,停藥後功能迅速恢復。
在子癇前症,胎盤來源的因子(如抗VEGF抗體樣物質)引起全身血管痙攣。脈絡膜 動脈痙攣導致脈絡膜 缺血,RPE 幫浦功能受損,oBRB破壞。6)
鞏膜 增厚和脈絡膜 變薄導致局部脈絡膜 循環異常。這種異常循環被認為降低了RPE 的液體轉運能力,引起慢性漿液性剝離。3)
挫傷等物理外力導致RPE 斷裂,局部oBRB急性破壞。RPE 撕裂後一週內,脫色素細胞開始填充和修復撕裂處,有時可自行消退。1)
Q
血-視網膜屏障(BRB)是什麼結構?
A
BRB是控制血液和視網膜 組織之間物質交換的屏障機制。它由兩層結構組成:視網膜 血管內皮細胞緊密連接形成的內側BRB(iBRB)和RPE 緊密連接形成的外側BRB(oBRB)。oBRB的破壞是許多滲出性視網膜剝離的共同病理。
對於傾斜視 盤症候群(TDS)相關的慢性漿液性視網膜剝離 ,已有病例報告顯示閾值下雷射 的有效性。3) 提示其可能在不留下光凝疤痕、保留RPE 功能的同時促進液體吸收,但尚缺乏對照試驗的充分驗證。
關於MEK抑制劑眼部不良反應(MEKAR)與抗腫瘤效果的相關性,目前尚無足夠數據。4) 如何平衡藥物持續使用與視功能保護是未來的重要研究課題。
OCT血管成像 (OCTA )與ICGA 的結合可以更詳細地評估脈絡膜微血管層 的血流變化。2) 這有望提高對滲出性視網膜剝離病因疾病病理機制的理解以及治療效果評估的準確性。
近年來,CSC 被重新歸類為以脈絡膜 增厚和粗大血管(擴張的大口徑脈絡膜 血管)為特徵的厚脈絡膜 譜系疾病的一種類型。9) 厚脈絡膜 的概念對於理解息肉狀脈絡膜血管病變 (PCV )和厚脈絡膜新生血管病變 (PNV )等相關疾病也很重要,並正在影響滲出性視網膜剝離的診斷和鑑別診斷體系。
隨著免疫檢查點抑制劑 (ICI )適應症的擴大,包括VKH樣發炎性葡萄膜炎 和漿液性視網膜剝離 在內的眼部不良事件正在增加。12) 眼科專家與腫瘤科之間的協作進行適當管理已成為重要課題。
對於類固醇 抗藥性或類固醇 依賴性VKH,已有使用英夫利昔單抗、阿達木單抗 等TNF -α抑制劑以及利妥昔單抗 等生物製劑 的報告。8) 雖然尚未成為標準治療,但作為難治病例的選擇,研究仍在繼續。
Panigrahi PK, et al. Spontaneous resolution of posttraumatic RPE tear and associated exudative retinal detachment. J Curr Ophthalmol. 2023;35:408-410.
Peng C, et al. Unilateral choroidal detachment in Vogt-Koyanagi-Harada disease. Front Immunol. 2025;16:1514306.
Minowa Y, et al. Subthreshold laser for serous retinal detachment in tilted disc syndrome. Case Rep Ophthalmol. 2021;12:978-986.
Sakumura M, et al. Bilateral serous retinal detachment with MEK inhibitor (binimetinib). Intern Med. 2022;61:1707-1712.
Zou H, Fletcher-Morehouse L. Exudative retinal detachment after retinopathy of prematurity laser treatment. Cureus. 2022;14(8):e27891.
Phang DSK, et al. Bilateral serous retinal detachment in pregnancy. Cureus. 2022;14(10):e30019.
日本眼炎症学会ぶどう膜炎診療ガイドライン作成委員会. ぶどう膜炎診療ガイドライン. 日眼会誌. 2019;123(3):224-318.
Tayal A, Bansal S. Vogt-Koyanagi-Harada disease: a narrative review. Ther Adv Ophthalmol. 2024;16:25158414241244681.
Cheung CMG, Lee WK, Koizumi H, et al. Pachychoroid disease. Eye (Lond). 2019;33(1):14-33.
Daruich A, Matet A, Moulin A, et al. Mechanisms of macular edema: beyond the surface. Prog Retin Eye Res. 2018;63:20-68.
Campbell M, Humphries P. The blood-retina barrier: tight junctions and barrier modulation. Adv Exp Med Biol. 2012;763:70-84.
Dalvin LA, Shields CL, Orloff M, et al. Checkpoint inhibitor immune therapy: systemic indications and ophthalmic side effects. Retina. 2018;38(6):1063-1078.
開啟下方的 AI 助手,並將複製的內容貼到聊天欄。