Luce di eccitazione
Viene irradiata luce blu con lunghezza d’onda 465-490 nm.
Nell’SLO si utilizza un laser a 488 nm.
Un filtro di eccitazione taglia le lunghezze d’onda indesiderate.

L’angiografia con fluoresceina (FA) è un esame che prevede la somministrazione endovenosa del colorante fluorescente fluoresceina sodica e la fotografia del fondo oculare con una fotocamera dotata di filtri speciali per visualizzare dinamicamente la circolazione sanguigna retinica e coroidale. Eccelle nella valutazione della dinamica circolatoria retinica e dello stato della barriera emato-retinica, ed è ampiamente utilizzata per la diagnosi e la pianificazione terapeutica delle malattie del fondo oculare. È utile non solo per le patologie vascolari retiniche, ma anche per la diagnosi differenziale di uveiti, tumori coroidali e malattie della papilla ottica.
Nel 1961, Harold R. Novotny e David L. Alvis riportarono per la prima volta il metodo originale della FA. Successivamente, a partire dal 1967, John Donald McIntyre Gass pubblicò descrizioni sistematiche dei reperti FA in varie malattie del fondo oculare, portando a una rapida diffusione dell’applicazione clinica.
La fluoresceina sodica emette fluorescenza giallo-verde (520–530 nm) quando viene irradiata con luce blu di eccitazione (lunghezza d’onda 465–490 nm). Nell’oftalmoscopia laser a scansione (SLO) viene utilizzato un laser blu a 488 nm. La fluoresceina sodica è un colorante idrosolubile con peso molecolare 376 Da; dopo somministrazione endovenosa, il legame proteico è di circa il 70–80%. Il restante 20–30% in forma libera emette fluorescenza. In presenza di una barriera emato-retinica integra, anche la forma libera non fuoriesce dai vasi. In caso di rottura della barriera, il colorante fuoriesce dai vasi e viene osservato come iperfluorescenza caratteristica.
La barriera emato-retinica (BER) è composta da due strati: la barriera interna formata dalle giunzioni strette delle cellule endoteliali dei vasi retinici, e la barriera esterna formata dalle giunzioni strette delle cellule dell’epitelio pigmentato retinico (EPR). La rottura della BER provoca la fuoriuscita di fluoresceina, che costituisce un indicatore diagnostico di varie malattie retiniche.
Luce di eccitazione
Viene irradiata luce blu con lunghezza d’onda 465-490 nm.
Nell’SLO si utilizza un laser a 488 nm.
Un filtro di eccitazione taglia le lunghezze d’onda indesiderate.
Emissione di fluorescenza
Viene emessa fluorescenza giallo-verde con lunghezza d’onda di emissione 520-530 nm.
La forma libera (circa 20-30%) è il principale responsabile della fluorescenza.
La forma legata alle proteine (circa 70-80%) emette difficilmente fluorescenza.
Filtro barriera
Viene trasmessa solo la fluorescenza con lunghezza d’onda superiore a 520 nm.
La luce di eccitazione viene bloccata, rendendo nitida l’immagine di fluorescenza.
L’extravasazione è una prova di rottura della barriera.
Fu riportata per la prima volta nel 1961 da Novotny e Alvis. Dal 1967, Gass ne ha sistematizzato l’applicazione a varie malattie del fondo oculare, e si è diffusa in tutto il mondo come metodo di esame standard per la diagnosi del fondo oculare.
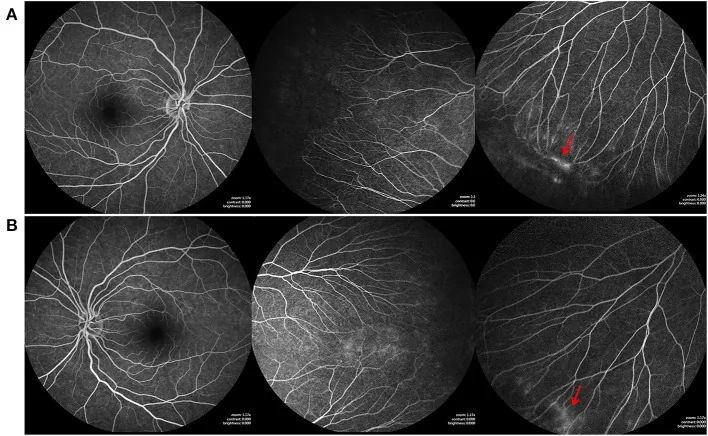
La FA è ampiamente utilizzata per visualizzare il sistema vascolare del fondo oculare. Di seguito sono elencate le principali indicazioni.
Nell’edema maculare che si verifica dopo la necrosi retinica acuta (ARN), la FA mostra un pattern di leakage petaloide, contribuendo alla diagnosi differenziale dell’edema maculare cistoide (CME) e alla valutazione dell’efficacia del trattamento1).
Durante la gravidanza può verificarsi un’occlusione vascolare retinica, ma dal punto di vista del passaggio placentare della FA, l’OCTA è raccomandata come esame alternativo2).
Prima dell’esame, spiegare il seguente contenuto e ottenere il consenso scritto4).
Secondo gli standard di esecuzione dell’angiografia del fondo oculare (versione rivista) della Società Giapponese di Oftalmologia, vengono eseguiti i seguenti punti 4).
I pazienti in terapia con beta-bloccanti o alfa-bloccanti presentano un rischio maggiore di effetti collaterali, pertanto è necessario accertarlo in anticipo 4). Il test di reazione cutanea ha un’utilità limitata; anche se negativo, non può escludere completamente effetti collaterali gravi 4).
Iniettare rapidamente per via endovenosa 3-5 mL di soluzione di fluoresceina al 10% 4). Nei bambini, la dose indicativa è di 0,1 mg/kg; nei pazienti con insufficienza renale, la dose deve essere ridotta a metà o meno della dose normale 4).
Subito dopo l’iniezione, si esegue una ripresa continua per circa 1 minuto, quindi si acquisiscono immagini tardive a 5 e 10 minuti. Includendo il tempo per la dilatazione pupillare, l’intera procedura richiede circa 15-20 minuti.
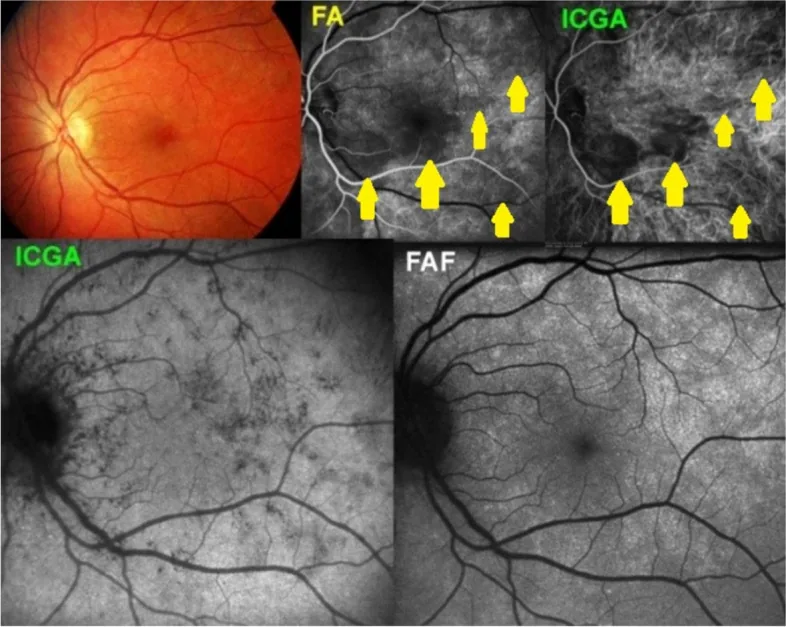
La FA viene osservata in più fasi in sequenza temporale.
I reperti dell’angiografia con fluoresceina sono suddivisi in tre categorie: ipofluorescenza, iperfluorescenza e anomalie morfologiche vascolari.
Blocco della fluorescenza (ipofluorescenza)
Definizione: emorragia, pigmentazione, essudati, ecc., mascherano la fluorescenza di fondo.
Caratteristiche: bordi netti, forma invariata nel tempo.
Malattie rappresentative: emorragia sottoretinica, essudati duri, nevo coroidale.
Difetto di riempimento (ipofluorescenza)
Definizione: assenza o ritardo del flusso del colorante fluorescente a causa di occlusione vascolare.
Caratteristiche: le aree di non perfusione capillare rimangono scure per tutto il decorso.
Malattie rappresentative: occlusione dell’arteria retinica, aree avascolari nella retinopatia diabetica.
Perdita di fluorescenza (iperfluorescenza)
Definizione: rottura della barriera emato-retinica con stravaso del colorante.
Caratteristiche: aumento di dimensioni nel tempo, bordi sfumati. Un pattern petaloide è caratteristico dell’edema maculare cistoide1).
Malattie rappresentative: edema maculare, neovascolarizzazione coroidale, vasculite retinica.
Fluorescenza di trasmissione (iperfluorescenza)
Definizione : La fluorescenza coroidale è visibile attraverso un difetto dell’RPE (window defect).
Caratteristiche : La forma non cambia nel tempo, ma può colorarsi debolmente in fase tardiva.
Malattie rappresentative : Atrofia geografica, confluenza di drusen, foro maculare, strie angioidi.
L’ipofluorescenza è suddivisa in base alla causa come segue.
| Tipo di ipofluorescenza | Causa / Meccanismo | Malattie rappresentative |
|---|---|---|
| Blocco della fluorescenza | Emorragia, essudato duro, nevo mascherano la fluorescenza di fondo | Emorragia sottoretinica, essudato duro, nevo coroidale |
| Difetto di riempimento: stenosi vascolare retino-coroidale | Occlusione o stenosi dei grandi vasi | Occlusione dell’arteria carotide interna, arterite di Takayasu |
| Difetto di riempimento: occlusione vascolare retinica | Occlusione arteriosa e venosa | Occlusione dell’arteria retinica (CRAO/BRAO), occlusione della vena retinica |
| Difetto di riempimento: occlusione capillare | Disturbo circolatorio periferico | Retinopatia diabetica (NPA), malattia di Eales |
| Difetto di riempimento: disturbo circolatorio coroidale | Insufficienza del flusso sanguigno coroidale | Malattia di Harada, APMPPE, coroidopatia ipertensiva |
| Atrofia corioretinica | Perdita di fluorescenza per atrofia tissutale | Distrofia maculare, retinite pigmentosa, AMD atrofica, miopia patologica |
| Ipofluorescenza papillare | Ischemia/infiltrazione del tessuto del nervo ottico | Neuropatia ottica ischemica, melanocitoma |
L’iperfluorescenza è suddivisa in base alla causa come segue.
Si osservano le seguenti anomalie morfologiche vascolari.
I vasi coroidali sono difficili da valutare a causa dell’oscuramento da parte dell’EPR. Per la valutazione della MNV di tipo 1 (neovascolarizzazione coroidale) con perdita di fluoresceina, si utilizza in modo complementare l’angiografia con verde di indocianina (ICGA).
Microaneurismi, aree non perfuse (NPA) e neovascolarizzazione sono i reperti principali. La FA distingue i pattern di perdita dell’edema maculare (focale/diffuso/cistoide) e costituisce la base per determinare i siti di irradiazione laser 3). Nelle fasi tardive si osserva una marcata perdita dalla neovascolarizzazione. La FA a campo ultra-largo migliora la precisione nella valutazione delle NPA periferiche.
Indispensabile per la valutazione dell’attività della CNV. La CNV classica (tipo 2) mostra una iperfluorescenza precoce ben delimitata e una perdita tardiva. La CNV occulta (tipo 1) è situata sotto l’EPR e si presenta come iperfluorescenza punteggiata tardiva o distacco fibrovascolare dell’EPR. L’atrofia geografica si manifesta come difetto finestra.
Utilizzata per valutare il ritardo di riempimento, la dilatazione e tortuosità venosa, le aree di non perfusione capillare e i circoli collaterali. Una NPA superiore a 10 aree di disco è considerata di tipo ischemico ed è un indicatore di rischio di glaucoma neovascolare. Importante anche per comprendere il pattern di perdita dell’edema maculare.
Si osservano punti di perdita caratteristici di tipo «inkblot» (macchia d’inchiostro) o «smokestack» (ciminiera) a livello dell’EPR. Punti di perdita multipli suggeriscono una CSC cronica. Per determinare l’area di irradiazione della terapia fotodinamica (PDT) si utilizzano FA e ICGA in combinazione.
Nella malattia di Harada si osservano iperfluorescenze puntiformi dovute a multiple perdite coroidali e accumulo di colorante nelle aree di distacco sieroso della retina. Nella malattia di Behçet si riscontrano colorazione delle pareti vascolari per vasculite retinica e aree di non perfusione arteriosa (NPA). Nella malattia di Eales sono caratteristiche NPA periferiche e neovascolarizzazione.
Vengono presentati i dati dello standard di esecuzione dell’angiografia del fondo oculare della Società Giapponese di Oftalmologia (edizione riveduta) 4).
Gli effetti collaterali si verificano con le seguenti frequenze in base alla gravità.
| Gravità | Incidenza |
|---|---|
| Tutti gli effetti collaterali | 1,1–11,2% |
| Lieve | 1,4–8,1% |
| Moderato | 0,2–1,5% |
| Grave | 0,005–0,48% |
| Morte | 0,0005–0,002 % |
Lieve (spesso si risolve spontaneamente)
Moderato
Grave (estremamente raro)
La diagnosi di anafilassi si basa su uno dei seguenti tre criteri4).
Algoritmo per la gestione dell’anafilassi :
Anche dopo un trattamento efficace, esiste il rischio di anafilassi bifasica (recidiva entro 6–8 ore dalla scomparsa dei sintomi); pertanto è necessario un monitoraggio di almeno 8 ore e si raccomanda il ricovero per osservazione (24 ore)4).
Diagnosi differenziale con il riflesso vagale: Il riflesso vagale si manifesta con bradicardia, ipotensione, pallore e sudorazione fredda, ma non presenta segni cutanei (orticaria, rossore), distinguendolo dall’anafilassi. Per il riflesso vagale sono efficaci il mantenimento della posizione supina, il sollevamento degli arti inferiori e la somministrazione di liquidi4).
Si tratta di una reazione normale all’escrezione renale della fluoresceina, non c’è motivo di preoccuparsi. La colorazione gialla della pelle scompare in 2-3 ore, quella delle urine entro il giorno successivo.
La fluoresceina attraversa la placenta ed è rilevabile nel latte materno per 72 ore, pertanto l’esame è in linea di principio evitato nelle donne in gravidanza o che allattano2)3). Se sono necessarie informazioni sui vasi retinici, si raccomanda l’angiografia OCT non invasiva (OCTA) come alternativa2).
La fluoresceina sodica è un colorante idrosolubile di colore giallo-rosso con peso molecolare di 376 Da. Se eccitata a una lunghezza d’onda di 465-490 nm (488 nm in SLO), emette fluorescenza giallo-verde a 520-530 nm. Dopo somministrazione endovenosa, circa il 70-80% si lega alle proteine plasmatiche (principalmente albumina) e circa il 20-30% è in forma libera ed emette fluorescenza. Viene escreta dai reni (scompare in 1-2 giorni) e il metabolismo epatico è scarso.
L’angiografia con verde indocianina (ICG) è utilizzata in modo complementare alla FA. Le caratteristiche di entrambe sono riportate di seguito.
| Parametro | FA | Angiografia ICG |
|---|---|---|
| Peso molecolare | 376 Da | 775 Da |
| Tasso di legame proteico | Circa 70-80% | Circa 98% |
| Principale oggetto di osservazione | Vasi retinici | Vasi coroideali |
| Lunghezza d’onda di eccitazione | 465–490 nm | circa 805 nm |
| Lunghezza d’onda di fluorescenza | 520–530 nm | circa 835 nm (vicino infrarosso) |
| Via di escrezione | Reni | Fegato |
L’ICG ha un tasso di legame proteico del 98%, quindi fuoriesce pochissimo dai vasi coroideali, rendendolo adatto per la valutazione del flusso sanguigno coroideale. Nella valutazione della vasculopatia coroideale polipoide (PCV), dell’angioma coroideale e della MNV di tipo 1, l’ICGA integra la FA.
L’OCTA è un esame non invasivo che analizza le informazioni di fase dell’OCT per visualizzare il movimento dei globuli rossi. Non utilizza mezzo di contrasto e consente di separare e visualizzare i plessi vascolari retinici in tre strati a livello capillare 3). È stata dimostrata la sua utilità come alternativa alla FA nella valutazione dei vasi retinici durante la gravidanza 2).
| Parametro | FA | OCTA |
|---|---|---|
| Mezzo di contrasto | Necessario | Non necessario |
| Invasività | Puntura venosa, possibili effetti collaterali | Non invasivo |
| Informazioni dinamiche | Valutazione possibile di perdite e ritardi di riempimento | Non valutabile (solo struttura) |
| Risoluzione in profondità | Solo immagine 2D | Analisi stratificata possibile |
| Campo di imaging | Grandangolare (fino a 200°) | Limitato (3–12 mm) |
| Valutazione periferica | Facile | Difficile |
Poiché l’OCTA non è in grado di rilevare la fuoriuscita di fluoresceina dai vasi, la FA rimane indispensabile per valutare l’attività dell’edema maculare, determinare l’attività della CNV (presenza di perdita) e valutare l’infiammazione della parete vascolare nella vasculite retinica. L’uso complementare di entrambe le tecniche consente una valutazione più precisa del fondo oculare.
L’angolo di campo osservabile e le caratteristiche variano a seconda del dispositivo di imaging utilizzato.
| Dispositivo | Angolo di campo | Caratteristiche principali |
|---|---|---|
| Camera del fondo oculare | 55° | Standard e ampiamente diffuso |
| SLO/HRA | 30–102° | Alto contrasto e confocale |
| Optos | 200° | Imaging ultra-grandangolare e periferico in un’unica acquisizione |
Il dispositivo di imaging ultra-grandangolare (Optos) cattura la periferia in una singola acquisizione, utile per la valutazione delle lesioni periferiche nella retinopatia diabetica e nelle malattie degenerative della retina.
Nell’edema maculare cistoide post-necrosi retinica acuta, è stato suggerito che il pattern di leakage a petali alla FA possa essere un biomarcatore predittivo della risposta al trattamento 1). La ricerca è in corso per quantificare le informazioni dinamiche della FA e utilizzarle per prevedere l’efficacia della terapia anti-VEGF e della terapia fotodinamica.
L’introduzione del RetCam3 ha reso possibile eseguire la FA nei bambini. Si prevede la sua applicazione per la valutazione vascolare nella retinopatia del prematuro e nelle malattie retiniche pediatriche.
La FA ultra-grandangolare a 200° con Optos ha ridotto significativamente il tempo di imaging delle lesioni periferiche. La sua utilità è stata dimostrata nella valutazione delle aree di non perfusione capillare periferica nella retinopatia diabetica e nella valutazione estesa delle malattie vascolari retiniche congenite (come la FEVR).
L’OCTA è non invasiva e può visualizzare in dettaglio la struttura dei capillari, ma non è in grado di rilevare la fuoriuscita di fluoresceina al di fuori dei vasi. La FA è necessaria per valutare l’attività dell’edema maculare e confermare la perdita di CNV. Le due tecniche sono complementari nelle informazioni 3).