نور تحریک
نور آبی با طول موج ۴۶۵ تا ۴۹۰ نانومتر تابانده میشود.
در SLO از لیزر ۴۸۸ نانومتر استفاده میشود.
فیلتر تحریک طول موجهای غیرضروری را قطع میکند.

آنژیوگرافی فلورسین (FA) روشی است که در آن فلورسین سدیم به عنوان رنگ فلورسنت به صورت داخل وریدی تزریق شده و با دوربین فوندوس مجهز به فیلتر مخصوص از فوندوس عکسبرداری میشود تا گردش خون شبکیه و مشیمیه به صورت پویا تصویربرداری شود. این روش در ارزیابی دینامیک گردش خون شبکیه و وضعیت سد خونی-شبکیه برتری دارد و به طور گسترده برای تشخیص و تعیین استراتژی درمانی بیماریهای فوندوس استفاده میشود. علاوه بر ضایعات عروق شبکیه، در افتراق یووئیت، تومورهای مشیمیه و بیماریهای دیسک بینایی نیز مفید است.
در سال 1961، هارولد آر. نووتنی و دیوید ال. آلويس برای اولین بار روش اصلی FA را گزارش کردند. پس از آن، از سال 1967، جان دونالد مکاینتایر گاس یافتههای سیستماتیک FA را در بیماریهای مختلف فوندوس منتشر کرد و کاربرد بالینی آن به سرعت گسترش یافت.
فلورسین سدیم هنگام تابش نور آبی برانگیخته (طول موج 465-490 نانومتر) فلورسانس زرد-سبز (520-530 نانومتر) ساطع میکند. در افتالموسکوپ لیزری اسکنینگ (SLO) از لیزر آبی 488 نانومتر استفاده میشود. فلورسین سدیم یک رنگ محلول در آب با وزن مولکولی 376 دالتون است و پس از تزریق وریدی، حدود 70-80٪ به پروتئین متصل میشود. حدود 20-30٪ باقیمانده به صورت آزاد فلورسانس میدهد. در شرایط طبیعی که سد خونی-شبکیه سالم است، حتی فرم آزاد نیز به خارج از عروق نشت نمیکند. هنگامی که سد شکسته شود، رنگ به خارج از عروق نشت کرده و به عنوان یافته هایپر فلورسنت مشخص مشاهده میشود.
سد خونی-شبکیه (BRB) از دو لایه تشکیل شده است. سد داخلی اتصالات محکم سلولهای اندوتلیال عروق شبکیه و سد خارجی اتصالات محکم سلولهای اپیتلیوم رنگدانهدار شبکیه (RPE) است. شکست BRB منجر به نشت فلورسین میشود که به عنوان شاخص تشخیصی بیماریهای مختلف شبکیه عمل میکند.
نور تحریک
نور آبی با طول موج ۴۶۵ تا ۴۹۰ نانومتر تابانده میشود.
در SLO از لیزر ۴۸۸ نانومتر استفاده میشود.
فیلتر تحریک طول موجهای غیرضروری را قطع میکند.
انتشار فلورسانس
فلورسانس زرد-سبز با طول موج نشر ۵۲۰ تا ۵۳۰ نانومتر منتشر میشود.
فرم آزاد (حدود ۲۰-۳۰٪) عامل اصلی فلورسانس است.
فرم متصل به پروتئین (حدود ۷۰-۸۰٪) به سختی فلورسانس منتشر میکند.
فیلتر مانع
فقط فلورسانس با طول موج بالای ۵۲۰ نانومتر عبور داده میشود.
نور تحریک مسدود شده و تصویر فلورسانس واضح میشود.
نشت خارج عروقی نشانه شکست سد خونی-شبکیه است.
اولین بار در سال ۱۹۶۱ توسط نووتنی و آلويس گزارش شد. پس از سال ۱۹۶۷، گاس کاربرد آن را در بیماریهای مختلف فوندوس سیستماتیک کرد و به عنوان یک روش استاندارد تشخیصی در سراسر جهان گسترش یافت.
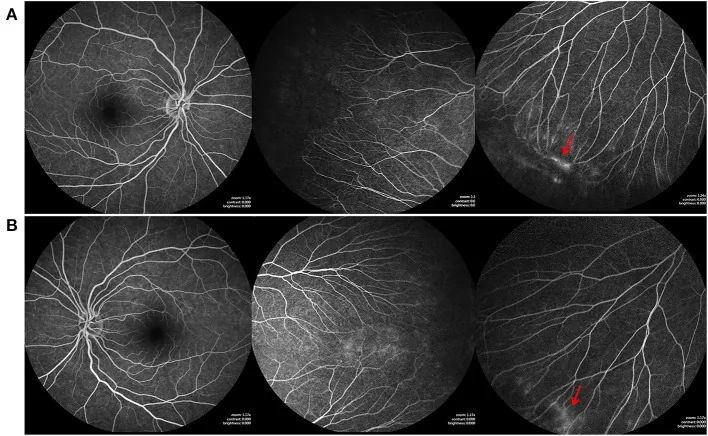
آنژیوگرافی فلورسین به طور گسترده برای تجسم عروق فوندوس استفاده میشود. در زیر بیماریهای اصلی اندیکاسیون آورده شده است.
در ادم ماکولا پس از نکروز حاد شبکیه (ARN)، FA الگوی نشت گلبرگی (petaloid) نشان میدهد که به تشخیص افتراقی ادم ماکولای کیستیک (CME) و تعیین اثربخشی درمان کمک میکند1).
در بارداری ممکن است انسداد عروق شبکیه رخ دهد، اما با توجه به عبور FA از جفت، OCTA به عنوان آزمایش جایگزین توصیه میشود2).
قبل از آزمایش، موارد زیر توضیح داده شده و رضایت کتبی اخذ میشود4).
بر اساس استانداردهای اجرای آنژیوگرافی عروق شبکیه انجمن چشمپزشکی ژاپن (نسخه اصلاحشده)، موارد زیر انجام میشود4).
بیمارانی که از داروهای مسدودکننده بتا یا آلفا استفاده میکنند، به دلیل افزایش خطر عوارض جانبی، باید از قبل شناسایی شوند4). تست واکنش پوستی کاربرد محدودی دارد و حتی در صورت منفی بودن، نمیتواند عوارض جانبی جدی را به طور کامل رد کند4).
۳ تا ۵ میلیلیتر از محلول فلورسئین ۱۰٪ را به سرعت به صورت وریدی تزریق کنید4). در کودکان، دوز ۰.۱ میلیگرم به ازای هر کیلوگرم وزن بدن توصیه میشود و در بیماران مبتلا به نارسایی کلیوی، دوز باید به نصف یا کمتر از مقدار معمول کاهش یابد4).
بلافاصله پس از تزریق، حدود ۱ دقیقه تصویربرداری پیوسته انجام میشود و سپس در دقایق ۵ و ۱۰ تصاویر فاز دیرهنگام گرفته میشود. با احتساب زمان گشاد کردن مردمک، کل فرآیند حدود ۱۵ تا ۲۰ دقیقه طول میکشد.
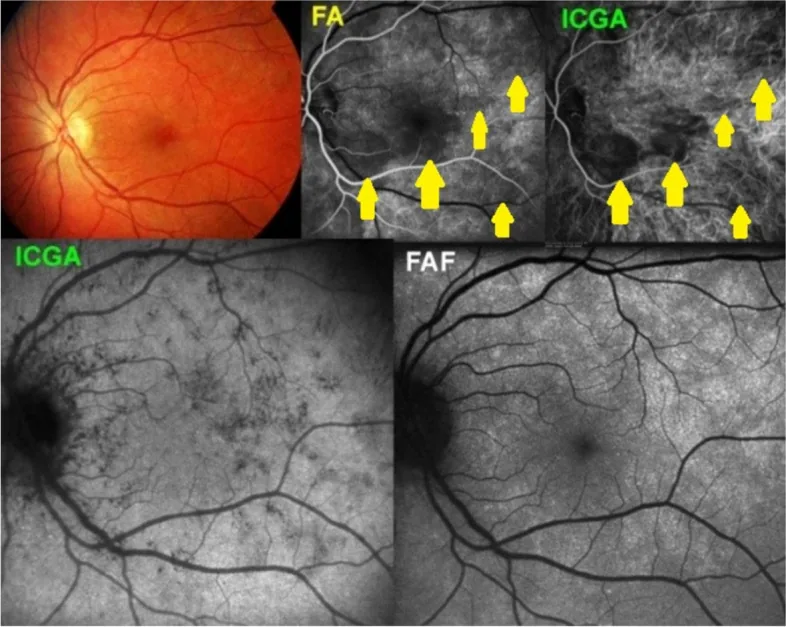
FA به صورت چندین فاز متوالی در طول زمان مشاهده میشود.
یافتههای FA به سه دسته کلی تقسیم میشوند: هیپوفلورسانس، هیپرفلورسانس و ناهنجاریهای عروقی.
انسداد فلورسانس (هیپوفلورسانس)
تعریف: خونریزی، رنگدانهگذاری، ترشحات و غیره فلورسانس زمینه را مسدود میکنند.
ویژگیها: مرزها واضح هستند و شکل در طول زمان تغییر نمیکند.
بیماریهای نماینده: خونریزی زیرشبکیه، اگزوداهای سخت، خال مشیمیه.
نقص پرشدگی (هیپوفلورسانس)
تعریف: به دلیل انسداد عروق، جریان رنگ فلورسنت وجود ندارد یا تأخیر دارد.
ویژگیها: نواحی بدون پرفیوژن مویرگی در طول کل دوره تیره باقی میمانند.
بیماریهای نماینده: انسداد شریان شبکیه، نواحی بدون عروق در رتینوپاتی دیابتی.
نشت فلورسنت (هیپرفلورسانس)
تعریف: به دلیل شکست سد خونی-شبکیه، رنگ به خارج از عروق نشت میکند.
ویژگیها: با گذشت زمان گسترش مییابد و مرزها نامشخص میشوند. الگوی گلبرگی (petaloid) برای ادم ماکولای کیستیک مشخص است 1).
بیماریهای نماینده: ادم ماکولا، CNV، واسکولیت شبکیه.
فلورسانس عبوری (هیپرفلورسانس)
تعریف: فلورسانس مشیمیه از طریق نقص RPE قابل مشاهده است (window defect).
ویژگی: شکل آن در طول زمان تغییر نمیکند، اما ممکن است در مراحل پایانی به طور خفیف رنگآمیزی شود.
بیماریهای نماینده: آتروفی جغرافیایی، همجوشی دروزن، سوراخ ماکولا، رگههای رنگی.
هیپوفلورسانس بر اساس علت به شرح زیر تقسیم میشود.
| نوع هیپوفلورسانس | علت/مکانیسم | بیماریهای نماینده |
|---|---|---|
| مسدود شدن فلورسانس | خونریزی، لکههای سفید، یا خال، فلورسانس زمینه را مسدود میکند | خونریزی زیر شبکیه، لکههای سفید سخت، خال مشیمیه |
| نقص پرشدگی: تنگی عروق شبکیه-مشیمیه | انسداد یا تنگی عروق بزرگ | انسداد شریان کاروتید داخلی، آرتریت تاکایاسو |
| نقص پرشدگی: انسداد عروق شبکیه | انسداد شریانی و وریدی | انسداد شریان شبکیه (CRAO/BRAO)، انسداد ورید شبکیه |
| نقص پرشدگی: انسداد مویرگی | اختلال گردش خون محیطی | رتینوپاتی دیابتی (NPA)، بیماری ایلز |
| نقص پرشدگی: اختلال گردش خون مشیمیه | نارسایی جریان خون مشیمیه | بیماری هارادا، APMPPE، کوروئیدوپاتی فشار خون بالا |
| آتروفی شبکیه و مشیمیه | از بین رفتن فلورسانس به دلیل آتروفی بافت | دیستروفی ماکولا، رتینیت پیگمانتوزا، AMD آتروفیک، نزدیکبینی پاتولوژیک |
| هیپوفلورسانس دیسک بینایی | ایسکمی یا نفوذ بافت عصب بینایی | نوروپاتی ایسکمیک بینایی، ملانوسیتوما |
هیپرفلورسانس بر اساس علت به شرح زیر طبقهبندی میشود:
ناهنجاریهای مورفولوژیک عروق به شرح زیر مشاهده میشود:
ارزیابی عروق مشیمیه به دلیل پوشیده شدن توسط اپیتلیوم رنگدانه شبکیه (RPE) دشوار است. برای ارزیابی MNV نوع 1 (نئوواسکولاریزاسیون مشیمیه) با نشت فلورسین، آنژیوگرافی با ایندوسیانین گرین (ICGA) به عنوان مکمل استفاده میشود.
میکروآنوریسم، ناحیه بدون پرفیوژن مویرگی (NPA) و نئوواسکولاریزاسیون یافتههای اصلی هستند. FA الگوی نشت ادم ماکولا (کانونی/منتشر/کیستی) را تشخیص داده و مبنای تعیین محل لیزر درمانی است 3). در فاز دیررس، نشت قابل توجه از نئوواسکولاریزاسیون مشاهده میشود. در FA با زاویه فوقعریض، دقت ارزیابی NPA محیطی افزایش مییابد.
FA برای ارزیابی فعالیت CNV ضروری است. CNV کلاسیک (نوع 2) از مراحل اولیه هیپرفلورسانس با مرز مشخص نشان میدهد و در فاز دیررس نشت میکند. CNV مخفی (نوع 1) در زیر RPE قرار دارد و در فاز دیررس به صورت هیپرفلورسانس خالخالی یا جداشدگی اپیتلیوم رنگدانه فیبروواسکولار (fibrovascular PED) ظاهر میشود. آتروفی جغرافیایی به صورت نقص پنجره (window defect) در طول زمان پیشرفت میکند.
FA برای ارزیابی تأخیر پرشدگی، اتساع و پیچخوردگی وریدها، ناحیه بدون پرفیوژن مویرگی و عروق جانبی استفاده میشود. NPA بزرگتر از 10 ناحیه دیسک بینایی به عنوان نوع ایسکمیک در نظر گرفته شده و نشانگر خطر گلوکوم نئوواسکولار است. همچنین برای درک الگوی نشت ادم ماکولا مهم است.
نقاط نشت مشخصه به صورت لکهجوهر (inkblot) یا دودکش (smokestack) در سطح RPE مشاهده میشود. نقاط نشت متعدد نشاندهنده CSC مزمن است. FA و ICGA برای تعیین محدوده درمان فتودینامیک (PDT) با هم استفاده میشوند.
در بیماری هارادا، هیپرفلورسانس نقطهای ناشی از نشت مشیمیهای متعدد و تجمع رنگ در محل جداشدگی سروز شبکیه دیده میشود. در بیماری بهجت، رنگپذیری دیواره عروق ناشی از واسکولیت شبکیه و NPA مشاهده میگردد. در بیماری ایلز، NPA محیطی و عروق جدید مشخصه هستند.
دادههای استاندارد آنژیوگرافی فوندوس چشم انجمن چشمپزشکی ژاپن (نسخه تجدید نظر شده) در اینجا نشان داده شده است 4).
عوارض جانبی با فراوانی زیر بر اساس شدت بروز میکنند.
| شدت | فراوانی |
|---|---|
| تمام عوارض جانبی | 1.1 تا 11.2% |
| خفیف | 1.4 تا 8.1% |
| متوسط | 0.2 تا 1.5% |
| شدید | 0.005 تا 0.48% |
| مرگ | 0.0005 تا 0.002٪ |
خفیف (اغلب خودبهخود بهبود مییابد)
متوسط
شدید (بسیار نادر)
تشخیص آنافیلاکسی در صورت وجود هر یک از سه معیار زیر است4).
فلودیاگرام مدیریت آنافیلاکسی:
حتی پس از درمان موفق، احتمال آنافیلاکسی دو فازی (عود علائم در عرض 6-8 ساعت پس از ناپدید شدن علائم) وجود دارد، بنابراین حداقل 8 ساعت پایش لازم است و بستری (24 ساعت) توصیه میشود4).
تشخیص افتراقی از رفلکس واگ: رفلکس واگ با برادیکاردی، افت فشار خون، رنگپریدگی و عرق سرد همراه است، اما با عدم وجود یافتههای پوستی (کهیر، قرمزی) از آنافیلاکسی قابل افتراق است. برای رفلکس واگ، حفظ وضعیت خوابیده، بالا بردن پاها و مایعات درمانی مؤثر است4).
این یک واکنش طبیعی به دلیل دفع فلورسئین از کلیهها است و جای نگرانی ندارد. زردی پوست طی ۲ تا ۳ ساعت و زردی ادرار تا روز بعد به طور خودبهخود برطرف میشود.
فلورسئین از جفت عبور کرده و تا ۷۲ ساعت در شیر مادر قابل تشخیص است، بنابراین انجام آن در زنان باردار و شیرده به طور کلی توصیه نمیشود2)3). در صورت نیاز به اطلاعات عروقی شبکیه، آنژیوگرافی OCT غیرتهاجمی (OCTA) به عنوان جایگزین توصیه میشود2).
فلورسئین سدیم یک رنگ زرد-قرمز محلول در آب با وزن مولکولی 376 دالتون است. هنگامی که با طول موج تحریک 465-490 نانومتر (488 نانومتر در SLO) تابش شود، فلورسانس زرد-سبز در 520-530 نانومتر منتشر میکند. پس از تزریق وریدی، حدود 70-80٪ به پروتئینهای پلاسما (عمدتاً آلبومین) متصل میشود و حدود 20-30٪ به صورت آزاد فلورسانس میدهد. از طریق کلیه دفع میشود (در 1-2 روز از بین میرود) و متابولیسم کبدی کمی دارد.
آنژیوگرافی با ایندوسیانین گرین (ICG) به صورت مکمل با FA استفاده میشود. ویژگیهای هر دو در زیر آورده شده است.
| ویژگی | FA | آنژیوگرافی ICG |
|---|---|---|
| وزن مولکولی | 376 دالتون | 775 دالتون |
| نرخ اتصال به پروتئین | حدود 70-80٪ | حدود 98٪ |
| هدف اصلی مشاهده | عروق شبکیه | عروق مشیمیه |
| طول موج تحریک | 465-490 نانومتر | حدود 805 نانومتر |
| طول موج فلورسانس | 520-530 نانومتر | حدود 835 نانومتر (نزدیک مادون قرمز) |
| مسیر دفع | کلیه | کبد |
ICG به دلیل نرخ بالای اتصال به پروتئین (98%) به ندرت از عروق مشیمیه نشت میکند و برای ارزیابی جریان خون مشیمیه مناسب است. در ارزیابی واسکولوپاتی پولیپوئیدال کوروئیدال (PCV)، همانژیوم مشیمیه و MNV نوع 1، ICGA مکمل FA است.
OCTA یک آزمایش غیرتهاجمی است که اطلاعات فاز OCT را تحلیل کرده و حرکت گلبولهای قرمز را تجسم میکند. بدون استفاده از ماده حاجب، میتواند شبکههای عروقی شبکیه را در سطح مویرگی به سه لایه جداگانه نمایش دهد3). در ارزیابی عروق شبکیه در دوران بارداری، به عنوان جایگزینی برای FA مفید نشان داده شده است2).
| ویژگی | FA | OCTA |
|---|---|---|
| ماده حاجب | نیاز است | نیاز نیست |
| تهاجمی بودن | وریدپونکسیون و عوارض جانبی دارد | غیرتهاجمی |
| اطلاعات دینامیک | قابل ارزیابی نشت و تأخیر پرشدگی | قابل ارزیابی نیست (فقط ساختاری) |
| تفکیک عمقی | فقط تصویر دوبعدی | تحلیل لایهای امکانپذیر است |
| محدوده تصویربرداری | زاویه باز (تا ۲۰۰ درجه) | محدود (۳ تا ۱۲ میلیمتر) |
| ارزیابی محیطی | آسان | دشوار |
از آنجایی که OCTA نمیتواند نشت فلورسین به خارج از عروق را تشخیص دهد، FA همچنان برای ارزیابی فعالیت ادم ماکولا، تعیین فعالیت CNV (وجود یا عدم وجود نشت) و ارزیابی التهاب دیواره عروق در واسکولیت شبکیه ضروری است. استفاده مکمل از هر دو امکان ارزیابی دقیقتر فوندوس را فراهم میکند.
زاویه دید قابل مشاهده و ویژگیها بسته به دستگاه تصویربرداری مورد استفاده متفاوت است.
| دستگاه | زاویه دید | ویژگیهای اصلی |
|---|---|---|
| دوربین فوندوس | ۵۵ درجه | استاندارد و پرکاربرد |
| SLO/HRA | ۳۰ تا ۱۰۲ درجه | کنتراست بالا و همکانون |
| Optos | 200° | تصویربرداری فوقعریض و یکپارچه از محیط |
دستگاه تصویربرداری فوقعریض (Optos) میتواند در یک بار عکسبرداری، نواحی محیطی را نیز ثبت کند و برای ارزیابی ضایعات محیطی در رتینوپاتی دیابتی و بیماریهای دژنراتیو شبکیه مفید است.
در ادم ماکولار کیستیک پس از نکروز حاد شبکیه، الگوی نشت گلبرگی در FA میتواند بهعنوان یک نشانگر زیستی برای پیشبینی پاسخ به درمان عمل کند1). تحقیقات در حال انجام است تا اطلاعات دینامیک FA را کمیسازی کرده و برای پیشبینی اثر درمانهای ضد VEGF و فوتودینامیک تراپی استفاده شود.
با معرفی RetCam3، انجام FA در کودکان امکانپذیر شده است. این روش برای ارزیابی عروق در رتینوپاتی نوزادان نارس و بیماریهای شبکیه کودکان کاربرد دارد.
با استفاده از Optos و FA فوقعریض 200 درجه، زمان تصویربرداری از ضایعات محیطی بهطور قابل توجهی کاهش یافته است. این روش برای ارزیابی نواحی غیرپرفیوژن مویرگی محیطی در رتینوپاتی دیابتی و ارزیابی گسترده بیماریهای عروقی مادرزادی شبکیه (مانند FEVR) مفید است.
OCTA غیرتهاجمی است و میتواند ساختار مویرگها را با جزئیات نشان دهد، اما نمیتواند نشت فلورسین به خارج از عروق را تشخیص دهد. برای ارزیابی فعالیت ادم ماکولا و تأیید نشت در CNV، آنژیوگرافی فلورسین (FA) ضروری است و این دو روش اطلاعات مکمل یکدیگر را فراهم میکنند 3).