Luz de excitación
Se irradia luz azul de longitud de onda 465–490 nm.
El SLO utiliza un láser de 488 nm.
Un filtro de excitación elimina las longitudes de onda no deseadas.

La angiografía fluoresceínica (FA) es una prueba en la que se administra fluoresceína sódica, un colorante fluorescente, por vía intravenosa, y se fotografía el fondo de ojo con una cámara de fondo de ojo equipada con filtros especiales para obtener imágenes dinámicas de la circulación sanguínea de la retina y la coroides. Es excelente para evaluar la dinámica de la circulación retiniana y el estado de la barrera hematorretiniana, y se utiliza ampliamente para el diagnóstico y la planificación del tratamiento de enfermedades del fondo de ojo. Es útil no solo para enfermedades vasculares retinianas, sino también para diferenciar uveítis, tumores coroideos y enfermedades del disco óptico.
En 1961, Harold R. Novotny y David L. Alvis informaron por primera vez del método original de la FA. Posteriormente, a partir de 1967, John Donald McIntyre Gass publicó hallazgos sistemáticos de FA en diversas enfermedades del fondo de ojo, lo que condujo a una rápida expansión de la aplicación clínica.
La fluoresceína sódica emite fluorescencia amarillo-verdosa (520–530 nm) cuando se irradia con luz de excitación azul (longitud de onda 465–490 nm). Los oftalmoscopios de barrido láser (SLO) utilizan un láser azul de 488 nm. La fluoresceína sódica es un colorante hidrosoluble con un peso molecular de 376 Da, y su tasa de unión a proteínas después de la administración intravenosa es de aproximadamente el 70–80%. El 20–30% restante está en forma libre y emite fluorescencia. En condiciones normales de la barrera hematorretiniana, incluso la forma libre no se filtra fuera de los vasos. Cuando la barrera se rompe, el colorante se filtra fuera de los vasos y se observa como hallazgos hiperfluorescentes característicos.
La barrera hematorretiniana (BRB) consta de dos capas. La barrera interna son las uniones estrechas de las células endoteliales vasculares de la retina, y la barrera externa son las uniones estrechas de las células del epitelio pigmentario de la retina (RPE). Cuando la BRB se rompe, se produce fuga de fluoresceína, que sirve como indicador diagnóstico de diversas enfermedades retinianas.
Luz de excitación
Se irradia luz azul de longitud de onda 465–490 nm.
El SLO utiliza un láser de 488 nm.
Un filtro de excitación elimina las longitudes de onda no deseadas.
Emisión de fluorescencia
Emite fluorescencia amarillo-verdosa con una longitud de onda de emisión de 520–530 nm.
La forma libre (aproximadamente 20–30%) es la principal fuente de fluorescencia.
La forma unida a proteínas (aproximadamente 70–80%) tiene menos probabilidad de fluorescer.
Filtro de barrera
Solo transmite fluorescencia por encima de 520 nm.
Bloquea la luz de excitación para nitidez de la imagen de fluorescencia.
La extravasación es evidencia de ruptura de la barrera.
Fue reportada por primera vez por Novotny y Alvis en 1961. Después de 1967, Gass sistematizó su aplicación a diversas enfermedades del fondo de ojo, convirtiéndose en un método de examen estándar para el diagnóstico del fondo de ojo y difundiéndose en todo el mundo.
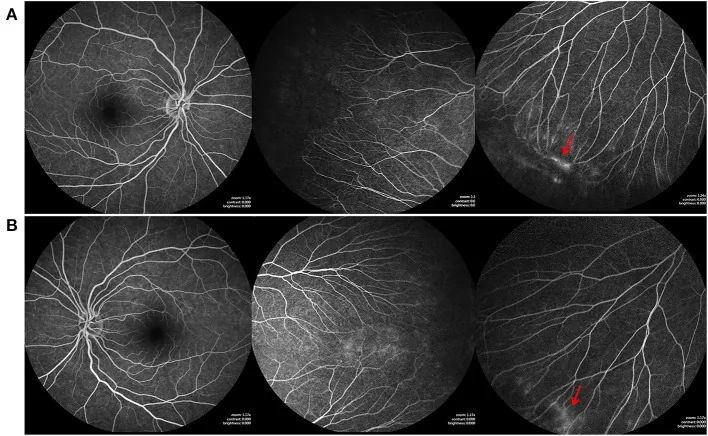
La FA se aplica ampliamente para la visualización del sistema vascular del fondo de ojo. A continuación se presentan las principales indicaciones.
En el edema macular posterior a la necrosis retiniana aguda (ARN), la FA muestra un patrón de fuga petaloide, que se ha informado que ayuda en el diagnóstico diferencial del edema macular quístico (CME) y en la evaluación de la eficacia del tratamiento1).
Durante el embarazo puede ocurrir oclusión vascular retiniana, pero desde la perspectiva de la transferencia placentaria de FA, se recomienda la OCTA como examen alternativo2).
Antes del examen, explique lo siguiente y obtenga el consentimiento por escrito4).
De acuerdo con los Estándares de Implementación de Angiografía de Fondo de Ojo de la Sociedad Japonesa de Oftalmología (Edición Revisada), se realiza lo siguiente4).
Los pacientes que toman betabloqueantes o alfabloqueantes tienen un mayor riesgo de efectos secundarios, por lo que debe identificarse de antemano 4). La prueba de reacción cutánea tiene una utilidad limitada, y un resultado negativo no puede descartar por completo los efectos secundarios graves 4).
Inyecte rápidamente por vía intravenosa 3-5 mL de solución de fluoresceína al 10% 4). En niños, se utiliza una dosis de 0,1 mg/kg como referencia, y en pacientes con insuficiencia renal, la dosis debe ser la mitad o menos de la cantidad habitual 4).
Inmediatamente después de la inyección, se realiza una captura continua durante aproximadamente 1 minuto, seguida de imágenes de fase tardía a los 5 y 10 minutos. Incluyendo el tiempo de dilatación pupilar, todo el procedimiento toma alrededor de 15 a 20 minutos.
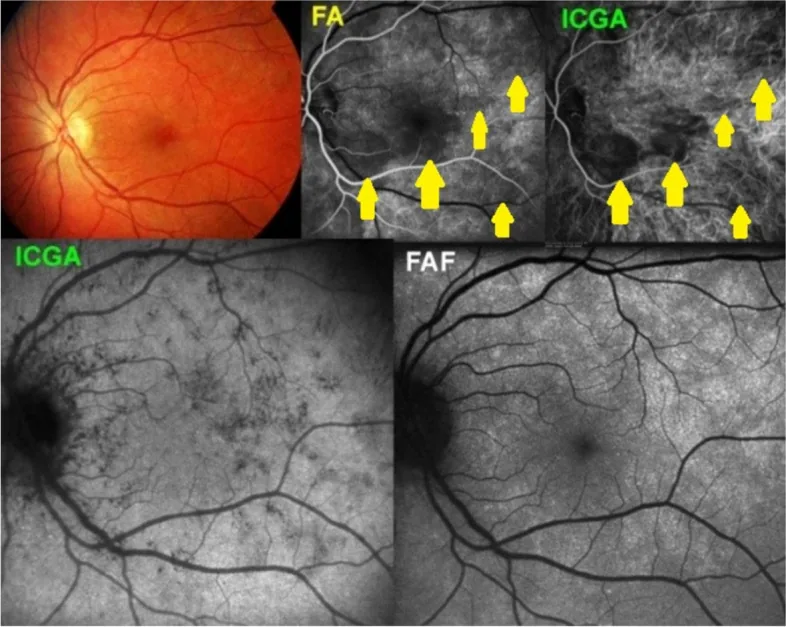
La FA se observa como múltiples fases a lo largo del tiempo.
Los hallazgos de la AF se clasifican en tres categorías: hipofluorescencia, hiperfluorescencia y anomalías morfológicas vasculares.
Bloqueo de fluorescencia (hipofluorescencia)
Definición: Hemorragia, pigmentación, exudados, etc., bloquean la fluorescencia de fondo.
Características: Bordes bien definidos, sin cambios de forma con el tiempo.
Enfermedades representativas: Hemorragia subretiniana, exudados duros, nevus coroideo.
Defecto de llenado (hipofluorescencia)
Definición: Ausencia o retraso en la entrada del colorante fluorescente debido a oclusión vascular.
Características: Las áreas de no perfusión capilar permanecen oscuras durante todo el curso.
Enfermedades representativas: Oclusión de la arteria retiniana, áreas avasculares en la retinopatía diabética.
Fuga de fluoresceína (hiperfluorescencia)
Definición: Ruptura de la barrera hematorretiniana que provoca la fuga del colorante fuera de los vasos.
Características: Se agranda con el tiempo, los bordes se vuelven indistintos. Un patrón petaloide es característico del edema macular quístico 1).
Enfermedades representativas: Edema macular, CNV, vasculitis retiniana.
Fluorescencia transmitida (hiperfluorescencia)
Definición: Fluorescencia coroidea visible a través de un defecto del EPR (defecto en ventana).
Características: No cambia de forma con el tiempo, pero puede mostrar una tinción tenue en la fase tardía.
Enfermedades representativas: Atrofia geográfica, drusas confluentes, agujero macular, estrías angioides.
La hipofluorescencia se subdivide según la causa de la siguiente manera.
| Tipo de hipofluorescencia | Causa/Mecanismo | Enfermedades representativas |
|---|---|---|
| Bloqueo de la fluorescencia | Hemorragia, exudado o nevus bloquean la fluorescencia de fondo | Hemorragia subretiniana, exudados duros, nevus coroideo |
| Defecto de llenado: Estenosis vascular retino-coroidal | Oclusión o estenosis de grandes vasos | Oclusión de la arteria carótida interna, arteritis de Takayasu |
| Defecto de llenado: oclusión vascular retiniana | Oclusión arterial/venosa | Oclusión de la arteria retiniana (CRAO/BRAO), oclusión de la vena retiniana |
| Defecto de llenado: oclusión capilar | Trastorno circulatorio periférico | Retinopatía diabética (NPDR), enfermedad de Eales |
| Defecto de llenado: trastorno circulatorio coroideo | Insuficiencia del flujo sanguíneo coroideo | Enfermedad de Harada, APMPPE, coroidopatía hipertensiva |
| Atrofia coriorretiniana | Pérdida de fluorescencia por atrofia tisular | Distrofia macular, retinitis pigmentosa, AMD atrófica, miopía patológica |
| Hipofluorescencia del disco óptico | Isquemia/infiltración del tejido del nervio óptico | Neuropatía óptica isquémica, melanocitoma |
La hiperfluorescencia se subdivide según la causa de la siguiente manera.
Se observan las siguientes anomalías morfológicas vasculares.
Los vasos coroideos son difíciles de evaluar porque están ocultos por el EPR. La angiografía con ICG (ICGA) se utiliza de forma complementaria para evaluar la MNV tipo 1 (neovascularización coroidea) con fuga de fluoresceína.
Microaneurismas, áreas de no perfusión (ANP) y neovascularización son los hallazgos principales. La AF ayuda a determinar el patrón de fuga del edema macular (focal/difuso/quístico) y proporciona la base para decidir los sitios de fotocoagulación con láser 3). En la fase tardía se observa fuga marcada de la neovascularización. La AF de campo ultraancho mejora la precisión de la evaluación de la ANP periférica.
La AF es esencial para evaluar la actividad de la CNV. La CNV clásica (tipo 2) muestra hiperfluorescencia bien definida en la fase temprana y fuga en la fase tardía. La CNV oculta (tipo 1) se localiza debajo del EPR y aparece como hiperfluorescencia punteada o DVP fibrovascular en la fase tardía. La atrofia geográfica aparece como un defecto de ventana durante todo el angiograma.
La AF se utiliza para evaluar el llenado retardado, la dilatación y tortuosidad venosa, las áreas de no perfusión capilar y la circulación colateral. Un ANP de 10 áreas de disco o más se considera isquémico e indica riesgo de glaucoma neovascular. También es importante para comprender el patrón de fuga del edema macular.
Se observan puntos de fuga característicos en forma de mancha de tinta o chimenea a nivel del EPR. Múltiples puntos de fuga sugieren CSC crónica. La AF y la ICGA se utilizan juntas para determinar el área de tratamiento para la terapia fotodinámica (TFD).
En la enfermedad de Vogt-Koyanagi-Harada, se observan hiperfluorescencias puntiformes debidas a fugas coroideas multifocales y acumulación de colorante en áreas de desprendimiento seroso de retina. En la enfermedad de Behçet, se observan tinción de la pared vascular por vasculitis retiniana y áreas de no perfusión (NPA). En la enfermedad de Eales, son características las NPA periféricas y la neovascularización.
Se muestran los datos de los Estándares de Implementación de Angiografía de Fondo de Ojo de la Sociedad Japonesa de Oftalmología (Edición Revisada) 4).
Los efectos secundarios ocurren con las siguientes frecuencias según la gravedad.
| Gravedad | Incidencia |
|---|---|
| Todos los efectos secundarios | 1.1–11.2% |
| Leve | 1.4–8.1% |
| Moderado | 0.2–1.5% |
| Grave | 0.005–0.48% |
| Muerte | 0.0005–0.002% |
Leve (a menudo se resuelve espontáneamente)
Moderado
Grave (extremadamente raro)
El diagnóstico de anafilaxia se realiza cuando se cumple cualquiera de los siguientes tres criterios4).
Algoritmo de manejo de la anafilaxia:
Incluso después del tratamiento exitoso, existe riesgo de anafilaxia bifásica (recurrencia dentro de las 6–8 horas posteriores a la resolución de los síntomas), por lo que es necesaria una observación de al menos 8 horas y se recomienda la hospitalización durante 24 horas4).
Diferenciación del reflejo vasovagal: El reflejo vasovagal se presenta con bradicardia, hipotensión, palidez y sudor frío, pero se puede diferenciar de la anafilaxia por la ausencia de hallazgos cutáneos (urticaria, rubor). Para el reflejo vasovagal, son efectivos la posición supina, la elevación de las piernas y la administración de líquidos4).
Esta es una reacción normal debida a la excreción de fluoresceína por los riñones, y no hay necesidad de preocuparse. La coloración amarillenta de la piel desaparece en 2 a 3 horas, y la orina amarilla desaparece al día siguiente.
La fluoresceína atraviesa la placenta y se detecta en la leche materna durante 72 horas, por lo que generalmente se evita su administración en mujeres embarazadas y en período de lactancia2)3). Si se necesita información vascular de la retina, se recomienda la angiografía por OCT (OCTA) no invasiva como alternativa2).
El fluoresceínato sódico es un colorante hidrosoluble de color amarillo-rojizo con un peso molecular de 376 Da. Cuando se excita a longitudes de onda de 465–490 nm (488 nm con SLO), emite fluorescencia amarillo-verdosa a 520–530 nm. Tras la administración intravenosa, aproximadamente el 70–80% se une a proteínas plasmáticas (principalmente albúmina), y alrededor del 20–30% fluoresce en forma libre. Se excreta por los riñones (se elimina en 1–2 días), con un metabolismo hepático mínimo.
La angiografía con verde de indocianina (ICG) se utiliza de forma complementaria con la AF. Sus características se muestran a continuación.
| Parámetro | AF | Angiografía con ICG |
|---|---|---|
| Peso molecular | 376 Da | 775 Da |
| Tasa de unión a proteínas | Aproximadamente 70–80% | Aproximadamente 98% |
| Principal objetivo de observación | Vasos retinianos | Vasos coroideos |
| Longitud de excitación | 465–490 nm | Aproximadamente 805 nm |
| Longitud de fluorescencia | 520–530 nm | Aproximadamente 835 nm (infrarrojo cercano) |
| Vía de excreción | Riñón | Hígado |
La ICG tiene una alta tasa de unión a proteínas del 98%, por lo que apenas se filtra fuera de los vasos coroideos, siendo adecuada para evaluar el flujo sanguíneo coroideo. La ICGA complementa la FA en la evaluación de la vasculopatía coroidea polipoidea (PCV), el hemangioma coroideo y la MNV tipo 1.
La OCTA es una prueba no invasiva que analiza la información de fase de la OCT para visualizar el movimiento de los glóbulos rojos. No requiere contraste y puede separar y representar el plexo vascular retiniano en tres capas a nivel capilar 3). Se ha demostrado su utilidad como alternativa a la FA en la evaluación de los vasos retinianos durante el embarazo 2).
| Ítem | FA | OCTA |
|---|---|---|
| Contraste | Necesario | No necesario |
| Invasividad | Punción venosa, posibles efectos secundarios | No invasivo |
| Información dinámica | Puede evaluar fuga y retraso de llenado | No se puede evaluar (solo estructura) |
| Resolución de profundidad | Solo imagen bidimensional | Análisis por capas posible |
| Rango de imagen | Gran angular (hasta 200°) | Limitado (3–12 mm) |
| Evaluación periférica | Fácil | Difícil |
La OCTA no puede detectar la fuga de fluoresceína fuera de los vasos, por lo que la AF sigue siendo esencial para evaluar la actividad del edema macular, determinar la actividad de la CNV (presencia de fuga) y evaluar la inflamación de la pared vascular en la vasculitis retiniana. El uso complementario de ambas permite una evaluación más precisa del fondo de ojo.
El campo de visión observable y las características difieren según el dispositivo de imagen utilizado.
| Dispositivo | Campo de visión | Características principales |
|---|---|---|
| Cámara de fondo de ojo | 55° | Estándar, ampliamente utilizado |
| SLO/HRA | 30–102° | Alto contraste, confocal |
| Optos | 200° | Imagen única de campo ultraancho de la periferia |
El dispositivo de imagen de campo ultraancho (Optos) puede capturar la retina periférica en una sola toma, y es útil para evaluar lesiones periféricas en la retinopatía diabética y enfermedades degenerativas de la retina.
En el edema macular quístico después de la necrosis retiniana aguda, se ha sugerido que el patrón de fuga en pétalos en la AF puede servir como biomarcador predictivo de la respuesta al tratamiento 1). Se están realizando investigaciones para cuantificar la información dinámica de la AF y utilizarla para predecir la eficacia de la terapia anti-VEGF y la terapia fotodinámica.
La introducción del RetCam3 ha hecho posible realizar AF en niños. Se espera su aplicación para la evaluación vascular en la retinopatía del prematuro y enfermedades retinianas pediátricas.
Con la AF de campo ultraancho de 200° utilizando Optos, el tiempo de imagen para las lesiones periféricas se ha reducido significativamente. Se ha demostrado su utilidad para evaluar áreas de no perfusión capilar periférica en la retinopatía diabética y para la evaluación extensa de enfermedades vasculares retinianas congénitas (p. ej., FEVR).