Lumière d'excitation
Une lumière bleue d’une longueur d’onde de 465 à 490 nm est émise.
En SLO, un laser de 488 nm est utilisé.
Un filtre d’excitation élimine les longueurs d’onde indésirables.

L’angiographie à la fluorescéine (FA) est une technique d’imagerie dynamique de la circulation sanguine rétinienne et choroïdienne après injection intraveineuse de fluorescéine sodique, un colorant fluorescent, et prise de photographies du fond d’œil avec une caméra équipée de filtres spéciaux. Elle excelle dans l’évaluation de la dynamique circulatoire rétinienne et de l’état de la barrière hémato-rétinienne, et est largement utilisée pour le diagnostic et la décision thérapeutique des maladies du fond d’œil. Elle est utile non seulement pour les pathologies vasculaires rétiniennes, mais aussi pour le diagnostic différentiel des uvéites, des tumeurs choroïdiennes et des maladies de la papille optique.
En 1961, Harold R. Novotny et David L. Alvis ont rapporté la méthode originale de la FA. Par la suite, à partir de 1967, John Donald McIntyre Gass a publié des descriptions systématiques des signes FA dans diverses maladies du fond d’œil, ce qui a rapidement élargi son application clinique.
La fluorescéine sodique émet une fluorescence jaune-vert (520-530 nm) lorsqu’elle est exposée à une lumière d’excitation bleue (longueur d’onde 465-490 nm). En ophtalmoscopie laser à balayage (SLO), un laser bleu de 488 nm est utilisé. La fluorescéine sodique est un colorant hydrosoluble de poids moléculaire 376 Da ; après injection intraveineuse, environ 70 à 80 % se lient aux protéines. Les 20 à 30 % restants, sous forme libre, émettent la fluorescence. En présence d’une barrière hémato-rétinienne intacte, même la forme libre ne s’échappe pas des vaisseaux. En cas de rupture de la barrière, le colorant s’échappe des vaisseaux et est observé comme une hyperfluorescence caractéristique.
La barrière hémato-rétinienne (BHR) est constituée de deux couches : la barrière interne formée par les jonctions serrées des cellules endothéliales des vaisseaux rétiniens, et la barrière externe formée par les jonctions serrées des cellules de l’épithélium pigmentaire rétinien (EPR). La rupture de la BHR entraîne une fuite de fluorescéine, qui constitue un indicateur diagnostique de diverses maladies rétiniennes.
Lumière d'excitation
Une lumière bleue d’une longueur d’onde de 465 à 490 nm est émise.
En SLO, un laser de 488 nm est utilisé.
Un filtre d’excitation élimine les longueurs d’onde indésirables.
Émission de fluorescence
Une fluorescence jaune-vert d’une longueur d’onde d’émission de 520 à 530 nm est émise.
La forme libre (environ 20 à 30 %) est le principal contributeur à la fluorescence.
La forme liée aux protéines (environ 70 à 80 %) émet difficilement de la fluorescence.
Filtre barrière
Seule la fluorescence d’une longueur d’onde supérieure à 520 nm est transmise.
La lumière d’excitation est bloquée, rendant l’image fluorescente nette.
L’extravasation est une preuve de rupture de la barrière.
Elle a été rapportée pour la première fois en 1961 par Novotny et Alvis. À partir de 1967, Gass a systématisé son application à diverses maladies du fond d’œil, et elle s’est répandue dans le monde entier comme méthode d’examen standard pour le diagnostic du fond d’œil.
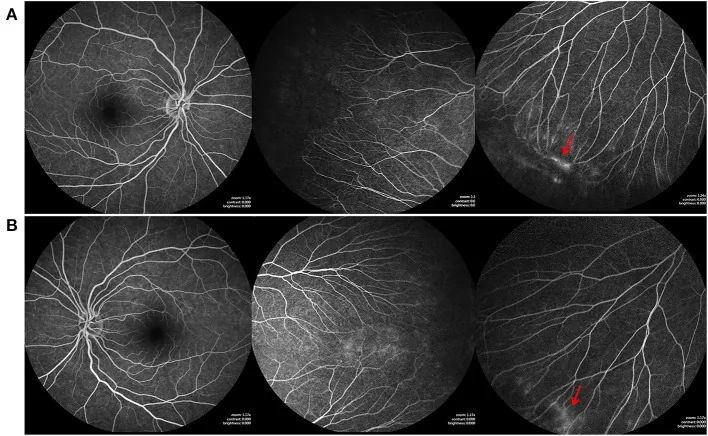
L’angiographie à la fluorescéine (FA) est largement utilisée pour visualiser le système vasculaire rétinien. Les principales indications sont énumérées ci-dessous.
Dans l’œdème maculaire survenant après une nécrose rétinienne aiguë (ARN), l’angiographie à la fluorescéine (FA) montre un motif de fuite pétaloïde, contribuant au diagnostic différentiel de l’œdème maculaire cystoïde (OMC) et à l’évaluation de l’efficacité du traitement1).
Pendant la grossesse, une occlusion vasculaire rétinienne peut survenir, mais du point de vue du passage placentaire de la FA, l’OCTA est recommandée comme examen alternatif2).
Avant l’examen, expliquer le contenu suivant et obtenir un consentement écrit4).
Conformément aux normes de réalisation de l’angiographie du fond d’œil (révisées) de la Société japonaise d’ophtalmologie, les éléments suivants sont mis en œuvre 4).
Les patients sous bêta-bloquants ou alpha-bloquants présentent un risque accru d’effets secondaires, il convient donc de le vérifier au préalable 4). Le test cutané a une utilité limitée ; même négatif, il ne peut totalement exclure des effets secondaires graves 4).
Injecter rapidement par voie intraveineuse 3 à 5 mL de solution de fluorescéine à 10 % 4). Chez l’enfant, la dose indicative est de 0,1 mg/kg ; chez les patients insuffisants rénaux, la dose doit être réduite à la moitié ou moins de la dose normale 4).
Immédiatement après l’injection, des clichés sont pris en continu pendant environ 1 minute, puis des clichés tardifs sont réalisés à 5 et 10 minutes. En incluant le temps de dilatation pupillaire, l’examen dure environ 15 à 20 minutes au total.
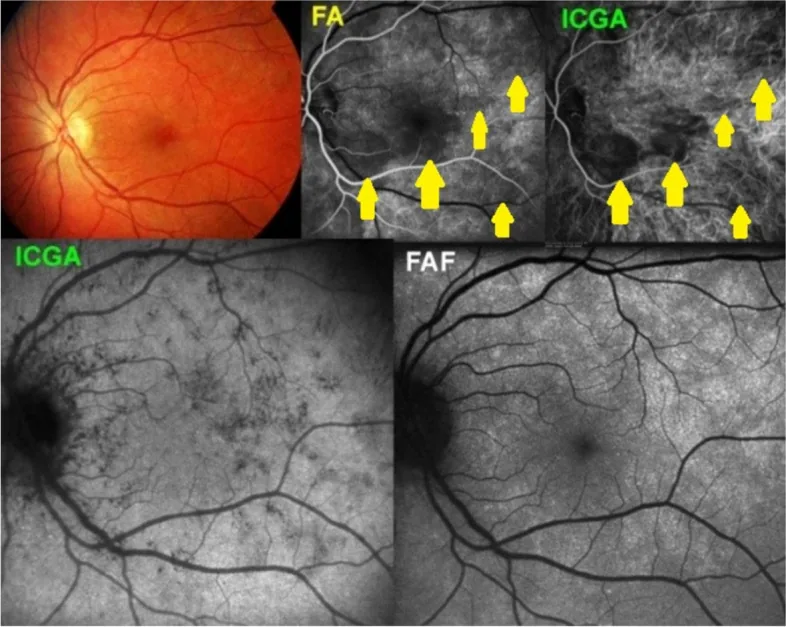
L’angiographie à la fluorescéine est observée en plusieurs phases chronologiques.
Les résultats de l’angiographie à la fluorescéine sont classés en trois catégories : hypofluorescence, hyperfluorescence et anomalies morphologiques vasculaires.
Blocage de la fluorescence (hypofluorescence)
Définition : l’hémorragie, la pigmentation, les exsudats, etc., masquent la fluorescence de fond.
Caractéristiques : limites nettes, pas de changement de forme au fil du temps.
Maladies représentatives : hémorragie sous-rétinienne, exsudats durs, naevus choroïdien.
Défaut de remplissage (hypofluorescence)
Définition : absence ou retard d’afflux du colorant fluorescent dû à une occlusion vasculaire.
Caractéristiques : les zones de non-perfusion capillaire restent sombres tout au long de l’examen.
Maladies représentatives : occlusion de l’artère rétinienne, zones avasculaires dans la rétinopathie diabétique.
Fuites de fluorescence (hyperfluorescence)
Définition : rupture de la barrière hémato-rétinienne entraînant une extravasation du colorant.
Caractéristiques : augmentation de taille au fil du temps, limites floues. Un motif pétaloïde est caractéristique de l’œdème maculaire cystoïde1).
Maladies représentatives : œdème maculaire, néovascularisation choroïdienne, vascularite rétinienne.
Fluorescence de transmission (hyperfluorescence)
Définition : La fluorescence choroïdienne est visible à travers une perte de l’EPR (window defect).
Caractéristiques : La forme ne change pas avec le temps, mais peut se colorer légèrement tardivement.
Maladies représentatives : Atrophie géographique, fusion de drusen, trou maculaire, stries angioïdes.
L’hypofluorescence est subdivisée selon la cause comme suit.
| Type d’hypofluorescence | Cause / Mécanisme | Maladies représentatives |
|---|---|---|
| Blocage de la fluorescence | Hémorragie, exsudat dur, naevus masquent la fluorescence de fond | Hémorragie sous-rétinienne, exsudat dur, naevus choroïdien |
| Défaut de remplissage : sténose vasculaire rétino-choroïdienne | Occlusion ou sténose des gros vaisseaux | Occlusion de l’artère carotide interne, artérite de Takayasu |
| Défaut de remplissage : occlusion vasculaire rétinienne | Occlusion artérielle et veineuse | Occlusion de l’artère rétinienne (CRAO/BRAO), occlusion de la veine rétinienne |
| Défaut de remplissage : occlusion capillaire | Trouble circulatoire périphérique | Rétinopathie diabétique (NPA), maladie d’Eales |
| Défaut de remplissage : trouble circulatoire choroïdien | Insuffisance du flux sanguin choroïdien | Maladie de Harada, APMPPE, choroïdopathie hypertensive |
| Atrophie chorio-rétinienne | Perte de fluorescence due à l’atrophie tissulaire | Dystrophie maculaire, rétinite pigmentaire, DMLA atrophique, myopie pathologique |
| Hypofluorescence papillaire | Ischémie/infiltration du tissu du nerf optique | Neuropathie optique ischémique, mélanocytome |
L’hyperfluorescence est subdivisée selon la cause comme suit.
Les anomalies morphologiques vasculaires suivantes sont observées.
Les vaisseaux choroïdiens sont difficiles à évaluer en raison de l’occlusion par l’EPR. L’angiographie au vert d’indocyanine (ICGA) est utilisée en complément pour évaluer la NVC de type 1 avec fuite de fluorescéine.
Les microanévrismes, les zones non perfusées (NPA) et la néovascularisation sont les principales observations. L’AF permet de distinguer les schémas de fuite de l’œdème maculaire (focal/diffus/kystoïde) et sert de base pour déterminer les sites d’irradiation laser 3). Dans les phases tardives, une fuite marquée de la néovascularisation est observée. L’AF ultra grand champ améliore la précision de l’évaluation des NPA périphériques.
Indispensable pour évaluer l’activité de la NVC. La NVC classique (type 2) montre une hyperfluorescence précoce bien délimitée et une fuite tardive. La NVC occulte (type 1) est située sous l’EPR et apparaît sous forme d’hyperfluorescence ponctuée tardive ou de décollement fibrovasculaire de l’EPR. L’atrophie géographique se manifeste par un effet de fenêtre.
Utilisée pour évaluer le retard de remplissage, la dilatation et la tortuosité veineuses, les zones de non-perfusion capillaire et les collatérales. Une NPA de plus de 10 disques optiques est considérée comme ischémique et constitue un indicateur de risque de glaucome néovasculaire. Important également pour comprendre le schéma de fuite de l’œdème maculaire.
On observe des points de fuite caractéristiques de type « inkblot » (tache d’encre) ou « smokestack » (cheminée) au niveau de l’EPR. De multiples points de fuite suggèrent une CRSC chronique. L’AF et l’ICGA sont utilisées conjointement pour déterminer la zone d’irradiation de la thérapie photodynamique (PDT).
Dans la maladie de Harada, on observe une hyperfluorescence ponctuée due à des fuites choroïdiennes multiples et une accumulation de colorant dans les zones de décollement séreux de la rétine. Dans la maladie de Behçet, on note une coloration des parois vasculaires due à une vascularite rétinienne et des zones de non-perfusion artérielle (NPA). Dans la maladie d’Eales, les caractéristiques sont des NPA périphériques et des néovaisseaux.
Les données de la norme de réalisation de l’angiographie du fond d’œil de la Société japonaise d’ophtalmologie (révision) sont présentées 4).
Les effets secondaires surviennent avec les fréquences suivantes selon la sévérité.
| Sévérité | Incidence |
|---|---|
| Tous effets secondaires | 1,1 à 11,2 % |
| Léger | 1,4 à 8,1 % |
| Modéré | 0,2 à 1,5 % |
| Sévère | 0,005 à 0,48 % |
| Décès | 0,0005 à 0,002 % |
Léger (souvent spontanément résolutif)
Modéré
Grave (extrêmement rare)
Le diagnostic d’anaphylaxie repose sur l’un des trois critères suivants4).
Algorithme de prise en charge de l’anaphylaxie :
Même après un traitement réussi, il existe un risque d’anaphylaxie biphasique (récidive dans les 6 à 8 heures suivant la disparition des symptômes) ; une surveillance d’au moins 8 heures est nécessaire, et une hospitalisation pour observation (24 heures) est recommandée4).
Diagnostic différentiel avec le réflexe vagal : Le réflexe vagal se manifeste par une bradycardie, une hypotension, une pâleur et des sueurs froides, mais ne s’accompagne pas de signes cutanés (urticaire, rougeur), ce qui permet de le distinguer de l’anaphylaxie. En cas de réflexe vagal, le maintien en position couchée, l’élévation des membres inférieurs et l’administration de liquides sont efficaces4).
Il s’agit d’une réaction normale due à l’excrétion rénale de la fluorescéine, il n’y a pas lieu de s’inquiéter. La coloration jaune de la peau disparaît en 2 à 3 heures, et celle des urines en un jour.
La fluorescéine traverse le placenta et est détectée dans le lait maternel pendant 72 heures, donc l’examen est en principe évité chez les femmes enceintes ou allaitantes2)3). Si des informations vasculaires rétiniennes sont nécessaires, l’angiographie OCT non invasive (OCTA) est recommandée comme alternative2).
La fluorescéine sodique est un colorant hydrosoluble de couleur jaune-rouge d’un poids moléculaire de 376 Da. Lorsqu’elle est excitée à une longueur d’onde de 465 à 490 nm (488 nm en SLO), elle émet une fluorescence jaune-vert à 520-530 nm. Après administration intraveineuse, environ 70 à 80 % se lient aux protéines plasmatiques (principalement l’albumine), et environ 20 à 30 % sont sous forme libre et émettent une fluorescence. Elle est excrétée par les reins (disparaît en 1 à 2 jours) et son métabolisme hépatique est faible.
L’angiographie au vert d’indocyanine (ICG) est utilisée en complément de l’angiographie à la fluorescéine (FA). Leurs caractéristiques sont présentées ci-dessous.
| Paramètre | FA | ICG angiographie |
|---|---|---|
| Poids moléculaire | 376 Da | 775 Da |
| Taux de liaison aux protéines | Environ 70 à 80 % | Environ 98 % |
| Principal objet d’observation | Vaisseaux rétiniens | Vaisseaux choroïdiens |
| Longueur d’onde d’excitation | 465–490 nm | Environ 805 nm |
| Longueur d’onde de fluorescence | 520–530 nm | Environ 835 nm (proche infrarouge) |
| Voie d’excrétion | Reins | Foie |
L’ICG a un taux de liaison aux protéines de 98 %, ce qui le fait peu fuir hors des vaisseaux choroïdiens, le rendant adapté à l’évaluation du flux sanguin choroïdien. L’ICGA complète l’FA dans l’évaluation de la polypose choroïdienne (PCV), de l’hémangiome choroïdien et de la MNV de type 1.
L’OCTA est un examen non invasif qui analyse les informations de phase de l’OCT pour visualiser le mouvement des globules rouges. Il ne nécessite pas de produit de contraste et permet de séparer et de visualiser les plexus vasculaires rétiniens en trois couches au niveau capillaire 3). Son utilité comme alternative à l’FA pour l’évaluation des vaisseaux rétiniens pendant la grossesse a été démontrée 2).
| Paramètre | FA | OCTA |
|---|---|---|
| Agent de contraste | Nécessaire | Non nécessaire |
| Invasivité | Piqûre veineuse, effets secondaires possibles | Non invasif |
| Informations dynamiques | Permet d’évaluer les fuites et les retards de remplissage | Non évaluable (structure uniquement) |
| Résolution en profondeur | Image 2D uniquement | Analyse par couches possible |
| Champ d’imagerie | Grand angle (jusqu’à 200°) | Limité (3 à 12 mm) |
| Évaluation périphérique | Facile | Difficile |
L’OCTA ne pouvant pas détecter la fuite de fluorescence hors des vaisseaux, l’angiographie à la fluorescéine (FA) reste indispensable pour évaluer l’activité de l’œdème maculaire, déterminer l’activité de la NVC (présence de fuite) et évaluer l’inflammation de la paroi vasculaire dans la vascularite rétinienne. L’utilisation complémentaire des deux techniques permet une évaluation plus précise du fond d’œil.
L’angle de vue et les caractéristiques observables diffèrent selon l’appareil d’imagerie utilisé.
| Appareil | Angle de vue | Principales caractéristiques |
|---|---|---|
| Caméra du fond d’œil | 55° | Standard et largement répandu |
| SLO/HRA | 30 à 102° | Haut contraste et confocal |
| Optos | 200° | Imagerie ultra grand angle et périphérique en une seule prise |
L’appareil de photographie ultra grand angle (Optos) permet de capturer la périphérie en une seule prise, utile pour l’évaluation des lésions périphériques dans la rétinopathie diabétique et les maladies dégénératives de la rétine.
Dans l’œdème maculaire cystoïde post-nécrose rétinienne aiguë, il a été suggéré que le schéma de fuite en pétales à l’angiographie à la fluorescéine (FA) pourrait être un biomarqueur prédictif de la réponse au traitement 1). Des recherches sont en cours pour quantifier les informations dynamiques de la FA et les utiliser pour prédire l’efficacité des traitements anti-VEGF et de la thérapie photodynamique.
L’introduction du RetCam3 a permis de réaliser des FA chez les enfants. Son application est attendue pour l’évaluation vasculaire de la rétinopathie du prématuré et des maladies rétiniennes pédiatriques.
La FA ultra grand angle à 200° utilisant l’Optos a considérablement réduit le temps d’imagerie des lésions périphériques. Son utilité a été démontrée pour l’évaluation des zones de non-perfusion capillaire périphérique dans la rétinopathie diabétique et pour l’évaluation étendue des maladies vasculaires rétiniennes congénitales (comme la FEVR).
L’OCTA est non invasive et permet de visualiser finement la structure des capillaires, mais elle ne peut pas détecter la fuite de fluorescence en dehors des vaisseaux. L’angiographie à la fluorescéine (FA) est nécessaire pour évaluer l’activité de l’œdème maculaire et confirmer la fuite de la néovascularisation choroïdienne (CNV). Les deux techniques sont complémentaires en termes d’informations 3).