Anregungslicht
Blaues Licht mit einer Wellenlänge von 465–490 nm wird eingestrahlt.
Im SLO wird ein Laser von 488 nm verwendet.
Ein Anregungsfilter schneidet unerwünschte Wellenlängen ab.

Die Fluoreszenzangiographie (FA) ist eine Untersuchungsmethode, bei der der fluoreszierende Farbstoff Natriumfluorescein intravenös verabreicht und der Augenhintergrund mit einer speziell gefilterten Funduskamera fotografiert wird, um die Blutzirkulation in Netzhaut und Aderhaut dynamisch darzustellen. Sie eignet sich hervorragend zur Beurteilung der retinalen Hämodynamik und des Zustands der Blut-Retina-Schranke und wird häufig für die Diagnose und Therapieplanung von Funduserkrankungen eingesetzt. Sie ist nicht nur bei retinalen Gefäßerkrankungen nützlich, sondern auch bei der Differenzialdiagnose von Uveitis, Aderhauttumoren und Erkrankungen der Papille.
1961 berichteten Harold R. Novotny und David L. Alvis erstmals über die ursprüngliche Methode der FA. Ab 1967 veröffentlichte John Donald McIntyre Gass systematische FA-Befunde bei verschiedenen Funduserkrankungen, was die klinische Anwendung rasch verbreitete.
Natriumfluorescein emittiert bei Anregung mit blauem Licht (Wellenlänge 465–490 nm) gelbgrüne Fluoreszenz (520–530 nm). Bei der Scanning-Laser-Ophthalmoskopie (SLO) wird ein blauer Laser von 488 nm verwendet. Natriumfluorescein ist ein wasserlöslicher Farbstoff mit einem Molekulargewicht von 376 Da; nach intravenöser Injektion beträgt die Proteinbindung etwa 70–80 %. Die restlichen etwa 20–30 % liegen in freier Form vor und emittieren die Fluoreszenz. Bei intakter Blut-Retina-Schranke tritt auch die freie Form nicht aus den Gefäßen aus. Bei Schrankenstörung tritt der Farbstoff aus und wird als charakteristische Hyperfluoreszenz beobachtet.
Die Blut-Retina-Schranke (BRB) besteht aus zwei Schichten: der inneren Schranke aus den Tight Junctions der retinalen Gefäßendothelzellen und der äußeren Schranke aus den Tight Junctions der retinalen Pigmentepithelzellen (RPE). Bei Störung der BRB kommt es zu Fluorescein-Leckage, die ein diagnostischer Indikator für verschiedene Netzhauterkrankungen ist.
Anregungslicht
Blaues Licht mit einer Wellenlänge von 465–490 nm wird eingestrahlt.
Im SLO wird ein Laser von 488 nm verwendet.
Ein Anregungsfilter schneidet unerwünschte Wellenlängen ab.
Fluoreszenzemission
Es wird gelb-grüne Fluoreszenz mit einer Emissionswellenlänge von 520–530 nm emittiert.
Die freie Form (ca. 20–30 %) ist der Hauptträger der Fluoreszenz.
Die protein gebundene Form (ca. 70–80 %) emittiert nur schwer Fluoreszenz.
Barrierefilter
Nur Fluoreszenz über 520 nm wird durchgelassen.
Das Anregungslicht wird blockiert, wodurch das Fluoreszenzbild klar wird.
Extravasation ist ein Beweis für eine Barrierezerstörung.
Sie wurde erstmals 1961 von Novotny und Alvis berichtet. Ab 1967 systematisierte Gass ihre Anwendung bei verschiedenen Augenhintergrunderkrankungen und sie verbreitete sich weltweit als Standarduntersuchungsmethode für die Augenhintergrunddiagnostik.
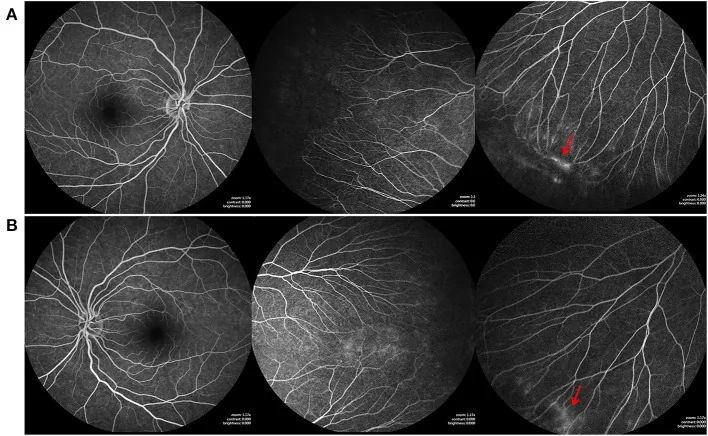
Die FA wird häufig zur Darstellung des Netzhautgefäßsystems eingesetzt. Nachfolgend sind die wichtigsten Indikationen aufgeführt.
Bei Makulaödem nach akuter Netzhautnekrose (ARN) zeigt die FA ein petaloides Leckagemuster, was zur Differenzialdiagnose des zystoiden Makulaödems (CME) und zur Beurteilung des Therapieerfolgs beiträgt1).
Während der Schwangerschaft kann ein Netzhautgefäßverschluss auftreten, aber aufgrund der plazentaren Durchlässigkeit der FA wird die OCTA als alternative Untersuchung empfohlen2).
Vor der Untersuchung folgende Inhalte erklären und schriftliche Einwilligung einholen4).
Gemäß den Durchführungsstandards für die Fundusangiographie (überarbeitete Version) der Japanischen Ophthalmologischen Gesellschaft werden die folgenden Maßnahmen durchgeführt 4).
Bei Patienten, die Betablocker oder Alphablocker einnehmen, ist das Risiko von Nebenwirkungen erhöht, daher sollte dies vorab abgeklärt werden 4). Der Hautreaktionstest hat eine begrenzte Aussagekraft; selbst bei negativem Ergebnis können schwerwiegende Nebenwirkungen nicht vollständig ausgeschlossen werden 4).
3–5 ml einer 10%igen Fluorescein-Lösung schnell intravenös injizieren 4). Bei Kindern beträgt die Richtdosis 0,1 mg/kg; bei Patienten mit Nierenfunktionsstörung sollte die Dosis auf die Hälfte oder weniger der normalen Dosis reduziert werden 4).
Unmittelbar nach der Injektion wird etwa 1 Minute lang kontinuierlich fotografiert, dann werden nach 5 und 10 Minuten Spätaufnahmen gemacht. Inklusive der Zeit für die Pupillenerweiterung dauert der gesamte Vorgang etwa 15–20 Minuten.
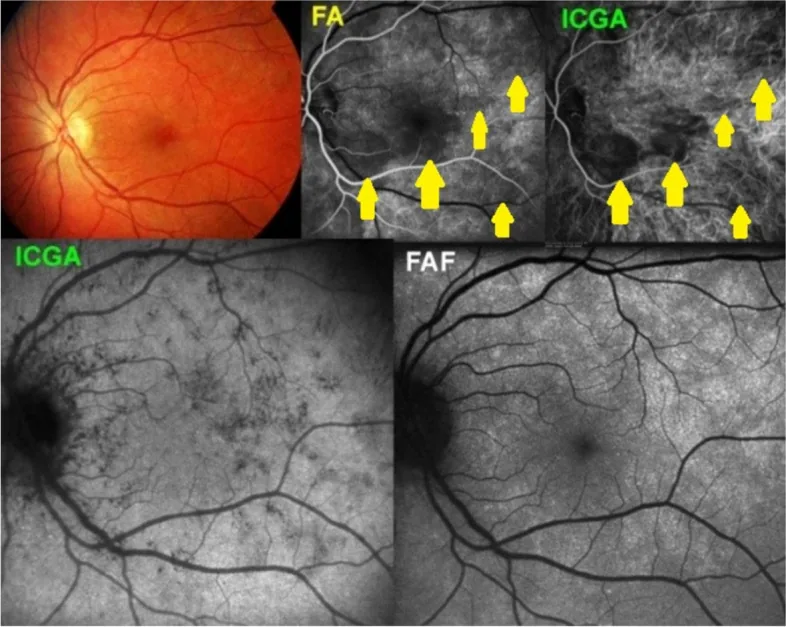
Die FA wird zeitlich in mehreren Phasen beobachtet.
FA-Befunde werden in drei Kategorien eingeteilt: Hypofluoreszenz, Hyperfluoreszenz und vaskuläre Formanomalien.
Fluoreszenzblockade (Hypofluoreszenz)
Definition: Blutungen, Pigmentierungen, Exsudate usw. blockieren die Hintergrundfluoreszenz.
Merkmale: Klare Grenzen, keine Formveränderung im zeitlichen Verlauf.
Repräsentative Erkrankungen: Subretinale Blutung, harte Exsudate, Aderhautnävus.
Füllungsdefekt (Hypofluoreszenz)
Definition: Aufgrund eines Gefäßverschlusses kommt es zu keinem oder verzögertem Einstrom des Fluoreszenzfarbstoffs.
Merkmale: Kapillare Nichtperfusionszonen bleiben während des gesamten Verlaufs dunkel.
Repräsentative Erkrankungen: Netzhautarterienverschluss, avaskuläre Areale bei diabetischer Retinopathie.
Fluoreszenzleckage (Hyperfluoreszenz)
Definition: Durchbruch der Blut-Retina-Schranke mit Austritt des Farbstoffs aus den Gefäßen.
Merkmale: Zeitliche Zunahme der Ausdehnung, unscharfe Grenzen. Ein blütenblattförmiges (petaloides) Muster ist charakteristisch für ein zystoides Makulaödem1).
Repräsentative Erkrankungen: Makulaödem, choroidale Neovaskularisation, Netzhautvaskulitis.
Transmissionsfluoreszenz (Hyperfluoreszenz)
Definition : Aderhautfluoreszenz ist durch einen RPE-Defekt sichtbar (Fensterdefekt).
Merkmale : Die Form ändert sich im Laufe der Zeit nicht, kann aber spät leicht anfärben.
Repräsentative Erkrankungen : Geografische Atrophie, Drusenkonfluenz, Makulaloch, angioide Streifen.
Hypofluoreszenz wird je nach Ursache wie folgt unterteilt.
| Art der Hypofluoreszenz | Ursache / Mechanismus | Repräsentative Erkrankungen |
|---|---|---|
| Fluoreszenzblockade | Blutung, harte Exsudate, Nävus verdecken die Hintergrundfluoreszenz | Subretinale Blutung, harte Exsudate, Aderhautnävus |
| Füllungsdefekt: Retinochoroidale Gefäßstenose | Verschluss oder Stenose großer Gefäße | Verschluss der A. carotis interna, Takayasu-Arteriitis |
| Füllungsdefekt: retinaler Gefäßverschluss | Arterien- und Venenverschluss | Retinaler Arterienverschluss (CRAO/BRAO), retinaler Venenverschluss |
| Füllungsdefekt: Kapillarverschluss | Periphere Durchblutungsstörung | Diabetische Retinopathie (NPA), Eales-Krankheit |
| Füllungsdefekt: choroidale Durchblutungsstörung | Choroidale Minderdurchblutung | Harada-Krankheit, APMPPE, hypertensive Choroidopathie |
| Netzhaut-Aderhaut-Atrophie | Fluoreszenzverlust durch Gewebeatrophie | Makuladystrophie, Retinitis pigmentosa, atrophe AMD, pathologische Myopie |
| Papillenhypofluoreszenz | Ischämie/Infiltration des Sehnervengewebes | Ischämische Optikusneuropathie, Melanozytom |
Die Hyperfluoreszenz wird je nach Ursache wie folgt unterteilt.
Folgende morphologische Gefäßanomalien werden beobachtet.
Chorioidalgefäße sind aufgrund der Abschirmung durch das RPE schwer zu beurteilen. Zur Beurteilung einer Typ-1-MNV (chorioidale Neovaskularisation) mit Fluoreszein-Leckage wird ergänzend die Indocyaningrün-Angiographie (ICGA) eingesetzt.
Mikroaneurysmen, nicht perfundierte Areale (NPA) und Neovaskularisation sind die Hauptbefunde. Die FA unterscheidet die Leckagemuster des Makulaödems (fokal/diffus/zystoid) und dient als Grundlage für die Festlegung der Laserbestrahlungsstellen 3). In der Spätphase ist eine deutliche Leckage aus Neovaskularisationen zu beobachten. Die Ultraweitwinkel-FA verbessert die Genauigkeit der Beurteilung peripherer NPA.
Unverzichtbar für die Beurteilung der CNV-Aktivität. Die klassische CNV (Typ 2) zeigt eine frühe, scharf begrenzte Hyperfluoreszenz und späte Leckage. Die okkulte CNV (Typ 1) liegt unter dem RPE und stellt sich als späte getüpfelte Hyperfluoreszenz oder fibrovaskuläre PED dar. Die geografische Atrophie zeigt sich als Fensterdefekt.
Wird zur Beurteilung von Füllungsverzögerung, venöser Dilatation und Tortuositas, kapillären Nichtperfusionsarealen und Kollateralen verwendet. Ein NPA von mehr als 10 Papillenflächen gilt als ischämischer Typ und ist ein Risikoindikator für ein Neovaskularisationsglaukom. Auch wichtig für das Verständnis des Leckagemusters des Makulaödems.
Charakteristische Leckagepunkte vom Tintenfleck- (inkblot) oder Schornstein- (smokestack) Typ auf RPE-Ebene. Mehrere Leckagepunkte deuten auf eine chronische CSC hin. Zur Bestimmung des Bestrahlungsbereichs der photodynamischen Therapie (PDT) werden FA und ICGA kombiniert eingesetzt.
Bei der Harada-Krankheit zeigen sich punktförmige Hyperfluoreszenzen durch multiple Aderhautlecks und Farbstoffansammlungen in Bereichen mit seröser Netzhautablösung. Bei Morbus Behçet finden sich eine Anfärbung der Gefäßwände durch retinale Vaskulitis und NPA (Non-Perfusion Areas). Bei der Eales-Krankheit sind periphere NPA und Neovaskularisationen charakteristisch.
Die Daten des Durchführungsstandards für Fundusangiographie der Japanischen Ophthalmologischen Gesellschaft (überarbeitete Version) werden gezeigt 4).
Nebenwirkungen treten je nach Schweregrad mit folgenden Häufigkeiten auf.
| Schweregrad | Inzidenz |
|---|---|
| Alle Nebenwirkungen | 1,1–11,2 % |
| Leicht | 1,4–8,1 % |
| Mäßig | 0,2–1,5 % |
| Schwer | 0,005–0,48 % |
| Tod | 0,0005 bis 0,002 % |
Leicht (klingt oft spontan ab)
Mäßig
Schwerwiegend (extrem selten)
Die Diagnose einer Anaphylaxie wird gestellt, wenn eines der folgenden drei Kriterien erfüllt ist4).
Algorithmus zur Behandlung der Anaphylaxie :
Auch nach erfolgreicher Behandlung besteht das Risiko einer biphasischen Anaphylaxie (Wiederauftreten innerhalb von 6–8 Stunden nach Symptomfreiheit); daher ist eine Überwachung von mindestens 8 Stunden erforderlich, und eine stationäre Beobachtung (24 Stunden) wird empfohlen4).
Abgrenzung zum vasovagalen Reflex: Der vasovagale Reflex äußert sich durch Bradykardie, Hypotonie, Blässe und kalten Schweiß, jedoch ohne Hauterscheinungen (Urtikaria, Flush), was ihn von der Anaphylaxie unterscheidet. Beim vasovagalen Reflex sind flache Lagerung, Beinhochlagerung und Flüssigkeitsgabe wirksam4).
Dies ist eine normale Reaktion auf die renale Ausscheidung von Fluorescein und kein Grund zur Sorge. Die Gelbfärbung der Haut verschwindet innerhalb von 2–3 Stunden, die des Urins bis zum nächsten Tag von selbst.
Fluorescein passiert die Plazenta und ist 72 Stunden in der Muttermilch nachweisbar, daher wird die Untersuchung bei Schwangeren und Stillenden grundsätzlich vermieden2)3). Falls retinale Gefäßinformationen benötigt werden, wird die nicht-invasive OCT-Angiographie (OCTA) als Alternative empfohlen2).
Fluorescein-Natrium ist ein gelb-roter wasserlöslicher Farbstoff mit einem Molekulargewicht von 376 Da. Bei Anregung mit einer Wellenlänge von 465–490 nm (488 nm im SLO) emittiert es gelb-grüne Fluoreszenz bei 520–530 nm. Nach intravenöser Verabreichung binden etwa 70–80 % an Plasmaproteine (hauptsächlich Albumin), und etwa 20–30 % liegen in freier Form vor und fluoreszieren. Es wird über die Nieren ausgeschieden (Verschwinden innerhalb von 1–2 Tagen) und der hepatische Metabolismus ist gering.
Die Indocyaningrün (ICG)-Angiographie wird ergänzend zur FA eingesetzt. Die Eigenschaften beider Verfahren sind unten aufgeführt.
| Parameter | FA | ICG-Angiographie |
|---|---|---|
| Molekulargewicht | 376 Da | 775 Da |
| Proteinbindungsrate | Etwa 70–80 % | Etwa 98 % |
| Hauptbeobachtungsobjekt | Netzhautgefäße | Aderhautgefäße |
| Anregungswellenlänge | 465–490 nm | ca. 805 nm |
| Fluoreszenzwellenlänge | 520–530 nm | ca. 835 nm (Nahinfrarot) |
| Ausscheidungsweg | Nieren | Leber |
ICG hat eine Proteinbindungsrate von 98 %, sodass es kaum aus den Aderhautgefäßen austritt und sich zur Beurteilung des Aderhautblutflusses eignet. Bei der Bewertung der polypoiden Aderhautvaskulopathie (PCV), des Aderhauthämangioms und der Typ-1-MNV ergänzt die ICGA die FA.
OCTA ist eine nicht-invasive Untersuchung, die die Phaseninformationen der OCT analysiert und die Bewegung der roten Blutkörperchen sichtbar macht. Es wird kein Kontrastmittel verwendet, und die Netzhautgefäßplexus können auf Kapillarebene in drei Schichten getrennt dargestellt werden 3). Seine Nützlichkeit als Alternative zur FA bei der Beurteilung der Netzhautgefäße während der Schwangerschaft wurde nachgewiesen 2).
| Parameter | FA | OCTA |
|---|---|---|
| Kontrastmittel | Erforderlich | Nicht erforderlich |
| Invasivität | Venenpunktion, Nebenwirkungen möglich | Nicht-invasiv |
| Dynamische Informationen | Beurteilung von Leckagen und Füllungsverzögerungen möglich | Nicht beurteilbar (nur Struktur) |
| Tiefenauflösung | Nur 2D-Bild | Schichtanalyse möglich |
| Aufnahmebereich | Weitwinkel (bis 200°) | Begrenzt (3–12 mm) |
| Periphere Beurteilung | Einfach | Schwierig |
Da die OCTA kein Austreten von Fluoreszenz aus den Gefäßen nachweisen kann, ist die FA nach wie vor unverzichtbar für die Beurteilung der Aktivität eines Makulaödems, die Bestimmung der CNV-Aktivität (Vorhandensein von Leckage) und die Bewertung der Gefäßwandentzündung bei retinaler Vaskulitis. Durch den komplementären Einsatz beider Verfahren ist eine präzisere Beurteilung des Augenhintergrunds möglich.
Der beobachtbare Bildwinkel und die Eigenschaften unterscheiden sich je nach verwendetem Bildgebungsgerät.
| Gerät | Bildwinkel | Hauptmerkmale |
|---|---|---|
| Funduskamera | 55° | Standard und weit verbreitet |
| SLO/HRA | 30–102° | Hoher Kontrast und konfokal |
| Optos | 200° | Ultraweitwinkel- und periphere Aufnahme in einem Schritt |
Das Ultraweitwinkel-Bildgebungsgerät (Optos) kann mit einer einzigen Aufnahme die Peripherie erfassen und ist nützlich für die Beurteilung peripherer Läsionen bei diabetischer Retinopathie und Netzhautdegenerationserkrankungen.
Bei zystoidem Makulaödem nach akuter Netzhautnekrose wurde vorgeschlagen, dass das blütenblattförmige Leckmuster in der FA ein prädiktiver Biomarker für das Therapieansprechen sein könnte 1). Die Forschung schreitet voran, um die dynamischen Informationen der FA zu quantifizieren und für die Vorhersage der Wirksamkeit von Anti-VEGF-Therapie und photodynamischer Therapie zu nutzen.
Durch die Einführung des RetCam3 ist die Durchführung von FA bei Kindern möglich geworden. Eine Anwendung wird für die Gefäßbeurteilung bei Frühgeborenenretinopathie und pädiatrischen Netzhauterkrankungen erwartet.
Die 200°-Ultraweitwinkel-FA mit Optos hat die Aufnahmezeit peripherer Läsionen erheblich verkürzt. Ihre Nützlichkeit wurde bei der Beurteilung peripherer kapillärer Nichtperfusionszonen bei diabetischer Retinopathie und bei der umfassenden Beurteilung angeborener Netzhautgefäßerkrankungen (wie FEVR) gezeigt.
OCTA ist nicht-invasiv und kann die Struktur der Kapillaren detailliert darstellen, kann jedoch kein Fluoreszenz-Leck außerhalb der Gefäße nachweisen. Zur Beurteilung der Aktivität eines Makulaödems und zur Bestätigung eines CNV-Leck ist eine FA erforderlich. Beide Verfahren ergänzen sich in ihrer Information 3).