Stadium 0–1
Stadium 0 (normal): Nasale, obere und untere Grenze unscharf. Radiäre Nervenfaserschicht.
Stadium 1 (sehr früh): Unscharfe nasale Papillengrenze. Keine Vorwölbung der Grenze. Subtil grauer Halo. Konzentrische oder radiäre Aderhautfalten.

Papillenödem (Papilledema) bezeichnet die Schwellung der Sehnervenpapille infolge eines erhöhten intrakraniellen Drucks (ICP). Dieser Begriff wird ausschließlich für die Papillenschwellung durch ICP-Erhöhung verwendet; Schwellungen aus anderen Ursachen werden als „Optikusdiskussödem“ (optic disc edema) bezeichnet. In Japan wird es auch als „Stauungspapille“ (うっ血乳頭) bezeichnet.
Das Papillenödem ist ein Warnsignal für schwere Erkrankungen wie Hirntumore, ZNS-Entzündungen, zerebrale Venenthrombose und idiopathische intrakranielle Hypertension (IIH) und ein ophthalmologischer Befund, der nicht übersehen werden darf. Die Abgrenzung zum Pseudopapillenödem (z. B. Drusen der Sehnervenpapille, schräge Papille, kleine Papille) ist ebenfalls wichtig.
Epidemiologie: Die jährliche Inzidenz der idiopathischen intrakraniellen Hypertension in den USA beträgt 1,15 pro 100.000 Personen2), häufiger bei Frauen (1,97 vs. 0,36 pro 100.000 bei Männern). Die höchste Inzidenz tritt im reproduktiven Alter von 18–44 Jahren auf (2,47 pro 100.000) und nimmt weltweit mit der Adipositas-Epidemie zu2). Der normale ICP bei Erwachsenen liegt unter 250 mmH2O (manometrisch gemessen), bei Kindern unter 280 mmH2O.
Papillenödem (Papilledema) ist ein Begriff, der auf eine ICP-Erhöhung beschränkt ist, während Papillenschwellungen aus anderen Ursachen (Optikusneuritis, Ischämie, infiltrative Läsionen usw.) als „Optikusdiskussödem“ (optic disc edema) bezeichnet werden. Diese Unterscheidung ist wichtig, da sie direkt zur Identifizierung der Ätiologie und zur Wahl der geeigneten Behandlung führt.
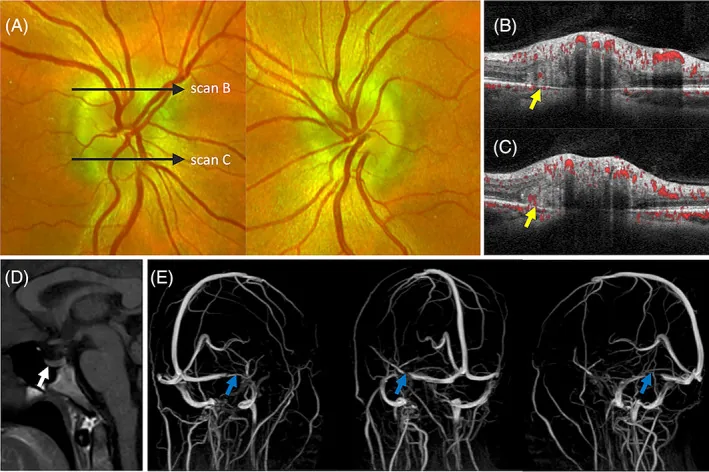
Im akuten Stadium des Papillenödems ist die zentripetale Sehfunktion (beste korrigierte Sehschärfe, Farbsehen) in der Regel erhalten, und anfangs sind subjektive Symptome oft gering.
Bei Kindern wird die intrakranielle Drucksteigerung häufig durch eine Esotropie infolge beidseitiger Abduzensparese entdeckt.
Fundusbefunde beim akuten Papillenödem:
Zusätzliche Befunde bei chronischem Papillenödem: Blässe der Papille, Gliose, optoziliärer Shunt (bei Zentralvenenverschluss, chronischer Stauungspapille, Optikusscheidenmeningeom), refraktile Körperchen.
Im chronischen Stadium schwellen abgestorbene Nervenfasern nicht mehr an, sodass das Ödem trotz anhaltender ICP-Erhöhung verschwinden kann.
Der Schweregrad des Papillenödems wird nach der Frisén-Skala (Stadium 0–5) beurteilt und als Indikator für die visuelle Prognose verwendet.
Stadium 0–1
Stadium 0 (normal): Nasale, obere und untere Grenze unscharf. Radiäre Nervenfaserschicht.
Stadium 1 (sehr früh): Unscharfe nasale Papillengrenze. Keine Vorwölbung der Grenze. Subtil grauer Halo. Konzentrische oder radiäre Aderhautfalten.
Stadium 2–3
Stadium 2 (früh): Unscharfe aller Grenzen. Vorwölbung der nasalen Grenze. Vollständiger peripapillärer Halo.
Stadium 3 (mäßig): Vergrößerung des Papillendurchmessers. Teilweise Unschärfe einiger Segmente der Hauptgefäße. Fingerförmige Fortsätze am äußeren Rand des Halos.
Stadium 4–5
Stadium 4 (ausgeprägt): Vorwölbung der gesamten Papille. Vollständige Unschärfe der Hauptgefäßsegmente auf der Papille.
Stadium 5 (schwer) : Kuppelförmige Vorwölbung. Der Hof ist schmal und die Ränder sind glatt. Verschwinden der physiologischen Exkavation.
TVO ist ein charakteristisches Symptom einer Stauungspapille, aber an sich kein direkter Vorbote eines Sehverlusts. Wenn der erhöhte intrakranielle Druck jedoch lange anhält, kann er von schweren peripheren Gesichtsfeldausfällen zu einer Verschlechterung des zentralen Sehvermögens fortschreiten. Wenn TVO häufig auftritt, ist es wichtig, schnell einen Spezialisten aufzusuchen und die Ursache abzuklären.
Die Geschwindigkeit der Entstehung einer Stauungspapille hängt von der Geschwindigkeit des Anstiegs des intrakraniellen Drucks ab. Ein leichter, langsamer ICP-Anstieg kann über mehrere Wochen auftreten, während eine schwere, plötzliche Veränderung innerhalb von Stunden bis zu einem Tag auftreten kann.
Bei idiopathischer intrakranieller Hypertonie wurde gezeigt, dass eine Gewichtsabnahme von 5–10 % die ICP-Symptome und das Papillenödem verbessert. Allerdings ist die Gewichtskontrolle nur ein Teil der konservativen Behandlung; je nach Schweregrad des Papillenödems und Vorhandensein von Sehstörungen kann eine Kombination mit medikamentöser oder chirurgischer Behandlung erforderlich sein.
Die Diagnose eines Papillenödems erfolgt durch eine Kombination aus augenärztlicher Untersuchung, Neurobildgebung und Lumbalpunktion (LP). Messen Sie zunächst den Blutdruck, um eine maligne Hypertonie auszuschließen, und führen Sie dann eine Notfallbildgebung (CT → MRT + kontrastverstärkte MRV) durch, um raumfordernde Läsionen und Sinusvenenthrombosen zu beurteilen. Nach Bestätigung, dass kein Risiko einer Hirnhernie besteht, führen Sie eine LP durch.
MRT + kontrastmittelgestützte MRV ist die optimale Bildgebung zur Beurteilung der folgenden Anzeichen eines erhöhten intrakraniellen Drucks (ICP):
Die definitive Diagnose einer idiopathischen intrakraniellen Hypertension erfordert die Erfüllung aller folgenden 5 Kriterien:
| Kriterium | Inhalt |
|---|---|
| 1. Papillenödem | Beidseitiges Papillenödem vorhanden |
| 2. Neurologische Untersuchung | Normal, außer Hirnnervenauffälligkeiten |
| 3. Neurobildgebung | Hirnparenchym normal, keine Ventrikelerweiterung, keine Raumforderung, keine abnormale Kontrastmittelanreicherung |
| 4. Liquorzusammensetzung | Normal |
| 5. Liquoreröffnungsdruck | Erwachsene ≥ 250 mmH2O, Kinder ≥ 280 mmH2O |
Verdachtsdiagnose: bilaterale Stauungspapille + Kriterien 1–4 erfüllt, aber Liquordruck unter dem Grenzwert.
Ein Pseudopapillenödem wird durch hohe Hyperopie, hohe Myopie, Drusen, schräge Papille, markhaltige Nervenfasern, Hamartome usw. verursacht. Es liegt eine Anomalie der Papillenmorphologie vor, aber kein echtes Ödem. Die folgenden Befunde deuten auf ein Pseudopapillenödem hin:
Differenzialdiagnose: Eingebettete Drusen, schräge Papille, diabetische Papillopathie, hypertensive Papillopathie, hintere Skleritis, Perineuritis, Uveitis (Sarkoidose, VKH), Optikusneuritis, endokrine Orbitopathie, CRVO, NAION, infiltrative Optikusneuropathie (Lymphom, Leukämie), Optikusscheidenmeningeom usw.
Die drei Ziele der Behandlung sind: ① Behandlung der zugrunde liegenden Ursache, ② Erhalt des Sehvermögens und ③ Linderung der Symptome (z. B. Kopfschmerzen).
In Japan bilden die folgenden Punkte die Grundlage der Behandlung des erhöhten intrakraniellen Drucks.
Komplikationen der chirurgischen Behandlung: Achten Sie auf Shunt-Dysfunktion, -Bruch, -Infektion sowie auf Sehstörungen im Zusammenhang mit dem chirurgischen Eingriff bei ONSF.
Prognose: Bei frühzeitigem Absinken des intrakraniellen Drucks bildet sich das Papillenödem schnell zurück und die Sehfunktion bleibt erhalten. Bei verzögerter Behandlung ist der Sehverlust irreversibel. Die Rezidivrate der idiopathischen intrakraniellen Hypertension beträgt 9–28 %, daher ist eine regelmäßige Nachsorge wichtig2). Die Sehprognose ist im Allgemeinen gut, in seltenen Fällen kann es jedoch zu schwerem Sehverlust kommen2).
Prognostisch ungünstige Faktoren: Gewichtszunahme, Schwere des Papillenödems, Ausmaß der Kopfschmerzen zu Beginn2).
Fulminante idiopathische intrakranielle Hypertension: Bei schweren Fällen mit ausgeprägter Sehverschlechterung, schwerem Papillenödem und Gesichtsfeldeinschränkung kann der anfängliche Liquordruck im Mittel 54,1 cmH2O (Spanne 29–70 cmH2O) erreichen1), 50 % entwickeln eine legale Blindheit, und alle weisen restliche Gesichtsfeldausfälle und Optikusatrophie auf1). Wenn der HVF-Ausgangs-MD unter -7 dB lag, erholte sich das Sehvermögen nicht1).
Acetazolamid ist als Mittel der ersten Wahl bei idiopathischer intrakranieller Hypertonie wirksam, ist jedoch bei zerebraler Venenthrombose kontraindiziert, da es die Erkrankung verschlimmern kann. Es ist wichtig, zunächst die Ursache zu identifizieren und die Behandlung entsprechend der zugrunde liegenden Ursache zu wählen. Zudem ist es in Japan nicht erstattungsfähig.
Die Stagnation des axonalen Flusses spielt eine zentrale Rolle bei der Entstehung des Papillenödems.
Mechanismus der axonalen Flussstagnation:
Pathophysiologie der idiopathischen intrakraniellen Hypertonie: Der genaue Mechanismus ist ungeklärt. Es wird eine Störung der CSF-Dynamik-Regulation sowie metabolische und hormonelle Faktoren vermutet 2). Auch ein erhöhter Sinusdruck durch Sinusvenenstenose und verminderte CSF-Resorption wurden vorgeschlagen. In letzter Zeit wird die idiopathische intrakranielle Hypertonie zunehmend als systemische Stoffwechselerkrankung mit gestörter Androgenregulation erkannt 1).
AVM-bedingte intrakranielle Hypertonie (seltener Mechanismus): Nicht rupturierte arteriovenöse Malformationen (AVM) können ohne Blutung oder Hydrozephalus eine intrakranielle Hypertonie und ein Papillenödem verursachen 3). Als Mechanismus wird eine abnorme Drainage durch Arterialisierung kortikaler Venen → erhöhter Pulsdruck im Subarachnoidalraum → Beeinträchtigung der CSF-Resorption angenommen. Eine Literaturübersicht berichtet über insgesamt 26 Fälle 3).
Das Stenting des Sinus transversus (TSS) wurde als sichere und wirksame Behandlungsmethode bei der Behandlung der idiopathischen intrakraniellen Hypertension beschrieben4).
Waser et al. (2021) berichteten über TSS bei einem Fall von Papillenödem mit Herniation des Hirnparenchyms in den Sinus durae matris (BHDVS) bei einem 52-jährigen Mann4). Sechs Monate nach der Stentimplantation wurden ein objektives Verschwinden des Papillenödems und eine Normalisierung des Sinusdruckgradienten (32 mmHg → 12 mmHg, Gradient >15 mmHg → 5 mmHg) erreicht.
Ghorbani et al. (2025) berichteten über eine endovaskuläre Embolisation bei 4 Fällen von nicht rupturierten AVM mit intrakranieller Hypertension und Papillenödem3). Innerhalb eines Monats nach der Behandlung verschwand das beidseitige Papillenödem, und bei vollständig embolisierten Fällen war keine Medikamentenanpassung erforderlich. Bei Fall 1 (35-jähriger Mann) normalisierte sich der anfängliche LP-Druck von 38 cmH2O auf 28 cmH2O eine Woche nach der Embolisation und auf 21 cmH2O nach einem Monat, mit bestätigtem Verschwinden des Papillenödems.
Die idiopathische intrakranielle Hypertension wird zunehmend als eine von der Adipositas unabhängige systemische Stoffwechselerkrankung betrachtet1). Eine randomisierte kontrollierte Studie (IIH Weight Trial, JAMA Neurol 2021) zum Vergleich von bariatrischer Chirurgie versus gemeindebasierter Gewichtsmanagement-Intervention zeigte die Wirksamkeit der bariatrischen Chirurgie1). Die Forschung zu neuen Behandlungen, die auf Androgenregulationsstörungen abzielen, ist im Gange1), und die Stärkung der Evidenz für chirurgische Eingriffe wird ebenfalls als Priorität angesehen1). Die Aufklärung der Ätiologie, zusätzlicher Faktoren der Funktionsstörung und der optimalen Behandlung der idiopathischen intrakraniellen Hypertension sind zukünftige Forschungsthemen2).
Bonelli L, Menon V, Arnold AC, Mollan SP. Managing idiopathic intracranial hypertension in the eye clinic. Eye. 2024;38:2472-2481.
Toshniwal SS, Kinkar J, Chadha Y, et al. Idiopathic intracranial hypertension: a comprehensive review. Cureus. 2024;16(3):e56256.
Ghorbani M, Griessenauer CJ, Wipplinger C, et al. Intracranial hypertension and papilledema secondary to an unruptured arteriovenous malformation: review of the literature. Neuroradiol J. 2025;38(4):387-393.
Waser B, Wood HM, Mews P, Lalloo S. Transverse sinus stenting for treatment of papilloedema secondary to a large brain herniation into a dural venous sinus with associated tectal plate lesion: case report and literature review. Interv Neuroradiol. 2021;27(6):756-762.