مرحله التهابی
پریفلبیت محیطی: تشکیل غلاف سفید در امتداد وریدهای شبکیه محیطی. نفوذ سلولهای التهابی اطراف عروق.
خونریزی شبکیه: خونریزیهای نقطهای و شعلهای در محیط.
نشت وریدی در FA: آنژیوگرافی فلورسئین میتواند التهاب فعال را تأیید کند.

بیماری ایلز (Eales disease) برای اولین بار در سال ۱۸۸۰ توسط هنری ایلز، چشمپزشک بریتانیایی، به عنوان خونریزی مکرر زجاجیه در مردان جوان سالم گزارش شد. این یک واسکولیت انسدادی ایدیوپاتیک شبکیه است که با پریفلبیت، انسداد عروق و نئوواسکولاریزاسیون در شبکیه محیطی مشخص میشود.
شیوع این بیماری از نظر جغرافیایی بسیار متفاوت است. در آمریکای شمالی نادر است، اما در مناطقی با شیوع بالای عفونت سل مانند هند، خاورمیانه و آسیا نسبتاً شایع است1). بیشتر در مردان ۲۰ تا ۳۰ ساله دیده میشود و نسبت مرد به زن حدود ۲۰ به ۱ است. تا ۸۷٪ موارد دوطرفه هستند1).
تشخیص پس از رد سایر واسکولیتهای شبکیه، بیماریهای سیستمیک و دیابت به عنوان یک تشخیص افتراقی تأیید میشود.
در آمریکای شمالی بسیار نادر است، اما در مناطق آندمیک سل مانند هند و خاورمیانه نسبتاً شایع است1). نسبت مرد به زن حدود ۲۰ به ۱ است و تا ۸۷٪ موارد دوطرفه هستند.
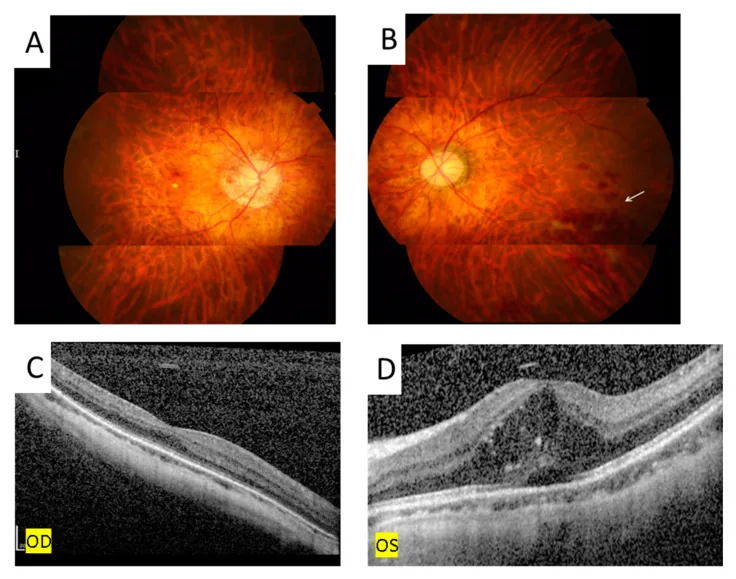
در مراحل اولیه، بیماری اغلب بدون علامت است و در مرحله پریفلبیت محیطی، علائم ذهنی وجود ندارد. با پیشرفت بیماری، علائم زیر ظاهر میشوند.
بیماری ایلز در سه مرحله التهابی، ایسکمیک و پرولیفراتیو پیشرفت میکند1).
مرحله التهابی
پریفلبیت محیطی: تشکیل غلاف سفید در امتداد وریدهای شبکیه محیطی. نفوذ سلولهای التهابی اطراف عروق.
خونریزی شبکیه: خونریزیهای نقطهای و شعلهای در محیط.
نشت وریدی در FA: آنژیوگرافی فلورسئین میتواند التهاب فعال را تأیید کند.
مرحله ایسکمیک
عدم پرفیوژن مویرگی: تشکیل نواحی گسترده عدم پرفیوژن در محیط.
شنت شریانی-وریدی: تغییرات عروقی جبرانی در پاسخ به ایسکمی.
تغییرات مهرهای وریدها: اتساع و تنگی نامنظم متناوب وریدها.
مرحله پرولیفراتیو
عروق جدید (شکل بادبزنی دریایی): عروق جدید پرولیفراتیو که در مجاورت نواحی ایسکمیک ایجاد میشوند.
خونریزی زجاجیه: خونریزی مکرر ناشی از پارگی عروق جدید.
جداشدگی شبکیه کششی (TRD): کشش ناشی از غشاهای فیبروواسکولار. ممکن است به جداشدگی مختلط شبکیه، گلوکوم نئوواسکولار، آب مروارید و آتروفی عصب بینایی منجر شود 4).
در طبقهبندی ساکسنا، مراحل بیماری به ۷ مرحله از Ia تا IVb تقسیم میشود. Ia/Ib: فلبیت محیطی، IIa: ایسکمی/عدم پرفیوژن، IIb: ظهور عروق جدید، IIIa/IIIb: شدت خونریزی زجاجیه، IVa/IVb: بر اساس وسعت TRD.
ادم ماکولا در ۵۸.۲٪ موارد مشاهده میشود 4) و یک عارضه مهم است که مستقیماً با پیشآگهی بینایی مرتبط است.
آنژیوگرافی فلورسئین (FA) میتواند نشت وریدی در التهاب فعال، رنگپذیری دیواره در مرحله اسکلروز مزمن و وسعت مناطق بدون پرفیوژن را ارزیابی کند.
علت ناشناخته است و ایدیوپاتیک در نظر گرفته میشود، اما واکنش حساسیتی به پروتئین مایکوباکتریوم توبرکلوزیس قویترین نظریه پاتوژنز است.
در ۵۰ تا ۷۰ درصد موارد غشای پیششبکیه، PCR برای مایکوباکتریوم مثبت گزارش شده است، اما در کشت باکتری یافت نمیشود 3). تصور میشود که مکانیسم بیماری به جای عفونت مستقیم با باکتری زنده، یک واکنش حساسیتزایی ایمنی به باکتریهای غیرزنده یا قطعات DNA باشد. به همین دلیل، در موارد مثبت شدن تست مانتو، مصرف همزمان داروهای ضد سل توصیه میشود.
بیماری ایلز یک تشخیص افتراقی است. تشخیص پس از رد سایر واسکولیتهای شبکیه و بیماریهای سیستمیک تأیید میشود 1).
یافتههای اصلی آزمایش در زیر آورده شده است.
| اقلام آزمایش | هدف/موارد رد شده |
|---|---|
| کوانتیفرون/مانتو | ارزیابی عفونت سل |
| ANA/ANCA/آنتیdsDNA | لوپوس اریتماتوز سیستمیک/واسکولیت |
| ACE/لیزوزیم سرم | سارکوئیدوز |
| قند خون/HbA1c | رتینوپاتی دیابتی |
| آزمایش خون (CBC، انعقاد) | کم خونی داسی شکل / اختلال انعقادی |
| سرولوژی سیفلیس / بیماری لایم | واسکولیت عفونی |
تشخیصهای افتراقی شامل رتینوپاتی دیابتی، انسداد شاخه ورید شبکیه (BRVO)، بیماری کوتس، سارکوئیدوز، لوپوس اریتماتوز سیستمیک (SLE)، رتینوپاتی داسی شکل و بیماری بهجت است 1)4).
این یک تشخیص افتراقی است و پس از رد بیماریهای سیستمیک مانند دیابت، سارکوئیدوز و SLE با آزمایش خون و تصویربرداری تشخیص داده میشود 1). آنژیوگرافی فلورسین (FA) مهمترین آزمایش است که پریفلبیت محیطی، مناطق بدون پرفیوژن و توزیع عروق نوزاد را تأیید میکند.
درمان بر اساس مرحله بیماری انتخاب میشود. درمانهای اصلی بر اساس مرحله در زیر آورده شده است.
| مرحله | درمان اصلی | درمان کمکی |
|---|---|---|
| فاز التهابی | استروئید خوراکی | ATT (در صورت مثبت بودن مانتو) |
| فاز ایسکمیک | فتوکوآگولاسیون شبکیه (PRP) | تزریق ضد VEGF |
| فاز پرولیفراتیو | ویترکتومی و فتوکوآگولاسیون | تزریق ضد VEGF |
استروئید خوراکی خط اول درمان است. روش معمول شروع با پردنیزون 40 میلیگرم در روز و کاهش تدریجی دوز است 1). همچنین گزارش شده است که تجویز دگزامتازون 1 میلیگرم/کیلوگرم/روز به مدت 4 ماه با کاهش تدریجی، به دید نهایی 20/20 منجر شده است 4). مطالعه بزرگ Biswas و همکاران (500 بیمار، 898 چشم) نشان داد که تجویز استروئید در فاز التهابی حاد به طور معنیداری دید را بهبود میبخشد 2)4).
برای ادم ماکولا (CME)، تزریق داخل زجاجیهای ایمپلنت دگزامتازون (Ozurdex) مؤثر است 2).
در موارد مثبت بودن تست مانتو، داروهای ضد سل تجویز میشود. رژیم RIPE (ریفامپین، ایزونیازید، پیرازینامید، اتامبوتول) به مدت 4 ماه و سپس ایزونیازید به تنهایی به مدت 5 ماه (مجموعاً 9 ماه) تجویز میشود 2)3). برای شروع ATT در موارد مشکوک به عفونت سل، الگوریتم بینالمللی (راهنمای COTS) مرجع است 2).
با درمان زودهنگام و مناسب، پیشآگهی بینایی خوبی قابل انتظار است. گزارش شده است که بینایی 20/20 به مدت 33 سال پس از ویترکتومی حفظ شده است2). از سوی دیگر، تأخیر در درمان میتواند منجر به جداشدگی کششی شبکیه، گلوکوم نئوواسکولار، آب مروارید و آتروفی عصب بینایی شود4).
پاتوفیزیولوژی بیماری ایلز به صورت یک فرآیند پیشرونده مرحلهای با شروع از پریفلبیت وریدهای محیطی درک میشود1)2).
مرحله اول (التهاب): نفوذ سلولهای التهابی و پریفلبیت در امتداد وریدهای محیطی شبکیه رخ میدهد. PCR برای مایکوباکتریوم توبرکلوزیس در 50-70% از غشاهای اپیرتینال مثبت است، اما کشت باکتری را نشان نمیدهد3). تصور میشود که باکتریهای غیرقابل کشت یا قطعات DNA سیستم ایمنی میزبان را فعال کرده و باعث التهاب واکنشی میشوند1).
مرحله دوم (ایسکمی): آسیب دیواره عروقی ناشی از التهاب منجر به تشکیل ترومبوز و انسداد عروق میشود. مناطق بدون پرفیوژن مویرگی گسترش یافته و ایسکمی پیشرفت میکند.
مرحله سوم (نئوواسکولاریزاسیون): VEGF به مقدار زیاد از شبکیه ایسکمیک ترشح میشود3). علاوه بر VEGF، غلظت بالای IL-6، IL-8 و MCP-1 در زجاجیه تشخیص داده میشود که یک حلقه پایدار از نئوواسکولاریزاسیون پاتولوژیک و التهاب را تشکیل میدهد3). عروق جدید به شکل بادبزن دریایی در مرز ایسکمی ظاهر شده و خونریزی از این عروق شکننده تکرار میشود.
لازم به ذکر است که بیماری ایلز و واسکولیت شبکیه مرتبط با سل (TRV) از نظر بالینی تقریباً غیرقابل تشخیص هستند و احتمال دارد که در یک طیف قرار داشته باشند2).
کوکائین میتواند از طریق انقباض عروق و آسیب اندوتلیال، تشکیل ترومبوز را تسریع کرده و به عنوان یک محرک ایمنی عمل کند4). هتروزیگوت جهش فاکتور V لیدن خطر ترومبوز را حدود ۷ برابر افزایش میدهد و یک عامل خطر ژنتیکی برای انسداد عروق است4).
دستورالعملهای اجماع بینالمللی (COTS) الگوریتم مدیریت TRV (واسکولیت شبکیه مرتبط با سل) را سازماندهی میکنند2). بیماری ایلز و TRV تاکنون به عنوان بیماریهای مجزا در نظر گرفته میشدند، اما مرز بین آنها در حال بازبینی است و تداوم تصویر بالینی و علتشناسی مورد بحث قرار گرفته است2).
مواردی گزارش شده است که در بیماری ایلز مقاوم به رانیبیزوماب، از آفلیبرسپت استفاده شده و پس از ۴۳ ماه دید ۲۰/۲۵ حفظ شده است، و همچنین موردی که با تزریق مکرر هر ۳ ماه به مدت ۲۸ ماه دید ۲۰/۲۰ حفظ شده است3). این اولین گزارش موارد استفاده از آفلیبرسپت در بیماری ایلز است و با اتصال همزمان VEGF-A، VEGF-B و PlGF ممکن است در موارد مقاوم به داروهای ضد VEGF موجود مؤثر باشد3).
عوامل خطر جدیدی مانند سوءمصرف کوکائین و جهش فاکتور V لیدن از موارد فردی شناسایی شدهاند4) و انتظار میرود که در آینده، بررسی عوامل ایمنی و ژنتیکی پیشرفت کند.