โรคจอประสาทตา เสื่อมตามอายุ (AMD ) เป็นสาเหตุสำคัญอันดับต้นๆ ของความบกพร่องทางการมองเห็น เป็นโรคที่มีหลายปัจจัยทำให้เกิดการเปลี่ยนแปลงแบบฝ่อหรือแบบมีน้ำซึม渗出ที่จุดรับภาพในผู้ที่มีอายุ 50 ปีขึ้นไป
แบ่งออกเป็นสามประเภทหลัก: รอยโรคก่อนเกิด (ดรูเซน ชนิดอ่อน, ความผิดปกติของเยื่อบุผิวรงควัตถุจอตา), ชนิดเส้นเลือดใหม่, และชนิดฝ่อ
ประมาณครึ่งหนึ่งของชนิดเส้นเลือดใหม่เป็นโรคหลอดเลือดคอรอยด์ แบบโพลิปอยด์ (PCV ) และมักมีพื้นหลังเป็นพาคิคอรอยด์
การรักษาทางเลือกแรกสำหรับชนิดเส้นเลือดใหม่คือการฉีดยา anti-VEGF เข้าในน้ำวุ้นตา และการแทรกแซงตั้งแต่เนิ่นๆ มีผลต่อพยากรณ์การมองเห็น
ชนิดฝ่อ (ฝ่อแบบแผนที่ ) ปัจจุบันยังไม่มีการรักษาที่เป็นมาตรฐาน และ 10-15% ของผู้ป่วยจะเกิดเส้นเลือดใหม่คอรอยด์ ในระหว่างดำเนินโรค
อาหารเสริม AREDS2 ช่วยลดความเสี่ยงของการดำเนินโรคจากระยะกลางไปสู่ระยะปลายของ AMD
หากคุณสังเกตเห็นภาพบิดเบี้ยว หรือการมองเห็น ส่วนกลางลดลงอย่างรวดเร็ว ควรรีบไปพบจักษุแพทย์ทันที
โรคจอประสาทตา เสื่อมตามอายุ (AMD ) เป็นโรคที่ทำให้เกิดการเปลี่ยนแปลงแบบฝ่อหรือแบบมีน้ำซึม渗出ที่จุดรับภาพเนื่องจากการเปลี่ยนแปลงตามอายุ ถือเป็นโรคที่มีหลายปัจจัยเกี่ยวข้องกับความโน้มเอียงทางพันธุกรรมและปัจจัยสิ่งแวดล้อม เช่น อายุ การสูบบุหรี่ การโดนแสงแดด โรคอ้วน และอาหารที่มีไขมันสูง
นิยามว่าเป็นความผิดปกติของจุดรับภาพที่เกี่ยวข้องกับอายุในรัศมี 6,000 ไมโครเมตรรอบรอยบุ๋มจอตา ในผู้ที่มีอายุ 50 ปีขึ้นไป และแบ่งเป็นรอยโรคก่อนเกิด ชนิดเส้นเลือดใหม่ และชนิดฝ่อ เป็นสาเหตุอันดับที่สี่ของความบกพร่องทางการมองเห็น
การศึกษา Hisayama (2012) รายงานความชุกของ AMD ระยะลุกลามเท่ากับ 1.6% (ชนิด渗出 1.5%, ชนิดฝ่อ 0.1%) ในขณะที่การศึกษา Nagahama (2008-) รายงานความชุกของรอยโรคก่อนเกิดเท่ากับ 22.8% (ดรูเซน 39.4%) เกิดในเพศชายและหญิงอายุมากกว่า 50 ปี (ชาย:หญิง = 3:1) และเกิดในตาข้างเดียวหรือทั้งสองข้าง (ประมาณ 40%) ทั้งรอยโรคก่อนเกิดและ AMD ระยะลุกลามมีแนวโน้มเพิ่มขึ้น การศึกษา Hisayama (ติดตาม 9 ปี) รายงานว่าการสูบบุหรี่เพิ่มความเสี่ยงของ AMD ระยะปลายถึง 4 เท่า 1)
มีความแตกต่างทางเชื้อชาติ ความชุกสูงในคนผิวขาวและชาวเอเชีย ต่ำในชาวฮิสแปนิกและแอฟริกัน 2) ความชุกของ AMD ชนิดฝ่อในการศึกษาตะวันตกอยู่ระหว่าง 0.66% ถึง 1.34% และมีรายงานว่าพบได้บ่อยกว่าชนิด渗出ถึง 4 เท่าในผู้ที่มีอายุมากกว่า 85 ปี ปัญหานี้อาจกลายเป็นปัญหาใหญ่ในญี่ปุ่นเมื่อประชากรสูงอายุขึ้น ทั่วโลกมีผู้ป่วย AMD ประมาณ 200 ล้านคน และคาดว่าจะเพิ่มขึ้นเป็นประมาณ 288 ล้านคนภายในปี 2040 2) ความชุกของ AMD ระยะปลายเพิ่มขึ้นแบบเอกซ์โพเนนเชียลตามอายุ จาก 0.1% ในกลุ่มอายุ 50-59 ปี เป็น 4.3% ในกลุ่มอายุ 80 ปีขึ้นไป 2)
ตามแนวทางปฏิบัติทางคลินิกของญี่ปุ่นล่าสุด (2024) โดยอ้างอิงการจำแนกของ Beckman AMD ถูกแบ่งออกเป็น 4 ระยะดังนี้ 1) :
ระยะ ลักษณะ AMD ระยะเริ่มต้นดรูเซน ชนิดนิ่มขนาดกลาง (63 ถึง <125 ไมครอน) อย่างน้อย 1 จุดAMD ระยะกลางดรูเซน ขนาดใหญ่ (≥125 ไมครอน), ความผิดปกติของเยื่อบุผิวเม็ดสีจอประสาทตา , สารคล้ายดรูเซน ใต้จอประสาทตา AMD ระยะปลายมีเส้นเลือดใหม่ในจอประสาทตา (รวมถึงเส้นเลือดใหม่ในคอรอยด์ ) หรือจอประสาทตา ฝ่อแบบแผนที่ AMD ระยะสุดท้ายแผลเป็นพังผืด หรือจอประสาทตา เสื่อมแบบถุงน้ำร่วมกับการสูญเสียการมองเห็น อย่างรุนแรง
ดรูเซน ขนาดเล็ก (ชนิดแข็ง) (น้อยกว่า 63 ไมครอน) ถือเป็นการเปลี่ยนแปลงทางสรีรวิทยาตามอายุ และไม่รวมอยู่ใน AMD ระยะเริ่มต้น อย่างไรก็ตาม หากพบดรูเซน ชนิดแข็งจำนวนมาก (20 ชิ้นขึ้นไป) ความเสี่ยงในการเกิด AMD จะสูง 1) อัตราการดำเนินโรคใน 5 ปีของ AMD ระยะกลางอยู่ที่ประมาณ 18% แต่หากมี pseudodrusen แบบร่างแห ความเสี่ยงจะเพิ่มขึ้นอย่างมีนัยสำคัญ (ความผิดปกติของเม็ดสี + ดรูเซน ขนาดใหญ่ + pseudodrusen แบบร่างแห ให้ความเสี่ยง 72% ใน 5 ปี) 2)
AMD ชนิดมีเส้นเลือดใหม่
เส้นเลือดใหม่ที่จอตา (MNV) : เส้นเลือดใหม่ที่เกิดจากคอรอยด์ หรือเส้นเลือดจอตา เกิดขึ้นที่จอตา ทำให้การมองเห็น ลดลงอย่างรวดเร็ว
ชนิดย่อย : MNV ชนิดที่ 1 (ใต้ RPE ), ชนิดที่ 2 (เหนือ RPE ), ชนิดที่ 3 (จากเส้นเลือดในจอตา, RAP ) และ PCV (MNV ชนิดที่ 1 + รอยโรคแบบโปลิป) 1)
ลักษณะเฉพาะในญี่ปุ่น : ประมาณครึ่งหนึ่งของ AMD ชนิดมีเส้นเลือดใหม่เป็นโรคเส้นเลือดใหม่คอรอยด์หนา (PNV ) และพบดรูเซน เพียงประมาณ 30% ของกรณี 1)
AMD ชนิดฝ่อ
การฝ่อแบบภูมิศาสตร์ (GA) : มีลักษณะการฝ่อที่ขอบเขตชัดเจนของ RPE , เซลล์รับแสง และเส้นเลือดฝอยคอรอยด์
การดำเนินโรคตามธรรมชาติ : เริ่มต้นรอบรอยบุ๋มจอตา และขยายเป็นรูปเกือกม้าแล้วเป็นวงแหวน อัตราการเติบโต 1.28–2.6 มม.²/ปี 3)
การเกิด CNV ระหว่างดำเนินโรค : ใน 10–15% ของกรณี เกิดเส้นเลือดใหม่คอรอยด์ นำไปสู่การเปลี่ยนเป็นชนิดมีน้ำซึม
Q
จอตาเสื่อมตามอายุเกิดขึ้นทั้งสองตาหรือไม่?
A
ประมาณ 40% ของกรณีเกิดขึ้นทั้งสองตา หากตาข้างหนึ่งเป็น AMD ระยะท้าย ตาอีกข้างมีความเสี่ยงสูงที่จะเกิด MNV มีรายงานว่าจีโนไทป์ ARMS 2 เป็นปัจจัยทำนายการเกิดในตาอีกข้าง 1) แนะนำให้ตรวจตาเป็นประจำและตรวจด้วยตนเองโดยใช้ตาราง Amsler
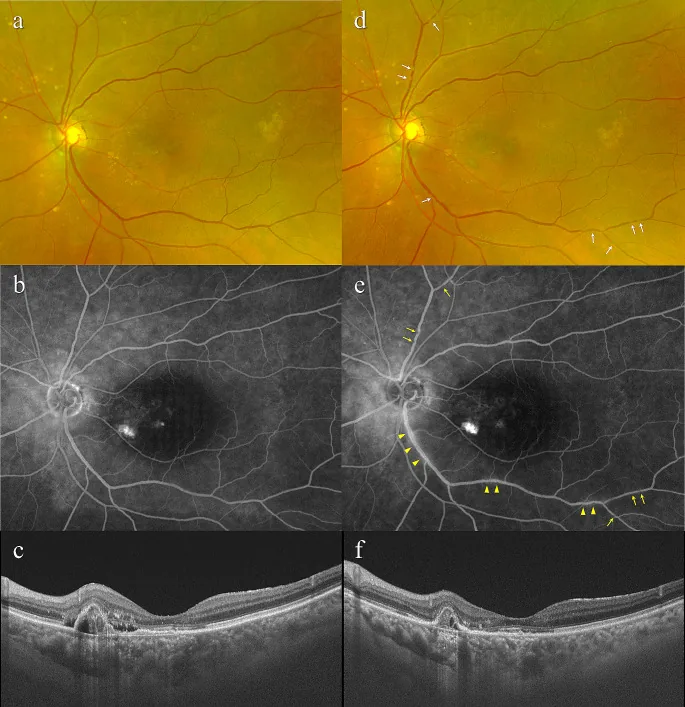
ภาพถ่ายจอตา, การฉีดสีหลอดเลือดฟลูออเรสซีน และ OCT ของจอตาเสื่อมตามอายุ แสดงการเปลี่ยนแปลงของ RPE บริเวณจอตา, PED และของเหลวใต้จอตา Matsumoto H, et al. Retinal vasculitis after intravitreal aflibercept 8 mg for neovascular age-related macular degeneration. Jpn J Ophthalmol. 2024. Figure 2. PM
CI D: PMC11420316. License: CC BY.
ในภาพถ่ายจอตา จะเห็นการเปลี่ยนแปลงของ
RPE ที่จอตา และการฉีดสีหลอดเลือด
ฟลูออเรสซีน ยืนยันการรั่วซึมที่จอตา
OCT แสดงการยกตัวของ
RPE (
PED ) และของเหลวใต้จอตา ทำให้เข้าใจได้ง่ายว่าเป็นผลการตรวจวินิจฉัยของจอตาเสื่อมตามอายุ
ในระยะแรกเริ่มด้วยภาพบิดเบี้ยว (เห็นภาพบิดเบี้ยว ) และจุดบอดกลาง ตา เมื่อดำเนินไป การมองเห็น ลดลงต่ำกว่า 0.1 ในกรณีที่มีเลือดออกมาก อาจเกิดการมองเห็น ลดลงอย่างฉับพลันและรุนแรง
ภาพบิดเบี้ยว (Metamorphopsia)2) จุดบอดกลาง ตาความบกพร่องของลานสายตา ในบริเวณกลางถึงกึ่งกลางตา ในฝ่อแบบภูมิศาสตร์ (geographic atrophy) จะเกิดจุดบอดสัมบูรณ์ที่สอดคล้องกับบริเวณฝ่อการมองเห็น ลดลงรอยบุ๋มจอตา (fovea) การมองเห็น จะลดลงต่ำกว่า 0.1ความไวต่อความต่างลดลง : เกิดขึ้นเร็วแม้ในชนิดฝ่อที่รอยบุ๋มจอตา ยังปกติ เป็นความผิดปกติทางการทำงานที่ตรวจไม่พบด้วยการทดสอบการมองเห็น 8) การปรับตัวในที่มืดลำบาก : ใช้เวลานานขึ้นในการปรับตัวกับที่มืด อาจเกิดขึ้นก่อนการมองเห็น ลดลง2) ความบกพร่องในการอ่าน และการมองเห็น ระยะไกลรอยบุ๋มจอตา ก็ส่งผลต่อคุณภาพชีวิต8) ผู้ป่วยฝ่อแบบภูมิศาสตร์ประมาณครึ่งหนึ่งมีการดำเนินโรคอย่างรวดเร็ว ส่งผลลบอย่างมากต่อคุณภาพชีวิต3) ภาพแสงวาบ (Photopsia) : ความรู้สึกเห็นแสงวาบ แม้พบน้อย แต่อาจมีรายงานในระยะเริ่มต้นของเส้นเลือดใหม่2)
ในกรณีที่เป็นตาเดียว มักไม่รู้สึกในชีวิตประจำวัน ความรุนแรงของอาการแตกต่างกันไปตามตำแหน่งและขนาดของ MNV ระดับของของเหลวใต้จอตา เลือดออก และแผลเป็นพังผืด ในชนิดเส้นเลือดใหม่ ระยะเวลาจนถึงภาวะตาบอดตามกฎหมายมักสั้นกว่าชนิดฝ่อ และแนะนำให้พบแพทย์ทันทีเมื่อมีภาพบิดเบี้ยว
รอยโรคเล็กกลม นูน สีขาวเหลืองที่จุดภาพชัด (macula) เกิดจากการสะสมของสารพหุสัณฐาน (เศษเยื่อหุ้มเซลล์ คอเลสเตอรอลที่ไม่ได้เอสเทอริฟายด์ คอมพลีเมนต์ ฯลฯ) ระหว่างเยื่อฐานของ RPE และชั้นคอลลาเจนชั้นในของเยื่อบรูค (Bruch’s membrane) ถือเป็นต้นกำเนิดของการอักเสบเรื้อรังซึ่งเป็นพื้นฐานของพยาธิสภาพของ AMD
ดรูเซน แข็งAMD ดรูเซน อ่อนAMD ดรูเซน เทียมร่างแห (reticular pseudodrusen)RPE และสัมพันธ์อย่างใกล้ชิดกับ AMD ชนิดฝ่อและ RAP (MNV ชนิดที่ 3)1)
MNV ชนิดที่ 1 : ใน OCT แสดง double layer sign (RPE ยกตัวไม่สม่ำเสมอและมีการสะท้อนปานกลางภายใน) แบ่งเป็นชนิดแบนเตี้ย และ PED ชนิด fibrovascular ที่ RPE ยกตัวเป็นรูปโดม ชนิดหลังมักดื้อต่อการรักษา 1) MNV ชนิดที่ 2 : ใน OCT ตรวจพบเป็นโครงสร้างสะท้อนปานกลางถึงสูงเหนือ RPE มักมี fibrin ตกตะกอนร่วมด้วย 1) MNV ชนิดที่ 3 (RAP ) : พบมากในผู้ป่วยที่มี drusen ชนิดอ่อนหลายจุดในตาทั้งสองข้าง OCT แสดง macular edema ชนิด cystoid และ PED ที่มี bump sign 1) PCV ICGA 1)
เป็นบริเวณฝ่อของ RPE ขอบเขตชัดเจน ซึ่งมองเห็นหลอดเลือดคอรอยด์ ได้ รอยโรคเริ่มรอบๆ fovea (parafoveal) และขยายเป็นรูปเกือกม้า → วงแหวน แล้วลุกลามเข้า fovea ค่ามัธยฐานของเวลาจนถึง fovea คือ 2.5 ปี 3) อัตราการเติบโต 1.28–2.6 มม.²/ปี; ในข้อมูลการทดลอง ranibizumab พื้นที่ GA เฉลี่ยเพิ่มขึ้นจาก 8.07 เป็น 12.05 มม.² ใน 2 ปี 3) GA หลายจุดโตเร็วกว่าจุดเดียว 3) อัตราการเปลี่ยนของตาข้างตรงข้ามเป็น GA สูงถึงประมาณ 30% ใน 12 เดือน และอัตราการเปลี่ยนเป็น CNV รายงานที่ 6.7%
การฝ่ออาจดำเนินไปอย่างรวดเร็วเมื่อ PED ขนาดใหญ่คล้าย drusen หดตัว รูปแบบ hyperautofluorescence ที่ขอบของบริเวณฝ่อในการตรวจ fundus autofluorescence มีประโยชน์ในการทำนายอัตราการดำเนินโรค
เลือดออกใต้จอประสาทตา หรือใต้ RPE : เลือดออกจาก MNV ถ้ามากอาจทำให้เกิด submaculr hematoma และอาจถึงขั้นเลือดออกในน้ำวุ้นตา จอประสาทตาลอก ชนิด serous หรือ PED ชนิด serousHard exudates : ตกตะกอนรอบ macula จากการรั่วเรื้อรังแผลเป็น fibrous : ผลการตรวจใน AMD ระยะสุดท้าย เนื้อเยื่อแผลเป็น fibrovascular ก่อตัวที่ macula 1)
Q
จอประสาทตาเสื่อมตามอายุสามารถสังเกตได้เองหรือไม่?
A
สามารถใช้ Amsler grid (แผ่นตรวจตนเองคล้ายตาราง) เพื่อตรวจหา metamorphopsia หรือ scotoma ได้ด้วยตนเอง อย่างไรก็ตาม ระยะแรกมักไม่มีอาการ ดังนั้นการตรวจตาเป็นประจำจึงจำเป็น โดยเฉพาะในกรณีที่เป็นตาเดียว ผู้ป่วยอาจไม่สังเกตเห็นในชีวิตประจำวัน
AMD เป็นโรคที่มีหลายปัจจัย โดยปัจจัยทางพันธุกรรมร่วมกับปัจจัยด้านสิ่งแวดล้อมและพฤติกรรมมีส่วนทำให้เกิดโรค
อายุ : ปัจจัยเสี่ยงที่ใหญ่ที่สุด ความชุกเพิ่มขึ้นอย่างรวดเร็วหลังจากอายุ 75 ปี 2) การสูบบุหรี่ : ปัจจัยเสี่ยงที่ปรับเปลี่ยนได้สำคัญที่สุด การศึกษา Hisayama รายงานว่าการสูบบุหรี่เพิ่มความเสี่ยงของ AMD ระยะท้ายถึง 4 เท่า 1) มีความสัมพันธ์แบบขนาด-การตอบสนอง และการสูบบุหรี่มือสองก็เกี่ยวข้องด้วย 2) ความโน้มเอียงทางพันธุกรรม : การกลายพันธุ์ Y402H ใน complement factor H (CF H) และ ARMS 2/HTRA1 เป็นตำแหน่งยีนเสี่ยงหลัก ยีนในระบบคอมพลีเมนต์ เช่น C2/CF B, C3, CF I และยีนเมแทบอลิซึมของไขมัน เช่น APOE และ CETP ก็มีส่วนเกี่ยวข้อง 1) Pachychoroid : การขยายตัวของหลอดเลือดใหญ่ในคอรอยด์ และการเพิ่มขึ้นของการซึมผ่านของหลอดเลือดถือเป็นพื้นหลังสำคัญสำหรับการพัฒนา AMD ชนิด neovascular ในคนญี่ปุ่น drusen พบได้น้อยกว่า (ประมาณ 30%) เมื่อเทียบกับชาวตะวันตก และ pachychoroid มีบทบาทสำคัญในการเกิดโรค 1) โรคหัวใจและหลอดเลือด ความดันโลหิตสูง และโรคอ้วน : สัมพันธ์กับความเสี่ยงที่เพิ่มขึ้นของ AMD 2) การรับประทานอาหาร : การบริโภคอาหารที่มีไขมันสูงเพิ่มความเสี่ยง ในขณะที่การรับประทานกรดไขมันโอเมก้า 3 สายยาวและผักใบเขียวลดความเสี่ยง 1) การปฏิบัติตามอาหารเมดิเตอร์เรเนียนช่วยลดความเสี่ยงของ AMD ระยะลุกลามได้ 41% 2) การสัมผัสแสงแดด : การสัมผัสรังสีอัลตราไวโอเลตและแสงที่มองเห็นได้ก็ถูกชี้ว่าเป็นปัจจัยเสี่ยงเช่นกันเพศ : พบในผู้ชายมากกว่า (อัตราส่วนชาย:หญิง 3:1) อย่างไรก็ตาม พบได้บ่อยในผู้หญิงสูงอายุเช่นกันสีม่านตา : ผู้ที่มีม่านตา สีอ่อน (สีฟ้าหรือสีเทา) มีแนวโน้มที่จะมีความเสี่ยงสูงกว่าประวัติครอบครัว : การมีญาติสายตรงที่ป่วยเป็น AMD จะเพิ่มความเสี่ยงสายตายาว สายตายาว มีความเสี่ยงสูงในการเกิด AMD
การเลิกบุหรี่เป็นการเปลี่ยนแปลงวิถีชีวิตที่มีประสิทธิภาพมากที่สุดในการป้องกันการลุกลามของ AMD อาหารเสริมตาม AREDS2 (วิตามินซี 500 มก., วิตามินอี 400 IU, ลูทีน 10 มก., ซีแซนทีน 2 มก., สังกะสี 25 มก., ทองแดง 2 มก.) ช่วยลดความเสี่ยงของการลุกลามจาก AMD ระยะกลางไปสู่ระยะท้าย แนะนำให้รับประทานปลา ผลไม้ และผักใบเขียวให้มาก และหลีกเลี่ยงอาหารที่มีไขมันสูง ควรตรวจตาเป็นประจำ (ปีละ 1-2 ครั้ง) และตรวจด้วยตนเองโดยใช้ตาราง Amsler อย่างต่อเนื่อง
Q
อาหารเสริมสามารถป้องกันจอประสาทตาเสื่อมตามอายุได้หรือไม่?
A
อาหารเสริม AREDS2 (ลูทีน ซีแซนทีน วิตามินซี วิตามินอี สังกะสี ทองแดง) ช่วยลดความเสี่ยงของการลุกลามจาก AMD ระยะกลางไปสู่ระยะปลายได้ประมาณ 25% 2) อย่างไรก็ตาม ยังไม่มีการพิสูจน์ประสิทธิภาพใน AMD ระยะต้นหรือเพื่อการป้องกันปฐมภูมิ เบตาแคโรทีนเพิ่มความเสี่ยงมะเร็งปอดในผู้สูบบุหรี่ ดังนั้นสำหรับผู้สูบบุหรี่ ควรเลือกผลิตภัณฑ์ที่มีลูทีน/ซีแซนทีน 1)
เกณฑ์การวินิจฉัย AMD ชนิด neovascular มีดังนี้ 1) :
มี MNV ในบริเวณจุดรับภาพ (เส้นผ่านศูนย์กลาง 6000 μm รอบรอยบุ๋มจอตา ) ร่วมกับ drusen, pachychoroid หรือความผิดปกติของ RPE
ควรยืนยัน MNV เพื่อการวินิจฉัยที่แน่นอน แต่สามารถวินิจฉัยได้หากมีข้อสงสัยเพียงพอว่ามี MNV จากการเปลี่ยนแปลงแบบเลือดออกหรือแผลเป็นพังผืด
การคัดออก: รอยโรคจากสายตาสั้น มาก, angioid streaks, โรคอักเสบ หรือการบาดเจ็บ
เกณฑ์การวินิจฉัย AMD ชนิดฝ่อ (geographic atrophy) คือต้องมีทั้งหมดดังต่อไปนี้ 1) :
รายการ เกณฑ์ ขนาด เส้นผ่านศูนย์กลาง ≥250 μm รูปร่าง กลม รูปไข่ รูปพวง หรือแบบแผนที่ ขอบเขต ชัดเจน การเปลี่ยนแปลงของ RPE การเปลี่ยนแปลงแบบสีจางหรือไม่มีสี คอรอยด์ มองเห็นหลอดเลือดขนาดกลางและใหญ่ได้ชัดเจน
OCT (เครื่องตรวจชั้นตาด้วยแสง)AMD ตรวจพบ double layer sign ใน MNV ชนิดที่ 1, โครงสร้างสะท้อนแสงสูงใต้จอประสาทตา ใน MNV ชนิดที่ 2, bump sign ใน MNV ชนิดที่ 3, และการฝ่อของชั้นนอกจอประสาทตา ใน geographic atrophy 1) .OCTA (การตรวจหลอดเลือดด้วยแสง)2) ไม่รุกราน และบางครั้งมีความสามารถในการตรวจหา MNV ชนิดที่ 1 สูงกว่า FA 1) .FA (การตรวจหลอดเลือดด้วยฟลูออเรสซีน )ภาพบิดเบี้ยว หรือสายตาลดลงโดยไม่ทราบสาเหตุ 2) .ICGA (การตรวจหลอดเลือดด้วยอินโดไซยานีนกรีน)PCV แสดงรอยโรคแบบ polypoid รอบ MNV ชนิดที่ 1 เป็นการเรืองแสงแบบ nodular 1) เนื่องจากเสี่ยงต่อภาวะภูมิแพ้รุนแรง ควรพิจารณางดหากสามารถวินิจฉัยได้ด้วยการตรวจอื่นการเรืองแสงเองของจอตา (FAF ) : ตรวจพบ geographic atrophy เป็นบริเวณที่มีการเรืองแสงเองลดลง ขอบเขตชัดเจน การเรืองแสงเองเพิ่มขึ้นที่ขอบมีประโยชน์ในการทำนายการดำเนินโรคตาราง Amsler : การคัดกรองภาพบิดเบี้ยว และจุดบอด แนะนำให้ตรวจด้วยตนเองเป็นประจำ 2) .Microperimetry : การวัดปริมาณความไวของจอประสาทตา สามารถวัดจุดบอดสัมบูรณ์และความไวที่ลดลงจาก geographic atrophy และประเมินความผิดปกติที่ BCVA ไม่สามารถตรวจพบได้ 8) .
หากพบการเปลี่ยนแปลงแบบมีการขับ渗出จาก MNV (เช่น IRF, SRF, ของเหลวใต้ RPE , ไฟบริน, เลือดออก) จะถือว่า “มีการดำเนินโรค” 1) การประเมินแบบไม่รุกล้ำด้วย OCT กลายเป็นมาตรฐานหลัก เนื่องจากตำแหน่งที่มีกิจกรรมของโรค MNV สูงไม่จำเป็นต้องอยู่ที่รอยบุ๋มจอตา เสมอไป จึงแนะนำให้สแกนทั่วทั้งจุดรับภาพเพื่อประเมิน 1)
ในความผิดปกติของจุดรับภาพร่วมกับ MNV จำเป็นต้องแยกโรคจากโรคต่อไปนี้
สายตาสั้น มากคอรอยด์ ฝ่อจากสายตาสั้น และ MNVคอริโอเรติโนพาทีชนิดเซรุ่มกลาง (CSC ) : อาจซ้อนทับกันเป็นกลุ่มโรคที่เกี่ยวข้องกับคอรอยด์หนา จอตาเสื่อมทางพันธุกรรม : สงสัยเป็นพิเศษหากเริ่มมีอาการตั้งแต่อายุน้อยโรคอักเสบ : กลุ่มอาการฮิสโทพลาสโมซิสที่ตา, คอรอยด์ อักเสบหลายจุด ฯลฯแองจิออยด์สตรีค : MNV เนื่องจากการฉีกขาดของเยื่อบรูค
Q
OCTA สามารถแทนที่การตรวจหลอดเลือดด้วยฟลูออเรสซีนได้หรือไม่?
A
OCTA มีความแม่นยำสูงในการตรวจหา MNV โดยมีความไว 0.87 และความจำเพาะ 0.97 2) และถูกใช้มากขึ้นเป็นการตรวจแบบไม่รุกล้ำ โดยเฉพาะในการตรวจหา MNV ชนิดที่ 1 อาจดีกว่าการตรวจหลอดเลือดด้วยฟลูออเรสซีน 1) อย่างไรก็ตาม ICGA ยังคงจำเป็นสำหรับการวินิจฉัย PCV และไม่ใช่การตรวจที่ใช้แทนกันได้อย่างสมบูรณ์
ไม่มีการรักษาตามหลักฐานสำหรับ AMD ระยะต้น 2) สำหรับ AMD ระยะกลางขึ้นไป นอกจากการให้คำแนะนำให้เลิกบุหรี่และปรับปรุงอาหารแล้ว แนะนำให้รับประทานอาหารเสริมตามสูตร AREDS2 1)
สูตรอาหารเสริมที่ใช้ใน AREDS2 1) :
วิตามินซี 500 มก.
วิตามินอี 400 IU
ลูทีน/ซีแซนทีน 10 มก./2 มก.
ซิงก์ออกไซด์ 25 มก.
คอปเปอร์ออกไซด์ 2 มก.
เบตาแคโรทีนถูกแทนที่ด้วยลูทีน/ซีแซนทีนเนื่องจากเพิ่มความเสี่ยงมะเร็งปอดในผู้สูบบุหรี่ 1) สูตร AREDS2 ช่วยลดความเสี่ยงของการลุกลามจาก AMD ระยะกลางไปสู่ระยะปลายได้ประมาณ 25%
การรักษาทางเลือกแรกสำหรับ AMD ชนิดเส้นเลือดงอกใหม่คือการฉีดยา Anti-VEGF เข้าแก้วตา 1) สำหรับ MNV ใต้จอประสาทตา ส่วนกลาง แนะนำให้ใช้ยา Anti-VEGF เพียงอย่างเดียวเป็นการรักษาเริ่มต้น
รานิบิซูแมบ
ขนาดยา : 0.5 มก. ฉีดเข้าแก้วตา
ระยะกระตุ้น : 3 ครั้ง ห่างกัน 1 เดือน
ระยะคงสภาพ : ฉีดเมื่อจำเป็น (PRN) การศึกษา MARINA พบว่ากลุ่มที่ได้รับยามีการมองเห็น ดีขึ้น 6.6 ตัวอักษร เทียบกับกลุ่มหลอกที่ลดลง 14.9 ตัวอักษร 1)
ยาชีววัตถุ คล้ายคลึงรานิบิซูแมบ BS มีจำหน่าย
อะฟลิเบอร์เซปต์
ขนาดยา : 2.0 มก. ฉีดเข้าแก้วตา
ระยะเริ่มต้น : ฉีด 3 ครั้ง ห่างกัน 1 เดือน
ระยะคงสภาพ : ฉีดคงที่ทุก 2 เดือน หรือวิธี treat-and-extend โดยขยายระยะห่างครั้งละ 2 สัปดาห์ (สูงสุด 3 เดือน) หากไม่มีการกลับมาของสารน้ำ และลดลง 2 สัปดาห์เมื่อมีการกลับมาเป็นซ้ำ 1)
PCV
Brolucizumab / Faricimab
Brolucizumab : ขนาด 6 มก. สามารถฉีดทุก 8-12 สัปดาห์ ต้องระวังการอักเสบในลูกตารวมถึง retinal vasculitis และ vascular occlusion 1)
Faricimab : แอนติบอดีแบบคู่จำเพาะต่อ VEGF-A และ Ang-2 ฉีดทุก 8-16 สัปดาห์ การศึกษา TENAYA/LUCERNE แสดงว่าไม่ด้อยกว่า aflibercept 1) 10)
มีสูตรการให้ยา 3 แบบ 1) :
แบบให้คงที่ : ให้ยาต่อเนื่องในระยะห่างคงที่แบบให้เมื่อจำเป็น (PRN) : ติดตามทุกเดือนและให้ยาเมื่อมีกิจกรรมของโรค การศึกษา CATT และ HARBOR รายงานว่ากลุ่ม PRN มีการมองเห็น ลดลงใน 2 ปีเมื่อเทียบกับกลุ่มที่ให้ยาทุกเดือน 11) วิธี treat-and-extend (TAE) : ปรับระยะห่างการให้ยาตามกิจกรรมของโรค การศึกษา TREX-AMD แสดงการมองเห็น ที่ดีขึ้นเทียบเท่าการให้ยาทุกเดือน การศึกษา ALTAIR (ในคนญี่ปุ่น) ยืนยันประสิทธิภาพของ TAE นาน 96 สัปดาห์ด้วยการปรับ 2/4 สัปดาห์ 1) การวิเคราะห์อภิมานแสดงว่า TAE ให้ผลการมองเห็น 2 ปีเทียบเท่าการให้คงที่ และดีกว่า PRN อย่างมีนัยสำคัญ 1)
สำหรับ MNV ชนิดที่ 2 หรือ PCV สามารถจี้เลเซอร์ทั่วทั้ง MNV โดยใช้ความยาวคลื่นสีเหลืองขึ้นไป ขนาดจุด 200-300 μm กำลัง 150-250 mW ระยะเวลาจี้ 0.2-0.5 วินาที โดยมีขอบปลอดภัย 100 μm รอบ MNV อย่างไรก็ตาม การจี้เลเซอร์ทำลาย RPE อย่างถาวร จึงไม่เหมาะกับ MNV ที่ใกล้รอยบุ๋มจอตา 1)
ทางเลือกในการรักษา PCV มีดังนี้ 1) :
การรักษาด้วยแสงไดนามิก (PDT ) ร่วมกับยาต้าน VEGF PDT มีผลทำให้ติ่งเนื้อหดตัวได้ดีกว่าการใช้ ranibizumab เพียงอย่างเดียวอย่างมีนัยสำคัญ ในด้านความปลอดภัย แนะนำให้ใช้ร่วมกับยาต้าน VEGF การรักษาด้วยยาต้าน VEGF เพียงอย่างเดียว
ใบสั่งยา PDT : ให้ verteporfin 6 มก./ตร.ม. ทางหลอดเลือดดำเป็นเวลา 10 นาที หลังจากเริ่มให้ยา 15 นาที ให้เลเซอร์ (689 นาโนเมตร, 600 มิลลิวัตต์/ตร.ซม., 83 วินาที) ขนาดการฉายรังสีคือเส้นผ่านศูนย์กลางสูงสุดของรอยโรค + 1,000 ไมโครเมตร หลีกเลี่ยงแสงแดดโดยตรงเป็นเวลา 2 วันหลังการรักษา
ในระยะยาว PDT อาจทำให้จอประสาทตา ฝ่อแย่ลง และควรหลีกเลี่ยงในกรณีที่คอรอยด์ บางหรือมีจอประสาทตา ฝ่ออยู่ก่อนแล้ว ไม่แนะนำให้ใช้ PDT สำหรับ MNV ชนิดที่ 3 1)
เมื่อผลการรักษาด้วยยาต้าน VEGF ไม่ดี (กรณีดื้อต่อการรักษา) หรือลดลง (ดื้อยา) การเปลี่ยนไปใช้ยาอื่นอาจได้ผล 1) นอกจากนี้ยังอาจเปลี่ยนยาโดยพิจารณาจากภาระการรักษา (ความถี่ในการมาโรงพยาบาลและการฉีดยา) ใน AMD ระยะสุดท้ายที่มีแผลเป็นพังผืดหรือการเปลี่ยนแปลงแบบฝ่อที่ไม่มีการเคลื่อนไหว ไม่ควรให้การรักษาเชิงรุก และควรพิจารณาติดตามอาการ 1)
ในตาที่มีสายตาดี การรักษาด้วยยาต้าน VEGF เพียงอย่างเดียวเป็นทางเลือก หากต้องการลดจำนวนครั้งในการรักษา สามารถเลือกการรักษาแบบผสมผสานระหว่าง PDT และสารยับยั้ง VEGF ในทางปฏิบัติทางคลินิก การรักษาด้วยยาต้าน VEGF เพียงอย่างเดียวเป็นหลัก
เลือดออกใต้จอประสาทตา จำนวนมากทำให้สายตาลดลงอย่างรวดเร็ว หากได้รับการรักษาตั้งแต่เนิ่นๆ การย้ายก้อนเลือดอาจช่วยให้สายตาดีขึ้น
การรักษาแบบประคับประคอง : สำหรับเลือดออกเล็กน้อยและสายตาค่อนข้างดี รับประทานยาเม็ด Adona 30 มก. × 3 (แบ่ง 3 ครั้ง), แคปซูลกรด Tranexamic 250 มก. × 3 (แบ่ง 3 ครั้ง) หากมีสารคัดหลั่ง ให้ยาต้าน VEGF การฉีดแก๊สเข้าในน้ำวุ้นตา : ฉีดซัลเฟอร์เฮกซะฟลูออไรด์ (SF₆) หรือเพอร์ฟลูออโรโพรเพน (C₃F₈) 0.3-0.5 มล. ร่วมกับการนอนคว่ำหลังผ่าตัดเพื่อย้ายก้อนเลือด อาจใช้ tPA ร่วมด้วย 1) การตัดน้ำวุ้นตา : ฉีด tPA ใต้จอประสาทตา หรือบีบก้อนเลือดออกด้วยของเหลวเพอร์ฟลูออโรคาร์บอน
ปัจจุบันยังไม่มีการรักษาสำหรับกรณีที่มีการฝ่อแบบ geographic atrophy ที่เกี่ยวข้องกับรอยบุ๋มจอประสาทตา ที่เกิดขึ้นแล้ว เชื่อว่าระบบคอมพลีเมนต์ มีส่วนเกี่ยวข้องอย่างมาก และยาที่มุ่งเป้าไปที่วิถีคอมพลีเมนต์ หลายชนิดกำลังอยู่ในระหว่างการพัฒนาและทดลองทางคลินิก
สำหรับจอประสาทตา ฝ่อแบบแผนที่ (geographic atrophy) ที่อยู่นอกโฟเวีย แนะนำให้รับประทานอาหารเสริม AREDS2 และปรับเปลี่ยนพฤติกรรมการใช้ชีวิต หากเกิด MNV ขึ้นในระหว่างการดำเนินโรค (10-15%) การรักษาด้วยยาต้าน VEGF จะเป็นมาตรฐาน
สำหรับผู้ป่วยที่การมองเห็น แย่ลง การดูแลด้านการมองเห็น ต่ำ (low vision care) เช่น การแนะนำอุปกรณ์ช่วยการมองเห็น เช่น แว่นตากันแสง แว่นขยาย และการช่วยเหลือในชีวิตประจำวัน เป็นสิ่งสำคัญ1)
การฉีดยาเข้าช่องว่างแก้วตา (intravitreal injection) ของยาต้าน VEGF มีความเสี่ยงต่อภาวะแทรกซ้อน เช่น เยื่อบุตาอักเสบ (endophthalmitis) ความดันลูกตา สูง และจอประสาทตาลอก
สำหรับยาโบรลูซิซูแมบ (brolucizumab) มีรายงานการอักเสบภายในลูกตา รวมถึงจอประสาทตา อักเสบ (retinal vasculitis) และการอุดตันของหลอดเลือด จำเป็นต้องเฝ้าระวังการตรวจพบตั้งแต่ระยะแรก1)
โรค AMD ชนิดมีเส้นเลือดงอกใหม่ไม่สามารถรักษาให้หายขาดได้ หากผู้ป่วยหยุดการรักษาเอง อาจเกิดการกลับมาเป็นซ้ำและการมองเห็น ลดลงอย่างรวดเร็ว1)
ยายับยั้งคอมพลีเมนต์ (pegcetacoplan และ avacincaptad pegol) สำหรับ AMD ชนิดฝ่อ ได้รับการอนุมัติจาก FDA สหรัฐอเมริกาในปี 2023 แต่ยังไม่ได้รับการอนุมัติในญี่ปุ่น
ในผู้ป่วยที่มีจอประสาทตา ฝ่อแบบแผนที่ ระยะลุกลาม ประโยชน์ของการรักษาด้วยยาต้าน VEGF อาจมีจำกัด
Q
ต้องฉีดยาต้าน VEGF บ่อยแค่ไหน?
A
ในระยะเริ่มต้น (induction phase) มักจะฉีด 3 ครั้ง ห่างกันเดือนละครั้ง หลังจากนั้นในระยะคงสภาพ (maintenance phase) แนะนำวิธี treat-and-extend (ค่อยๆ เพิ่มระยะห่าง) การศึกษา ALTAIR (ในคนญี่ปุ่น) ยืนยันประสิทธิภาพนาน 96 สัปดาห์1) สำหรับยา faricimab บางกรณีสามารถรักษาระยะห่างได้ถึง 16 สัปดาห์10)
Q
มีวิธีการรักษาที่ได้ผลสำหรับจอประสาทตาฝ่อแบบแผนที่หรือไม่?
A
ปัจจุบันยังไม่มีการรักษาที่เป็นมาตรฐาน ในสหรัฐอเมริกา ยายับยั้งคอมพลีเมนต์ 2 ชนิดได้รับการอนุมัติจาก FDA ในปี 20239) แต่ยังไม่ได้รับการอนุมัติในญี่ปุ่น อาหารเสริม AREDS2 ช่วยลดความเสี่ยงของการลุกลามไปสู่ AMD ระยะท้าย แต่ไม่แสดงผลในการชะลอการดำเนินของจอประสาทตา ฝ่อแบบแผนที่ เอง เมื่อการมองเห็น แย่ลง การดูแลด้านการมองเห็น ต่ำจึงมีความสำคัญ
พยาธิสภาพของ AMD เริ่มต้นจากความเสียหายของเซลล์ RPE ดรูเซน (drusen) สะสมระหว่างเยื่อฐานของ RPE และชั้นคอลลาเจนชั้นในของเยื่อบรูช ส่วนประกอบของดรูเซน รวมถึงเศษเยื่อหุ้มเซลล์ คอเลสเตอรอลที่ไม่ได้ถูกเอสเทอริฟายด์ และคอมพลีเมนต์ ซึ่งเป็นแหล่งที่มาของการอักเสบเรื้อรัง ความเครียดออกซิเดชัน ความผิดปกติของการเผาผลาญไขมัน และการกระตุ้นภูมิคุ้มกันโดยกำเนิดมีส่วนเกี่ยวข้องอย่างซับซ้อน นำไปสู่การเสียสมดุลของสารประกอบ RPE -เยื่อบรูช-หลอดเลือดฝอยคอรอยด์ หลังจากนั้น เส้นทางจะแยกออกเป็นสองทิศทาง
วิถีฝ่อ (Atrophic pathway) : การอักเสบและความเครียดออกซิเดชันทำให้เซลล์ RPE เสื่อมและฝ่อ เกิดการฝ่อแบบแผนที่ (geographic atrophy) ในหน่วยรับแสง-RPE -หลอดเลือดฝอยคอรอยด์ ชั้นนอกของจอประสาทตา (RPE และชั้น ellipsoid) จะหายไปก่อน และในรายที่ลุกลาม หลอดเลือดฝอยคอรอยด์ ก็ฝ่อเช่นกัน3) วิถี渗出 (Exudative pathway) : เกิดเส้นเลือดใหม่ (MNV) ใต้ RPE หรือในชั้นนอกของจอประสาทตา ทำให้เลือดออกและมีสารน้ำรั่ว ในของเหลวในลูกตา IL-6, IL-8, MCP -1 และ VEGF สูงขึ้น5)
เซลล์ RPE ที่ชรามีฟีโนไทป์การหลั่งที่เกี่ยวข้องกับความชรา (SASP ) โดยมีการแสดงออกของ SA-β-gal, p53, p21 และ p16 เพิ่มขึ้น7) ฟีโนไทป์ของเซลล์ RPE ที่ชรานี้สอดคล้องกับผลตรวจในผู้ป่วย AMD ชนิดฝ่อ และการกำจัดแบบเลือกสรรด้วย senolytics กำลังเป็นเป้าหมายการรักษาที่น่าสนใจ
ความหลากหลายทางพันธุกรรมของยีน CF H, C3 และ ARMS 2 เกี่ยวข้องกับความไวต่อการเกิด AMD 2) ความผิดปกติของการควบคุมวิถีคอมพลีเมนต์ (วิถีคลาสสิก วิถีทางเลือก และวิถีเลคติน) ขับเคลื่อนการขยายตัวของการฝ่อแบบแผนที่ 3) การยับยั้งคอมพลีเมนต์ C3 คาดว่าจะยับยั้งวิถีปลายทางทั้งหมดหลังจาก C5 ในขณะที่การยับยั้ง C5 ป้องกันการสร้างเมมเบรนแอทแทคคอมเพล็กซ์ (MAC)
Anegondi และคณะ (2025) ในการวิเคราะห์ข้อมูลการทดลอง lampalizumab แสดงให้เห็นว่าอัตราการเติบโตของการฝ่อแบบแผนที่ ที่เร็วกว่าสัมพันธ์กับการลดลงของ BCVA ที่เร็วกว่า โดยประมาณ 75% สูญเสีย ≥5 ตัวอักษร ประมาณ 50% สูญเสีย ≥10 ตัวอักษร และประมาณ 25% สูญเสีย ≥15 ตัวอักษรใน 2 ปี3)
Pachychoroid เป็นภาวะที่มีการขยายของหลอดเลือดคอรอยด์ ขนาดใหญ่ (pachyvessel) และเพิ่มการซึมผ่านของหลอดเลือดคอรอยด์ 1) จอประสาทตา อักเสบชนิดเซรุ่มส่วนกลาง (CSC ) เป็นโรค pachychoroid ที่เป็นตัวแทน และ MNV ที่เกิดขึ้นบนพื้นหลังของ CSC หรือ pachychoroid pigment epitheliopathy (PPE) เรียกว่า pachychoroid neovasculopathy (PNV ) ยีน CF H มีรายงานว่าเกี่ยวข้องกับการเกิด pachychoroid และ CSC เช่นกัน1)
Ribatti และคณะ (2024) รายงานว่าการสลายเมมเบรนของ Bruch โดย tryptase ที่หลั่งจากแมสต์เซลล์คอรอยด์ ทำให้เกิดการตายของ RPE และการปล่อย VEGF-A, FGF-2, IL-8 และ NGF ส่งเสริมการสร้างเส้นเลือดใหม่5)
MNV ชนิดไม่渗出ยังคงมีฤทธิ์ทางชีวภาพแม้ไม่มีอาการ และพื้นที่ของมันเพิ่มขึ้นอย่างต่อเนื่อง4)
Wang และคณะ (2023) ในการศึกษา SS-OCTA ใน 45 ตา รายงานว่า MNV ที่เติบโต (พื้นที่เพิ่มขึ้น ≥50%) มีระยะเวลาจนถึงการเปลี่ยนเป็นชนิด渗出สั้นกว่าอย่างมีนัยสำคัญเมื่อเทียบกับ MNV ที่ไม่เติบโต (13.60 เดือน เทียบกับ 31.11 เดือน, HR 12.51) และประวัติการสูบบุหรี่และภาวะไตรกลีเซอไรด์สูงสัมพันธ์กับการเติบโตอย่างมีนัยสำคัญ (P=0.021)4)
การฝ่อแบบจีโอกราฟิกมักเริ่มต้นรอบๆ รอยบุ๋มจอตา (fovea) และรอยบุ๋มจอตา จะมีความต้านทานต่อการฝ่อค่อนข้างมาก 3) สิ่งนี้ทำให้เกิดรูปร่างคล้ายเกือกม้าหรือวงแหวนของการฝ่อแบบจีโอกราฟิก ค่ามัธยฐานของเวลาที่การฝ่อถึงรอยบุ๋มจอตา คือ 2.5 ปี และในช่วงเวลานี้ การมองเห็น ความคมชัดสูงยังคงอยู่ แต่การทำงานทางการมองเห็น ในชีวิตประจำวัน เช่น ความไวต่อแสง ในที่มืดและความเร็วในการอ่าน จะถูกทำลายตั้งแต่เนิ่นๆ 8)
เนื้อหาต่อไปนี้อยู่ในขั้นตอนการวิจัยหรือการทดลองทางคลินิกในปัจจุบัน และไม่ใช่การรักษามาตรฐานที่สามารถรับได้ในโรงพยาบาลทั่วไป เป็นข้อมูลอ้างอิงสำหรับผู้เชี่ยวชาญเกี่ยวกับความก้าวหน้าทางการแพทย์ในอนาคต
ในปี 2023 ยายับยั้งคอมพลีเมนต์ สองชนิดสำหรับการฝ่อแบบจีโอกราฟิกได้รับการอนุมัติจาก FDA ในสหรัฐอเมริกา
เพกเซทาโคพลาน (SYFOVRE) : ยับยั้ง C3. 15 มก./0.1 มล. ฉีดเข้าแก้วตา ทุก 25–60 วัน การทดลอง OAKS (637 คน) และ DERBY (621 คน) แสดงให้เห็นการลดอัตราการเติบโตของการฝ่อแบบจีโอกราฟิกได้ถึง 21% 9) อาวาซินแคปแทด เพกอล (Izervay) : ยับยั้ง C5. 2 มก. ฉีดเข้าแก้วตา เดือนละครั้ง การทดลอง GAT HER 2 (448 คน) แสดงให้เห็นการลดอัตราการเติบโต 14–19%
อย่างไรก็ตาม ยาทั้งสองชนิดไม่แสดงความแตกต่างที่มีนัยสำคัญในการปรับปรุงการมองเห็น ซึ่งเป็นผลลัพธ์หลักที่กำหนดไว้ล่วงหน้า ทำให้เกิดปัญหา “การแยกตัวระหว่างโครงสร้างและการทำงาน” 3) 8) สำนักงานยาแห่งยุโรป (EMA) ปฏิเสธการอนุมัติเพกเซทาโคพลาน โดยเรียกร้องให้มีการพิสูจน์ประโยชน์ทางการทำงาน 8)
การทดลองระยะที่ III CHROMA (906 คน) และ SPECTR I (975 คน) ของยับยั้งแฟกเตอร์ D คอมพลีเมนต์ แลมพาลิซูแมบ ถูกยุติลงเนื่องจากไม่สามารถยับยั้งพื้นที่ GA ได้ การทดลอง SEATTLE (580 คน) ของยับยั้งวงจรการมองเห็น เอมิกซ์สแตท ก็ไม่แสดงประสิทธิผลเช่นกัน
ในการทบทวนของ Dinah และคณะ (2025) BCVA ไม่สามารถจับผลกระทบเชิงหน้าที่ของการฝ่อแบบจีโอกราฟิกได้อย่างเพียงพอ และแนะนำให้ใช้ไมโครเพอริเมทรี การมองเห็น ในที่แสงน้อย (LLVA) และความเร็วในการอ่านเป็นตัวชี้วัดแทน 8) การสร้างการประเมินเชิงหน้าที่แบบหลายรูปแบบที่ครอบคลุมจะเป็นกุญแจสำคัญสำหรับการทดลองทางคลินิกในอนาคต
อะฟลิเบอร์เซปต์ขนาดสูง (8 มก.) : การทดลอง PULSAR แสดงให้เห็นถึงความเป็นไปได้ในการฉีดโดยมีช่วงห่างสูงสุด 16 สัปดาห์ 2) คาดว่าจะช่วยลดภาระการรักษาการปลูกถ่ายที่ปล่อยรานิบิซูแมบ แบบต่อเนื่อง (ระบบนำส่งทางพอร์ต) : การทดลอง Archway รายงานว่าการเติมยาใหม่ทุก 24 สัปดาห์ให้ประสิทธิภาพเทียบเท่ากับการให้ยารายเดือน 2) ไบโอซิมิลาร์ ไบโอซิมิลาร์ ของรานิบิซูแมบ และอะฟลิเบอร์เซปต์หลายตัวได้รับการอนุมัติแล้ว 2)
Ji และคณะ (2025) รายงานกรณีของ AMD ชนิดแห้งที่ได้รับการบำบัดด้วยแสงชีวภาพ (แสงสีแดงถึงอินฟราเรดใกล้ 650–1300 นาโนเมตร) 6) ภายใน 8 เดือน พื้นที่ของดรูเซน ในตาขวาลดลง 58% และในตาซ้ายหายไป 100% การมองเห็น ดีขึ้นจาก 20/30 เป็น 20/20 ในทั้งสองตา การทดลองระยะที่ 3 Lightsite III ก็ยืนยันการลดปริมาตรดรูเซน และการมองเห็น ที่ดีขึ้นเช่นกัน
Chung & Kim (2022) รายงานว่าสารยับยั้ง MDM2 Nutlin-3a เป็นแนวทางใหม่ที่มีแนวโน้มในการกำจัดเซลล์ RPE ที่แก่ชราแบบเลือกสรร 7) การพัฒนาเซโนไลติกส์ที่จำเพาะต่อไมโตคอนเดรียจะเป็นความท้าทายในอนาคต
การบำบัดด้วยสเต็มเซลล์โดยใช้การปลูกถ่ายเซลล์ RPE อยู่ในขั้นตอนการวิจัย และมีการทดลองหลายรายการที่กำลังดำเนินอยู่ การบำบัดด้วยยีน ที่กำหนดเป้าหมายปัจจัยคอมพลีเมนต์ ก็กำลังถูกพิจารณาเช่นกัน
Q
ฉันควรตรวจยีนสำหรับโรคจอประสาทตาเสื่อมตามอายุหรือไม่?
A
ความหลากหลายทางพันธุกรรม เช่น CF H, ARMS 2 และ C3 เกี่ยวข้องกับความเสี่ยงในการเกิด AMD การตรวจสอบจีโนไทป์สามารถช่วยทำนายการพยากรณ์โรค เช่น การเกิดโรคในตาอีกข้างได้ 1) อย่างไรก็ตาม ในปัจจุบันยังไม่มีมาตรฐานแนวทางการรักษาตามการตรวจยีน 2) และไม่แนะนำให้ตรวจเป็นประจำ
AMD ชนิดฝ่อดำเนินไปอย่างช้าๆ แต่เมื่อจอประสาทตา ฝ่อลามถึงรอยบุ๋มจอตา การมองเห็น จะลดลงเหลือ 0.1 หรือน้อยกว่า รายงานระบุว่าค่ามัธยฐานของเวลาจนถึงภาวะตาบอดตามกฎหมาย (น้อยกว่า 20 ตัวอักษร ETDRS ) คือ 6.2 ปี 3) การวิเคราะห์ข้อมูลการทดลองแลมพาลิซูแมบพบว่า BCVA เฉลี่ยลดลงจาก 66 เป็น 57 ตัวอักษร (เทียบเท่าประมาณ 20/50 ถึง 20/80) ในระยะเวลา 2 ปี 3)
ยิ่งอัตราการเติบโตของจอประสาทตา ฝ่อเร็วเท่าใด BCVA ก็ยิ่งลดลงเร็วขึ้น โดยเฉพาะในตาที่มีรอยโรคเดี่ยวใต้รอยบุ๋มจอตา กลุ่มที่เติบโตเร็วที่สุดมีการลดลงประมาณ 4 บรรทัด (17.75 ตัวอักษร) ใน 2 ปี 3) ในทางตรงกันข้าม กลุ่มที่เติบโตช้าที่สุดมีการลดลงเพียง 1.69 ตัวอักษรใน 2 ปี แม้ว่ารอยบุ๋มจอตา จะยังคงอยู่ ความไวต่อแสง มืด ความไวต่อคอนทราสต์ และความเร็วในการอ่านจะบกพร่องตั้งแต่ระยะแรก ดังนั้นการพึ่งพาเพียงค่าการมองเห็น จะประเมินผลกระทบต่อการทำงานต่ำเกินไป 8)
นอกจากนี้ ยังมีความน่าจะเป็นที่แน่นอนที่จะเกิด MNV และเปลี่ยนเป็น AMD ชนิด neovascular ซึ่งทำให้การมองเห็น ลดลงอย่างรุนแรงมากขึ้น
การควบคุม MNV ด้วยยาต้าน VEGF ช่วยปรับปรุงการพยากรณ์โรคทางสายตาอย่างมีนัยสำคัญ ในการศึกษา CATT ที่ติดตามผล 5 ปี พบว่า 50% ของดวงตามีการมองเห็น 20/40 หรือดีกว่า 11) อย่างไรก็ตาม หากปล่อยไว้ไม่รักษา ประมาณ 90% ของกรณีจะมีการมองเห็น ลดลงเหลือ 0.1 หรือน้อยกว่า และทิ้งรอยแผลเป็นชนิดพังผืดหรือฝ่อไว้ที่จอประสาทตา ในกรณีที่มีเลือดออกมากจาก MNV อาจทำให้เกิดข้อบกพร่องของลานสายตากว้าง รวมถึงตาบอดสนิทหรือความบกพร่องทางการมองเห็น ที่รุนแรงมากขึ้น
MNV ไม่สามารถรักษาให้หายขาดได้ และหากไม่ได้รับการรักษาที่เหมาะสมและการจัดการระยะยาว อาจทำให้การมองเห็น ลดลงอย่างถาวรได้ง่าย 1) แม้ว่ากิจกรรมของ MNV จะสงบลงชั่วคราว แต่ก็อาจกลับมาเป็นซ้ำในระยะยาว และเมื่อมีการรั่วซึมซ้ำๆ จะเกิดการเปลี่ยนแปลงแบบฝ่อหรือแผลเป็นพังผืด ควรระลึกไว้เสมอว่า MNV เกิดขึ้นในดวงตาข้างตรงข้ามด้วยอัตราที่สูง ดังนั้นการรักษาต่อเนื่องและการติดตามอย่างสม่ำเสมอจึงเป็นสิ่งจำเป็น 1) แนะนำให้ดูแลผู้ที่มีสายตาเลือนรางอย่างจริงจังสำหรับผู้ป่วยที่มีความบกพร่องทางการมองเห็น อย่างรุนแรง
日本網膜硝子体学会 新生血管型加齢黄斑変性診療ガイドライン作成ワーキンググループ. 新生血管型加齢黄斑変性の診療ガイドライン. 日眼会誌. 2024;128(9):680-696.
Flaxel CJ, Adelman RA, Bailey ST, et al. Age-Related Macular Degeneration Preferred Practice Pattern. Ophthalmology. 2024;131(8):S1-S50.
Anegondi N, Steffen V, Sadda SR, et al. Visual loss in geographic atrophy: learnings from the lampalizumab trials. Ophthalmology. 2025;132(4):420-430.
Wang Y, Sun J, Wu J, et al. Growth of nonexudative macular neovascularization in age-related macular degeneration: an indicator of biological lesion activity. Eye (Lond). 2023;37(10):2048-2054.
Ribatti D, Dammacco R. Mast cells in human choroid and their role in age-related macular degeneration (AMD ). Clin Exp Med. 2024;24(1):98.
Ji PX, Pickel L, Berger AR, Sivachandran N. Improvement in dry age-related macular degeneration with photobiomodulation. Case Rep Ophthalmol. 2025;16(1):155-162.
Chung H, Kim C. Nutlin-3a for age-related macular degeneration. Aging (Albany NY). 2022;14(14):5613-5616.
Dinah C, Esmaeelpour M, Rachitskaya AV, De Salvo G, Munk MR. Functional endpoints in patients with geographic atrophy: what to consider when designing a clinical trial. Surv Ophthalmol. 2025. doi:10.1016/j.survophthal.2025.02.004.
Heier JS, Lad EM, Holz FG, et al. Pegcetacoplan for the treatment of geographic atrophy secondary to age-related macular degeneration (OAKS and DERBY): two multicentre, randomised, double-masked, sham-controlled, phase 3 trials. Lancet. 2023;402:1434-1448.
Khanani AM, Kotecha A, Chang A, et al. TENAYA and LUCERNE: two-year results from the phase 3 neovascular age-related macular degeneration trials of faricimab. Ophthalmology. 2024;131:914-926.
Martin DF, Maguire MG, Ying GS, et al; CATT Research Group. Ranibizumab and bevacizumab for neovascular age-related macular degeneration. N Engl J Med. 2011;364:1897-1908.