裂孔性視網膜剝離是一種眼科急症 ,液化的玻璃體 經由視網膜裂孔 進入視網膜 下腔,導致神經視網膜 與色素上皮分離。
年發生率為每1萬人1~1.5例。近視 (占病因40%~80%)、格子狀變性 、玻璃體 後剝離是主要危險因子。
飛蚊症 與閃光感突然加劇,或視野缺損 (窗簾感),是需要緊急就醫的徵兆。診斷基於散瞳 下間接眼底鏡檢查與鞏膜 壓迫。Shafer徵(前部玻璃體 中的菸草塵樣色素)強烈暗示存在視網膜裂孔 。
手術(鞏膜扣帶術 、玻璃體切除術 、氣體視網膜復位術 )是唯一的根治療法。首次手術復位率超過90%,多次手術可達98%。
黃斑部 剝離會導致不可逆的感光細胞 變性。黃斑 前剝離的緊急手術決定視力 預後。增殖性玻璃體視網膜病變 (PVR )是最大的併發症,選擇合適的手術方式並避免過度凝固是預防的關鍵。 裂孔性視網膜剝離(Rhegmatogenous Retinal Detachment; RRD)是指視網膜 上形成裂孔,液化的玻璃體 進入視網膜 下腔,導致神經視網膜 (感覺視網膜 )從視網膜色素上皮 (RPE )層剝離的病理狀態。rhegmatogenous一詞源自希臘語「裂口」。
視網膜剝離 有三種類型。裂孔源性視網膜剝離 (RRD)最為常見,需與牽引性視網膜剝離 (TRD:增殖膜 引起的機械性牽引)和滲出性視網膜剝離 (ERD:脈絡膜 及視網膜 血管滲出的液體積聚)區別。本文主要介紹裂孔源性視網膜剝離 。
滲出性視網膜剝離 不伴有裂孔,其特徵是體位改變時剝離部位移動(shifting fluid)。治療以原發疾病治療為主,與裂孔源性視網膜剝離 根本不同。
滲出性網膜剥離
血液網膜関門の破綻による非裂孔原性網膜剥離の病態と治療
通過封閉裂孔進行修復的概念由Jules Gonin在1920年代確立。在此之前,治癒率低於5%,但Gonin的燒灼術(熱凝固)將其提高到30–60%。後續發展如下:
1949年 :Ernst Custodis報告了聚乙烯醇鞏膜扣帶術 1950年代 :Charles Schepens推廣了矽橡膠材料、間接檢眼鏡和冷凍凝固 術,奠定了鞏膜扣帶術 的基礎Harvey Lincoff :建立了裂孔位置估計的Lincoff法則1960年代後期 :Robert Machemer開發了閉合式玻璃體切除術 (PPV )2002年起 :25G微切口玻璃體 手術(MIVS)出現,近年來27G超小切口也在推進
目前首次手術復位率超過90%,多次手術可達98%。
發生率 :每年每1萬人中1~1.5人(0.01~0.015%)2) 雙眼性 :約10%家族內發生 :約20%年齡分布 :雙峰型。20歲左右為高峰(格子狀變性 內萎縮性圓孔引起的扁平剝離)和50歲左右為高峰(急性玻璃體 後剝離伴瓣狀裂孔 引起的高聳剝離)與近視 的關聯 :近視 占病因的40%~80%發生率增加趨勢 :德國登記數據顯示年發生率從15.6/10萬增加到24.8/10萬,背景因素包括人口老化、近視 人口增加和白內障 手術數量增加 2) 白內障 術後風險白內障手術史 。術後RRD風險約為0.21%(約1/500),隨著手術方式的改進呈下降趨勢 2) 外傷性 :約佔所有RRD的10%,好發於年輕男性2) 黃斑裂孔 性視網膜剝離 高度近視 女性,約佔所有視網膜剝離 病例的5%(高於歐美的0.5%~2.0%)
Q
裂孔原性視網膜剝離有多罕見?
A
每年每1萬人中約有1~1.5人發病,是一種相對罕見的疾病。但在近視 人口較多的地區或族群中,發病數有增加趨勢。約10%的患者雙眼發病,因此單眼手術後的患者需定期觀察對側眼。
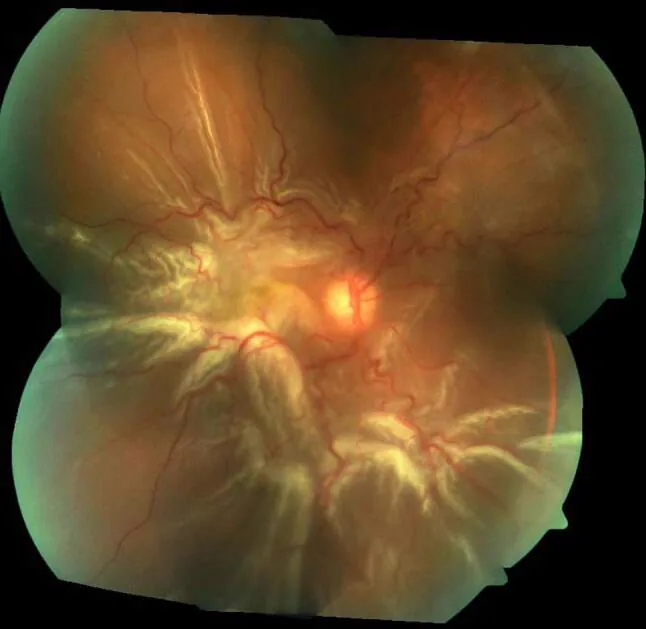
裂孔原性視網膜剝離的眼底照片。可見廣泛的剝離視網膜及由PVR引起的星狀皺褶。 Xiong J, et al. A review of rhegmatogenous retinal detachment: past, present and future. Wien Med Wochenschr. 2025. Figure 3. PM
CI D: PMC12031774. License: CC BY.
飛蚊症 玻璃體 剝離導致的玻璃體混濁 。約6%的飛蚊症 患者存在視網膜裂孔 。急劇增加或出現新形狀需注意。閃光感 :由玻璃體 牽拉視網膜 引起。在暗處增強,閉眼時也可出現,眼球運動可誘發。閃光感出現在裂孔對側,因此詢問發生部位有助於推測病因裂孔的位置。視野缺損 青光眼 進展或眼瞼下垂 混淆。視力 下降和視物變形視網膜剝離 累及黃斑 時出現。
眼壓 脈絡膜 剝離時降低更明顯。Schwartz症候群 :伴有眼壓 升高的視網膜剝離 。由剝離視網膜 脫落的視細胞外節堵塞小樑網引起。Shafer’s sign :前部玻璃體 內漂浮的菸草塵樣色素(來自視網膜色素上皮 細胞)。是強烈提示裂孔發生的重要所見。前房 所見
瓣狀裂孔(馬蹄形裂孔)
由玻璃體 牽引引起的視網膜 撕裂。視網膜 瓣呈馬蹄形。
中老年人後玻璃體 剝離時,好發於顳上象限(60%) 。易引起高聳的視網膜剝離 。
伴有蓋膜的圓孔
由玻璃體 牽引導致裂孔瓣完全脫離而形成。脫離的瓣膜(operculum)漂浮在玻璃體 內。
由於牽引解除,進展較慢。但液化玻璃體 容易通過擴大的孔流入。
萎縮性圓孔
由格子狀變性 內視網膜 的萎縮性變化引起。不伴有蓋膜(operculum)。
多見於年輕人、女性和高度近視 。由於不伴有玻璃體 牽引,進展通常緩慢。
裂孔的好發部位是視網膜 周邊部,佔全部病例的2/3。按象限分:顳上方60%,顳下方15%,鼻上方15%,鼻下方10%。
Q
出現閃光感時應立即就醫嗎?
A
閃光感是後玻璃體 剝離引起的視網膜 牽拉徵象,可能是裂孔形成的前驅症狀。特別是與飛蚊症 同時出現或伴有視野缺損 時,建議當天就診。急性PVD 症狀就診的患者中5.4%~8%發現視網膜裂孔 ,伴有玻璃體出血 時2/3可發現裂孔。2)
裂孔性視網膜剝離的發生需要兩個絕對條件:(1)視網膜 存在孔洞,(2)玻璃體 液化。視網膜 出現孔洞需要視網膜 有變薄的變性灶,或玻璃體 牽引及眼球受到強外力作用。
近視 近視 (-1~-3D)風險增加約4倍,超過-3D風險增加約10倍。2) 主要機制是眼軸 延長導致周邊視網膜 變薄。格子狀變性 視網膜剝離 患者眼中約占30%。2) 參與所有RRD病例的20-30%。有症狀的馬蹄形裂孔 未經治療至少半數會進展為RRD,但雷射光凝固 可將其抑制到5%以下。無症狀馬蹄形裂孔 自然病程中RRD轉化率約為5%。2) 後玻璃體 剝離(PVD ) :急性PVD 伴隨的玻璃體 牽拉是瓣狀裂孔 形成的主要機轉。在老年人中作為生理性變化發生。約88%伴有玻璃體出血 的患者裂孔位於上方象限。2) 白內障手術史 白內障手術史 。2) 術後RRD風險約為0.21%,後囊膜Nd:YAG雷射切開後風險增加約4倍。2) 外傷 :占所有RRD病例的約10%。2) 多見於年輕男性,是鋸齒緣 斷裂和巨大裂孔的主要原因。對側眼病史 :約10%的病例出現雙眼發病。遺傳性結締組織疾病 :Stickler症候群、Marfan症候群和Ehlers-Danlos症候群需注意早期發病和嚴重化。Stickler症候群推薦360°預防性雷射光凝固 。2)
以下高風險的視網膜裂孔 是預防性雷射視網膜光凝固術 的積極對象。
有飛蚊症 或光視症 等自覺症狀的視網膜裂孔
視網膜剝離 對側眼發生的視網膜裂孔 無水晶體 眼、人工水晶體 植入眼或白內障 手術前的視網膜裂孔
有視網膜剝離 家族史的視網膜裂孔
格子狀變性 預防性治療的危險因子:①對側眼有視網膜剝離 病史,②無水晶體 眼或人工水晶體 眼,③高度近視 伴有嚴重格子狀變性 ,④視網膜剝離 家族史,⑤合併馬凡症候群、Stickler症候群或Ehlers-Danlos症候群。
雷射光凝固 條件:從0.2秒、150 mW、200 μm開始逐漸增加功率,達到厚白色程度的凝固斑。對於格子狀變性 ,使用三面鏡或廣角倒像接觸鏡,用23排無間隙的凝固斑包圍病灶(凝固大小400500 μm)。
Q
近視的人都會發生視網膜剝離嗎?
A
近視 是RRD的最大危險因子,但發生率為人口的0.010.015%,即使有近視 ,大多數人也不會發病。但高度近視 (-6D以上)合併格子狀變性 的比例較高,格子狀變性 內的萎縮性圓孔進展為RRD的報告為0.30.5%。定期眼底檢查 尤為重要。
診斷透過使用間接檢眼鏡、前置鏡或三面鏡的裂隙燈 顯微鏡進行眼底檢查 ,確認剝離的視網膜 和引起剝離的裂孔。裂隙燈 顯微鏡同時觀察玻璃體 ,評估是否有後玻璃體 剝離以及裂孔處的玻璃體 牽引。是否波及黃斑部 會影響術後視力 預後,因此必須確認。
在門診檢查中,使用雙眼間接檢眼鏡進行鞏膜 壓迫檢查最為有用。鑑別真性裂孔和假性裂孔、評估裂孔周圍有無視網膜下液 以及剝離範圍,對制定治療方針至關重要。
病史詢問中以下資訊對診斷和治療方針制定很重要:2)
閃光感和飛蚊症 的有無及出現時間
視野缺損 的有無和範圍(簾幕感的方向)近視 的有無和程度眼手術史(白內障 手術、Nd:YAG雷射後囊切開術)
外傷史
家族史(RRD、Stickler症候群)
OCT (光學同調斷層掃描 )黃斑部 細微剝離。有助於與視網膜 分裂症鑑別及確認黃斑 下液是否存在。2) 也用於預測術後視力 預後。B超 音波掃描玻璃體出血 等混濁介質時必不可少。可評估剝離範圍、形態及增殖膜 。2)
根據剝離形態估計病因裂孔位置的實用法則。
剝離形態 預測裂孔位置 準確率 耳側或鼻側的上方剝離 在較高邊界1.5個鐘點以內 98% 越過12點向兩側下降的上方剝離 在12點頂點的三角形內 93% 下方視網膜剝離 裂孔位於較高邊界側 95% 下方水泡性視網膜剝離 源自上方裂孔 —
視網膜 分裂症(Retinoschisis)視網膜 層間分離。OCT 顯示內層與外層的雙層結構。若外層無穿孔,則不會發生剝離。滲出性視網膜剝離 Vogt-小柳-原田病 、脈絡膜 腫瘤等)很重要。牽引性視網膜剝離 糖尿病視網膜病變 等。脈絡膜 剝離眼壓 降低時。超音波檢查可見增厚的脈絡膜 剝離。
Q
僅靠眼底檢查就能診斷嗎?
A
倒像鏡による散瞳 眼底検査が診断の基本であるが、硝子体出血などで眼底透見が不良な場合はBスキャン超音波が必須となる。また黄斑部の微細な剥離はOCT による補助が有用である。裂孔の完全な同定のために強膜圧迫法を組み合わせた全周検査が推奨される。
網膜剥離は緊急的な手術治療が原則である。治療の必須条件は裂孔の完全閉塞であり、裂孔が残存すると再剥離を生じる。初回手術で90%以上が、複数回の手術で98%が復位する。
術後視力 は術前の黄斑部剥離の有無・剥離期間に大きく左右される。黄斑部が既に剥離している症例では可及的速やかに手術を予定する。適切な時期に手術を行えば95%以上が治癒するが、網膜復位後の視力 は約半数が0.5以下であり、視野欠損や歪視症が残ることも多い。
Cochrane系統的レビューおよびメタ解析では、硝子体手術(PPV )と強膜バックリング術(SB)の解剖学的・視力 転帰に有意差はなく(低〜極めて低いエビデンス)、術式選択は個々の症例の特性に基づいて判断する。2)
當黃斑部 剝離時,感光細胞 開始發生不可逆的變性。黃斑 未剝離型視網膜剝離 術後2個月,73%的患者矯正視力 達到0.5以上。黃斑 剝離型中約半數視力 停留在0.5以下。
術前體位保持可抑制液體流入黃斑部 :
上方泡狀剝離 → 仰臥位(頭低腳高位)
下方剝離 → 坐位
根據年齡、有無後玻璃體 剝離、裂孔的位置和大小等選擇術式。
年輕患者的萎縮性圓孔 :鞏膜扣帶術 (鞏膜 入路)為首選中老年患者的瓣狀裂孔 :玻璃體 手術(玻璃體 入路)為主合併難治性PVR :需要矽油 填充局限性上方裂孔 :門診氣體視網膜復位術 也是一種選擇
這是一種眼外手術,將矽膠扣帶縫合固定在眼球外側的鞏膜 上,使眼球壁向內壓陷,從而封閉裂孔。
適應症 :
年輕患者、有水晶體 眼、單純性RRD
裂孔侷限於周邊部
可保留水晶體 的病例
手術流程 :
結膜 切開及外眼肌暴露冷凍凝固 :對裂孔邊緣和變性區域進行最小限度的凝固。避免過度凝固,因其可能促進PVR 。鞏膜 扣帶的選擇與放置:局部扣帶(單一裂孔)或環扎帶(多發裂孔或合併PVR 病例)
扣帶材料 形狀 主要用途 矽膠海綿 局部隆起型 單一/局部裂孔 矽膠帶 帶狀/環狀 環紮/360°環紮扣 矽膠輪胎 寬帶狀 大範圍裂孔、格子狀變性
引流視網膜下液 (必要時):當有大量視網膜下液 時,透過部分鞏膜 切開引流。也可選擇非引流法,併發症風險較低。
氣體注入(必要時):使用SF₆或C₃F₈進行額外內部填塞。
結果 :初次解剖復位率超過90%。在有水晶體 眼中,視力 結果可能優於玻璃體 手術,5, 6) 在黃斑 未剝離型中,有報告顯示SB的結果顯著較好。6)
主要併發症 :再剝離、PVR 、SINS(鞏膜 扣帶引起的感染、壞死、暴露)、4) 屈光 改變(近視 化)、眼球運動障礙 /複視 。
適應症 :
方法 :玻璃體 切除後封閉裂孔,使用氣體(20% SF₆、14% C₃F₈)或矽油 進行眼內填充。
成績 :初次解剖復位率與鞏膜扣帶術 相當。2) 缺點是加速白內障 進展,對於有水晶體 眼的年輕患者需謹慎適應。
黃斑 未剝離型術中黃斑 保護黃斑 未剝離的病例中,術中黃斑 保護尤為重要。
使用帶閥套管針防止術中眼壓 波動
避免通過大的開放性裂孔使灌注液流入視網膜 下
如果存在泡狀剝離,先通過引流性視網膜 切開術減少視網膜下液
在後極部放置全氟碳液體(PFCL),防止液體向中心凹下移動
在完全氣液交換前充分引流視網膜下液 (引流不充分可能引起黃斑 剝離)
蒸汽滾筒法 :在黃斑 附近的泡狀剝離中,通過將氣體滾過黃斑 來防止醫源性黃斑 剝離的技術。這是黃斑 未剝離型RRD中獨特的術中管理方法。
這是一種門診處置,將膨脹性氣體注入玻璃體 內,利用氣體的浮力封閉裂孔,然後以冷凍凝固 或光凝固使裂孔周圍形成疤痕。
適應症:
裂孔位於上方(10點至2點方向)120–180°範圍內的RRD
瓣狀裂孔 (單一或鄰近的簇狀裂孔)PVR B級或以下能夠維持術後姿勢的患者
氣體的種類與特性 :
氣體 注入量 膨脹倍率 眼內滯留時間 SF₆(六氟化硫) 0.5~0.6 mL 約2倍 約2週 C₃F₈(八氟丙烷) 0.3 mL 約4倍 約8週
操作流程:
散瞳 和表面麻醉(或球後麻醉 )凝固治療(先行冷凍凝固 或在氣體注入後進行光凝)
前房穿刺 :用27–30G針排出0.2–0.4 mL房水 氣體注入:從顳側睫狀體 平坦部(有晶狀體眼在角膜緣 後4 mm)注入
檢查眼壓 和血流:確認視網膜 中央動脈血流。如果搏動消失持續數分鐘,則再次減壓
體位指導:保持氣體位於裂孔部位5–8天
PIVOT試驗(PR與PPV 的隨機對照試驗)結果:
評估指標 氣體網膜復位術(PR)組 玻璃體切除術 (PPV )組初次復位率 80.8% 93.2% 最終復位率 98.7% 98.6% 術後視力 (6個月) 78.4±12.3個字母 68.5±17.8個字母 白內障 手術(12個月,有水晶體 眼)16% 65%
最終復位率幾乎相同,PR組在術後視力 和較少視物變形方面較優。
主要併發症 :視網膜 下氣體迷入(魚卵現象)、10) 新裂孔形成、視網膜中央動脈阻塞 、白內障 進展。
這是一種不進行引流的節段性鞏膜扣帶術 ,據報導適用於約90%的裂孔性視網膜剝離。良好結果報告:初次復位率91%,再次手術後97.4%,PVR 發生率0.9%。
禁忌症如下:
位於不同緯度的多個裂孔
後極部裂孔
超過70°的廣泛剝離
巨大裂孔
C2以上之PVR
術式 主要適應症 初次復位率 特點 鞏膜扣帶術 年輕、萎縮性裂孔 、單純RRD 90%以上 保留水晶體 、眼外手術 玻璃體 手術複雜、多裂孔、PVR 約90% 廣泛適用、加速白內障 氣體視網膜復位術 上方侷限性裂孔 80.8% 門診、體位限制、視力 良好 Lincoff-Kreissig法 約90%的RRD 91% 非引流、微創
根據增殖性玻璃體視網膜病變 (PVR )的嚴重程度選擇手術方式。
A級、B級、輕度C級 :通常可透過鞏膜扣帶術 治療視網膜 固定皺襞位於裂孔附近或後極的病例、深部裂孔玻璃體 手術填充材料 :20% SF₆、14% C₃F₈或矽油
眼内ガス残存中の航空機搭乗・急速な高所移動は禁忌。気圧変化でガスが膨張し眼圧が急上昇して中心網膜動脈閉塞を起こす危険がある。SF₆では注入後約2週間、C₃F₈では約8週間が禁忌期間の目安。
黄斑部剥離がある場合は待機せず早急に手術を予定する。
全身麻酔を受ける場合は眼内ガスの存在を必ず麻酔科医に伝えること。亜酸化窒素(笑気)はガスを膨張させるため禁忌となる。
Q
手術後の視力はどの程度回復するか?
A
初回手術で90%以上が解剖学的に復位するが、術後視力 は約半数が0.5以下であり、視野欠損や歪視症が残ることも多い。視力 予後を決定する最大因子は黄斑部剥離の有無と持続期間である。黄斑剥離前の早期手術では視力 予後が良好だが、黄斑剥離後でも早期手術ほど良好な転帰が期待できる。
Q
玻璃體手術與鞏膜扣帶術哪個比較好?
A
在有水晶體 眼的單純性RRD(尤其是年輕患者)中,鞏膜扣帶術 可能獲得較佳的視力 結果。2, 5, 6) 對於高度PVR 或伴有後極部裂孔的複雜性RRD,則選擇玻璃體 手術。手術方式的選擇需綜合考量裂孔的性質、位置、PVR 嚴重程度、患者背景以及術者的熟練程度。
裂孔源性視網膜剝離 的發生條件包括:(1)視網膜 存在裂孔;(2)玻璃體 液化。
瓣狀裂孔 的形成玻璃體 剝離引起的玻璃體 牽拉集中在格子狀變性 或玻璃體 視網膜 強附著區域。存在格子狀變性 或玻璃體 視網膜 強附著部位時,會導致裂孔形成。好發於顳上象限(60%)。
萎縮性裂孔 的形成玻璃體 牽引的情況下,由格子狀變性 區域內的視網膜 變薄和壞死形成。多見於年輕人、女性和高度近視 者。由於發生在後玻璃體 剝離之前,玻璃體 仍附著,進展通常緩慢。
發生視網膜剝離 時,感光細胞 和視網膜色素上皮 細胞分離,脈絡膜 的氧氣和營養供應受阻。早期即出現感光細胞 外節的變性和脫落,逐漸導致不可逆性變性。
視網膜下液 向黃斑部 進展的主要因素如下。
重力 :上方裂孔的液體因重力易向黃斑部 移動。下方剝離時,重力會延遲黃斑 受累。眼球運動的慣性力 :掃視(快速眼球運動)對裂孔邊緣施加牽拉力,促進液體流入。這是術前休息有效的理論依據。玻璃體 液化程度玻璃體 容易流入,導致大泡性視網膜剝離 快速進展。年輕人玻璃體 呈凝膠狀,流入緩慢,常形成淺層剝離。
不進行引流而僅透過鞏膜 扣帶使視網膜 復位的機制如下。
眼壁和視網膜 向中央移動減少玻璃體 視網膜 牽拉
視網膜下液 從扣帶位置移動(重新分佈到眼底周邊部)術後扣帶高度增加帶來的進一步效果
裂孔與相鄰玻璃體 凝膠的接近
增加對通過裂孔的流體流動的阻力
PVR 是RRD術後最常見的併發症,定義為由視網膜 前和視網膜 下增殖膜 形成引起的牽引性再剝離。
機制:視網膜剝離 →血-視網膜屏障 破壞→RPE 細胞、膠質細胞和巨噬細胞進入玻璃體 腔→細胞因子(如TGF-β)刺激→細胞上皮-間質轉化和增殖→收縮性膜形成→再剝離。
RPE 細胞轉化為成纖維細胞樣細胞,產生膠原蛋白,形成膜狀或索狀增殖組織。舊的PVR 嚴重程度分類(視網膜 學會1983年)如下。
A級 :玻璃體混濁 、玻璃體 中色素塊、視網膜 上色素塊B級 :視網膜 表層皺褶形成、視網膜 血管迂曲、裂孔邊緣翹起、玻璃體 活動性降低C級 :視網膜 全層皺褶(C-1:1個象限,C-2:2個象限,C-3:3個象限)D級 :4個象限的視網膜 全層皺褶(D-1:寬漏斗,D-2:窄漏斗,D-3:閉合漏斗)
1991年的Machemer新分類考慮了前部PVR 和視網膜 下病變,並以時鐘方位描述病變範圍。
Arndt等人(2023)針對73名非糖尿病RRD患者和64名ERD患者的研究報告指出,RD眼的玻璃體 內葡萄糖濃度(2.28 mmol/L)顯著高於ERM 眼(1.60 mmol/L)(p<0.0001)。1) 玻璃體 內葡萄糖與巨噬細胞密度顯著相關(p=0.002),也與RD範圍相關(r=0.38)。與術後中心凹厚度(MFT)呈負相關(r=-0.51),上皮細胞密度與PVR -C分級之間存在顯著相關性(p=0.002)。1) 也有假說認為,晚期糖基化終產物(AGE)引起的膠原交聯參與玻璃體 硬化。1)
Arndt等人(2023)的數據表明,胰島素可能對視錐細胞 起到保護作用。1) 基於RD眼高糖環境加劇光感受器損傷的假說,通過代謝介入改善視力 預後已成為研究課題。
德國登記數據顯示,年發生率從每10萬人15.6例增加到24.8例,老齡化、近視 人口增加和白內障 手術數量增多被認為是背景因素。2) 隨著手術方式的改進,白內障 術後RRD風險已降至0.21%。2)
對未治療ROP 病史眼的長期觀察發現,18歲以下者18.4%、19-30歲者35.1%出現視網膜裂孔 。3) 主要機製是後玻璃體 剝離前玻璃體 視網膜 的強附著,視網膜剝離 病例的再手術率高達36%。根據兒童和青少年基礎疾病優化手術策略是一個挑戰。3)
此技術結合廣角觀察系統與吊燈照明,以彌補傳統手術視野受限的不足。7) 統合分析顯示,視力 與解剖成功率與傳統方法相當,且手術時間縮短。9)
術後光感受器重新排列可能影響功能預後,目前正作為解釋鞏膜扣帶術 與玻璃體切除術 後視功能差異的因素進行研究。6)
對於RRD修復後發生的囊樣黃斑水腫 (CME ),正在研究地塞米松緩釋植入物等新型治療方法。8)
Ahmed Iら(2025)は、RRD修復後にドルーゼンが消失した83歳女性の1例を報告した。11) 機序として網膜下液の溶解および局所炎症応答の関与が示唆されている。
ガス注入による硝子体黄斑牽引(VMT )や黄斑円孔の非手術的解除を目指す研究段階の手技である。
RCOphth iFTMH Guideline(2025年版)では、pneumatic vitreolysisによる黄斑円孔閉鎖率は47.8%、黄斑円孔の新規発生率は5.3%と報告されている。12)
AAO ERM /VMT PPP(2019)が引用するDRCR無作為化比較試験では、C₃F₈による硝子体黄斑牽引解除率が78% vs 9%(偽手術群)であったが、安全性上の懸念により試験は早期中止となっている。13) 現時点では適応が限定的であり、標準治療には至っていない。
Al-Saleh等人(2025)對創傷性黃斑 未剝離的RRD使用SF₆氣體進行氣體視網膜復位術 ,在24小時內達成復位,最終視力 為20/40。14) 這表明在適當選擇病例的情況下,該術式對創傷性RRD也可能有效。
Dean等人(2023)報告了一例玻璃體 手術聯合鞏膜扣帶術 後2-3週出現發炎加重、角膜 後沉著物和玻璃體混濁 的病例。15) 透過增加類固醇 和全身使用NSAIDs後改善,表明HLA-B27檢測對術後遷延性發炎的鑑別診斷有用。
Au Eong等人(2024)報告了一例照片記錄持續30年的特發性黃斑裂孔 合併急性黃斑 在位RRD的病例,透過PPV 聯合ILM 剝離和C₃F₈填充同時實現了復位和裂孔閉合。16) 儘管由於長期光感受器損傷,視力 改善有限(仍為6/45),但該報告因展示了同期手術的可能性而受到關注。
3D手術顯微鏡 :優點包括減輕術者姿勢負擔、共享視野、便於影像記錄27G系統(外徑0.36mm) :減少術後散光 和傷口閉合問題眼內內視鏡 :擴大角膜 混濁、瞳孔 散大不良病例的適應症
Arndt C, Hubault B, Hayate F, et al. Increased intravitreal glucose in rhegmatogenous retinal detachment. Eye (Lond). 2023;37(4):638-643. doi:10.1038/s41433-022-01968-w.
American Academy of Ophthalmology. Posterior Vitreous Detachment, Retinal Breaks, and Lattice Degeneration Preferred Practice Pattern. San Francisco, CA: American Academy of Ophthalmology; 2024.
Hamad AE, Moinuddin O, Blair MP, et al. Late-Onset Retinal Findings and Complications in Untreated Retinopathy of Prematurity. Ophthalmol Retina. 2020;4(6):602-612. doi:10.1016/j.oret.2019.12.015.
Jayallan B, Goswami P, Bhakat A. Rhegmatogenous retinal detachment in anterior scleritis associated with ulcerative colitis: a case report. Cureus. 2024;16(6):e61819.
Ferro Desideri L, Bonfiglio V, Russo A, et al. Scleral buckling: a review of clinical aspects and current concepts. J Clin Med. 2022;11(2):314.
Cruz-Pimentel M, Huang CY, Wu L. Scleral buckling: a look at the past, present and future in view of recent findings on the importance of photoreceptor re-alignment following retinal re-attachment. Clin Ophthalmol. 2022;16:1971-1984.
Genovese L, Crisafulli C, Mancuso S, et al. Chandelier-assisted scleral buckling: a literature review. Vision (Basel). 2023;7(3):47.
Bernardi E, Shah N, Ferro Desideri L, et al. Cystoid macular edema following rhegmatogenous retinal detachment repair surgery: incidence, pathogenesis, risk factors and treatment. Clin Ophthalmol. 2025;19:629-639.
Ziafati M, Mirshahi R, Sanadgol N, et al. Functional outcome of chandelier-assisted scleral buckling in rhegmatogenous retinal detachment: a systematic review and meta-analysis. J Curr Ophthalmol. 2025;37:172-182.
Wang JC, Tang WM, Eliott D. Management of large subretinal gas bubble after pneumatic retinopexy with head-positioning maneuver. J VitreoRetin Dis. 2022;6(2):167-170.
Ahmed I, Wu DM. Drusen Disappearance After Retinal Detachment Repair. J VitreoRetin Dis. 2025;9(1):109-112. doi:10.1177/24741264241276603.
Royal College of Ophthalmologists. Idiopathic Full Thickness Macular Holes. Clinical Guideline. London: RCOphth; 2025. Available from: https://www.rcophth.ac.uk/resources-listing/idiopathic-full-thickness-macular-holes/
American Academy of Ophthalmology. Epiretinal Membrane and Vitreomacular Traction Preferred Practice Pattern. San Francisco, CA: American Academy of Ophthalmology; 2019.
Al-Saleh A, Al-Otabi A, Al-Shammari Y, et al. Successful management of macula-sparing retinal detachment following blunt ocular trauma using pneumatic retinopexy. Cureus. 2025;17(6):e85709.
Dean J, McTavish S, Feng Y, et al. Persistent inflammation associated with HLA-B27 after pars plana vitrectomy with scleral buckle placement. J VitreoRetinal Dis. 2023;7(6):557-561.
Au Eong JTW, Lim JHM, George SM, et al. Successful anatomical closure of a photographically documented 30-year-old idiopathic full-thickness macular hole following surgery for concurrent repair of an acute macula-on rhegmatogenous retinal detachment. J Surg Case Rep. 2024;4:rjae231.