早期表現
視神經乳頭炎(papillitis):輕度視神經盤水腫、充血。
玻璃體炎:輕度至中度玻璃體混濁(約grade 1)1)。
聚集的灰白色視網膜下病灶:呈簇狀分布的多發白點1)。
移動性視網膜下軌跡:線蟲移動的痕跡。在91.7%的病例中可觀察到1)4)。
血管炎:視網膜血管周圍的炎症表現1)4)。

瀰漫性單側亞急性視神經視網膜炎(Diffuse Unilateral Subacute Neuroretinitis; DUSN)是由線蟲在視網膜下腔移動所引起的多灶性脈絡視網膜炎。1978年Gass等人首次報告,最初也被稱為「單側抹除症候群」3)。好發於健康的兒童及年輕成人1),典型表現為單側,但也有雙側發病的報告3)。
已知有多種線蟲可致病,根據蟲體大小及推測的流行地區進行分類。
| 蟲種 | 體長參考 | 主要流行區域 |
|---|---|---|
| Baylisascaris procyonis | 1500〜2000 μm | 美國中西部・北美 |
| Toxocara canis | 400〜1000 μm | 美國東南部・熱帶地區 |
| Ancylostoma caninum | 400〜1000 μm | 熱帶・亞熱帶 |
| Gnathostoma spinigerum | 400〜1000 μm | 亞洲(泰國等) |
流行區域廣泛,包括美國中西部及東南部、巴西、加勒比海群島、印度、馬來西亞等地。據報導,馬來西亞的土壤傳播性線蟲(STH)盛行率達52%至76%4)。
雖然典型表現為單側,但也有雙側發病的報告3)。若一眼治療延遲或免疫狀態不佳,可能波及對側眼。但雙眼同時發病罕見,若一眼所見與另一眼不對稱,則需考慮DUSN並進行詳細檢查。
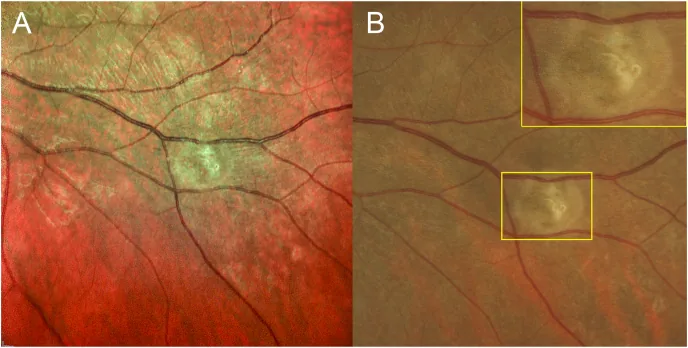
DUSN的臨床表現因病程階段而有顯著差異。
早期表現
視神經乳頭炎(papillitis):輕度視神經盤水腫、充血。
玻璃體炎:輕度至中度玻璃體混濁(約grade 1)1)。
聚集的灰白色視網膜下病灶:呈簇狀分布的多發白點1)。
移動性視網膜下軌跡:線蟲移動的痕跡。在91.7%的病例中可觀察到1)4)。
血管炎:視網膜血管周圍的炎症表現1)4)。
晚期表現
非典型的臨床表現包括廣泛滲出性視網膜剝離(視力下降至手動辨別至無光感)1)、肉芽腫性前部葡萄膜炎(mutton-fat KP、前房炎症4+、繼發性高眼壓38 mmHg)4)、黃斑部囊樣水腫(CME)4)等。
DUSN的感染途徑主要是接觸宿主動物或暴露於受污染的環境。
好發於健康的兒童及年輕成人,但無特定基礎疾病也可能發病1)。風險因子包括:曾前往或居住於流行地區(美國中西部及東南部、巴西、亞洲熱帶地區)、接觸浣熊等野生動物、以及食用未充分加熱的食物。
確定診斷需要直接在眼底看到線蟲,但僅約25-39%的病例能做到1)。透過連續眼底照片比對確認蟲體移動模式是有用的1)。
主要影像檢查的特徵如下表所示。
| 檢查方法 | 主要所見與特徵 |
|---|---|
| 紅外線活體成像 | 以900 nm光追蹤可視化避光性線蟲2) |
| Enface swept-source OCT | 線蟲移動路徑的「蟲洞」空洞(首次報告)3) |
| MultiColor掃描式雷射 | GR(515 nm)・BR(488 nm)顯示蟲體3) |
| OCT(斷層) | 視網膜下積液中的捲曲狀線蟲描繪1) |
| FFA | 瀰漫性RPE變化、視乳頭滲漏1)4) |
| FAF | 視乳頭周圍及黃斑部自體螢光增強1) |
在Enface swept-source玻璃體OCT中,可觀察到內界膜(ILM)層級因線蟲移動路徑形成的空洞「蟲洞」,此為線蟲移動至玻璃體時留下的痕跡,首次被報導3)。此外,紅外線即時影像利用線蟲對可見光(450–490 nm)表現趨避行為的避光性,可在900 nm近紅外線模式下即時追蹤蟲體2)。
需要與中心性漿液性脈絡網膜病變、弓形蟲性視網膜脈絡膜炎、類肉瘤病、梅毒性視網膜炎、多發性消失性白點症候群(MEWDS)、貓抓病(CSD)等進行鑑別診斷。已有CSD與DUSN合併感染的案例報告4),因此不應固守單一診斷。
僅約25%至39%的病例可直接觀察到線蟲1)。若無法看見,需綜合單側多發性白點病變、視神經乳頭炎、玻璃體炎的組合、嗜酸性球增多、流行地區旅遊史及動物接觸史等進行臨床診斷。建議使用紅外線即時影像及Enface OCT等多模式影像技術,嘗試偵測線蟲。
DUSN的治療方針取決於是否能看到線蟲。雷射光凝固、口服阿苯達唑、全身性類固醇三種藥物合併使用被認為預後最佳1)。
當線蟲可視時,為第一線治療選擇1)。
阿苯達唑的標準劑量與療程尚未確立1)2),但已有數種給藥方案被報告。
| 給藥方案 | 備註 |
|---|---|
| 400毫克/日 × 30天 | 標準單純方案2) |
| 400 mg × 2次/日 × 30天 | 高剂量方案2) |
| 200 mg × 2次/日 × 6周 | 分次给药1) |
| 400 mg × 2次/日 × 6週 | 高劑量・長期1) |
| 400 mg/日 × 6週 | 單次給藥・長期4) |
阿苯達唑在合併玻璃體炎的眼睛中,因血-視網膜屏障(BRB)破壞而提高眼內移行性,治療效果增強1)。
類固醇(腎上腺皮質類固醇):為抑制發炎,使用潑尼松龍40〜60 mg/日,並在2〜4週內逐漸減量(例如:30 mg→20 mg→10 mg→5 mg的排程)2)。
併存感染的治療:CSD合併病例使用多西環素100 mg × 2/日 × 6週4)。續發性高眼壓則使用噻嗎洛爾、溴莫尼定、乙醯唑胺4)。
雷射光凝固
阿苯達唑
類固醇
適應症:作為發炎嚴重時的輔助治療。
用法:從prednisolone 40-60 mg/天開始逐漸減量2)。
目的:抑制玻璃體炎、血管炎、視神經炎。
早期進行雷射光凝固治療時,可望恢復視力。但若已發生視神經萎縮或廣泛性RPE變性的晚期病例,則會留下不可逆的視力障礙1)。20歲以上患者在1個月內早期就診與最終視力改善相關1),因此早期介入很重要。
DUSN的視網膜損傷是由線蟲在視網膜下腔移動造成的局部機械性與毒性刺激,以及宿主免疫反應(發炎反應)共同引起。此機制被稱為「毒性自體免疫性線蟲視網膜病變」1)。
線蟲最初局限於視網膜下腔移動,但也可能轉移至玻璃體腔。在Enface swept-source玻璃體OCT中觀察到的「蟲洞」首次被報告為線蟲在玻璃體內移動後留下的空洞痕跡3),B. procyonis可能隨機穿過視網膜全層移動3)。
病理時序如下:
線蟲產生的毒素和宿主的免疫反應共同引起視網膜損傷1)。早期僅為可逆的光感受器功能下降,但晚期會出現視神經萎縮、瀰漫性RPE變性和視網膜動脈狹窄,導致不可逆的視力障礙。因此,線蟲在眼內停留時間越長,視力預後越差。
Hänsli等人(2024)報告一名14歲男性,在前往泰國後發生DUSN(最佳矯正視力20/100),使用紅外線即時影像(900 nm)即時追蹤線蟲,並以導航雷射(Navilas 577s)進行雷射光凝固治療2)。
結合雷射照射前的紅外線模式線蟲可視化與4×4模式(100 μm、400 mW、20 ms、41點)照射,在抑制趨光性線蟲的逃避行為的同時,精確完成光凝固2)。治療後追加阿苯達唑(400 mg/日 × 30日)和潑尼松龍(30 mg→逐漸減量),並確認血清弓首線蟲抗體陽性。
Sodhi等人(2021)對一名37歲女性(最佳矯正視力CF、玻璃體細胞1+)的DUSN病例進行Enface掃頻源玻璃體OCT檢查,在全球首次記錄到ILM層級與線蟲移動路徑一致的空洞(「蟲洞」)3)。
傳統斷層OCT在ILM層級確認線蟲,但Enface玻璃體OCT影像則將移動路徑本身連續描繪為空洞3)。此發現證明線蟲已侵入玻璃體,支持B. procyonis隨機移動於視網膜全層的假說。
在同一病例中,使用MultiColor掃描式雷射影像(綠色反射515 nm・藍色反射488 nm),可呈現出在白色光眼底照片中難以確認的線蟲整體影像3)。這些多模式方法有望提升在無法直接觀察到線蟲的病例中的診斷率1)2)3)。