초기 소견

미만성 편측성 아급성 시신경망막염(DUSN)
한눈에 보는 포인트
섹션 제목: “한눈에 보는 포인트”1. 미만성 편측성 아급성 시신경망막염(DUSN)이란
섹션 제목: “1. 미만성 편측성 아급성 시신경망막염(DUSN)이란”미만성 편측성 아급성 시신경망막염(Diffuse Unilateral Subacute Neuroretinitis; DUSN)은 선충이 망막하 공간을 이동하면서 발생하는 다국소 맥락망막염입니다. 1978년 Gass 등이 처음 보고했으며, 초기에는 ‘unilateral wipeout syndrome’이라고도 불렸습니다3). 건강한 소아 및 젊은 성인에서 호발하며1), 편측성이 전형적이나 양측성 발병 사례도 보고되었습니다3).
원인 선충은 여러 종류가 알려져 있으며, 충체의 크기와 추정 유행 지역에 따라 분류됩니다.
| 벌레 종류 | 몸길이 기준 | 주요 유행 지역 |
|---|---|---|
| Baylisascaris procyonis | 1500~2000 μm | 미국 중서부·북미 |
| Toxocara canis | 400~1000 μm | 미국 남동부·열대 지역 |
| Ancylostoma caninum | 400~1000 μm | 열대·아열대 |
| Gnathostoma spinigerum | 400~1000 μm | 아시아(태국 등) |
유행 지역은 미국 중서부·남동부, 브라질, 카리브해 제도, 인도, 말레이시아 등 광범위하다. 말레이시아에서는 토양 매개 선충(STH) 유병률이 52~76%에 이른다고 한다4).
편측성이 전형적이지만, 양측성 발병 보고도 존재합니다3). 한쪽 눈의 치료가 지연되거나 면역 상태에 따라 반대쪽 눈으로 파급될 수 있습니다. 그러나 양안 동시 발병은 드물며, 한쪽 눈의 소견이 다른 쪽 눈과 비대칭이면 DUSN을 염두에 둔 정밀 검사가 필요합니다.
2. 주요 증상과 임상 소견
섹션 제목: “2. 주요 증상과 임상 소견”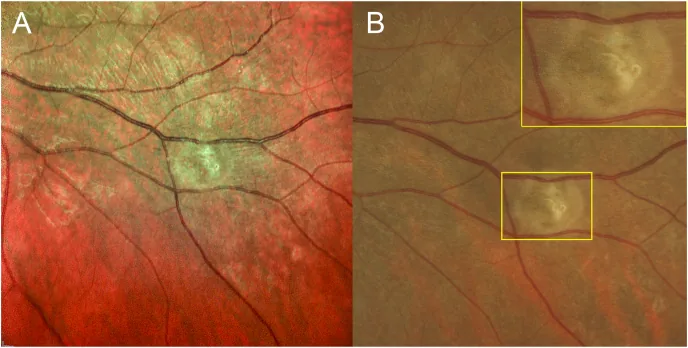
자각 증상
섹션 제목: “자각 증상”- 시력 저하: 급성기(초기)에는 경도에서 중등도이나, 말기에는 심각한 비가역적 저하를 초래합니다.
- 중심 암점 및 중심주위 암점: 황반부 병변에 따라 발생합니다.
- 시야 결손 : 망막 전체에 병변이 퍼짐에 따라 확대됩니다.
- 비문증 : 유리체염에 동반된 부유감으로 자각됩니다.
- 안통 : 일반적이지는 않지만, 육아종성 포도막염을 합병한 증례에서는 통증을 호소하는 경우가 있습니다4).
임상 소견
섹션 제목: “임상 소견”DUSN의 임상 소견은 병기에 따라 크게 다릅니다.
후기 소견
시신경 위축: 유두의 창백화. 조기 치료가 없는 경우 수개월 내에 나타남1).
망막 세동맥 협착: 18개월 이상 경과한 증례에서 관찰됨1).
미만성 RPE 변성: 망막색소상피의 미만성 위축·변성.
RAPD 양성: 상대적 구심성 동공 반응 장애. 시신경 장애의 증거1)3).
비전형적인 임상 양상으로 광범위 삼출성 망막박리(수동변~광각 없음까지 시력 저하)1), 육아종성 전방 포도막염(mutton-fat KP, 전방 염증 4+, 속발성 고안압 38 mmHg)4), 황반부 낭포성 부종(CME)4) 등이 보고되었다.
3. 원인 및 위험 요인
섹션 제목: “3. 원인 및 위험 요인”DUSN의 감염 경로는 숙주 동물과의 접촉·오염된 환경에의 노출이 주를 이룬다.
- 숙주 동물의 분변 접촉: 너구리(B. procyonis의 최종 숙주)의 분변이 감염원이 될 수 있다3).
- 오염된 음식 섭취 : 덜 익힌 고기·해산물 섭취. 태국 여행력이 있는 증례2), 파키스탄 길거리 음식 섭취력이 있는 증례3)가 보고되었다.
- 야외 활동 : 캠핑이나 야외 작업으로 인한 토양·동물 배설물 노출1).
- 연령 : 40세 미만의 젊은 연령층에 많다. 20세 이상에서는 1개월 이내 조기 내원이 최종 시력 개선과 관련된다1).
- 유행 지역 여행·거주 : 앞서 언급한 유행 지역에서의 생활력은 위험 인자가 된다.
건강한 소아·청년 성인에 호발하지만, 특정 기저 질환이 없어도 발병할 수 있습니다1). 유행 지역(미국 중서부·남동부, 브라질, 아시아 열대 지역)으로의 여행·거주력, 너구리 등 야생 동물과의 접촉력, 불충분하게 가열된 음식 섭취력이 위험 인자입니다.
4. 진단과 검사 방법
섹션 제목: “4. 진단과 검사 방법”확진 진단
섹션 제목: “확진 진단”확진 진단을 위해서는 안저에서 선충을 직접 시각화해야 하지만, 이는 전체 증례의 약 25~39%에서만 가능합니다1). 연속 안저 사진 비교를 통한 충체 이동 패턴 확인이 유용합니다1).
다중 모달 이미징
섹션 제목: “다중 모달 이미징”주요 영상 검사의 특징을 아래 표에 제시합니다.
| 검사법 | 주요 소견·특징 |
|---|---|
| 적외선 라이브 이미징 | 혐광성 선충을 900nm 광으로 추적 가시화2) |
| Enface swept-source OCT | 선충 이동 경로의 ‘웜홀’ 공동 (최초 보고)3) |
| MultiColor 주사 레이저 | GR(515 nm)·BR(488 nm)에서 충체 묘사3) |
| OCT(단층) | 망막하액 내의 코일형 선충 묘사1) |
| FFA | 미만성 RPE 변화, 유두에서의 누출1)4) |
| FAF | 유두주위·황반부의 자가형광 증가1) |
Enface swept-source 유리체 OCT에서는 내경계막(ILM) 수준에서 선충의 이동 경로에 생긴 공동 ‘웜홀’이 관찰되며, 이는 선충이 유리체로 이동한 흔적으로 처음 보고되었다3). 또한 적외선 라이브 이미징은 선충이 가시광선(450~490 nm)에 대해 회피 행동을 보이는 혐광성을 이용하여 900 nm 근적외선 모드로 충체를 실시간 추적할 수 있다2).
보조 검사
섹션 제목: “보조 검사”- 혈액 검사: 호산구 증가증이 보조 소견이 됩니다1)4).
- 혈청학적 검사: Toxocara, B. procyonis 항체 검사2). 고양이 할큄병(CSD) 합병이 의심되는 경우 Bartonella henselae 항체도 검사합니다4).
- ERG: b파 진폭의 감소가 관찰됩니다.
감별 진단
섹션 제목: “감별 진단”중심성 장액성 맥락망막병증, 톡소포자충 맥락망막염, 사르코이드증, 매독성 망막염, 다발성 소실성 백점 증후군(MEWDS), 고양이 할큄병(CSD) 등과의 감별이 필요하다. CSD와 DUSN의 중복 감염 사례도 보고되어 있어4), 단일 진단에 집착하지 않는 것이 중요하다.
선충이 직접 가시화되는 경우는 약 25~39%에 불과하다1). 보이지 않는 경우, 편측성 다국소 백색 병변·시신경 유두염·유리체염의 조합, 호산구 증가증, 유행 지역 여행력·동물 접촉력 등을 종합하여 임상적으로 진단한다. 적외선 라이브 이미징이나 Enface OCT 등 다중 모달 이미징을 활용하여 선충 검출을 시도하는 것이 권장된다.
5. 표준적 치료법
섹션 제목: “5. 표준적 치료법”DUSN의 치료는 선충의 시인 가능 여부에 따라 방침이 다릅니다. 레이저 광응고술, 알벤다졸 경구 투여, 스테로이드 전신 투여의 3제 병용이 가장 예후가 좋은 것으로 알려져 있습니다1).
레이저 광응고술
섹션 제목: “레이저 광응고술”선충이 확인된 경우의 일차 선택 치료입니다1).
- 표준 파라미터: 스팟 크기 200 μm, 출력 150~200 mW, 조사 시간 0.2초1).
- 네비게이티드 레이저(Navilas 577s) : 스팟 100μm, 출력 400mW, 조사 시간 20ms, 4×4 패턴으로 조사2).
- 적외선 라이브 이미징 보조 : 혐광성 선충을 근적외선 모드로 관찰하면서 실시간으로 조사 위치를 결정한다2). 선충에 청색광(450~490nm)을 조사하면 회피 행동을 보이므로, 직전까지 적외선 모드를 사용하고 조사 직전에 전환하는 기술이 개발되었다3).
약물 요법
섹션 제목: “약물 요법”알벤다졸의 표준 투여량 및 기간은 확립되지 않았지만1)2), 여러 요법이 보고되었다.
| 투여 요법 | 비고 |
|---|---|
| 400 mg/일 × 30일 | 표준 단순 요법2) |
| 400 mg × 2회/일 × 30일 | 고용량 요법2) |
| 200 mg × 2회/일 × 6주 | 분할 투여1) |
| 400 mg × 2회/일 × 6주 | 고용량·장기1) |
| 400 mg/일 × 6주 | 단회 투여·장기4) |
알벤다졸은 유리체염을 동반한 눈에서 혈액망막장벽(BRB)의 파괴로 인해 안내 이행성이 향상되어 치료 효과가 높아집니다1).
스테로이드(부신피질 스테로이드) : 염증 억제 목적으로 프레드니손 4060mg/일을 24주에 걸쳐 점감합니다(예: 30mg→20mg→10mg→5mg 스케줄)2).
동반 감염에 대한 치료 : CSD 동반 시 독시사이클린 100mg × 2회/일 × 6주4). 속발성 고안압에는 티몰롤, 브리모니딘, 아세타졸아미드가 사용됩니다4).
레이저 광응고
적응증: 안저에서 선충이 직접 확인되는 경우.
원칙: 확인 후 즉시 조사한다. 선충의 위치에서 1~2 DD 떨어진 후방에서 포위한다.
주의: 삼출성 망막박리 합병증에서는 레이저가 도달하지 못할 수 있다1).
알벤다졸
적응증: 선충이 육안으로 확인되지 않는 경우, 또는 레이저 치료의 보조로 사용.
용량: 400mg/일400mg×2/일로 30일6주간1)2).
특기: 유리체염 합병증례에서 안내 이행성이 향상됨1).
스테로이드
조기에 레이저 광응고술을 시행한 경우 시력 회복이 기대될 수 있습니다. 그러나 시신경 위축이나 광범위한 RPE 변성이 발생한 말기 증례에서는 비가역적인 시력 장애가 남습니다1). 20세 이상 환자에서 1개월 이내의 조기 내원이 최종 시력 개선과 관련이 있는 것으로 나타나1), 조기 중재가 중요합니다.
6. 병태생리학·상세한 발병 기전
섹션 제목: “6. 병태생리학·상세한 발병 기전”DUSN의 망막 손상은 선충이 망막하 공간을 이동함으로 인한 국소적인 기계적·독성 자극과 숙주 측의 면역 반응(염증 반응)의 조합으로 발생합니다. 이 기전은 ‘독성 자가면역 선충 망막증’으로 표현됩니다1).
선충은 초기에 망막하 공간에 국한되어 이동하지만 유리체강으로 이동하기도 합니다. Enface swept-source 유리체 OCT에서 관찰된 ‘웜홀’은 선충이 유리체 내를 이동한 흔적의 공동으로 처음 보고되었으며3), B. procyonis는 망막의 전층을 무작위로 이동할 가능성이 시사됩니다3).
병태의 시계열은 다음과 같습니다.
- 초기: 선충의 이동을 따라 국소적인 염증이 발생하여 회백색의 망막하 병변(클러스터 모양의 백점)으로 나타납니다. 유리체염, 유두염이 동시에 진행됩니다.
- 중기: 망막하 트랙이 형성되고 RPE 및 외층 광수용체에 장애가 축적됩니다. 미만성 RPE 변성이 확산됩니다.
- 후기: 시신경 위축과 망막 세동맥의 협소화가 발생하고, ERG의 b파 진폭이 현저히 감소한다. 이러한 변화는 비가역적이며1), 선충이 최대 3년간 안구 내에 생존할 수 있으므로, 진단 지연이 최종 예후를 결정적으로 악화시킨다.
선충이 생성하는 독소와 숙주의 면역 반응이 모두 망막 손상을 유발한다1). 초기에는 가역적인 광수용체 기능 저하에 그치지만, 후기에는 시신경 위축, 미만성 RPE 변성, 망막 동맥 협소화가 진행되어 비가역적인 시력 장애를 초래한다. 따라서 선충이 안구 내에 오래 머무를수록 시력 예후가 악화된다.
7. 최신 연구와 향후 전망 (연구 단계 보고)
섹션 제목: “7. 최신 연구와 향후 전망 (연구 단계 보고)”적외선 라이브 이미징 + 네비게이티드 레이저
섹션 제목: “적외선 라이브 이미징 + 네비게이티드 레이저”Hänsli 등(2024)은 태국 여행 후 DUSN이 발생한 14세 남아(최대교정시력 20/100)에게 적외선 라이브 이미징(900 nm)으로 선충을 실시간 추적하고, 네비게이티드 레이저(Navilas 577s)를 이용한 레이저 광응고술을 시행했습니다2).
레이저 조사 직전 적외선 모드로 선충을 시각화하고 4×4 패턴(100 μm, 400 mW, 20 ms, 41 스팟) 조사를 결합하여, 혐광성 선충의 회피 행동을 억제하면서 정확하게 광응고를 완료했습니다2). 치료 후 알벤다졸(400 mg/일 × 30일)과 프레드니손(30 mg→점감)을 추가했으며, 혈청 Toxocara 항체 양성이 확인되었습니다.
Enface swept-source 유리체 OCT ‘웜홀’
섹션 제목: “Enface swept-source 유리체 OCT ‘웜홀’”Sodhi 등(2021)은 37세 여성(최대교정시력 CF, 유리체 세포 1+)의 DUSN 증례에서 Enface swept-source 유리체 OCT를 시행하여 ILM 수준에 선충의 이동 경로와 일치하는 공동(「웜홀」)을 세계 최초로 기록했다3).
기존의 단층 OCT에서는 ILM 수준에서 선충이 확인되었지만, Enface 유리체 OCT 이미지에서는 이동 경로 자체가 공동으로 연속적으로 묘사되었다3). 이 소견은 선충이 유리체에 침입했다는 증거이며, B. procyonis가 망막 전층을 무작위로 이동한다는 가설을 지지한다.
MultiColor 주사 레이저 이미징
섹션 제목: “MultiColor 주사 레이저 이미징”동일 증례에서 MultiColor 주사형 레이저 이미징(녹색 반사 515 nm, 청색 반사 488 nm)을 사용함으로써 백색광 안저 사진에서는 확인하기 어려운 선충의 전체 모습이 묘사되었습니다3). 이러한 다중 모달 접근법은 선충을 직접 시각화할 수 없는 증례에서 진단율 향상에 기여할 것으로 기대됩니다1)2)3).
8. 참고 문헌
섹션 제목: “8. 참고 문헌”- Nurul-Farhana M, Roslin-Azni A, Sor-Earn T, Shatriah I, Shelina OM. Diffuse unilateral subacute neuroretinitis: challenges in diagnosis and management. Cureus. 2024;16(4):e58510.
- Hänsli C, Staehelin C, Bograd A, Tappeiner C. Infrared live imaging and navigated laser for nematode photocoagulation in a child with DUSN. Am J Ophthalmol Case Rep. 2024;36:102102.
- Sodhi SK, Golding J, Mandelcorn ED, Boggild アカントアメーバ角膜炎, Choudhry N. Enface vitreous OCT ‘worm holes’: a novel finding in a patient with DUSN. Am J Ophthalmol Case Rep. 2021;23:101112.
- Siti-Khadijah AR, Azhany Y, Norwazilah MA, Nor-Azita AT. Presumed DUSN and cat-scratch disease: dual infection in a single patient. Taiwan J Ophthalmol. 2022;12(3):349-353.
