外視網膜主導型

白點症候群
一目瞭然的要點
Section titled “一目瞭然的要點”1. 什麼是白點症候群?
Section titled “1. 什麼是白點症候群?”白點症候群(white dot syndromes)是1977年由Gass命名的概念,指眼底出現多個白色或黃白色斑點狀病變的一群炎症性疾病。雖然研究者對目標疾病的定義有所不同,但目前廣泛將其視為主要累及外視網膜、RPE、脈絡膜毛細血管層和脈絡膜的非感染性特發性炎症性疾病群1)。
在葡萄膜炎診療指南(日眼會誌 2019;123(6):635-696)中,APMPPE、MEWDS、PIC、多灶性脈絡膜炎、鳥槍彈樣視網膜脈絡膜病變、蛇行狀脈絡膜炎和AZOOR被列為後葡萄膜炎的獨立疾病類型,當使用「白點症候群」這一統稱時,則涵蓋這些疾病2)。
隨著多模態影像(包括OCT-A)的進步,白點症候群現在根據病變主要所在的層次分為以下三類1)。
脈絡膜微血管板主導型
脈絡膜間質主導型
- 原發病變為脈絡膜基質淋巴球浸潤
- OCT-A顯示Haller層血流空區,早期脈絡膜微血管層保留
- 慢性進行性,與HLA-A29強相關
此外,還提出了AZOOR複合體的概念,將MEWDS、AZOOR、PIC、MFC、AMN、AIBSE和AAOR視為具有共同遺傳性自體免疫/發炎機制的連續體3)。
日本流行病學
Section titled “日本流行病學”根據日本眼炎症學會統計,白點症候群各疾病在全部葡萄膜炎中所佔比例如下2)。
| 疾病 | 佔全部葡萄膜炎的比例 |
|---|---|
| MEWDS | 約1-2%(國內報告) |
| APMPPE | 罕見(無明確年發生率統計) |
| PIC | 罕見 |
| 蛇行狀脈絡膜炎 | 約0.3% |
| 鳥槍彈樣視網膜脈絡膜病變 | 罕見(白人多見,日本極為罕見) |
| AZOOR | 罕見(近年報告數增加) |
2. 共同的臨床表現
Section titled “2. 共同的臨床表現”各疾病的症狀雖不同,但以下臨床特徵為白點症候群所共有1, 2)。
自覺症狀的共同模式
Section titled “自覺症狀的共同模式”- 視力下降:程度從輕度(MEWDS、AZOOR)到重度(蛇行狀脈絡膜炎、PIC合併CNV)不等
- 閃光感(光視症):反映外層視網膜和感光細胞損傷的最常見症狀
- 暗點/視野缺損:多為與病變部位對應的旁中心或中心暗點
- 視物變形:發生於黃斑病變或合併CNV時
眼前段炎症的有無
Section titled “眼前段炎症的有無”| 疾病組 | 前房/玻璃體炎症 |
|---|---|
| MEWDS、APMPPE、PIC | 通常無(APMPPE 可能有輕度) |
| MFC(MFCwP) | 前房發炎 + 玻璃體炎(與 PIC 鑑別點) |
| Birdshot | 無至輕微前房發炎,有玻璃體炎 |
| 蛇行狀脈絡膜炎 | 前房炎症及玻璃體炎通常輕微 |
| AZOOR | 通常無 |
3. 鑑別診斷的思考方式
Section titled “3. 鑑別診斷的思考方式”按年齡、性別、單眼 vs 雙眼、復發性分類
Section titled “按年齡、性別、單眼 vs 雙眼、復發性分類”年輕女性、單眼、自然緩解
年輕至中年女性、雙眼、CNV風險
年輕至中年、雙眼、急性發作
- 好發於20–30歲(平均25歲),無性別差異
- 雙眼性、急性、有自然緩解傾向
- 注意合併腦血管炎(出現神經症狀時需緊急檢查)
中老年、雙眼、慢性進行性
- 鳥槍彈樣:40~60歲,女性略多
- 匐行性:30~50歲,男性略多
- 兩種疾病均為慢性、復發性,需長期免疫抑制治療
- 鳥槍彈樣HLA-A29陽性率(白人):80~98%
鑑別診斷流程圖
Section titled “鑑別診斷流程圖”眼底に白点状病変 │ ├─ 片眼性? │ ├─ YES → MEWDS・AZOOR・AMN を考慮 │ │ ↳ FA で初期過蛍光 → MEWDS │ │ ↳ 眼底ほぼ正常・ERG 異常 → AZOOR │ └─ NO(両眼性) │ ├─ 急性発症・後極部大型白斑? │ └─ YES → APMPPE(FA 蛍光逆転現象を確認) │ ├─ 後極部小病変・近視女性・硝子体炎なし? │ └─ YES → PIC を考慮(CNV 検索:OCTA 必須) │ ├─ 小病変・硝子体炎あり・周辺部にも病変? │ └─ YES → MFC(MFCwP)を考慮 │ ├─ 乳頭周囲から蛇行状に進展・男性多め? │ └─ YES → 蛇行状脈絡膜炎(結核除外が最優先) │ └─ 後極部散弾状病変・中高年・HLA-A29? └─ YES → Birdshot 網脈絡膜症4. 主要疾病比較
Section titled “4. 主要疾病比較”主要比較表:7種疾病矩陣
Section titled “主要比較表:7種疾病矩陣”| 項目 | APMPPE | MEWDS | PIC | MFC(MFCwP) | Birdshot | 蛇行狀脈絡膜炎 | AZOOR |
|---|---|---|---|---|---|---|---|
| 好發年齡 | 20~30歲(平均25歲) | 20~50歲 | 18~40歲(平均36歲) | 平均30歲 | 40~60歲 | 30~50歲 | 以35歲左右為中心 |
| 性別 | 無性別差異 | 女性優勢(1:4) | 女性優勢(約90%) | 女性優勢(白人女性多見) | 女性略多 | 男性略多 | 女性優勢(約75%) |
| 單眼/雙眼 | 多為雙眼 | 單眼(≥95%) | 多為雙眼(80%) | 雙眼 | 雙眼 | 雙眼 | 單眼→雙眼進展(最終76%雙眼) |
| 主要症狀 | 視力下降、中心暗點、視物變形 | 視力下降、閃光感、視物模糊 | 暗點、視力下降、視物變形 | 飛蚊症、視力下降、閃光感 | 視力下降、夜盲、色覺異常 | 視力下降、旁中心暗點 | 閃光感、視野缺損(眼底基本正常) |
| 眼底白斑的特徵 | 後極部大型奶油色白斑(1/4~1/2 視盤直徑) | 後極部至赤道部淡灰白色多發性小斑(100~200μm) | 後極部黃白色小斑(100~300μm),12~25個 | 後極部至周邊黃灰色斑(45~350μm),伴玻璃體炎 | 後極部至赤道部散彈狀奶油色斑(1/4~1/2 視盤直徑) | 視盤周圍蜿蜒狀擴展的地圖狀灰黃色病變 | 眼底幾乎正常(急性期),後期外層萎縮 |
| OCT 所見 | 橢圓體帶紊亂 + 外網膜高反射,恢復後部分萎縮殘留 | 橢圓體帶明顯紊亂/消失(急性期)→ 恢復 | RPE 下高反射隆起 + EZ 斷裂(5 階段演變) | RPE 下高反射 + EZ 斷裂(類似 PIC) | 脈絡膜病變、囊樣黃斑水腫,EZ 消失預後不良 | 活動期:外網膜高反射、視網膜下液。瘢痕期:RPE 萎縮 | EZ(IS/OS)消失為最重要所見(與視野缺損部位一致) |
| FA 所見 | 早期低螢光→晚期高螢光(螢光逆轉現象) | 從早期開始持續的花環狀高螢光 | 活動期:動脈期早期高螢光→晚期滲漏 | 活動期:早期低螢光→晚期滲漏 | 病灶高螢光(無滲漏)+ 血管滲漏及視盤高螢光 | 活動期:早期低螢光→晚期高螢光(滲漏) | 通常正常或輕微異常 |
| ICGA 所見 | 全相低螢光(直接反映脈絡膜毛細血管板缺血) | 晚期低螢光(範圍比白點更廣) | 中期低螢光,有助於檢測亞臨床病變 | 早期至全相低螢光 | 早期/中期低螢光→晚期等螢光(初期)→進展期:全相低螢光 | 全相低螢光(反映脈絡膜循環障礙) | 通常正常 |
| FAF 所見 | 急性期:低或過自發螢光。緩解期:低自發螢光 | 急性期:高自發螢光(多發高螢光點)。恢復後:正常化 | 活動期:低自發螢光(hypoAF),邊緣高自發螢光暈 | 活動期:低自發螢光 | 視乳頭周圍融合性低自發螢光(73%可見) | 活動期:高自發螢光邊緣+低自發螢光暈。靜止期:低自發螢光 | 帶狀高至低自發螢光異常 |
| OCT-A 表現 | 脈絡膜微血管層血流缺失(與FA/ICGA高度一致) | 脈絡膜微血管層原則保留(部分一過性血流缺失) | 脈絡膜微血管層血流缺失(發炎病變部位) | 脈絡膜微血管層血流缺失 | Haller層血流缺失(早期)→進展期:全層血流缺失 | 脈絡膜微血管層血流缺失(重度) | 脈絡膜微血管層原則保留 |
| 復發性 | 罕見(基本上單次發作) | 約10%復發 | 高(慢性復發性) | 高(反覆發炎發作) | 高(慢性,反覆復發緩解) | 高(每3個月至4年間隔反覆) | 多數6個月內穩定,部分進展 |
| CNV 合併率 | 罕見 | 罕見 | 40–76%(高風險) | 最高 60% | 視網膜下 CNV:罕見 | 最高 35% | 幾乎沒有 |
| HLA 相關 | 無 | HLA-B51(初步報告) | HLA-DR2、HLA-DRB1*15 | IL-10 單倍型相關 | HLA-A29(白人中80-98%) | HLA-B7、HLA-A2(相關報告) | 無(免疫學易感性) |
| 治療方針 | 觀察(自然緩解),重症:類固醇 | 觀察,重症:短期類固醇,CNV:抗VEGF | 觀察(無CNV),CNV:抗VEGF+類固醇,免疫抑制劑 | 類固醇+免疫調節治療,CNV:抗VEGF | 類固醇+黴酚酸酯/阿達木單抗(長期) | 類固醇+免疫抑制劑(包括烷化劑),CNV:抗VEGF | 觀察,重症:類固醇脈衝 |
| 視力預後 | 良好(多可自然緩解) | 良好(注意復發和CNV) | 合併CNV時預後不良風險高 | CNV和黃斑水腫導致預後不良風險 | 未經治療,10年內16%~22%視力≤0.1 | 累及中心凹則不可逆,最多25%的眼睛最終視力<20/200 | 多數穩定。外層進行性損害者預後不良 |
各疾病的詳細臨床表現
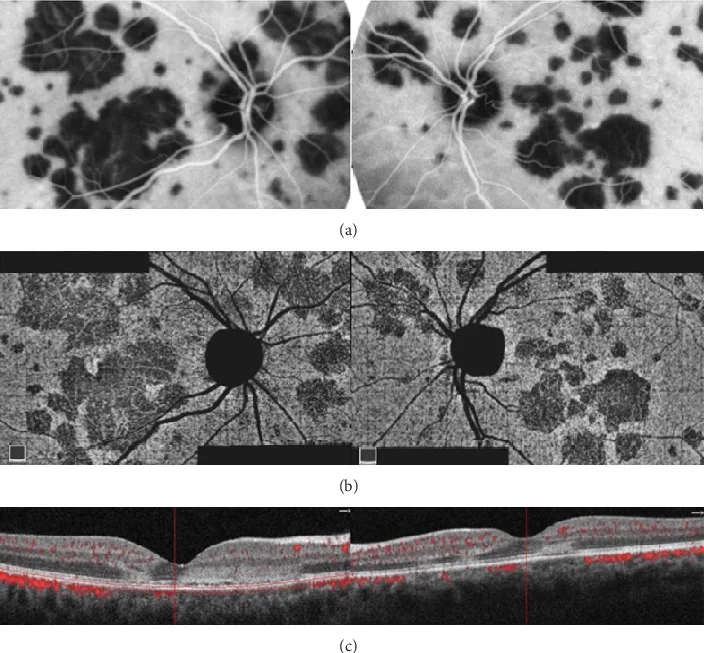
Section titled “各疾病的詳細臨床表現”APMPPE(急性後部多發性斑狀色素上皮病變)
Section titled “APMPPE(急性後部多發性斑狀色素上皮病變)”APMPPE好發於20~30歲(平均25歲),無性別差異。其本質被認為是脈絡膜毛細血管板輸入小動脈的閉塞性血管炎,病毒感染等可能為誘因1, 2)。
前驅症狀與病程
- 約半數患者有感冒樣症狀(流感、EB病毒、水痘、鏈球菌感染等)
- 雙眼後極部出現多個1/4至1/2視盤直徑的奶油色盤狀白斑
- 白斑在數天內從中心開始消退,7-12天後消失,留下輕度色素脫失
- 通常單次發作可自然緩解(復發罕見)
- 視力預後通常良好,但重症或進展為地圖狀脈絡膜炎的病例可能預後不良
特殊併發症:腦血管炎(MCAT)
APMPPE合併中樞神經系統血管炎(MCAT:多發性腦動脈血栓形成)是一種嚴重的併發症。如果出現頭痛、發燒或神經症狀,需要緊急進行腦部MRI和MRA檢查。合併腦血管炎的病例需要進行甲基潑尼松龍脈衝治療並與神經內科協作2)。
與placoid脈絡膜視網膜炎譜系的關係
APMPPE與PPM(持續性placoid黃斑病變)和RPC(頑固性placoid脈絡膜視網膜炎)共同構成「placoid脈絡膜視網膜炎譜系」,其共同病理基礎是脈絡膜毛細血管板缺血5)。
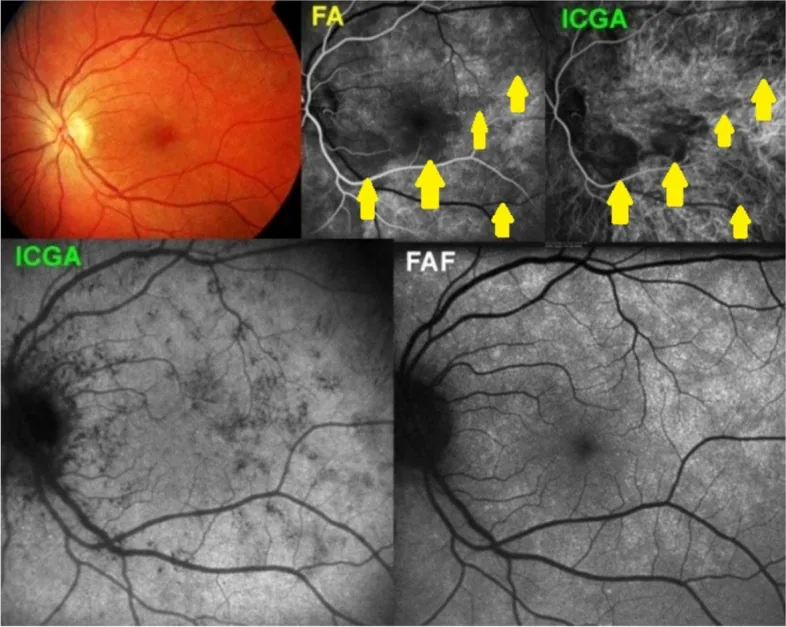
MEWDS(多發性消失性白點症候群)
Section titled “MEWDS(多發性消失性白點症候群)”MEWDS好發於20~50歲女性(男女比1:4),特徵為單眼、急性、自然緩解。
特有的臨床表現
- 後極部至赤道部視網膜深層至RPE層次的淡灰白色多發性小斑點(100~200 μm)
- 中心凹顆粒狀變化:74%~96%的患者可見,白點消失後可能成為唯一殘留表現。近紅外FAF(NIR-FAF)顯示特徵性模式9)
- 橙色小點:眼底照相和近紅外眼底攝影的特徵性表現
- 象牙色病變:眼底後極部淡而模糊的白色變化
- 約50%病例有感冒樣前驅症狀
- 年發生率約為每10萬人0.22例,10%出現復發
FA上的花冠狀高螢光
FA早期特徵性的花冠狀高螢光是診斷MEWDS的關鍵。白點病變在FA早期即出現高螢光,晚期不擴大。這種早期高螢光是與APMPPE早期低螢光(螢光逆轉現象)的重要鑑別點1, 9)。
與AZOOR複合體的連續性
MEWDS 主要涉及感光細胞橢圓體帶(IS/OS 線)的短暫破壞,被理解為屬於 AZOOR 複合體的疾病。OCT 可在急性期確認橢圓體帶的紊亂或消失,並隨視力恢復而改善3)。
PIC(點狀內層脈絡膜病變)
Section titled “PIC(點狀內層脈絡膜病變)”PIC 好發於 18-40 歲患有近視(平均約 -5 D)的年輕女性(約 90%)。
特有的臨床表現
- 僅局限於後極部的100~300 μm黃白色小斑點,通常12~25個
- 無前房炎症或玻璃體炎(這是與MFC最重要的鑑別點)
- 活動性病變在OCT上表現為RPE下的高反射隆起
- 瘢痕化後留下小的萎縮性病變
CNV合併(40%~76%)是最大的臨床問題
PIC最重要的併發症是CNV,其發生率據報導為40–76%7, 8)。CNV易由以下因素引起:
- 近視性脈絡膜變薄導致的Bruch膜脆弱
- RPE下發炎導致的Bruch膜破壞
- 發炎性細胞因子(如VEGF)的局部產生增加
OCT-A已被證明在CNV篩檢中比FA更敏感,建議定期進行OCT-A監測。視物變形的突然惡化是CNV發生的徵兆,需要及時檢查。
與全身疾病的關聯
已有報告指出PIC與類肉瘤病合併發生;對於有多發性肺部病變的病例,應進行胸部CT、血清ACE及溶菌酶檢查。也有報告指出與HLA-DR2及HLA-DRB1*15相關3)。
MFC(多灶性脈絡膜炎,MFCwP)
Section titled “MFC(多灶性脈絡膜炎,MFCwP)”MFC(全葡萄膜炎伴多灶性脈絡膜炎;MFCwP)與PIC屬於同一疾病譜,但最大的鑑別點是伴有玻璃體炎及前房炎症7)。
特有的臨床表現
- 不僅在後極部,在周邊部也出現多發45~350μm的黃灰色斑。
- 特徵為慢性復發性病程(反覆發炎發作)
- 視網膜前膜(ERM) 合併頻率高(高達35%),影響長期視力預後
- 部分病例無法在不使用免疫抑制治療的情況下控制發炎
治療注意事項
MFC不易自然緩解,許多病例需要長期免疫調節治療。單用類固醇不足時,可使用甲氨蝶呤(MTX)、硫唑嘌呤(AZA)或嗎替麥考酚酯(MMF)。合併CNV時,抗VEGF治療與免疫調節治療的雙向方法至關重要7, 8)。
鳥槍彈樣脈絡膜視網膜病變(散彈狀脈絡視網膜病變)
Section titled “鳥槍彈樣脈絡膜視網膜病變(散彈狀脈絡視網膜病變)”鳥槍彈樣病變好發於4060歲的中老年人(平均50多歲),女性略多(1.5:1)。在白人中更常見,是與HLA-A29關聯最強的已知疾病之一(白人相對風險為50224倍)4)。
特徵性眼底表現
特有的功能變化
日本患者的注意事項
日本人HLA-A29攜帶頻率低,因此HLA-A29的診斷敏感性受限。診斷需重視SUN 2021分類標準中的臨床所見(眼底散彈狀病變、前房炎症輕微、玻璃體炎存在)10)。
長期併發症
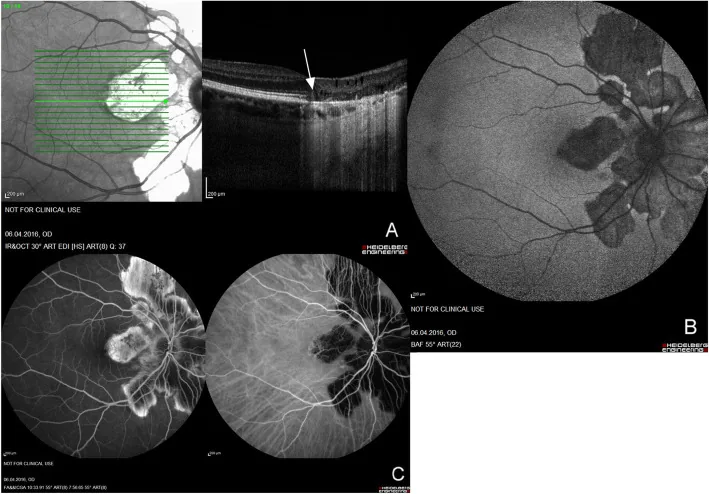
匐行性脈絡膜病變
Section titled “匐行性脈絡膜病變”蛇行狀脈絡膜炎是30~50歲(男性略多)的雙側慢性脈絡膜炎,特徵為從視乳頭周圍呈蛇行狀擴展的地圖狀灰黃色病變。
特有的進展模式
- 從視乳頭周圍(peripapillary)向心性開始,病變邊緣逐漸呈蛇行狀擴大
- 活動期:病變邊緣出現灰白色邊界
- 瘢痕期:固定為視網膜脈絡膜萎縮病變
- 復發時,新炎症總是從現有瘢痕的邊緣出現(這是特徵性的)
- 復發間隔為3個月至4年,個體差異很大。
最重要:與結核相關型(SLC)的鑑別
結核性蛇行樣脈絡膜炎(SLC)與蛇行狀脈絡膜炎在影像學表現上非常相似,但治療原則根本不同:
| 鑑別點 | 蛇行狀脈絡膜炎 | 結核相關型(SLC) |
|---|---|---|
| 病變分布 | 視乳頭周圍、向心性 | 後極部至周邊部、多發性 |
| IGRA/TST | 陰性 | 陽性 |
| 病變形狀 | 地圖狀、連續性 | 多發不連續的小病灶常見 |
| 治療 | 類固醇+免疫抑制劑 | 抗結核藥物為必需 |
由於使用免疫抑制劑會導致結核病顯著惡化,因此治療前的IGRA(QuantiFERON)檢查絕對不能省略2)。
CNV合併(最高35%)的處理
蛇行狀脈絡膜炎中CNV合併率高達35%,累及中心凹時可導致不可逆的視力障礙。抗VEGF療法(貝伐珠單抗、雷珠單抗)的玻璃體內注射有效18)。
AZOOR(急性帶狀潛在性視網膜外層病變)
Section titled “AZOOR(急性帶狀潛在性視網膜外層病變)”AZOOR 是 Gass 於 1992 年提出的疾病概念,是一種眼底幾乎正常但突然出現視力下降、視野缺損和閃光感的外層視網膜病變3)。
AZOOR 複合體的概念
Jampol 等人提出的 AZOOR 複合體概念將 MEWDS、AZOOR、PIC、MFC、AMN(急性黃斑神經視網膜病變)、AIBSE 和 AAOR 理解為具有共同遺傳性自體免疫/發炎機制的連續體3)。
特有的臨床表現
- 好發於 20 至 50 歲患有近視的年輕女性。
- 閃光感(光視症)在發病初期常出現(尤其是帶狀或弧狀的光)
- 單眼發病,最終76%變為雙眼
- 急性期眼底幾乎正常(視力下降與眼底表現不一致是特徵)
- 視野缺損呈不規則帶狀模式(常與盲點相連)
- 可合併自體免疫疾病(橋本病、多發性硬化症)
OCT和ERG是診斷關鍵
- OCT上橢圓體帶(IS/OS線)的消失或模糊是最重要的發現。
- OCT顯示外層消失的部位無法期待功能恢復(對預後預測也有用)。
- 多焦ERG可在眼底正常時檢測到振幅降低(多焦ERG比全視野ERG更敏感)。
- 紅外FAF有時可描繪出病變區與正常區的邊界。
治療與預後
AZOOR尚無確立的治療方法。輕症病例僅需觀察,但重症病例(視力下降或廣泛視野缺損)需進行甲潑尼龍脈衝療法(1000 mg × 3天)後口服潑尼松龍2)。多數病例在6個月內穩定,但外層損傷殘留部位的視野不會恢復。
5. 影像檢查的使用
Section titled “5. 影像檢查的使用”不同模態的角色分工
Section titled “不同模態的角色分工”明確了解每種影像檢查的作用對於準確診斷和評估白點症候群的活動性至關重要1, 5)。
| 檢查方式 | 最強適應症/角色 |
|---|---|
| FA(螢光素眼底血管攝影) | 評估視網膜血管、RPE和脈絡膜微血管的滲漏。確認APMPPE的螢光逆轉現象。確認MEWDS的花環樣高螢光。評估血管炎(Birdshot)。 |
| ICGA(靛青綠血管攝影) | 直接評估脈絡膜循環障礙。比FA更早發現病變(尤其是Birdshot、APMPPE、匐行性)。發現比臨床所見更廣泛的病變(MEWDS、PIC)。對活動性病變的檢測最敏感。 |
| FAF(眼底自體螢光) | RPE損傷的非侵入性評估。活動性判定(APMPPE、蛇行狀)。MEWDS的診斷(早期白點處高自體螢光)。Birdshot的慢性化評估(視乳頭周圍低自體螢光73%) |
| OCT(光學同調斷層掃描) | 橢圓體帶評估(MEWDS、AZOOR的診斷性發現)。病變5階段進展評估(PIC)。CNV、黃斑水腫的評估。預後預測(EZ消失→視力預後不良) |
| OCT-A | 脈絡膜毛細血管血流空缺的非侵入性檢測(APMPPE、蛇行狀、PIC)。CNV的早期、靈敏檢測(PIC、MFC中比FA更敏感)。Birdshot的脈絡膜分層血流評估。治療效果監測 |
| 多焦ERG / 全視野ERG | AZOOR的診斷(即使眼底基本正常,ERG振幅也降低)。Birdshot的活動性監測(30Hz閃爍延遲最敏感)。治療效果評估。 |
按疾病分類的「首先做哪項檢查」指南
Section titled “按疾病分類的「首先做哪項檢查」指南”懷疑MEWDS時
懷疑APMPPE時
- FA(確認螢光逆轉現象)
- ICGA(直接評估脈絡膜微血管缺血)
- OCT-A(評估血流空區)
- 如有神經症狀:腦部MRI/MRA(排除血管炎)
當懷疑PIC/MFC時
懷疑蛇行狀脈絡膜炎時
ICGA 低螢光病變的意義
Section titled “ICGA 低螢光病變的意義”ICGA 上白點症候群病變的低螢光是**脈絡膜血流中斷(脈絡膜毛細血管閉塞)**的直接反映1)。ICGA 作為評估脈絡膜循環的模態,比 FA 更敏感,具有以下特徵:
- 全相低螢光:見於 APMPPE、匐行性脈絡膜炎、PIC 和 MFC。反映脈絡膜毛細血管缺血的嚴重閉塞。
- 晚期低螢光(FA正常):MEWDS的ICGA晚期低螢光被解釋為由RPE異常引起的ICG攝取變化,而非脈絡膜微血管層受累(OCT-A顯示脈絡膜微血管層通常保留)1)。
- Haller層流空→晚期全層流空:Birdshot特有的從脈絡膜基質到脈絡膜微血管的兩階段進展模式14)。
ICGA相比FA和OCT-A在檢測臨床不可見的亞臨床病變方面更具優勢,尤其在MEWDS和PIC中,能顯示比白點更廣泛的脈絡膜病變1, 15)。
FAF低螢光與高螢光模式疾病圖譜
Section titled “FAF低螢光與高螢光模式疾病圖譜”FAF(眼底自發螢光)模式反映RPE的代謝狀態,對白點症候群的診斷和活動性評估有用16)。
| FAF模式 | 疾病/分期 | 意義 |
|---|---|---|
| 高自發螢光(高AF) | MEWDS急性期、匍行性脈絡膜炎活動邊緣 | 光感受器變性產物(如A2E)在RPE中的積累 |
| 低自發螢光(低AF) | APMPPE瘢痕期、PIC活動病變、Birdshot視乳頭周圍 | RPE消失或功能喪失 |
| 中心低螢光伴周邊高螢光暈 | 匍行性活動邊緣、PIC | 活動邊緣的RPE損傷模式 |
| 帶狀異常螢光 | AZOOR | 與感光細胞外層損傷分布一致 |
| 中心凹顆粒狀高自體螢光 | MEWDS(近紅外自體螢光) | 中心凹顆粒狀變化的非侵入性顯示 |
在Birdshot病中,73%的患者可見視盤周圍融合性低自體螢光,可作為慢性化的指標17)。
OCT上橢圓體帶(EZ)缺損模式
Section titled “OCT上橢圓體帶(EZ)缺損模式”橢圓體帶(EZ,原IS/OS線)的評估在白點症候群的活動性和預後預測中扮演核心角色1)。
| EZ 所見 | 疾病/分期 | 預後 |
|---|---|---|
| EZ 明顯紊亂 → 恢復 | MEWDS 急性期 → 恢復期 | 良好(EZ 恢復與視力恢復相關) |
| EZ消失(與病變一致) | AZOOR活動期 | 消失部位無功能恢復 |
| EZ紊亂+外網膜高反射 | APMPPE急性期 | 恢復後部分萎縮殘留 |
| RPE下高反射隆起+EZ斷裂 | PIC/MFC(5階段演變) | 合併CNV預後不良 |
| EZ消失(合併囊樣黃斑水腫) | Birdshot進展期 | 視力預後不良的危險因子 |
OCT-A 上的 脈絡膜毛細血管血流缺失 與 FA 和 ICGA 發現高度一致(在 APMPPE 和匍行性脈絡膜炎中尤其有用)5, 13)。
FA 螢光模式:充盈延遲 vs 高螢光 vs 滲漏
Section titled “FA 螢光模式:充盈延遲 vs 高螢光 vs 滲漏”| FA 模式 | 疾病 | 臨床意義 |
|---|---|---|
| 早期低螢光 → 晚期高螢光(螢光逆轉現象) | APMPPE | 脈絡膜毛細血管缺血。早期充盈缺損 → 周圍組織延遲染料滲漏。 |
| 早期花環狀高螢光 | MEWDS | 直接反映RPE/感光細胞損傷。鑑別點:晚期不擴大 |
| 早期低螢光→晚期滲漏 | 活動性匍行性/MFC | 活動性脈絡膜炎的證據 |
| 動脈早期過螢光→晚期滲漏 | PIC活動期 | 提示發炎性CNV |
| 血管滲漏+視盤過螢光(無滲漏) | Birdshot | 視網膜血管炎的直接證據 |
| 通常正常至輕微 | AZOOR | 特徵為分離現象:FA陰性但存在視野缺損和ERG異常 |
6. 治療總論
Section titled “6. 治療總論”治療策略的選擇
Section titled “治療策略的選擇”白點症候群的治療因疾病的自然病程、嚴重度以及是否合併CNV而有很大差異。
以觀察(無需治療)為原則的疾病
Section titled “以觀察(無需治療)為原則的疾病”以類固醇治療為主的疾病
Section titled “以類固醇治療為主的疾病”APMPPE(重症、合併乳頭炎)· PIC(中心凹附近活動性病變)· AZOOR(重症病例)
- 從prednisolone 30–60 mg/日開始,逐漸減量
- APMPPE合併腦血管炎時,需methylprednisolone脈衝治療並會診神經內科
- AZOOR重症標準:較好眼矯正視力 < 0.3(日本眼科學會診斷指引)
需要長期免疫抑制治療的疾病
Section titled “需要長期免疫抑制治療的疾病”鳥槍彈視網膜脈絡膜病變、蛇行狀脈絡膜炎、MFC
鳥槍彈(長期管理)
- Prednisolone 起始劑量0.5–1 mg/kg/日
- Mycophenolate mofetil(MMF)2–3 g/日(第一線免疫抑制劑)
- Methotrexate(MTX)10–25 mg/週
- Azathioprine(AZA)1–3 mg/kg/日
- 難治病例:阿達木單抗(93.2%作為第一線生物製劑使用)
- 未治療情況下,10年內16~22%視力降至0.1以下
匐行性脈絡膜炎(長期管理)
MFC的免疫調節治療
Section titled “MFC的免疫調節治療”由於MFC呈慢性復發性病程,在類固醇減量後常需免疫調節藥物作為維持治療。
| 藥物 | 劑量參考 | 備註 |
|---|---|---|
| 甲氨蝶呤(MTX) | 10~25 mg/週 | 併用葉酸1 mg/日。監測肝毒性。 |
| 硫唑嘌呤(AZA) | 1~3 mg/kg/日 | 建議確認TPMT活性。注意血球抑制。 |
| 黴酚酸嗎替乙酯(MMF) | 1~3克/日 | 胃腸道症狀是常見副作用 |
| 環孢素(CsA) | 3~5毫克/公斤/日 | 必須監測腎功能和血壓 |
| 阿達木單抗 | 40 mg/2週(皮下注射) | 難治性/類固醇依賴性病例。必須進行結核篩檢。 |
合併CNV的處理
Section titled “合併CNV的處理”CNV是影響視力預後的最重要併發症,在PIC、MFC和蛇行狀脈絡膜炎中尤其常見。
| 疾病 | CNV合併率 | 治療 |
|---|---|---|
| PIC | 40~76% | 抗VEGF玻璃體內注射(貝伐珠單抗、雷珠單抗、阿柏西普)+類固醇。OCTA PRN策略。 |
| MFC | 最高60% | 抗VEGF玻璃體內注射+免疫調節治療 |
| 蛇行狀脈絡膜炎 | 最高35% | 抗VEGF(貝伐珠單抗、雷珠單抗)玻璃體內注射 |
| MEWDS/APMPPE | 罕見 | 抗VEGF(確認合併CNV時) |
| Birdshot | 罕見 | 全身免疫抑制治療+合併CNV時抗VEGF |
治療注意事項
Section titled “治療注意事項”| 注意事項 | 相關疾病 |
|---|---|
| 優先排除結核(免疫抑制前) | 蛇行狀脈絡膜炎、MFC |
| 考慮HLA-A29(診斷) | 鳥槍彈樣脈絡膜視網膜病變(日本人敏感性低) |
| 類固醇植入物的眼壓升高風險 | 鳥槍彈樣脈絡膜視網膜病變(最多40%需要小樑切除術) |
| 苯丁酸氮芥的骨髓抑制和惡性腫瘤風險 | 匍行性脈絡膜炎(必須每週進行血液檢查) |
| COVID-19感染或疫苗接種後復發 | PIC・MEWDS(有復發報告) |
| 合併腦血管炎時的緊急處理 | APMPPE(頭痛、神經症狀→緊急腦部MRI) |
對白點症候群開始使用免疫抑制劑前應進行的必要檢查如下:①透過IGRA(QuantiFERON)排除結核(蛇行狀脈絡膜炎中優先),②透過HBs抗原、HBc抗體、HCV抗體進行病毒性肝炎篩檢(防止免疫抑制引起的再活化),③胸部X光/CT(排除結核和類肉瘤病),④全血球計數和肝腎功能檢查(確認基準值)。對於阿達木單抗等生物製劑,根據藥品仿單也必須進行結核篩檢19, 20)。
6.5 與全身疾病的關聯
Section titled “6.5 與全身疾病的關聯”白點症候群的每種疾病都與特定的全身疾病或感染相關,治療前進行系統性的排除檢查很重要。
| 疾病 | 相關全身疾病/狀態 | 臨床意義 |
|---|---|---|
| APMPPE | 腦血管炎(MCAT)、鏈球菌感染、EB病毒 | 頭痛、神經症狀→緊急腦部MRI |
| Birdshot | HLA-A29(白人80~98%)、類似類肉瘤病 | HLA檢查輔助診斷(日本人敏感度低) |
| 蛇行狀脈絡膜炎 | 結核(SLC)·HLA-B7/A2 | IGRA陽性→原則上先使用抗結核藥物 |
| PIC | 類肉瘤病·HLA-DRB1*15 | 考慮胸部CT和ACE檢測 |
| MFC | IL-10 單倍型、EB病毒、類肉瘤病 | 慢性復發者需重新評估全身檢查 |
| MEWDS | COVID-19感染、疫苗接種後、HLA-B51 | SARS-CoV-2感染作為免疫觸發因素 |
| AZOOR | 橋本病、多發性硬化症、自體免疫疾病 | 考慮甲狀腺功能及自體抗體檢查 |
7. 各疾病的特殊事項與最新見解
Section titled “7. 各疾病的特殊事項與最新見解”APMPPE 與 placoid chorioretinitis 譜系
Section titled “APMPPE 與 placoid chorioretinitis 譜系”APMPPE 現與持續性斑塊狀黃斑病變(PPM)和頑固性斑塊狀脈絡膜視網膜炎(RPC)一起被統稱為「placoid chorioretinitis 譜系」。這三種疾病在 OCT-A 上均顯示脈絡膜毛細血管層血流缺失的共同模式,表明脈絡膜毛細血管缺血是其共同的病理基礎 5)。
Klufas 等人(2017)報告,在 APMPPE、PPM 和 RPC 中,OCT-A 檢測脈絡膜毛細血管層血流缺失與 FA 和 ICGA 具有高度一致性,支持了 placoid chorioretinitis 譜系的概念 5)。
MEWDS 與中心凹顆粒狀改變
Section titled “MEWDS 與中心凹顆粒狀改變”中心凹顆粒狀改變(foveal granularity)是 MEWDS 中 74%–96% 病例可見的診斷性表現,在白點消失後可能仍作為唯一體徵存在。近紅外 FAF(NIR-FAF)可顯示特徵性的中心凹顆粒狀模式 9)。
PIC與MFC的疾病譜
Section titled “PIC與MFC的疾病譜”PIC和MFC(MFCwP)具有共同的遺傳背景(IL-10單倍型、HLA-DRB1*15),被認為是同一疾病譜的不同表現型。主要鑑別點是玻璃體炎和前房炎症的有無以及病變分佈區域1, 3)。
| 鑑別點 | PIC | MFC(MFCwP) |
|---|---|---|
| 玻璃體炎 | 無 | 有(重要鑑別點) |
| 前房發炎 | 無 | 輕度 |
| 病變分佈 | 侷限於後極部 | 後極部+中周邊部 |
| 病變大小 | 100~300μm | 45~350μm |
| CNV合併率 | 40~76% | 最高60% |
Birdshot與HLA-A29
Section titled “Birdshot與HLA-A29”Birdshot與HLA-A29的關聯是已知所有疾病中最強的遺傳關聯之一,在白人患者中相對風險升高50~224倍4)。但日本人中HLA-A29攜帶者較少,因此診斷中HLA-A29陽性率的敏感性有限。應重視SUN 2021分類標準的臨床所見項目(眼底所見、前房炎症輕微、玻璃體炎)進行診斷10)。
AZOOR複合體與病毒觸發因素
Section titled “AZOOR複合體與病毒觸發因素”AZOOR被認為是在遺傳易感性(如IL-10單倍型等)基礎上,加上病毒感染、疫苗、藥物等環境觸發因素而發病,與MEWDS、PIC、AMN、AIBSE一起被理解為AZOOR複合體3)。COVID-19感染或疫苗接種後的MEWDS發病例在全球增加,提示SARS-CoV-2可能作為免疫觸發因素發揮作用11)。
8. 相關文章
Section titled “8. 相關文章”9. 參考文獻
Section titled “9. 參考文獻”- Testi I, Modugno RL, Pavesio C. Multimodal imaging supporting the pathophysiology of white dot syndromes. J Ophthalmic Inflamm Infect. 2021;11:32.
- 日本眼炎症学会・日本眼科学会. ぶどう膜炎診療ガイドライン(13〜18節:APMPPE・MEWDS・PIC・多発性脈絡膜炎・バードショット・蛇行状脈絡膜炎・AZOOR). 日本眼科学会雑誌. 2019;123(6):635-696.
- Jampol LM, Becker KG. White spot syndromes of the retina: a hypothesis based on the common genetic hypothesis of autoimmune/inflammatory disease. Am J Ophthalmol. 2003;135(3):376-379.
- Agrawal R, et al. The role of HLA-A29 in birdshot chorioretinopathy and immune checkpoint inhibitor-related uveitis. Am J Ophthalmol. 2025. doi:10.1016/j.ajo.2024.01.007
- Klufas MA, Phasukkijwatana N, Iafe NA, et al. Optical coherence tomography angiography reveals choriocapillaris flow reduction in placoid chorioretinitis. Ophthalmol Retina. 2017;1(1):77-91.
- Stattin M, Forster J, Ahmed D, Krepler K, Ansari-Shahrezaei S. Swept Source-Optical Coherence Tomography Angiography for Management of Secondary Choroidal Neovascularization in Punctate Inner Choroidopathy. Case Rep Ophthalmol. 2021;12:232-238.
- Spaide RF, Goldberg N, Freund KB. Redefining multifocal choroiditis and panuveitis and punctate inner choroidopathy through multimodal imaging. Retina. 2013;33(7):1315-1324.
- Leclaire MD, Clemens CR, Eter N, Mihailovic N. Choroidale Neovaskularisation infolge einer “punctate inner choroidopathy”, dargestellt mittels optischer Kohärenztomographie-Angiographie. Ophthalmologe. 2021;118:842-846.
- Mantovani A, Invernizzi A, Staurenghi G, Herbort CP Jr. Multiple evanescent white dot syndrome: a multimodal imaging study of foveal granularity. Ocul Immunol Inflamm. 2019;27(1):141-147.
- Standardization of Uveitis Nomenclature (SUN) Working Group. Classification criteria for birdshot chorioretinitis. Am J Ophthalmol. 2021;228:65-71.
- Chen N, Mandell M, Arjmand P. Multimodal imaging findings of multiple evanescent white dot syndrome in COVID-19 patients. IDCases. 2024;38:e02110.
- Seddigh S, Pinto A, Zaki AM, Gupta RR. Serpiginous choroiditis after COVID-19 infection. J Vitreoretinal Dis. 2025;9(2):246-252.
- Pakzad-Vaezi K, Khaksari K, Chu Z, Van Gelder RN, Wang RK, Pepple KL. Swept-source OCT angiography of serpiginous choroiditis. Ophthalmol Retina. 2018;2(7):712-719.
- Pepple KL, Chu Z, Weinstein J, Munk MR, Van Gelder RN, Wang RK. Use of en face swept-source optical coherence tomography angiography in identifying choroidal flow voids in 3 patients with birdshot chorioretinopathy. JAMA Ophthalmol. 2018;136(11):1288-1292. doi:10.1001/jamaophthalmol.2018.3474. PMID:30128478. PMCID:PMC6248174
- Khochtali S, Dridi T, Abroug N, et al. Swept-source optical coherence tomography angiography shows choriocapillaris flow reduction in multiple evanescent white dot syndrome. J Curr Ophthalmol. 2020;32(2):211-215.
- Yeh S, Forooghian F, Wong WT, et al. Fundus autofluorescence imaging of the white dot syndromes. Arch Ophthalmol. 2010;128(1):46-56.
- Minos E, Barry RJ, Southworth S, et al. Birdshot chorioretinopathy: current knowledge and new concepts in pathophysiology, diagnosis, monitoring and treatment. Orphanet J Rare Dis. 2016;11(1):61.
- Maleki A, Maldonado Cerda A, Garcia CM, et al. Chlorambucil combination therapy in refractory serpiginous choroiditis: a cure? Am J Ophthalmol Case Rep. 2021;21:101014.
- Niederer RL, Al-Janabi A, Engelbrecht C, et al. Immunomodulatory therapy prescribing practices for non-infectious uveitis: a survey of international experts. Br J Ophthalmol. 2024;108:482-489.
- Tomkins-Netzer O, et al. Treatment of non-infectious uveitis with biologics: a survey of the International Ocular Inflammation Society. Br J Ophthalmol. 2022;106:482-488.
