Tipo de retina externa predominante

Síndrome dos Pontos Brancos
Pontos-chave em Resumo
Seção intitulada “Pontos-chave em Resumo”1. O que é a Síndrome dos Pontos Brancos?
Seção intitulada “1. O que é a Síndrome dos Pontos Brancos?”A síndrome dos pontos brancos (white dot syndromes) é um conceito cunhado por Gass em 1977, referindo-se a um grupo de doenças inflamatórias caracterizadas por múltiplos pontos brancos ou branco-amarelados no fundo de olho. As definições das doenças incluídas variam entre pesquisadores, mas atualmente o termo é amplamente utilizado para se referir a um grupo de doenças inflamatórias idiopáticas não infecciosas que afetam principalmente a retina externa, o epitélio pigmentar da retina, os capilares coroidais e a coroide 1).
Nas Diretrizes de Prática Clínica para Uveíte (Jornal da Sociedade Japonesa de Oftalmologia 2019;123(6):635-696), APMPPE, MEWDS, PIC, coroidite multifocal, coroidopatia de Birdshot, coroidite serpiginosa e AZOOR são listados como doenças independentes na classificação de uveíte posterior, e o termo “síndrome dos pontos brancos” é usado como um conceito abrangente para essas doenças 2).
Conceito de Classificação
Seção intitulada “Conceito de Classificação”Com os avanços recentes na imagem multimodal (incluindo OCT-A), a síndrome dos pontos brancos passou a ser classificada em três grupos com base na camada principal da lesão 1).
Tipo predominante da lâmina coriocapilar
APMPPE, Coroidite serpiginosa, PIC
- Vasculite oclusiva da coriocapilar é o núcleo da patogênese
- OCT-A mostra flow void na coriocapilar
- Alterações na retina externa e EPR são secundárias
Tipo predominante do estroma coroidal
Corioretinopatia Birdshot
- Infiltração linfocítica no estroma coroidal é a lesão primária
- Na OCT-A, a camada de Haller apresenta flow void, e no início a coriocapilar é poupada
- Crônico progressivo e fortemente associado ao HLA-A29
Além disso, foi proposto o conceito de complexo AZOOR, que integra MEWDS, AZOOR, PIC, MFC, AMN, AIBSE e AAOR como um continuum com base genética autoimune/inflamatória comum, permitindo uma compreensão unificada3).
Epidemiologia no Japão
Seção intitulada “Epidemiologia no Japão”De acordo com as estatísticas da Sociedade Japonesa de Oftalmologia, a proporção de cada doença da síndrome dos pontos brancos em relação ao total de uveítes é a seguinte 2).
| Doença | Proporção em relação ao total de uveítes |
|---|---|
| MEWDS | Cerca de 1-2% (relatos nacionais) |
| APMPPE | Raro (sem estatísticas claras sobre incidência anual) |
| PIC | Raro |
| Coroidite serpiginosa | Cerca de 0,3% |
| Coriorretinopatia birdshot | Raro (mais comum em brancos, extremamente raro no Japão) |
| AZOOR | Raro (aumento de relatos nos últimos anos) |
2. Quadro clínico comum
Seção intitulada “2. Quadro clínico comum”Os sintomas de cada doença são diferentes, mas as seguintes características clínicas são comuns ao grupo das síndromes de pontos brancos1, 2).
Padrões comuns de sintomas subjetivos
Seção intitulada “Padrões comuns de sintomas subjetivos”- Redução da acuidade visual: A gravidade varia de leve (MEWDS, AZOOR) a grave (coroidite serpentina, PIC com CNV)
- Fotopsia (visão de luzes): Sintoma mais comum que reflete dano à retina externa e fotorreceptores
- Escotoma e defeitos de campo visual: Frequentemente escotoma paracentral ou central correspondente ao local da lesão
- Metamorfopsia (distorção visual): Ocorre com lesão macular ou CNV
Presença de inflamação do segmento anterior
Seção intitulada “Presença de inflamação do segmento anterior”| Grupo de doenças | Inflamação da câmara anterior e vítreo |
|---|---|
| MEWDS・APMPPE・PIC | Geralmente ausente (APMPPE pode ser leve) |
| MFC (MFCwP) | Inflamação da câmara anterior + vitreíte presente (ponto de diferenciação da PIC) |
| Birdshot | Inflamação da câmara anterior ausente a mínima, vitreíte presente |
| Coroidite serpiginosa | Inflamação da câmara anterior e vitrite geralmente leves |
| AZOOR | Geralmente ausente |
3. Como pensar no diagnóstico diferencial
Seção intitulada “3. Como pensar no diagnóstico diferencial”Idade, sexo, unilateral vs bilateral, recorrência
Seção intitulada “Idade, sexo, unilateral vs bilateral, recorrência”Mulher jovem, unilateral, melhora espontânea
Mulheres jovens a meia-idade • Ambos os olhos • Risco de CNV
Jovem a meia-idade • Ambos os olhos • Início agudo
- Ocorre predominantemente entre 20–30 anos (média 25 anos), sem diferença entre sexos
- Bilateral • Agudo • Tendência à resolução espontânea
- Atenção para vasculite cerebral associada (investigação urgente se surgirem sintomas neurológicos)
Meia-idade, ambos os olhos, crônico progressivo
Birdshot · Coroidite serpentina
- Birdshot: 40-60 anos, ligeiramente mais comum em mulheres
- Coroidite serpentina: 30-50 anos, ligeiramente mais comum em homens
- Ambas as doenças são crônicas, recorrentes, necessitam de imunossupressão prolongada
- Positividade do HLA-A29 no Birdshot (caucasianos): 80-98%
Fluxograma de Diagnóstico Diferencial
Seção intitulada “Fluxograma de Diagnóstico Diferencial”眼底に白点状病変 │ ├─ 片眼性? │ ├─ YES → MEWDS・AZOOR・AMN を考慮 │ │ ↳ FA で初期過蛍光 → MEWDS │ │ ↳ 眼底ほぼ正常・ERG 異常 → AZOOR │ └─ NO(両眼性) │ ├─ 急性発症・後極部大型白斑? │ └─ YES → APMPPE(FA 蛍光逆転現象を確認) │ ├─ 後極部小病変・近視女性・硝子体炎なし? │ └─ YES → PIC を考慮(CNV 検索:OCTA 必須) │ ├─ 小病変・硝子体炎あり・周辺部にも病変? │ └─ YES → MFC(MFCwP)を考慮 │ ├─ 乳頭周囲から蛇行状に進展・男性多め? │ └─ YES → 蛇行状脈絡膜炎(結核除外が最優先) │ └─ 後極部散弾状病変・中高年・HLA-A29? └─ YES → Birdshot 網脈絡膜症4. Comparação das Principais Doenças
Seção intitulada “4. Comparação das Principais Doenças”Tabela Comparativa Principal: Matriz de 7 Doenças
Seção intitulada “Tabela Comparativa Principal: Matriz de 7 Doenças”| Item | APMPPE | MEWDS | PIC | MFC (MFCwP) | Birdshot | Coroidite Serpentina | AZOOR |
|---|---|---|---|---|---|---|---|
| Idade de início mais comum | 20–30 anos (média 25 anos) | 20–50 anos | 18–40 anos (média 36 anos) | Média 30 anos | 40–60 anos | 30–50 anos | Principalmente meados dos 30 anos |
| Sexo | Sem diferença de sexo | Predomínio feminino (1:4) | Predomínio feminino (cerca de 90%) | Predomínio feminino (mais comum em mulheres brancas) | Ligeiramente mais mulheres | Ligeiramente mais homens | Predomínio feminino (cerca de 75%) |
| Unilateral/bilateral | Frequentemente bilateral | Unilateral (>95%) | Frequentemente bilateral (80%) | Bilateral | Bilateral | Bilateral | Unilateral → bilateral progressivo (eventualmente 76% bilateral) |
| Sintomas principais | Baixa acuidade visual, escotoma central, metamorfopsia | Baixa acuidade visual, fotopsia, visão turva | Escotoma, baixa acuidade visual, metamorfopsia | Moscas volantes, baixa acuidade visual, fotopsia | Baixa acuidade visual, cegueira noturna, anomalia de visão de cores | Baixa acuidade visual, escotoma paracentral | Fotopsia, defeito de campo visual (fundo de olho quase normal) |
| Características das Manchas Brancas do Fundo | Manchas grandes cor de creme no polo posterior (1/4 a 1/2 diâmetro do disco) | Pequenas manchas acinzentadas múltiplas do polo posterior ao equador (100-200 μm) | Pequenas manchas amareladas no polo posterior (100-300 μm), 12-25 manchas | Manchas acinzentadas do polo posterior à periferia (45-350 μm), com vitreíte | Manchas cor de creme em formato de tiro de espingarda do polo posterior ao equador (1/4 a 1/2 diâmetro do disco) | Lesões acinzentadas em forma de mapa que se estendem serpiginosamente ao redor do disco | Fundo quase normal (fase aguda), atrofia da camada externa na fase tardia |
| Achados de OCT | Desorganização da zona elipsoide + hiperrefletividade da retina externa, com atrofia parcial residual após recuperação | Desorganização acentuada e desaparecimento da zona elipsoide (fase aguda) → recuperação | Elevação hiperrefletiva abaixo do EPR + ruptura da zona elipsoide (evolução em 5 estágios) | Hiperrefletividade abaixo do EPR + ruptura da zona elipsoide (semelhante à PIC) | Lesões coroidais e edema macular cistóide, desaparecimento da zona elipsoide como mau prognóstico | Fase ativa: hiperrefletividade da retina externa e líquido sub-retiniano. Fase cicatricial: atrofia do EPR | Desaparecimento da zona elipsoide (IS/OS) é o achado mais importante (correlaciona-se com defeitos de campo visual) |
| Achados da FA | Hipofluorescência precoce → hiperfluorescência tardia (fenômeno de inversão fluorescente) | Hiperfluorescência persistente em forma de coroa (wreath-like) desde o início | Fase ativa: hiperfluorescência precoce na fase arterial → vazamento tardio | Fase ativa: hipofluorescência precoce → vazamento tardio | Hiperfluorescência da lesão (sem vazamento) + vazamento vascular e hiperfluorescência papilar | Fase ativa: hipofluorescência precoce → hiperfluorescência tardia (vazamento) | Normalmente normal ou anormalidade leve |
| Achados da ICGA | Hipofluorescência em todas as fases (reflete diretamente isquemia da camada capilar coroidal) | Hipofluorescência tardia (mais extensa que os pontos brancos) | Hipofluorescência na fase intermediária, útil para detectar lesões subclínicas | Hipofluorescência da fase inicial a todas as fases | Hipofluorescência inicial e intermediária → isofluorescência tardia (inicial) → fase avançada: hipofluorescência em todas as fases | Hipofluorescência em todas as fases (reflete distúrbio circulatório coroidal) | Geralmente normal |
| Achados de FAF | Fase aguda: autofluorescência baixa ou excessiva. Fase de remissão: autofluorescência baixa | Fase aguda: autofluorescência alta (hiperfluorescência múltipla). Após recuperação: normalização | Fase ativa: autofluorescência baixa (hipoAF), halo de autofluorescência alta na borda | Fase ativa: autofluorescência baixa | Autofluorescência baixa confluente peripapilar (presente em 73%) | Fase ativa: borda de autofluorescência alta + halo de autofluorescência baixa. Fase inativa: autofluorescência baixa | Anormalidade de autofluorescência alta a baixa em faixa |
| Achados de OCT-A | Vazio de fluxo da coriocapilar (alta concordância com FA/ICGA) | Coriocapilar preservada em princípio (vazio de fluxo transitório parcial) | Vazio de fluxo da coriocapilar (local da lesão inflamatória) | Vazio de fluxo da coriocapilar | Vazio de fluxo da camada de Haller (inicial) → fase avançada: vazio de fluxo em todas as camadas | Vazio de fluxo da coriocapilar (grave) | Coriocapilar preservada em princípio |
| Recorrente | Raro (basicamente uma vez) | Cerca de 10% recorrem | Alto (crônico recorrente) | Alto (episódios inflamatórios recorrentes) | Alto (crônico com remissões e recaídas repetidas) | Alto (recorre a cada 3 meses a 4 anos) | A maioria estabiliza em 6 meses. Alguns progridem |
| Taxa de CNV | Raro | Raro | 40–76% (alto risco) | Até 60% | CNV sub-retiniana: Raro | Até 35% | Quase nenhum |
| Relacionado ao HLA | Nenhum | HLA-B51 (relatos preliminares) | HLA-DR2 · HLA-DRB1*15 | Relacionado ao haplótipo IL-10 | HLA-A29 (80-98% em brancos) | HLA-B7 · HLA-A2 (relatos associados) | Nenhum (predisposição imunológica) |
| Plano de Tratamento | Observação (melhora espontânea), grave: corticoides | Observação, grave: corticoides de curta duração, CNV: anti-VEGF | Observação (sem CNV), CNV: anti-VEGF + corticoides, imunossupressores | Corticoides + terapia imunomoduladora, CNV: anti-VEGF | Corticoides + micofenolato de mofetila / adalimumabe (longo prazo) | Corticoides + imunossupressores (incluindo agentes alquilantes), CNV: anti-VEGF | Observação, grave: pulsoterapia com corticoides |
| Prognóstico visual | Bom (muitas vezes melhora espontaneamente) | Bom (cuidado com recidiva/CNV) | Alto risco de mau prognóstico com CNV | Risco de mau prognóstico com CNV e edema macular | Sem tratamento, 16-22% têm visão ≤0,1 em 10 anos | Se atingir a fóvea, irreversível; até 25% dos olhos têm visão final <20/200 | A maioria é estável. Mau prognóstico em casos de progressão do dano às camadas externas |
A coroidite serpiginosa e a coroidite birdshot têm o pior prognóstico visual. Na coroidite serpiginosa, até 25% dos olhos apresentam acuidade visual final inferior a 20/200, e na birdshot, 16-22% dos pacientes têm acuidade visual de 0,1 ou menos em 10 anos sem tratamento 2, 4). PIC e MFC apresentam maior risco de mau prognóstico em casos com CNV. APMPPE e MEWDS têm forte tendência à melhora espontânea e bom prognóstico.
Quadro clínico detalhado de cada doença
Seção intitulada “Quadro clínico detalhado de cada doença”APMPPE (Epiteliopatia Pigmentar Placóide Multifocal Posterior Aguda)
Seção intitulada “APMPPE (Epiteliopatia Pigmentar Placóide Multifocal Posterior Aguda)”APMPPE ocorre predominantemente na faixa dos 20-30 anos (média de 25 anos), sem diferença entre sexos. Acredita-se que vasculite oclusiva nas arteríolas aferentes dos capilares coroidais seja a causa subjacente, e infecções virais são suspeitas como fatores desencadeantes 1, 2).
Sintomas prodrômicos e evolução
- Cerca de metade dos casos apresenta sintomas gripais (influenza, vírus EB, varicela, infecção estreptocócica, etc.)
- Manchas branco-cremosas em forma de disco, de 1/4 a 1/2 diâmetro do disco óptico, aparecem múltiplas no polo posterior de ambos os olhos
- As manchas começam a desaparecer do centro em poucos dias e somem em 7-12 dias, deixando leve despigmentação
- Geralmente, há resolução espontânea em um único episódio (recorrência rara)
- O prognóstico visual geralmente é bom, mas pode ser ruim em casos graves ou naqueles que evoluem para coroidite geográfica
Complicação característica: Vasculite cerebral (MCAT)
A APMPPE e a vasculite do sistema nervoso central (MCAT: trombose arterial cerebral múltipla) são complicações graves. Se surgirem cefaleia, febre ou sintomas neurológicos, é necessário realizar urgentemente RM e ARM cerebrais. Nos casos com vasculite cerebral, são necessários pulsoterapia com metilprednisolona e colaboração com neurologia2).
Relação com o espectro da coriorretinite placóide
A APMPPE, juntamente com a PPM (maculopatia placóide persistente) e a RPC (coriorretinite placóide implacável), forma o “espectro da coriorretinite placóide”, tendo a isquemia da lâmina coriocapilar como base fisiopatológica comum5).
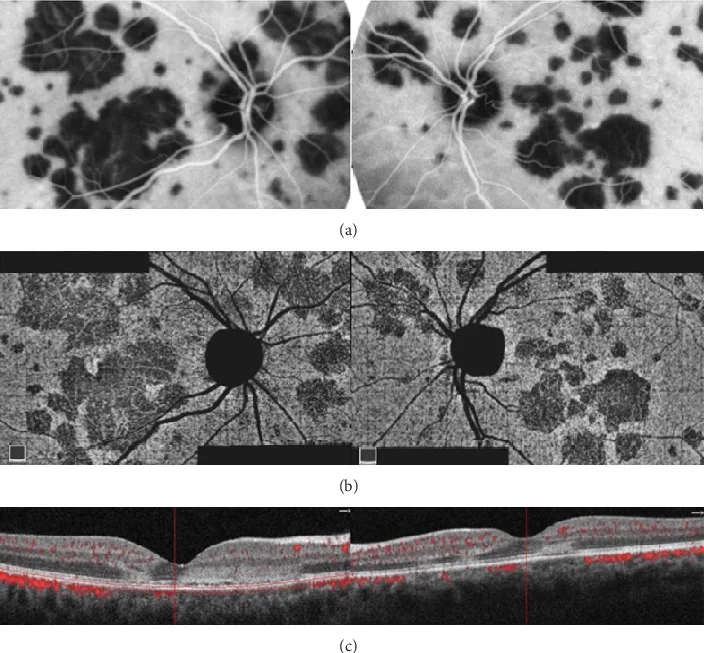
MEWDS (Síndrome dos Pontos Brancos Múltiplos Evanescentes)
Seção intitulada “MEWDS (Síndrome dos Pontos Brancos Múltiplos Evanescentes)”MEWDS é mais comum em mulheres de 20 a 50 anos (proporção homem:mulher 1:4), caracterizada por unilateral, aguda e resolução espontânea.
Quadro clínico característico
- Pequenas manchas múltiplas acinzentadas-esbranquiçadas pálidas (100-200 μm) na camada profunda da retina até o nível do EPR, do polo posterior ao equador
- Granularidade foveal (foveal granularity): presente em 74-96% dos pacientes, pode ser o único achado residual após o desaparecimento dos pontos brancos. Apresenta padrão característico na FAF de infravermelho próximo (NIR-FAF)9)
- Aspecto de ponto laranja (orange-dot appearance): achado característico na fotografia de fundo de olho ou imagem de infravermelho próximo
- Lesão marfim (ivory lesion): Alteração branca difusa e pálida no polo posterior do fundo de olho
- Sintomas prodrômicos semelhantes a resfriado precedem cerca de 50% dos casos
- Incidência anual de aproximadamente 0,22 por 100.000 pessoas, com 10% de recorrência
Hiperfluorescência em forma de coroa (wreath-like) na angiografia fluoresceínica (FA)
A hiperfluorescência em forma de coroa característica nas fases iniciais da FA é o ponto-chave para o diagnóstico de MEWDS. As lesões brancas apresentam hiperfluorescência precoce na FA sem expansão nas fases tardias. Essa hiperfluorescência precoce é um importante ponto de diferenciação da hipofluorescência precoce na APMPPE (fenômeno de inversão fluorescente)1, 9).
Continuidade com o complexo AZOOR
A MEWDS envolve destruição transitória da zona elipsoide (linha IS/OS) dos fotorreceptores, sendo compreendida como uma doença pertencente ao complexo AZOOR. Na OCT, é possível observar desorganização e desaparecimento da zona elipsoide na fase aguda, que melhoram com a recuperação da visão3).
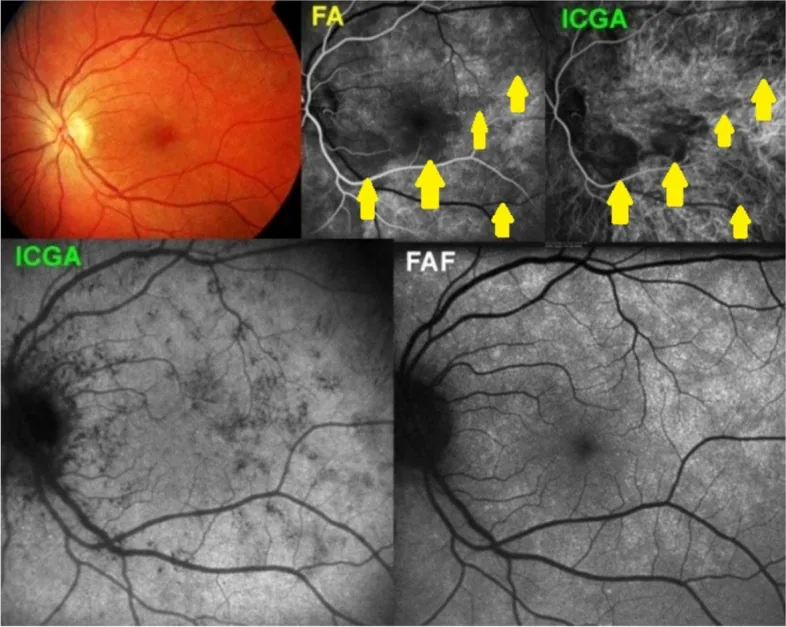
PIC (Coroidopatia Interna Punctata)
Seção intitulada “PIC (Coroidopatia Interna Punctata)”A PIC ocorre predominantemente em mulheres jovens (cerca de 90%) entre 18 e 40 anos com miopia (média de aproximadamente -5 D).
Quadro clínico característico
- Pequenas manchas amareladas-esbranquiçadas de 100–300 μm, limitadas apenas ao polo posterior, geralmente 12–25 manchas
- Sem inflamação da câmara anterior ou vitreíte (este é o ponto de diferenciação mais importante da MFC)
- Lesões ativas podem ser vistas como elevações hiper-refletivas sob o EPR na OCT
- Após cicatrização, deixam pequenas lesões atróficas
Complicação por CNV (40–76%) é o maior problema clínico
A complicação mais importante da PIC é a CNV, com taxa de incidência de 40-76% 7, 8). A CNV ocorre mais frequentemente devido aos seguintes fatores:
- Fragilidade da membrana de Bruch devido ao afinamento coroidal miópico
- Destruição da membrana de Bruch devido à inflamação sub-RPE
- Aumento da produção local de citocinas inflamatórias (como VEGF)
O OCT-A demonstrou ser mais sensível que a FA para rastreamento de CNV, sendo recomendado monitoramento regular com OCT-A. A piora súbita da metamorfopsia é um sinal de desenvolvimento de CNV e requer avaliação imediata.
Associação com doenças sistêmicas
A associação entre PIC e sarcoidose foi relatada, e em casos com lesões pulmonares múltiplas, são realizados exames de TC de tórax, ACE sérico e lisozima. A associação com HLA-DR2 e HLA-DRB1*15 também foi relatada 3).
MFC (Coroidite Multifocal, MFCwP)
Seção intitulada “MFC (Coroidite Multifocal, MFCwP)”MFC (coroidite multifocal com panuveíte; MFCwP) é uma doença no mesmo espectro da PIC, mas a presença de vitrite e inflamação da câmara anterior é o principal ponto de diferenciação 7).
Achados clínicos característicos
- Manchas amarelo-acinzentadas de 45 a 350 μm aparecem múltiplas não apenas no polo posterior, mas também na região periférica média.
- Curso crônico recidivante (episódios inflamatórios recorrentes) é característico
- Alta frequência de complicação de membrana epirretiniana (ERM) (até 35%), afetando o prognóstico visual de longo prazo
- Em alguns casos, a inflamação não pode ser controlada sem terapia imunossupressora
Notas sobre o tratamento
A MFC raramente melhora espontaneamente, e muitos casos necessitam de terapia imunomoduladora de longo prazo. Quando apenas esteroides são insuficientes, usa-se metotrexato (MTX), azatioprina (AZA) ou micofenolato de mofetila (MMF). Quando há CNV, uma abordagem bidirecional com anti-VEGF e imunomodulação é importante7, 8).
Corioretinite de Birdshot (Corioretinite em chumbo de espingarda)
Seção intitulada “Corioretinite de Birdshot (Corioretinite em chumbo de espingarda)”A doença de Birdshot (birdshot) ocorre em adultos de meia-idade a idosos (40-60 anos, média de 50 anos), com leve predominância feminina (1,5:1). É mais comum em brancos e é uma das associações genéticas mais fortes conhecidas com HLA-A29 (risco relativo de 50 a 224 vezes em brancos)4).
Achados fundoscópicos característicos
- Manchas cor de creme semelhantes a marcas de chumbo de espingarda (1/4 a 1/2 diâmetro do disco óptico) múltiplas e simétricas em ambos os olhos, do polo posterior ao equador
- As manchas evoluem para lesões cicatriciais sem pigmentação
- Pode ser acompanhada de vasculite retiniana e edema de papila
Alterações funcionais características
- Cegueira noturna e discromatopsia: Aparecem precocemente e podem preceder a diminuição da acuidade visual
- Tipo negativo no ERG de campo total: Observado nas fases iniciais, com progressão, a amplitude da onda a diminui
- Atraso no ERG flicker de 30Hz: Indicador mais sensível para monitoramento de atividade, capaz de detectar anormalidades antes da diminuição da acuidade visual17)
Atenções para japoneses
Devido à baixa frequência de portadores de HLA-A29 em japoneses, a sensibilidade diagnóstica do HLA-A29 é limitada. O diagnóstico deve enfatizar os achados clínicos nos critérios de classificação SUN 2021 (lesões de fundo de olho em chumbo, inflamação leve da câmara anterior, presença de vitrite)10).
Complicações de longo prazo
- Edema macular cistóide (EMC): principal causa de redução da acuidade visual
- Edema de papila e atrofia do nervo óptico
- Em casos de uso de implante de esteroide (fluocinolona), a elevação da pressão intraocular é observada em até 40%, podendo necessitar de trabeculectomia
Coriopatia serpiginosa (Serpiginous choroidopathy)
Seção intitulada “Coriopatia serpiginosa (Serpiginous choroidopathy)”A coroidopatia serpentina é uma coroidite crônica bilateral que ocorre entre os 30 e 50 anos (ligeiramente mais comum em homens), caracterizada por lesões amarelo-acinzentadas em forma de mapa que se estendem serpentinamente a partir da região peripapilar.
Padrão de progressão característico
- Inicia-se centripetamente a partir da região peripapilar, com as bordas da lesão se expandindo gradualmente de forma serpentina
- Fase ativa: surge uma borda acinzentada nas margens da lesão
- Fase cicatricial: fixa-se como uma lesão de atrofia retinocoroidal
- Nas recidivas, a nova inflamação sempre surge a partir das bordas da cicatriz pré-existente (isto é característico)
- O intervalo entre recidivas varia de 3 meses a 4 anos, com grande variação individual
Mais importante: Diferenciação do tipo relacionado à tuberculose (SLC)
A coroidite serpiginosa-like relacionada à tuberculose (serpiginous-like choroiditis; SLC) tem achados de imagem muito semelhantes à coroidite serpiginosa, mas a abordagem terapêutica é fundamentalmente diferente:
| Ponto de diferenciação | Coroidite serpiginosa | Tipo relacionado à tuberculose (SLC) |
|---|---|---|
| Distribuição das lesões | Centrada na papila, centrípeta | Polo posterior à periferia, múltipla |
| IGRA/TST | Negativo | Positivo |
| Forma da lesão | Geográfica e contínua | Múltiplas lesões pequenas e descontínuas |
| Tratamento | Esteroides + imunossupressores | Fármacos antituberculose são essenciais |
Como o uso de imunossupressores na SLC agrava significativamente a tuberculose, o teste IGRA (Quantiferon) antes do tratamento é absolutamente indispensável2).
Manejo da CNV associada (até 35%)
Na coroidite serpiginosa, a CNV está associada em até 35% dos casos e, se atingir a fóvea, causa perda visual irreversível. A injeção intravítrea de anti-VEGF (bevacizumabe, ranibizumabe) é eficaz18).
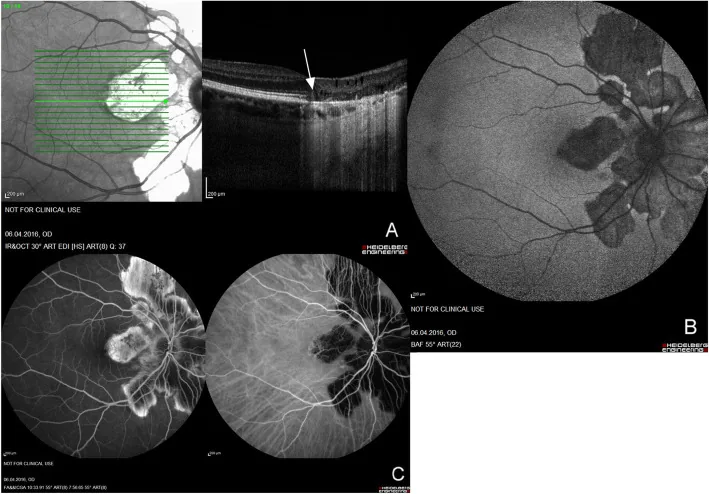
AZOOR (Retinopatia Externa Aguda Zonal Oculta)
Seção intitulada “AZOOR (Retinopatia Externa Aguda Zonal Oculta)”AZOOR é um conceito de doença proposto por Gass em 1992, sendo uma retinopatia externa que causa diminuição aguda da visão, defeitos de campo visual e fotopsia, apesar do fundo de olho estar quase normal3).
Conceito do complexo AZOOR
O complexo AZOOR proposto por Jampol et al. é um conceito que entende MEWDS, AZOOR, PIC, MFC, AMN (neuroretinopatia macular aguda), AIBSE e AAOR como um continuum com base comum autoimune/inflamatória genética3).
Quadro clínico característico
- Ocorre predominantemente em mulheres jovens de 20 a 50 anos com miopia
- Fotopsia (photopsia) aparece frequentemente no início (especialmente luz em forma de faixa ou arco)
- Começa unilateral e, eventualmente, 76% tornam-se bilaterais
- O fundo de olho é quase normal na fase aguda (a característica é a discrepância entre a baixa acuidade visual e os achados de fundo)
- O defeito de campo visual tem padrão de faixa irregular (frequentemente contínuo com o ponto cego)
- Pode haver associação com doenças autoimunes (doença de Hashimoto, esclerose múltipla)
OCT e ERG são a chave para o diagnóstico
- O desaparecimento ou obscurecimento da zona elipsoide (linha IS/OS) na OCT é o achado mais importante
- Não se espera recuperação funcional em áreas onde a camada externa desapareceu na OCT (também útil para prognóstico)
- A redução da amplitude no ERG multifocal pode ser detectada mesmo com fundo de olho normal (mfERG é mais sensível que o ERG de campo total)
- A FAF infravermelha pode, às vezes, delinear a borda entre a lesão e a área normal
Tratamento e Prognóstico
Não há terapia estabelecida para AZOOR. Casos leves necessitam apenas de observação, mas casos graves (baixa acuidade visual ou defeitos extensos de campo visual) são tratados com pulsoterapia de metilprednisolona (1000 mg × 3 dias) seguida de prednisolona oral2). A maioria dos casos estabiliza em 6 meses, mas o campo visual em áreas com dano à camada externa não se recupera.
Tanto a AZOOR quanto a neurite óptica retrobulbar causam diminuição da acuidade visual e do campo visual com fundo de olho quase normal, necessitando de diagnóstico diferencial. Os pontos de diferenciação são: ① Na AZOOR, há redução da amplitude do ERG multifocal, enquanto na neurite óptica retrobulbar o ERG é normal; ② Na AZOOR, o defeito de campo visual mostra um padrão em faixa ou arqueado irregular, enquanto na neurite óptica retrobulbar o escotoma central é mais comum; ③ Na AZOOR, o RAPD geralmente é leve, enquanto na neurite óptica retrobulbar há RAPD acentuado; ④ Na OCT, a AZOOR mostra desaparecimento da zona elipsoide, enquanto a neurite óptica retrobulbar mostra edema de papila ou afinamento da RNFL, auxiliando no diagnóstico diferencial2, 3).
5. Como usar exames de imagem
Seção intitulada “5. Como usar exames de imagem”Divisão de papéis por modalidade
Seção intitulada “Divisão de papéis por modalidade”Compreender claramente o papel de cada exame de imagem é essencial para o diagnóstico preciso e a avaliação da atividade da síndrome do ponto branco 1, 5).
| Modalidade | Indicação e papel mais fortes |
|---|---|
| AF (Angiografia Fluoresceínica) | Avaliação de vazamento vascular retiniano, EPR e coriocapilar. Confirmação do fenômeno de inversão fluorescente na APMPPE. Confirmação da hiperfluorescência em forma de grinalda na MEWDS. Avaliação de vasculite (Birdshot). |
| ICGA (Angiografia com Verde de Indocianina) | Avaliação direta do distúrbio da circulação coroidal. Detecção de lesões mais precoce que a FA (especialmente Birdshot, APMPPE, Serpiginosa). Detecção de lesões mais extensas do que os achados clínicos (MEWDS, PIC). Mais sensível para detectar lesões ativas. |
| FAF (Autofluorescência de Fundo) | Avaliação não invasiva da disfunção do EPR. Determinação de atividade (APMPPE, serpiginosa). Diagnóstico de MEWDS (pontos brancos precoces hiperautofluorescentes). Avaliação de cronicidade em Birdshot (hipoautofluorescência peripapilar em 73%) |
| OCT (Tomografia de Coerência Óptica) | Avaliação da zona elipsoide (achados diagnósticos em MEWDS e AZOOR). Avaliação da evolução da lesão em 5 estágios (PIC). Avaliação de CNV e edema macular. Predição prognóstica (perda da EZ → mau prognóstico visual) |
| OCT-A | Detecção não invasiva de flow void na coriocapilar (APMPPE, serpiginosa, PIC). Detecção precoce e sensível de CNV (mais sensível que FA em PIC e MFC). Avaliação do fluxo sanguíneo coroidal por camadas em Birdshot. Monitoramento da resposta terapêutica |
| ERG multifocal / campo total | Diagnóstico de AZOOR (amplitude do ERG reduzida mesmo com fundo quase normal). Monitoramento de atividade de Birdshot (atraso no flicker de 30Hz é o mais sensível). Avaliação de resposta ao tratamento |
Guia «Qual exame primeiro» por doença
Seção intitulada “Guia «Qual exame primeiro» por doença”Quando houver suspeita de MEWDS
Quando há suspeita de APMPPE
Quando houver suspeita de PIC/MFC
Quando suspeitar de coroidite serpiginosa
A estratégia difere conforme a doença. Na APMPPE e na coroidite serpiginosa, a ICGA visualiza mais diretamente o distúrbio circulatório coroidal, portanto, realizar a ICGA simultaneamente ou após a FA aprofunda a compreensão da doença. Na MEWDS, a hiperfluorescência em forma de grinalda (wreath-like) na FA é importante para o diagnóstico. No entanto, como esses exames são invasivos, muitas informações agora podem ser substituídas pelo OCT-A, e a combinação de FAF com OCT-A é utilizada como avaliação inicial1, 5).
Significado das lesões hipofluorescentes na ICGA
Seção intitulada “Significado das lesões hipofluorescentes na ICGA”A hipofluorescência que as lesões da síndrome dos pontos brancos mostram na ICGA é um reflexo direto da interrupção do fluxo sanguíneo coroidal (oclusão da coriocapilar)1). A ICGA é uma modalidade mais sensível que a FA na avaliação da circulação coroidal, com as seguintes características:
- Hipofluorescência em todas as fases: Observada na APMPPE, coroidite serpiginosa, PIC e MFC. Reflete oclusão grave da isquemia da camada capilar coroidal.
- Hipofluorescência tardia (sem anormalidades na FA): A hipofluorescência tardia na ICGA na MEWDS é explicada como uma alteração na captação de ICG devido a anormalidade do EPR, não por localização primária na coriocapilar (a coriocapilar é geralmente preservada na OCT-A) 1).
- Flow void na camada de Haller → flow void em todas as camadas na fase avançada: Padrão de progressão em duas etapas característico da Birdshot, do estroma coroidal para a coriocapilar 14).
A ICGA também é superior na detecção de lesões ocultas clinicamente invisíveis (lesões subclínicas) em comparação com FA e OCT-A, especialmente na MEWDS e PIC, revelando lesões coroidais mais extensas do que os pontos brancos 1, 15).
Mapa de doenças por padrões de hipo e hiperfluorescência na FAF
Seção intitulada “Mapa de doenças por padrões de hipo e hiperfluorescência na FAF”O padrão de FAF (autofluorescência de fundo) reflete o estado metabólico do EPR e é útil para o diagnóstico e avaliação de atividade da síndrome dos pontos brancos 16).
| Padrão de FAF | Doença/Estágio | Significado |
|---|---|---|
| Autofluorescência alta (hiper AF) | MEWDS fase aguda · Borda ativa da Serpiginosa | Acúmulo de produtos de degeneração fotorreceptora (ex.: A2E) no EPR |
| Autofluorescência baixa (hipo AF) | APMPPE fase cicatricial · Lesões ativas de PIC · Peripapilar em Birdshot | Perda de EPR ou perda de função |
| Halo de baixa AF central + alta AF periférica | Borda ativa de serpiginoso e PIC | Padrão de dano ao EPR na borda ativa |
| AF anormal em faixa | AZOOR | Corresponde à distribuição do dano à camada externa dos fotorreceptores |
| Hiperautofluorescência granular foveal | MEWDS (NIR-FAF) | Visualização não invasiva da granularidade foveal |
Na Birdshot, hipoautofluorescência confluente peripapilar é observada em 73% dos casos, sendo útil como indicador de cronicidade17).
Padrão de defeito da zona elipsoide (EZ) na OCT
Seção intitulada “Padrão de defeito da zona elipsoide (EZ) na OCT”A avaliação da EZ (zona elipsoide, antiga linha IS/OS) desempenha papel central na avaliação da atividade e prognóstico das síndromes de pontos brancos1).
| Achado de EZ | Doença/Estágio | Prognóstico |
|---|---|---|
| EZ acentuadamente desorganizado → recuperação | MEWDS fase aguda → fase de recuperação | Bom (recuperação da EZ associada à recuperação da visão) |
| Desaparecimento da EZ (correspondente à lesão) | Fase ativa da AZOOR | Sem recuperação funcional na área de desaparecimento |
| Desorganização da EZ + hiper-refletividade da retina externa | Fase aguda da APMPPE | Pode haver atrofia parcial residual após recuperação |
| Elevação hiper-refletiva sub-RPE + ruptura da EZ | PIC/MFC (evolução de 5 estágios) | Prognóstico ruim com CNV associada |
| Perda da EZ (com edema macular cístico) | Birdshot em estágio avançado | Fator de risco para mau prognóstico visual |
O vazio de fluxo da coriocapilar na OCT-A mostra alta concordância com os achados de FA e ICGA (particularmente útil na APMPPE e coroidite serpiginosa) 5, 13).
Padrões de fluorescência na FA: atraso de preenchimento vs hiperfluorescência vs vazamento
Seção intitulada “Padrões de fluorescência na FA: atraso de preenchimento vs hiperfluorescência vs vazamento”| Padrão FA | Doença | Significado clínico |
|---|---|---|
| Hipofluorescência precoce → hiperfluorescência tardia (fenômeno de inversão fluorescente) | APMPPE | Isquemia da coriocapilar. Distúrbio de fluxo precoce → vazamento tardio de corante dos tecidos circundantes |
| Hiperfluorescência precoce em forma de coroa (wreath-like) | MEWDS | Reflete diretamente dano ao EPR/fotorreceptores. Não se expande na fase tardia, auxiliando no diagnóstico diferencial |
| Hipofluorescência precoce → vazamento tardio | Fase ativa de Serpiginous/MFC | Evidência de coroidite ativa |
| Hiperfluorescência precoce na fase arterial → vazamento tardio | Fase ativa da PIC | Sugere presença de CNV inflamatória |
| Vazamento vascular + hiperfluorescência do disco (sem vazamento) | Birdshot | Evidência direta de vasculite retiniana |
| Normal a leve | AZOOR | Caracterizado por dissociação: defeitos de campo visual e anormalidades no ERG são encontrados mesmo com FA negativo |
6. Tratamento Geral
Seção intitulada “6. Tratamento Geral”Escolha da Estratégia de Tratamento
Seção intitulada “Escolha da Estratégia de Tratamento”O tratamento da síndrome dos pontos brancos varia muito dependendo da história natural da doença, gravidade e presença de CNV.
Observação (sem necessidade de tratamento) é o princípio para doenças
Seção intitulada “Observação (sem necessidade de tratamento) é o princípio para doenças”- Forte tendência à melhora espontânea, frequentemente se recupera sem tratamento especial2)
- MEWDS: Os pontos brancos desaparecem e a visão melhora em semanas. Apenas em casos graves ou com edema de papila, corticosteroides orais são usados
- APMPPE: As manchas brancas regridem em 7-12 dias, o prognóstico visual geralmente é bom
Doenças em que a corticoterapia é o tratamento principal
Seção intitulada “Doenças em que a corticoterapia é o tratamento principal”APMPPE (grave/com papilite) · PIC (lesão ativa próxima à fóvea) · AZOOR (casos graves)
- Prednisolona 30–60 mg/dia, iniciar e reduzir gradualmente
- APMPPE com vasculite cerebral requer pulsoterapia com metilprednisolona e colaboração com neurologia
- Critério de gravidade do AZOOR: acuidade visual corrigida do olho melhor < 0,3 (Diretrizes de Diagnóstico da Sociedade Japonesa de Oftalmologia)
Doenças que necessitam de terapia imunossupressora de longo prazo
Seção intitulada “Doenças que necessitam de terapia imunossupressora de longo prazo”Coriorretinite birdshot, coroidite serpentina e MFC
Birdshot (Manejo de Longo Prazo)
- Prednisolona 0,5-1 mg/kg/dia como dose inicial
- Micofenolato de mofetila (MMF) 2-3 g/dia (imunossupressor de primeira linha)
- Metotrexato (MTX) 10-25 mg/semana
- Azatioprina (AZA) 1-3 mg/kg/dia
- Casos refratários: Adalimumabe (93,2% usado como agente biológico de primeira linha)
- Sem tratamento, 16-22% têm acuidade visual ≤0,1 em 10 anos
Coroidite serpentina (manejo de longo prazo)
- Prednisolona 40-80 mg/dia como dose inicial (redução gradual)
- Azatioprina 1-2,5 mg/kg/dia (terapia de manutenção de primeira linha)
- Micofenolato de mofetila / Metotrexato (alternativas)
- Casos refratários: clorambucil (mais potente; ≤0,2 mg/kg/dia, hemograma semanal obrigatório)
- Agentes biológicos: adalimumabe (91,0% recomendado como primeira escolha)
- Após excluir tuberculose (se IGRA positivo, administrar medicamentos antituberculose primeiro), introduzir imunossupressores
Terapia de imunomodulação para MFC
Seção intitulada “Terapia de imunomodulação para MFC”Como a MFC segue um curso crônico e recidivante, muitos casos necessitam de medicamentos imunomoduladores como terapia de manutenção após a redução gradual dos corticosteroides.
| Medicamento | Dose de Referência | Notas especiais |
|---|---|---|
| Metotrexato (MTX) | 10–25 mg/semana | Usar com ácido fólico 1 mg/dia. Monitorar hepatotoxicidade |
| Azatioprina (AZA) | 1–3 mg/kg/dia | Recomenda-se verificar atividade da TPMT. Atenção à supressão medular |
| Micofenolato de mofetila (MMF) | 1-3 g/dia | Sintomas gastrointestinais são efeitos colaterais comuns |
| Ciclosporina (CsA) | 3-5 mg/kg/dia | Monitoramento da função renal e pressão arterial obrigatório |
| Adalimumabe | 40 mg a cada 2 semanas (subcutâneo) | Casos refratários ou dependentes de esteroides. Triagem de tuberculose obrigatória |
Manejo da CNV associada
Seção intitulada “Manejo da CNV associada”A CNV é a complicação mais importante que afeta o prognóstico visual, ocorrendo com frequência em PIC, MFC e coroidite serpentina.
| Doença | Taxa de CNV | Tratamento |
|---|---|---|
| PIC | 40–76% | Injeção intravítrea de anti-VEGF (bevacizumabe, ranibizumabe, aflibercepte) + esteroide. Estratégia OCTA PRN |
| MFC | Até 60% | Injeção intravítrea de anti-VEGF + terapia imunomoduladora |
| Coroidite serpentina | Até 35% | Injeção intravítrea de anti-VEGF (bevacizumabe, ranibizumabe) |
| MEWDS・APMPPE | Raro | Anti-VEGF (se CNV confirmado) |
| Birdshot | Raro | Terapia imunossupressora sistêmica + anti-VEGF se houver CNV |
A CNV inflamatória (iCNVM) difere da CNV da degeneração macular relacionada à idade; controlar a inflamação subjacente também é importante para prevenir a recorrência da CNV. Na PIC e MFC, a abordagem bidirecional com anti-VEGF e esteroides (ou imunossupressores) é considerada eficaz, enquanto o anti-VEGF isolado deixa risco de recidiva 7, 8).
Avisos sobre o Tratamento
Seção intitulada “Avisos sobre o Tratamento”| Aviso | Doença Relacionada |
|---|---|
| Exclusão de tuberculose como prioridade máxima (antes da imunossupressão) | Coroioidite serpiginosa / MFC |
| Considerar HLA-A29 (diagnóstico) | Birdshot (baixa sensibilidade em japoneses) |
| Risco de aumento da pressão intraocular com implante de esteroide | Birdshot (até 40% necessitam de trabeculectomia) |
| Risco de supressão da medula óssea e neoplasia com clorambucila | Coroidite serpentina (exame de sangue semanal obrigatório) |
| Ressurgimento após infecção ou vacina contra COVID-19 | PIC e MEWDS (relatos de ressurgimento) |
| Manejo de emergência na vasculite cerebral | APMPPE (cefaleia, sintomas neurológicos → RM cerebral urgente) |
Os exames obrigatórios a serem realizados antes de iniciar imunossupressores para a síndrome dos pontos brancos são: ① Exclusão de tuberculose com IGRA (Quantiferon) (prioridade máxima na coroidite serpentina), ② Triagem de hepatite viral com HBsAg, anti-HBc e anti-HCV (para prevenir reativação por imunossupressão), ③ Radiografia de tórax e TC (para excluir tuberculose e sarcoidose), ④ Hemograma completo e testes de função hepática e renal (para verificar valores basais). Para agentes biológicos como adalimumabe, a triagem de tuberculose também é obrigatória conforme a bula do medicamento19, 20).
Diferentemente da degeneração macular relacionada à idade, a CNV inflamatória (iCNVM) pode regredir espontaneamente quando a inflamação é controlada. Geralmente, utiliza-se a estratégia PRN (conforme necessário), administrando-se sempre que uma CNV ativa for confirmada na OCT-A. Pode-se realizar uma dose de ataque inicial (3 doses consecutivas), mas o número de doses necessárias pode ser reduzido quando combinado com terapia imunossupressora. O risco de recidiva é alto apenas com anti-VEGF, sendo importante uma abordagem bidirecional com controle da inflamação subjacente 7, 8).
6.5 Associação com Doenças Sistêmicas
Seção intitulada “6.5 Associação com Doenças Sistêmicas”Cada doença das síndromes de pontos brancos é conhecida por estar associada a doenças sistêmicas ou infecções específicas, sendo importante uma investigação sistemática de exclusão antes do tratamento.
| Doença | Doenças ou condições sistêmicas associadas | Significância clínica |
|---|---|---|
| APMPPE | Vasculite cerebral (MCAT) · Infecção estreptocócica · Vírus EB | Cefaleia · Sintomas neurológicos → RM cerebral de urgência |
| Birdshot | HLA-A29 (80-98% em brancos) · Semelhante à sarcoidose | Teste de HLA auxilia no diagnóstico (baixa sensibilidade em japoneses) |
| Coroidite serpentina | Tuberculose (SLC) · HLA-B7/A2 | IGRA positivo → princípio de tratamento anti-tuberculose prévio |
| PIC | Sarcoidose · HLA-DRB1*15 | Considerar TC de tórax e medição de ACE |
| MFC | Haplótipo IL-10 · EBV · sarcoidose | Reavaliar a investigação sistêmica em casos crônicos recorrentes |
| MEWDS | Infecção por COVID-19 · pós-vacinação · HLA-B51 | A infecção por SARS-CoV-2 atua como gatilho imunológico |
| AZOOR | Doença de Hashimoto, esclerose múltipla, doenças autoimunes | Considerar testes de função tireoidiana e autoanticorpos |
7. Observações Especiais e Descobertas Recentes para Cada Doença
Seção intitulada “7. Observações Especiais e Descobertas Recentes para Cada Doença”APMPPE e o Espectro da Coriorretinite Placóide
Seção intitulada “APMPPE e o Espectro da Coriorretinite Placóide”A APMPPE é agora compreendida de forma integrada dentro do “espectro da coriorretinite placóide”, juntamente com a maculopatia placóide persistente (PPM) e a coriorretinite placóide implacável (RPC). Nessas três doenças, a OCT-A mostra um padrão comum de ausência de fluxo na coriocapilar, indicando que a isquemia da lâmina coriocapilar é a base fisiopatológica comum5).
Klufas et al. (2017) relataram que a OCT-A detecta ausência de fluxo na coriocapilar na APMPPE, PPM e RPC com alta concordância com a angiografia fluoresceínica e a angiografia com indocianina verde, apoiando o conceito de espectro da coriorretinite placóide5).
MEWDS e Granularidade Foveal
Seção intitulada “MEWDS e Granularidade Foveal”A granularidade foveal é um achado diagnóstico presente em 74-96% dos casos de MEWDS, podendo permanecer como o único achado após o desaparecimento dos pontos brancos. A autofluorescência de infravermelho próximo (NIR-FAF) revela um padrão granular foveal característico9).
Espectro de Doenças PIC e MFC
Seção intitulada “Espectro de Doenças PIC e MFC”PIC e MFC (MFCwP) compartilham uma base genética comum (haplótipo IL-10 · HLA-DRB1*15) e são considerados fenótipos diferentes do mesmo espectro de doença. Os principais pontos de diferenciação são a presença ou ausência de vitrite e inflamação da câmara anterior, bem como a distribuição das lesões1, 3).
| Ponto de diferenciação | PIC | MFC (MFCwP) |
|---|---|---|
| Vitrite | Ausente | Presente (ponto de diferenciação importante) |
| Inflamação da câmara anterior | Ausente | Leve |
| Distribuição das lesões | Limitado ao polo posterior | Polo posterior + região periférica média |
| Tamanho da lesão | 100–300 μm | 45–350 μm |
| Taxa de complicação de CNV | 40–76% | Até 60% |
Birdshot e HLA-A29
Seção intitulada “Birdshot e HLA-A29”A associação entre Birdshot e HLA-A29 é uma das mais fortes associações genéticas conhecidas, com risco relativo aumentado de 50 a 224 vezes em pacientes brancos4). No entanto, como portadores de HLA-A29 são raros no Japão, a sensibilidade do HLA-A29 no diagnóstico é limitada. O diagnóstico deve enfatizar os achados clínicos dos critérios SUN 2021 (achados de fundo de olho, inflamação anterior leve, vitrite)10).
Complexo AZOOR e gatilhos virais
Seção intitulada “Complexo AZOOR e gatilhos virais”Acredita-se que o AZOOR ocorra devido a uma predisposição genética (como haplótipo IL-10) combinada com gatilhos ambientais como infecção viral, vacina ou medicamentos, sendo compreendido como parte do complexo AZOOR junto com MEWDS, PIC, AMN e AIBSE3). Casos de MEWDS após infecção ou vacinação por COVID-19 aumentaram globalmente, sugerindo que o SARS-CoV-2 pode atuar como gatilho imunológico11).
Sim. Vários casos de MEWDS, PIC e coroidite serpentina foram relatados após infecção por COVID-19, sugerindo que a infecção por SARS-CoV-2 pode funcionar como um gatilho imunológico11, 12). Para MEWDS, há uma revisão sistemática de 27 casos após vacinação contra COVID-19, sendo a vacina de mRNA (Pfizer-BioNTech) a mais frequente. Pacientes com histórico prévio devem consultar um oftalmologista sobre o acompanhamento antes e após a vacinação.
Ao suspeitar inicialmente de síndrome dos pontos brancos, a ordem de prioridade dos exames recomendada é: ① FAF + OCT (não invasivo e permite avaliação inicial de quase todas as doenças; pode mostrar autofluorescência elevada na MEWDS, avaliação da zona elipsoide e elevação sub-RPE na PIC) → ② OCT-A (detecção precoce de CNV e avaliação de flow void coriocapilar) → ③ FA + ICGA (quando necessário para diagnóstico definitivo e avaliação de atividade). Se houver suspeita de coroidite serpentina, IGRA (para excluir tuberculose) deve ser priorizado antes da FA. Se houver suspeita de AZOOR, o ERG (multifocal) é obrigatório1, 2).
8. Artigos Relacionados
Seção intitulada “8. Artigos Relacionados”9. Referências
Seção intitulada “9. Referências”- Testi I, Modugno RL, Pavesio C. Multimodal imaging supporting the pathophysiology of white dot syndromes. J Ophthalmic Inflamm Infect. 2021;11:32.
- 日本眼炎症学会・日本眼科学会. ぶどう膜炎診療ガイドライン(13〜18節:APMPPE・MEWDS・PIC・多発性脈絡膜炎・バードショット・蛇行状脈絡膜炎・AZOOR). 日本眼科学会雑誌. 2019;123(6):635-696.
- Jampol LM, Becker KG. White spot syndromes of the retina: a hypothesis based on the common genetic hypothesis of autoimmune/inflammatory disease. Am J Ophthalmol. 2003;135(3):376-379.
- Agrawal R, et al. The role of HLA-A29 in birdshot chorioretinopathy and immune checkpoint inhibitor-related uveitis. Am J Ophthalmol. 2025. doi:10.1016/j.ajo.2024.01.007
- Klufas MA, Phasukkijwatana N, Iafe NA, et al. Optical coherence tomography angiography reveals choriocapillaris flow reduction in placoid chorioretinitis. Ophthalmol Retina. 2017;1(1):77-91.
- Stattin M, Forster J, Ahmed D, Krepler K, Ansari-Shahrezaei S. Swept Source-Optical Coherence Tomography Angiography for Management of Secondary Choroidal Neovascularization in Punctate Inner Choroidopathy. Case Rep Ophthalmol. 2021;12:232-238.
- Spaide RF, Goldberg N, Freund KB. Redefining multifocal choroiditis and panuveitis and punctate inner choroidopathy through multimodal imaging. Retina. 2013;33(7):1315-1324.
- Leclaire MD, Clemens CR, Eter N, Mihailovic N. Choroidale Neovaskularisation infolge einer “punctate inner choroidopathy”, dargestellt mittels optischer Kohärenztomographie-Angiographie. Ophthalmologe. 2021;118:842-846.
- Mantovani A, Invernizzi A, Staurenghi G, Herbort CP Jr. Multiple evanescent white dot syndrome: a multimodal imaging study of foveal granularity. Ocul Immunol Inflamm. 2019;27(1):141-147.
- Standardization of Uveitis Nomenclature (SUN) Working Group. Classification criteria for birdshot chorioretinitis. Am J Ophthalmol. 2021;228:65-71.
- Chen N, Mandell M, Arjmand P. Multimodal imaging findings of multiple evanescent white dot syndrome in COVID-19 patients. IDCases. 2024;38:e02110.
- Seddigh S, Pinto A, Zaki AM, Gupta RR. Serpiginous choroiditis after COVID-19 infection. J Vitreoretinal Dis. 2025;9(2):246-252.
- Pakzad-Vaezi K, Khaksari K, Chu Z, Van Gelder RN, Wang RK, Pepple KL. Swept-source OCT angiography of serpiginous choroiditis. Ophthalmol Retina. 2018;2(7):712-719.
- Pepple KL, Chu Z, Weinstein J, Munk MR, Van Gelder RN, Wang RK. Use of en face swept-source optical coherence tomography angiography in identifying choroidal flow voids in 3 patients with birdshot chorioretinopathy. JAMA Ophthalmol. 2018;136(11):1288-1292. doi:10.1001/jamaophthalmol.2018.3474. PMID:30128478. PMCID:PMC6248174
- Khochtali S, Dridi T, Abroug N, et al. Swept-source optical coherence tomography angiography shows choriocapillaris flow reduction in multiple evanescent white dot syndrome. J Curr Ophthalmol. 2020;32(2):211-215.
- Yeh S, Forooghian F, Wong WT, et al. Fundus autofluorescence imaging of the white dot syndromes. Arch Ophthalmol. 2010;128(1):46-56.
- Minos E, Barry RJ, Southworth S, et al. Birdshot chorioretinopathy: current knowledge and new concepts in pathophysiology, diagnosis, monitoring and treatment. Orphanet J Rare Dis. 2016;11(1):61.
- Maleki A, Maldonado Cerda A, Garcia CM, et al. Chlorambucil combination therapy in refractory serpiginous choroiditis: a cure? Am J Ophthalmol Case Rep. 2021;21:101014.
- Niederer RL, Al-Janabi A, Engelbrecht C, et al. Immunomodulatory therapy prescribing practices for non-infectious uveitis: a survey of international experts. Br J Ophthalmol. 2024;108:482-489.
- Tomkins-Netzer O, et al. Treatment of non-infectious uveitis with biologics: a survey of the International Ocular Inflammation Society. Br J Ophthalmol. 2022;106:482-488.
