Type à prédominance rétinienne externe

Syndrome des points blancs
Points clés en un coup d’œil
Section intitulée « Points clés en un coup d’œil »1. Qu’est-ce que le syndrome des points blancs ?
Section intitulée « 1. Qu’est-ce que le syndrome des points blancs ? »Le syndrome des points blancs (white dot syndromes) est un concept nommé par Gass en 1977, désignant un groupe de maladies inflammatoires caractérisées par de multiples lésions tachetées blanches ou blanc-jaunâtre au fond d’œil. Bien que la définition des maladies cibles varie selon les chercheurs, il est aujourd’hui largement utilisé pour désigner un groupe de maladies inflammatoires idiopathiques non infectieuses touchant principalement la rétine externe, l’EPR, la choriocapillaire et la choroïde 1).
Selon les directives cliniques pour l’uvéite (Journal de la Société japonaise d’ophtalmologie 2019;123(6):635-696), les classifications des uvéites postérieures incluent l’APMPPE, le MEWDS, la PIC, la choriorétinite multifocale, la choriorétinopathie de Birdshot, la choriorétinite serpigineuse et l’AZOOR comme entités distinctes. Le terme générique « syndrome des points blancs » est utilisé pour les regrouper2).
Concept de classification
Section intitulée « Concept de classification »Grâce aux progrès récents de l’imagerie multimodale (y compris l’OCT-A), le syndrome des points blancs est désormais classé en trois groupes selon la couche principale de la lésion1).
Type à prédominance de la choriocapillaire
Type à prédominance du stroma choroïdien
Choriorétinopathie de Birdshot
- Infiltration lymphocytaire du stroma choroïdien comme lésion primaire
- À l’OCT-A, flow void dans la couche de Haller, épargne initiale des choriocapillaires
- Évolution chronique progressive et forte association avec HLA-A29
De plus, le concept de complexe AZOOR a été proposé, intégrant MEWDS, AZOOR, PIC, MFC, AMN, AIBSE et AAOR comme un continuum partageant une base génétique auto-immune/inflammatoire commune3).
Épidémiologie au Japon
Section intitulée « Épidémiologie au Japon »Selon les statistiques de la Société japonaise d’inflammation oculaire, la proportion de chaque maladie du syndrome des points blancs dans l’ensemble des uvéites est la suivante 2).
| Maladie | Proportion dans l’ensemble des uvéites |
|---|---|
| MEWDS | Environ 1 à 2 % (rapports nationaux) |
| APMPPE | Rare (pas de statistiques claires sur l’incidence annuelle) |
| PIC | Rare |
| Choroïdite serpigineuse | Environ 0,3 % |
| Choriorétinopathie en pastilles (birdshot) | Rare (plus fréquente chez les Blancs, extrêmement rare au Japon) |
| AZOOR | rare (nombre de cas en augmentation récente) |
2. Tableau clinique commun
Section intitulée « 2. Tableau clinique commun »Les symptômes de chaque maladie diffèrent, mais les caractéristiques cliniques suivantes sont communes au groupe des syndromes des points blancs 1, 2).
Schéma commun des symptômes subjectifs
Section intitulée « Schéma commun des symptômes subjectifs »- Baisse de l’acuité visuelle : l’étendue varie de légère (MEWDS, AZOOR) à sévère (choriorétinite serpigineuse, CNV compliquant PIC)
- Photopsie : symptôme le plus courant reflétant une atteinte de la rétine externe et des photorécepteurs
- Scotome et déficit du champ visuel : souvent paracentral ou central, correspondant à la lésion
- Métamorphopsie : survient en cas de lésion maculaire ou de CNV
Présence d’inflammation du segment antérieur
Section intitulée « Présence d’inflammation du segment antérieur »| Groupe de maladies | Inflammation de la chambre antérieure et du vitré |
|---|---|
| MEWDS, APMPPE, PIC | Généralement absente (APMPPE peut être légère) |
| MFC (MFCwP) | Inflammation de la chambre antérieure + hyalite (point de différenciation avec PIC) |
| Birdshot | Inflammation de la chambre antérieure absente à minime, hyalite présente |
| Choroïdite serpigineuse | Inflammation de la chambre antérieure et vitréite généralement légères |
| AZOOR | Généralement absente |
3. Approche du diagnostic différentiel
Section intitulée « 3. Approche du diagnostic différentiel »Âge, sexe, unilatéral vs bilatéral, récidive
Section intitulée « Âge, sexe, unilatéral vs bilatéral, récidive »Jeune femme, unilatéral, amélioration spontanée
Femmes jeunes à d'âge moyen, bilatéral, risque de CNV
Jeune à moyen âge, bilatéral, apparition aiguë
- Survient principalement chez les 20-30 ans (âge moyen 25 ans), pas de différence de sexe
- Bilatéral, aigu, tendance à la résolution spontanée
- Attention à la complication de vascularite cérébrale (examen urgent en cas de symptômes neurologiques)
Âge moyen/avancé, bilatéral, chronique et progressif
Birdshot·Choroïdite serpigineuse
- Birdshot : 40-60 ans, légèrement plus fréquent chez les femmes
- En forme de serpent : 30-50 ans, légèrement plus fréquent chez les hommes
- Les deux maladies sont chroniques, récurrentes et nécessitent une immunosuppression à long terme.
- Taux de positivité HLA-A29 dans la maladie de Birdshot (population blanche) : 80 à 98 %
Arbre décisionnel de diagnostic différentiel
Section intitulée « Arbre décisionnel de diagnostic différentiel »眼底に白点状病変 │ ├─ 片眼性? │ ├─ YES → MEWDS・AZOOR・AMN を考慮 │ │ ↳ FA で初期過蛍光 → MEWDS │ │ ↳ 眼底ほぼ正常・ERG 異常 → AZOOR │ └─ NO(両眼性) │ ├─ 急性発症・後極部大型白斑? │ └─ YES → APMPPE(FA 蛍光逆転現象を確認) │ ├─ 後極部小病変・近視女性・硝子体炎なし? │ └─ YES → PIC を考慮(CNV 検索:OCTA 必須) │ ├─ 小病変・硝子体炎あり・周辺部にも病変? │ └─ YES → MFC(MFCwP)を考慮 │ ├─ 乳頭周囲から蛇行状に進展・男性多め? │ └─ YES → 蛇行状脈絡膜炎(結核除外が最優先) │ └─ 後極部散弾状病変・中高年・HLA-A29? └─ YES → Birdshot 網脈絡膜症4. Comparaison des principales maladies
Section intitulée « 4. Comparaison des principales maladies »Tableau comparatif principal : matrice des 7 maladies
Section intitulée « Tableau comparatif principal : matrice des 7 maladies »| Élément | APMPPE | MEWDS | PIC | MFC (MFCwP) | Birdshot | Choroïdite serpigineuse | AZOOR |
|---|---|---|---|---|---|---|---|
| Âge de prédilection | 20-30 ans (moyenne 25 ans) | 20-50 ans | 18-40 ans (moyenne 36 ans) | Moyenne 30 ans | 40-60 ans | 30-50 ans | Principalement autour de 35 ans |
| Sexe | Pas de différence de sexe | Prédominance féminine (1:4) | Prédominance féminine (environ 90%) | Prédominance féminine (surtout chez les femmes blanches) | Légèrement plus fréquent chez les femmes | Légèrement plus fréquent chez les hommes | Prédominance féminine (environ 75%) |
| Unilatéral/Bilatéral | Surtout bilatéral | Unilatéral (>95%) | Surtout bilatéral (80%) | Bilatéral | Bilatéral | Bilatéral | Unilatéral puis bilatéral (finalement 76% bilatéral) |
| Principaux symptômes | Baisse de l’acuité visuelle, scotome central, métamorphopsie | Baisse de l’acuité visuelle, photopsie, vision trouble | Scotome, baisse de l’acuité visuelle, métamorphopsie | Myodésopsies, baisse de l’acuité visuelle, photopsie | Baisse de l’acuité visuelle, héméralopie, dyschromatopsie | Baisse de l’acuité visuelle, scotome paracentral | Photopsie, déficit du champ visuel (fond d’œil quasi normal) |
| Caractéristiques des taches blanches du fond d’œil | Grandes taches blanc crème au pôle postérieur (1/4 à 1/2 diamètre papillaire) | Petites taches multiples gris-blanc pâles du pôle postérieur à l’équateur (100–200 μm) | Petites taches jaune-blanc au pôle postérieur (100–300 μm), 12–25 | Taches gris-jaune du pôle postérieur à la périphérie (45–350 μm), avec hyalite | Taches blanc crème en plombs de fusil du pôle postérieur à l’équateur (1/4 à 1/2 diamètre papillaire) | Lésions gris-jaune géographiques s’étendant en serpentin depuis la région péripapillaire | Fond d’œil presque normal (phase aiguë), atrophie des couches externes en phase tardive |
| Résultats OCT | Zone ellipsoïde perturbée + hyperréflectivité rétinienne externe, atrophie partielle résiduelle après récupération | Zone ellipsoïde nettement perturbée/disparue (phase aiguë) → récupération | Élévation hyperréflective sous-EPR + rupture de la zone ellipsoïde (évolution en 5 stades) | Hyperréflectivité sous-EPR + rupture de la zone ellipsoïde (similaire à la PIC) | Lésions choroïdiennes, œdème maculaire cystoïde, disparition de la zone ellipsoïde de mauvais pronostic | Phase active : hyperréflectivité rétinienne externe et liquide sous-rétinien. Phase cicatricielle : atrophie de l’EPR | Disparition de la zone ellipsoïde (IS/OS) : signe le plus important (correspond aux déficits du champ visuel) |
| Résultats de l’angiographie à la fluorescéine (FA) | Hypofluorescence précoce → hyperfluorescence tardive (phénomène d’inversion de fluorescence) | Hyperfluorescence en couronne (wreath-like) persistante dès le début | Phase active : hyperfluorescence précoce à la phase artérielle → fuite tardive | Phase active : hypofluorescence précoce → fuite tardive | Hyperfluorescence lésionnelle (sans fuite) + fuite vasculaire et hyperfluorescence papillaire | Phase active : hypofluorescence précoce → hyperfluorescence tardive (fuite) | Généralement normal ou anomalies mineures |
| Résultats ICGA | Hypofluorescence dans toutes les phases (reflète directement l’ischémie de la choriocapillaire) | Hypofluorescence tardive (plus étendue que les points blancs) | Hypofluorescence intermédiaire, utile pour détecter les lésions infracliniques | Hypofluorescence précoce à toutes les phases | Hypofluorescence précoce et intermédiaire → isofluorescence tardive (stade initial) → stade avancé : hypofluorescence dans toutes les phases | Hypofluorescence dans toutes les phases (reflète un trouble de la circulation choroïdienne) | Normalement normal |
| Résultats FAF | Phase aiguë : hypo- ou hyperautofluorescence. Phase de rémission : hypoautofluorescence | Phase aiguë : hyperautofluorescence (surtout hyperfluorescence). Après récupération : normalisation | Phase active : hypoautofluorescence (hypoAF), halo hyperautofluorescent en bordure | Phase active : hypoautofluorescence | Hypoautofluorescence confluente péripapillaire (observée dans 73% des cas) | Phase active : bordure hyperautofluorescente + halo hypoautofluorescent. Phase quiescente : hypoautofluorescence | Anomalies d’autofluorescence en bande, de l’hyper à l’hypoautofluorescence |
| Résultats OCT-A | Vide de flux choriocapillaire (forte concordance avec FA/ICGA) | Choriocapillaire généralement préservée (vide de flux transitoire partiel) | Vide de flux choriocapillaire (site de lésion inflammatoire) | Vide de flux choriocapillaire | Vide de flux de la couche de Haller (début) → stade avancé : vide de flux de pleine épaisseur | Vide de flux choriocapillaire (sévère) | Choriocapillaire généralement préservée |
| Récurrent | Rare (essentiellement unique) | Récidive dans environ 10% | Élevée (chronique récurrente) | Élevée (épisodes inflammatoires récurrents) | Élevée (chronique avec rémissions et rechutes) | Élevée (répétition tous les 3 mois à 4 ans) | Stable dans les 6 mois pour la plupart. Progression chez certains |
| Taux de CNV | rare | rare | 40–76 % (haut risque) | Jusqu’à 60 % | CNV sous-rétinienne : rare | Jusqu’à 35 % | Presque aucune |
| Associé au HLA | Aucun | HLA-B51 (rapport préliminaire) | HLA-DR2 · HLA-DRB1*15 | Associé à l’haplotype IL-10 | HLA-A29 (80 à 98 % chez les Caucasiens) | HLA-B7 · HLA-A2 (rapport d’association) | Aucun (prédisposition immunologique) |
| Stratégie thérapeutique | Surveillance (résolution spontanée), cas sévères : corticostéroïdes | Surveillance, cas sévères : corticostéroïdes à court terme, CNV : anti-VEGF | Surveillance (pas de CNV), CNV : anti-VEGF + corticostéroïdes, immunosuppresseurs | Corticostéroïdes + immunomodulateurs, CNV : anti-VEGF | Corticostéroïdes + mycophénolate mofétil / adalimumab (long terme) | Corticostéroïdes + immunosuppresseurs (incluant alkylants), CNV : anti-VEGF | Surveillance, cas sévères : bolus de corticostéroïdes |
| Pronostic visuel | Bon (résolution spontanée fréquente) | Bon (attention aux récidives et à la CNV) | Risque élevé de mauvais pronostic en cas de CNV associée | Risque de mauvais pronostic en cas de CNV et d’œdème maculaire | Sans traitement, 16 à 22 % ont une acuité visuelle ≤ 0,1 à 10 ans | Irréversible si atteinte fovéale, acuité finale < 20/200 dans jusqu’à 25 % des yeux | Souvent stable. Mauvais pronostic en cas de progression des lésions des couches externes |
La choriorétinopathie serpigineuse et la choriorétinopathie en plomb de fusil de chasse ont le pronostic visuel le plus défavorable. Dans la choriorétinopathie serpigineuse, jusqu’à 25% des yeux ont une acuité visuelle finale inférieure à 20/200, et dans la choriorétinopathie en plomb de fusil de chasse, sans traitement, 16 à 22% des patients ont une acuité visuelle inférieure à 0,1 après 10 ans2, 4). Les PIC et MFC présentent un risque élevé de mauvais pronostic en cas de complication par CNV. L’APMPPE et le MEWDS ont une forte tendance à la régression spontanée et un bon pronostic.
Tableau clinique détaillé de chaque maladie
Section intitulée « Tableau clinique détaillé de chaque maladie »APMPPE (épithéliopathie pigmentaire postérieure aiguë en plaques)
Section intitulée « APMPPE (épithéliopathie pigmentaire postérieure aiguë en plaques) »L’APMPPE survient préférentiellement chez les personnes âgées de 20 à 30 ans (moyenne 25 ans), sans différence de sexe. On pense qu’elle est due à une vascularite occlusive des artérioles afférentes du lit capillaire choroïdien, et une infection virale est suspectée comme facteur déclenchant1, 2).
Symptômes prodromiques et évolution
- Environ la moitié des patients présentent des symptômes pseudo-grippaux (grippe, virus EB, varicelle, infection streptococcique, etc.).
- Des taches blanches crème discoïdes de 1/4 à 1/2 diamètre papillaire apparaissent en grand nombre dans la région postérieure des deux yeux.
- Les taches blanches commencent à disparaître du centre en quelques jours et disparaissent en 7 à 12 jours, laissant une légère dépigmentation.
- Généralement, un seul épisode se résout spontanément (les récidives sont rares).
- Le pronostic visuel est généralement bon, mais peut être mauvais dans les cas graves ou ceux évoluant vers une choriorétinite en carte géographique.
Complication spécifique : vascularite cérébrale (MCAT)
APMPPE と中枢神経血管炎の合併(MCAT: multiple cerebral arterial thrombosis)は重篤な合併症であり、頭痛・発熱・神経症状が出現した場合は緊急で脳 MRI・MRA を施行する必要がある。脳血管炎合併例ではメチルプレドニゾロンパルス療法と神経内科連携が必要となる2)。
placoid chorioretinitis spectrum との関連
APMPPE は PPM(persistent placoid maculopathy)・RPC(relentless placoid chorioretinitis)とともに「placoid chorioretinitis spectrum」を形成し、脈絡膜毛細血管板虚血を共通病態基盤とする5)。
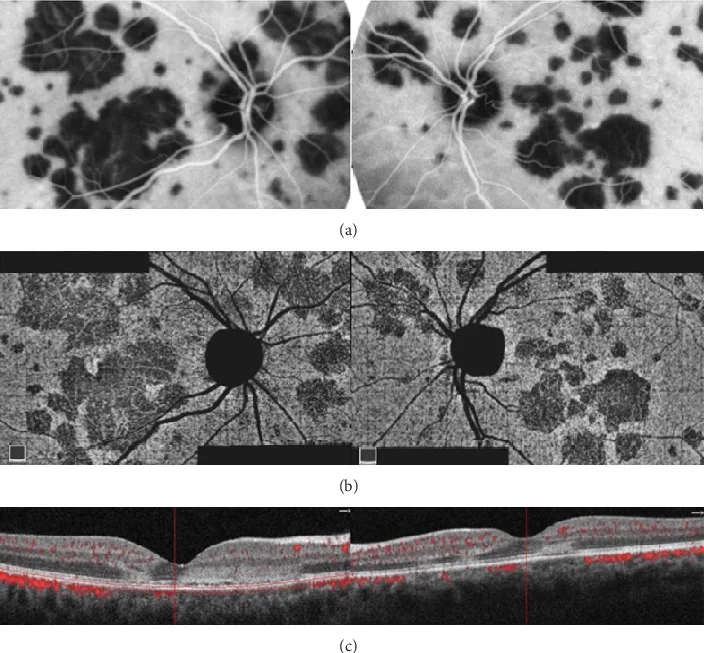
MEWDS (syndrome des points blancs évanescents multiples)
Section intitulée « MEWDS (syndrome des points blancs évanescents multiples) »Le MEWDS survient principalement chez les femmes âgées de 20 à 50 ans (ratio hommes-femmes 1:4) et se caractérise par une atteinte unilatérale, aiguë et une résolution spontanée.
Caractéristiques cliniques distinctives
- Petites taches gris-blanc pâles (100-200 μm) dans les couches profondes de la rétine au niveau de l’EPR, du pôle postérieur à l’équateur
- foveal granularity (granularité fovéale) : observée chez 74 à 96 % des patients, elle peut être la seule séquelle persistante après la disparition des points blancs. Elle présente un motif caractéristique en NIR-FAF (autofluorescence proche infrarouge)9)
- apparence de points orange (orange-dot appearance) : signe caractéristique observé sur les photographies du fond d’œil et l’imagerie infrarouge
- lésion ivoire : changement blanc pâle et flou au pôle postérieur du fond d’œil
- Des symptômes pseudo-grippaux précèdent environ 50 % des cas
- L’incidence annuelle est d’environ 0,22 cas pour 100 000 personnes, avec une récidive dans 10 % des cas
Hyperfluorescence en couronne (wreath-like) à l’angiographie à la fluorescéine (FA)
L’hyperfluorescence en couronne caractéristique dès le début de la FA est un point clé du diagnostic du MEWDS. Les lésions blanches deviennent hyperfluorescentes tôt à la FA et ne s’étendent pas tardivement. Cette hyperfluorescence précoce est un point de différenciation important avec l’hypofluorescence précoce de l’APMPPE (phénomène d’inversion de fluorescence)1, 9).
Continuité avec le complexe AZOOR
La MEWDS est principalement due à une destruction transitoire de la zone ellipsoïde (ligne IS/OS) des photorécepteurs et est comprise comme une maladie appartenant au complexe AZOOR. L’OCT montre une perturbation ou une disparition de la zone ellipsoïde en phase aiguë, qui s’améliore avec la récupération visuelle3).
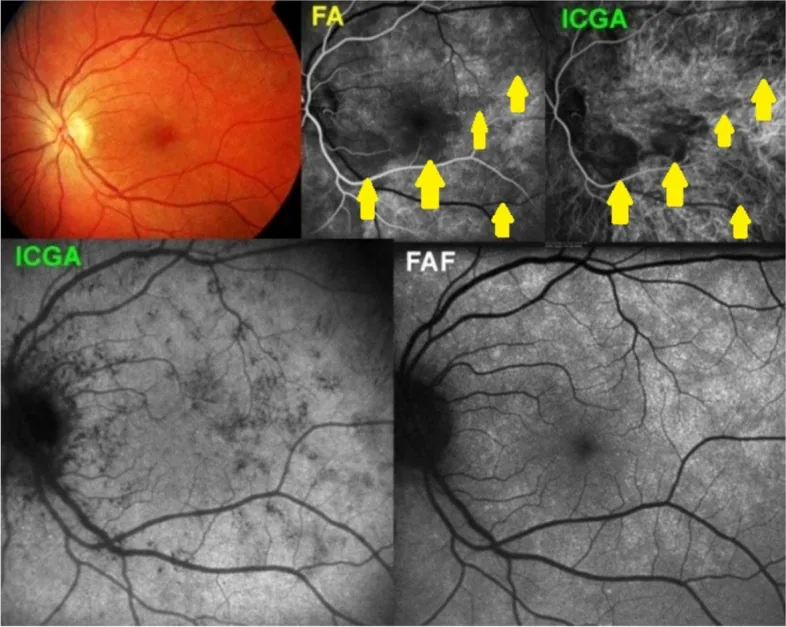
PIC (Punctate Inner Choroidopathy)
Section intitulée « PIC (Punctate Inner Choroidopathy) »La PIC survient principalement chez les jeunes femmes (environ 90 %) âgées de 18 à 40 ans présentant une myopie (environ -5 D en moyenne).
Tableau clinique caractéristique
- Petites taches jaune-blanc de 100 à 300 μm limitées au pôle postérieur, généralement 12 à 25
- Absence d’inflammation de la chambre antérieure et de vitréite (point clé de différenciation avec la MFC)
- Les lésions actives sont visibles en OCT comme des élévations hyperréflectives sous l’EPR
- La cicatrisation laisse de petites lésions atrophiques
La complication par CNV (40-76 %) est le principal problème clinique
La complication la plus importante de la PIC est la CNV, dont le taux de complication est rapporté entre 40 et 76 %7, 8). La CNV survient plus facilement en raison des facteurs suivants :
- Fragilité de la membrane de Bruch due à un amincissement choroïdien myopique
- Destruction de la membrane de Bruch par inflammation sous-EPR
- Augmentation de la production locale de cytokines inflammatoires (VEGF, etc.)
L’OCT-A s’est avéré plus sensible que l’AG pour le dépistage de la CNV, et une surveillance régulière par OCT-A est recommandée. Une aggravation soudaine de la métamorphopsie est un signe de développement de la CNV et nécessite un examen rapide.
Association avec des maladies systémiques
Une association entre PIC et sarcoïdose a été rapportée ; chez les patients présentant des lésions pulmonaires multiples, un scanner thoracique, un dosage de l’ACE sérique et du lysozyme doivent être réalisés. Une association avec HLA-DR2 et HLA-DRB1*15 a également été rapportée3).
MFC (choriorétinite multifocale, MFCwP)
Section intitulée « MFC (choriorétinite multifocale, MFCwP) »La MFC (choriorétinite multifocale avec panuvéite ; MFCwP) est une maladie du même spectre que la PIC, mais le principal élément de différenciation est la présence de vitréite et d’inflammation de la chambre antérieure7).
Caractéristiques cliniques spécifiques
- Apparition de multiples taches jaune-gris de 45 à 350 μm non seulement au pôle postérieur mais aussi dans la région périphérique moyenne.
- Évolution chronique récurrente (épisodes inflammatoires répétés) caractéristique
- Fréquence élevée de complication de membrane épirétinienne (ERM) (jusqu’à 35 %), influençant le pronostic visuel à long terme
- Dans certains cas, l’inflammation ne peut être contrôlée sans traitement immunosuppresseur
Points d’attention dans le traitement
La MFC a tendance à ne pas se résorber spontanément et nécessite souvent un traitement immunomodulateur à long terme. Lorsque les stéroïdes seuls sont insuffisants, on utilise le méthotrexate (MTX), l’azathioprine (AZA) ou le mycophénolate mofétil (MMF). En cas de complication par CNV, une approche bidirectionnelle associant un traitement anti-VEGF et un traitement immunomodulateur est importante7, 8).
Birdshot choroïdopathie (choroïdite en plombs)
Section intitulée « Birdshot choroïdopathie (choroïdite en plombs) »La Birdshot survient chez les personnes d’âge moyen à avancé (40-60 ans, moyenne 50 ans), avec une légère prédominance féminine (1,5:1). Elle est plus fréquente chez les Caucasiens et constitue l’une des associations génétiques les plus fortes connues avec HLA-A29 (risque relatif de 50 à 224 fois chez les Caucasiens)4).
Signes caractéristiques du fond d’œil
- Taches crème de taille 1/4 à 1/2 diamètre papillaire, ressemblant à des impacts de chevrotine, apparaissant symétriquement des deux côtés, du pôle postérieur à l’équateur.
- Les taches évoluent en lésions cicatricielles sans pigmentation.
- Une vascularite rétinienne et un œdème papillaire peuvent être associés.
Modifications fonctionnelles caractéristiques
- Cécité nocturne et dyschromatopsie : apparaissent précocement, parfois avant la baisse d’acuité visuelle
- ERG en champ total de type négatif : observé précocement, l’amplitude de l’onde a diminue avec la progression
- Retard du flicker ERG à 30 Hz : indicateur le plus sensible pour le suivi de l’activité, détectant des anomalies avant la baisse d’acuité visuelle17)
Précautions pour les patients japonais
La fréquence de l’HLA-A29 étant faible chez les Japonais, la sensibilité diagnostique de l’HLA-A29 est limitée. Le diagnostic doit se baser sur les signes cliniques des critères SUN 2021 (lésions en plombs de fusil au fond d’œil, inflammation antérieure minime, présence de vitrite)10).
Complications à long terme
- Œdème maculaire cystoïde (OMC) : principale cause de baisse de l’acuité visuelle
- Œdème papillaire et atrophie optique
- Avec les implants de stéroïdes (fluocinolone), une élévation de la pression intraoculaire est observée chez jusqu’à 40 % des patients, pouvant nécessiter une trabéculectomie
Choroïdopathie serpigineuse (Serpiginous choroidopathy)
Section intitulée « Choroïdopathie serpigineuse (Serpiginous choroidopathy) »La choriorétinite serpigineuse est une choriorétinite chronique bilatérale survenant chez les personnes âgées de 30 à 50 ans (légère prédominance masculine), caractérisée par des lésions gris-jaune en carte géographique s’étendant de manière serpigineuse à partir de la région péripapillaire.
Mode d’extension caractéristique
- Débute de manière centripète autour de la papille optique (péripapillaire), avec une extension progressive et serpigineuse des bords de la lésion
- Phase active : apparition d’un liseré gris-blanc au bord de la lésion
- Phase cicatricielle : fixation sous forme d’une atrophie chorio-rétinienne
- Lors des récidives, une nouvelle inflammation apparaît toujours au bord de la cicatrice existante (ce qui est caractéristique)
- L’intervalle entre les récidives varie de 3 mois à 4 ans selon les individus.
Le plus important : distinction avec le type lié à la tuberculose (SLC)
La choroidite serpigineuse-like tuberculeuse (serpiginous-like choroiditis ; SLC) ressemble beaucoup à la choroidite serpigineuse en imagerie, mais la stratégie thérapeutique est fondamentalement différente :
| Point de distinction | Choroidite serpigineuse | Type lié à la tuberculose (SLC) |
|---|---|---|
| Distribution des lésions | Centrée autour de la papille, centripète | Pôle postérieur à la périphérie, multiples |
| IGRA/TST | Négatif | Positif |
| Forme de la lésion | En carte, continue | Petites lésions multiples et discontinues |
| Traitement | Corticoïdes + immunosuppresseurs | Antituberculeux obligatoires |
L’utilisation d’immunosuppresseurs dans la SLC aggrave considérablement la tuberculose, donc le test IGRA (Quantiféron) avant traitement est absolument indispensable 2).
Prise en charge de la complication par CNV (jusqu’à 35%)
Dans la choriorétinopathie serpigineuse, une CNV survient dans jusqu’à 35% des cas et entraîne une perte de vision irréversible si elle atteint la fovéa. Les injections intravitréennes d’anti-VEGF (bévacizumab, ranibizumab) sont efficaces 18).
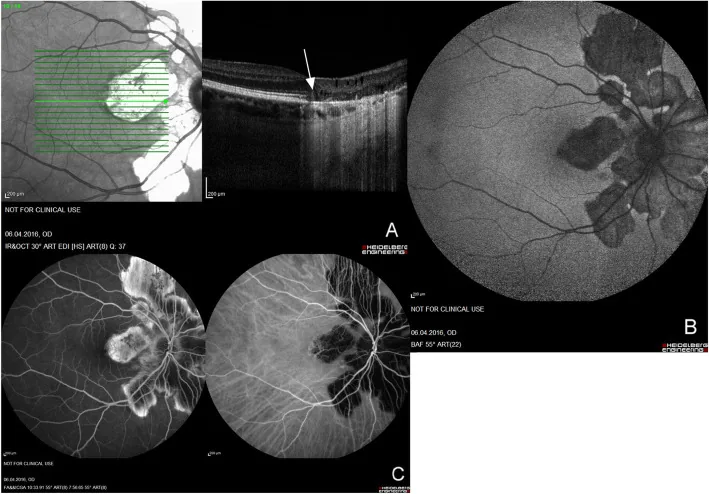
AZOOR (nécrose rétinienne externe aiguë zonale occulte)
Section intitulée « AZOOR (nécrose rétinienne externe aiguë zonale occulte) »L’AZOOR est un concept de maladie proposé par Gass en 1992. Il s’agit d’une rétinopathie externe qui provoque une baisse brutale de l’acuité visuelle, un déficit du champ visuel et une photopsie, malgré un fond d’œil quasi normal3).
Concept du complexe AZOOR
Le complexe AZOOR, proposé par Jampol et al., est un concept qui comprend MEWDS, AZOOR, PIC, MFC, AMN (acute macular neuroretinopathy), AIBSE et AAOR comme un continuum partageant une base génétique auto-immune/inflammatoire commune3).
Caractéristiques cliniques spécifiques
- Survient principalement chez les jeunes femmes myopes âgées de 20 à 50 ans.
- photopsie (vision de lumières) apparaît souvent au début (en particulier des lumières en forme de bande ou d’arc)
- Débute unilatéralement et devient finalement bilatéral dans 76 % des cas
- Le fond d’œil est presque normal en phase aiguë (caractérisé par un décalage entre la baisse d’acuité visuelle et les signes du fond d’œil)
- Les déficits du champ visuel sont en bandes irrégulières (souvent contigus à la tache aveugle)
- Des maladies auto-immunes (thyroïdite de Hashimoto, sclérose en plaques) peuvent être associées
L’OCT et l’ERG sont les clés du diagnostic
- La disparition ou l’opacification de la zone ellipsoïde (ligne IS/OS) à l’OCT est le signe le plus important.
- La récupération fonctionnelle des zones où la couche externe a disparu à l’OCT n’est pas attendue (également utile pour le pronostic).
- Une diminution de l’amplitude à l’ERG multifocal peut être détectée même si le fond d’œil est normal (l’ERG multifocal est plus sensible que l’ERG champ total).
- La FAF infrarouge peut parfois délimiter la frontière entre la lésion et la zone normale.
Traitement et pronostic
Il n’existe pas de traitement établi pour l’AZOOR. Les cas légers peuvent simplement être surveillés, mais les cas graves (baisse de l’acuité visuelle ou déficit étendu du champ visuel) nécessitent une thérapie par bolus de méthylprednisolone (1 000 mg × 3 jours) suivie d’une corticothérapie orale par prednisolone2). La plupart des cas se stabilisent en 6 mois, mais le champ visuel ne se rétablit pas dans les zones où persistent des lésions de la couche externe.
L’AZOOR et la névrite optique rétrobulbaire nécessitent une différenciation car tous deux présentent un fond d’œil presque normal avec une diminution de l’acuité visuelle et du champ visuel. Les points clés de la différenciation sont : ① dans l’AZOOR, il y a une diminution de l’amplitude de l’ERG multifocal, tandis que dans la névrite optique rétrobulbaire, l’ERG est normal ; ② dans l’AZOOR, les défauts du champ visuel montrent un motif irrégulier en bande ou en arc, alors que dans la névrite optique rétrobulbaire, un scotome central est fréquent ; ③ dans l’AZOOR, le RAPD est généralement léger, tandis que dans la névrite optique rétrobulbaire, un RAPD marqué est observé ; ④ à l’OCT, l’AZOOR montre une disparition de la zone ellipsoïde, tandis que la névrite optique rétrobulbaire montre un gonflement papillaire ou un amincissement de la RNFL, ce qui aide à la différenciation2, 3).
5. Utilisation des examens d’imagerie
Section intitulée « 5. Utilisation des examens d’imagerie »Répartition des rôles par modalité
Section intitulée « Répartition des rôles par modalité »Comprendre clairement le rôle de chaque examen d’imagerie est essentiel pour un diagnostic précis et une évaluation de l’activité du syndrome des points blancs1, 5).
| Modalité | Indication/rôle le plus fort |
|---|---|
| AGF (angiographie à la fluorescéine) | Évaluation des fuites des vaisseaux rétiniens, de l’EPR et de la choriocapillaire. Confirmation du phénomène d’inversion de fluorescence dans l’APMPPE. Identification de l’hyperfluorescence en couronne dans le MEWDS. Évaluation de la vascularite (Birdshot). |
| ICG (angiographie au vert d’indocyanine) | Évaluation directe des troubles de la circulation choroïdienne. Détection des lésions plus précoce que l’AGF (notamment Birdshot, APMPPE, serpigineuse). Détection de lésions plus étendues que les signes cliniques (MEWDS, PIC). La plus sensible pour détecter les lésions actives. |
| FAF (autofluorescence du fond d’œil) | Évaluation non invasive des lésions de l’EPR. Détermination de l’activité (APMPPE, serpentine). Diagnostic de MEWDS (points blancs précoces hyperautofluorescents). Évaluation de la chronicité de Birdshot (hypoautofluorescence péripapillaire 73%) |
| OCT (tomographie par cohérence optique) | Évaluation de la zone ellipsoïde (signes diagnostiques de MEWDS et AZOOR). Évolution lésionnelle en 5 stades (PIC). Évaluation des CNV et de l’œdème maculaire. Pronostic visuel (disparition de l’EZ → mauvais pronostic visuel) |
| OCT-A | Détection non invasive des zones de non-perfusion choriocapillaire (APMPPE, serpentine, PIC). Détection précoce et sensible des CNV (plus sensible que l’angiographie à la fluorescéine dans PIC et MFC). Évaluation du flux sanguin choroïdien par couche dans Birdshot. Suivi de l’efficacité thérapeutique |
| ERG multifocal / ERG global | Diagnostic de l’AZOOR (diminution de l’amplitude de l’ERG même si le fond d’œil est quasi normal). Surveillance de l’activité de la Birdshot (retard du flicker à 30 Hz le plus sensible). Évaluation de la réponse au traitement. |
Guide « quel examen en premier » par maladie
Section intitulée « Guide « quel examen en premier » par maladie »En cas de suspicion de MEWDS
- Réaliser d’abord une FAF (la plus sensible, détectable même si les points blancs ne sont pas visibles)
- Angiographie à la fluorescéine (confirmation de l’hyperfluorescence en couronne)
- OCT (évaluation de la zone ellipsoïde)
- OCT-A (évaluation de la choriocapillaire, recherche de CNV)
En cas de suspicion d'APMPPE
Lorsqu’une PIC/MFC est suspectée
- OCT-A (détection précoce des CNV)
- Angiographie à la fluorescéine (évaluation des fuites et du réseau de CNV)
- Angiographie au vert d’indocyanine (détection des lésions infracliniques)
- Autofluorescence du fond d’œil (surveillance de l’activité)
Lorsqu'une choroïdite serpigineuse est suspectée
La stratégie varie selon la maladie. Dans l’APMPPE et la choriorétinite serpigineuse, l’ICGA visualise plus directement les troubles de la circulation choroïdienne, donc la réaliser en même temps ou après la FA approfondit la compréhension de la pathologie. Dans le MEWDS, l’hyperfluorescence en couronne de la FA est importante pour le diagnostic. Cependant, comme il s’agit d’examens invasifs, l’OCT-A fournit désormais de nombreuses informations alternatives, et la combinaison FAF et OCT-A est utilisée pour l’évaluation initiale1, 5).
Signification des lésions hypofluorescentes à l’ICGA
Section intitulée « Signification des lésions hypofluorescentes à l’ICGA »L’hypofluorescence des lésions du syndrome des points blancs à l’ICGA est le reflet direct d’une interruption du flux sanguin choroïdien (occlusion des choriocapillaires)1). L’ICGA est plus sensible que la FA pour évaluer la circulation choroïdienne et présente les caractéristiques suivantes :
- Hypofluorescence totale : observée dans l’APMPPE, la choriorétinite serpigineuse, la PIC et la MFC. Elle reflète une occlusion sévère de l’ischémie du lit capillaire choroïdien.
- Hypofluorescence tardive (FA normale) : L’hypofluorescence tardive en ICGA dans le MEWDS est expliquée par une altération de la capture de l’ICG due à une anomalie de l’EPR, et non par une atteinte de la choriocapillaire (la choriocapillaire est généralement préservée en OCT-A)1).
- Flow void de la couche de Haller → flow void de pleine épaisseur au stade avancé : Progression en deux étapes caractéristique de la Birdshot, débutant dans le stroma choroïdien puis s’étendant à la choriocapillaire14).
L’ICGA est également supérieure à l’FA et à l’OCT-A pour détecter les lésions subcliniques invisibles cliniquement, et en particulier dans le MEWDS et la PIC, elle révèle des lésions choroïdiennes plus étendues que les points blancs1, 15).
Carte des maladies selon les motifs d’hypo- et d’hyperfluorescence en FAF
Section intitulée « Carte des maladies selon les motifs d’hypo- et d’hyperfluorescence en FAF »Les motifs de FAF (autofluorescence du fond d’œil) reflètent l’état métabolique de l’EPR et sont utiles pour le diagnostic et l’évaluation de l’activité des syndromes des points blancs16).
| Motif FAF | Maladie/stade | Signification |
|---|---|---|
| Hyperautofluorescence (hyper-AF) | MEWDS phase aiguë · bord actif de Serpiginous | Accumulation de produits de dégénérescence des photorécepteurs (A2E, etc.) dans l’EPR |
| Hypoautofluorescence (hypo-AF) | APMPPE phase cicatricielle · lésion active PIC · péripaillaire Birdshot | Disparition/perte de fonction de l’EPR |
| Hypo-AF centrale avec halo hyper-AF périphérique | Bord actif de serpigineux, PIC | Motif de lésion de l’EPR au bord actif |
| AF anormal en bande | AZOOR | Correspond à la distribution de la lésion de la couche externe des photorécepteurs |
| HyperAF granulaire fovéolaire | MEWDS (NIR-FAF) | Visualisation non invasive de la granularité fovéolaire |
Dans la maladie de Birdshot, une hypoAF confluente péripapillaire est observée dans 73 % des cas, utile comme indicateur de chronicité17).
Motif de déficit de la zone ellipsoïde (EZ) en OCT
Section intitulée « Motif de déficit de la zone ellipsoïde (EZ) en OCT »L’évaluation de la zone ellipsoïde (EZ, anciennement ligne IS/OS) joue un rôle central dans l’activité et le pronostic du syndrome des points blancs1).
| Aspect de l’EZ | Maladie/stade | Pronostic |
|---|---|---|
| EZ nettement perturbé → récupération | MEWDS phase aiguë → phase de récupération | Bon (récupération de l’EZ et de l’acuité visuelle liées) |
| Disparition de l’EZ (correspondant à la lésion) | Phase active de l’AZOOR | Pas de récupération fonctionnelle de la zone disparue |
| Désorganisation de l’EZ + hyperréflectivité de la rétine externe | Phase aiguë de l’APMPPE | Atrophie partielle résiduelle après récupération |
| Élévation hyperréflective sous RPE + rupture de la zone ellipsoïde | PIC·MFC (évolution en 5 stades) | Mauvais pronostic en cas de CNV associée |
| Disparition de la zone ellipsoïde (avec œdème maculaire cystoïde) | Birdshot à un stade avancé | Facteur de risque de mauvais pronostic visuel |
Les choriocapillaris flow void en OCT-A montrent une concordance élevée avec les résultats de l’angiographie à la fluorescéine (FA) et de l’ICGA (particulièrement utiles dans l’APMPPE et la choriorétinite serpigineuse) 5, 13).
Motifs de fluorescence en FA : retard de remplissage vs hyperfluorescence vs fuite
Section intitulée « Motifs de fluorescence en FA : retard de remplissage vs hyperfluorescence vs fuite »| Motif FA | Maladie | Signification clinique |
|---|---|---|
| Hypofluorescence précoce → hyperfluorescence tardive (phénomène d’inversion de fluorescence) | APMPPE | Ischémie de la choriocapillaire. Défaut de remplissage précoce → fuite tardive de colorant depuis les tissus environnants. |
| Hyperfluorescence précoce en couronne (wreath-like) | MEWDS | Reflète directement l’atteinte des photorécepteurs/RPE. Ne s’étend pas tardivement, point clé pour le diagnostic différentiel. |
| Hypofluorescence précoce → fuite tardive | Serpigineux / MFC en phase active | Signe de choroidite active |
| Hyperfluorescence précoce de la phase artérielle → fuite tardive | Phase active de la PIC | Suggère la présence d’une CNV inflammatoire |
| Fuite vasculaire + hyperfluorescence papillaire (sans fuite) | Birdshot | Preuve directe d’une vascularite rétinienne |
| Normal à léger | AZOOR | Caractérisé par une discordance : déficit du champ visuel et anomalies à l’ERG malgré une FA négative |
6. Principes généraux du traitement
Section intitulée « 6. Principes généraux du traitement »Choix de la stratégie thérapeutique
Section intitulée « Choix de la stratégie thérapeutique »Le traitement du syndrome des points blancs varie considérablement selon l’évolution naturelle de la maladie, sa gravité et la présence ou non d’une CNV.
Observation (pas de traitement nécessaire) comme principe de base
Section intitulée « Observation (pas de traitement nécessaire) comme principe de base »- Forte tendance à la régression spontanée, souvent sans traitement spécifique2)
- MEWDS : disparition des points blancs et récupération visuelle en quelques semaines. Corticostéroïdes oraux uniquement en cas de sévérité ou d’œdème papillaire associé.
- APMPPE : régression des taches blanches en 7 à 12 jours, pronostic visuel généralement bon.
Maladies où la corticothérapie est le traitement principal
Section intitulée « Maladies où la corticothérapie est le traitement principal »APMPPE (sévère, avec papillite) · PIC (lésion active proche de la fovéa) · AZOOR (cas sévères)
- Commencer par prednisolone 30–60 mg/jour puis diminuer progressivement
- En cas de vascularite cérébrale associée à l’APMPPE, une corticothérapie par méthylprednisolone en bolus et une collaboration avec un neurologue sont nécessaires
- Critère de sévérité de l’AZOOR : acuité visuelle corrigée du meilleur œil < 0,3 (directives de la Société japonaise d’ophtalmologie)
Maladies nécessitant un traitement immunosuppresseur à long terme
Section intitulée « Maladies nécessitant un traitement immunosuppresseur à long terme »Choriorétinopathie de Birdshot, choriorétinite serpigineuse, MFC
Birdshot (prise en charge à long terme)
- Prednisolone 0,5 à 1 mg/kg/jour en début de traitement
- Mycophénolate mofétil (MMF) 2 à 3 g/jour (immunosuppresseur de première intention)
- Méthotrexate (MTX) 10 à 25 mg/semaine
- Azathioprine (AZA) 1 à 3 mg/kg/jour
- Cas réfractaires : adalimumab (93,2 % utilisé comme traitement biologique de première intention)
- Sans traitement, 16 à 22 % ont une acuité visuelle ≤ 0,1 en 10 ans
Choroïdite serpigineuse (prise en charge à long terme)
- Prednisolone 40–80 mg/jour en débutant (décroissance progressive)
- Azathioprine 1–2,5 mg/kg/jour (traitement d’entretien de première intention)
- Mycophénolate mofétil / méthotrexate (alternative)
- Cas réfractaires : chlorambucil (le plus puissant ; ≤0,2 mg/kg/jour, hémogramme hebdomadaire obligatoire)
- Agents biologiques : adalimumab (91,0 % le recommandent en première intention)
- Exclure la tuberculose (si IGRA positif, traiter d’abord par antituberculeux) avant d’introduire un immunosuppresseur
Traitement immunomodulateur de la MFC
Section intitulée « Traitement immunomodulateur de la MFC »La MFC évoluant de manière chronique et récurrente, un traitement immunomodulateur est souvent nécessaire en entretien après la décroissance des corticoïdes.
| Médicament | Dose indicative | Remarques |
|---|---|---|
| Méthotrexate (MTX) | 10 à 25 mg/semaine | Associer acide folique 1 mg/jour. Surveillance hépatotoxicité |
| Azathioprine (AZA) | 1 à 3 mg/kg/jour | Vérification de l’activité TPMT recommandée. Attention à la myélosuppression |
| Mycophénolate mofétil (MMF) | 1 à 3 g/jour | Les symptômes gastro-intestinaux sont des effets secondaires fréquents |
| Ciclosporine (CsA) | 3 à 5 mg/kg/jour | Surveillance obligatoire de la fonction rénale et de la tension artérielle |
| Adalimumab | 40 mg/2 semaines (sous-cutané) | Cas réfractaires ou dépendants aux stéroïdes. Dépistage de la tuberculose obligatoire |
Prise en charge de la CNV associée
Section intitulée « Prise en charge de la CNV associée »La CNV est la complication la plus importante affectant le pronostic visuel, et elle est particulièrement fréquente dans la PIC, la MFC et la choriorétinite serpigineuse.
| Maladie | Taux de CNV associée | Traitement |
|---|---|---|
| PIC | 40 à 76 % | Injection intravitréenne d’anti-VEGF (bévacizumab, ranibizumab, aflibercept) + stéroïdes. Stratégie OCTA PRN. |
| MFC | Jusqu’à 60% | Injection intravitréenne d’anti-VEGF + thérapie immunomodulatrice |
| Choroïdite serpentine | Jusqu’à 35% | Injection intravitréenne d’anti-VEGF (bévacizumab, ranibizumab) |
| MEWDS·APMPPE | Rare | Anti-VEGF (si CNV confirmée) |
| Birdshot | Rare | Immunosuppression systémique + anti-VEGF en cas de CNV |
Contrairement à la CNV de la DMLA, la CNV inflammatoire (iCNVM) nécessite le contrôle de l’inflammation sous-jacente pour prévenir les récidives. Dans la PIC et la MFC, une approche bidirectionnelle associant anti-VEGF et stéroïdes (ou immunosuppresseurs) est considérée comme efficace ; l’anti-VEGF seul laisse un risque de récidive 7, 8).
Précautions thérapeutiques
Section intitulée « Précautions thérapeutiques »| Point d’attention | Maladie concernée |
|---|---|
| Exclure la tuberculose en priorité (avant immunosuppression) | Choroïdite serpigineuse · MFC |
| Considérer HLA-A29 (diagnostic) | Birdshot (faible sensibilité chez les Japonais) |
| Risque d’élévation de la pression intraoculaire avec l’implant de stéroïdes | Birdshot (jusqu’à 40% nécessitent une trabéculectomie) |
| Risque de myélosuppression et de tumeur maligne avec le chlorambucil | Choroïdite serpigineuse (nécessite une analyse sanguine hebdomadaire) |
| Récurrence après infection ou vaccination par la COVID-19 | PIC・MEWDS (rapport de récidive) |
| Réponse d’urgence en cas de vascularite cérébrale | APMPPE (céphalées, symptômes neurologiques → IRM cérébrale en urgence) |
Avant de commencer un immunosuppresseur pour le syndrome des points blancs, les examens obligatoires à effectuer sont les suivants : ① exclusion de la tuberculose par IGRA (Quantiferon) (priorité absolue dans la choriorétinite serpigineuse), ② dépistage des hépatites virales par antigène HBs, anticorps HBc et anticorps HCV (prévention de la réactivation sous immunosuppression), ③ radiographie thoracique et TDM (exclusion de la tuberculose et de la sarcoïdose), ④ numération formule sanguine complète et tests de la fonction hépatique et rénale (vérification des valeurs de base). Pour les agents biologiques comme l’adalimumab, le dépistage de la tuberculose est également obligatoire selon la notice du médicament19, 20).
Contrairement à la DMLA, la CNV inflammatoire (iCNVM) peut régresser spontanément lorsque l’inflammation est contrôlée. La stratégie PRN (au besoin) est généralement utilisée, avec injection chaque fois qu’une CNV active est confirmée par OCT-A. Une dose de charge initiale (3 injections consécutives) peut être administrée, mais associée à un traitement immunosuppresseur, le nombre d’injections nécessaires peut être réduit. Le risque de récidive est élevé avec l’anti-VEGF seul, d’où l’importance d’une approche bidirectionnelle combinant le contrôle de l’inflammation sous-jacente 7, 8).
6.5 Association avec des maladies systémiques
Section intitulée « 6.5 Association avec des maladies systémiques »Chaque maladie du syndrome des points blancs est associée à des maladies systémiques ou infections spécifiques, et une recherche systématique d’exclusion avant traitement est importante.
| Maladie | Maladies systémiques/conditions associées | Signification clinique |
|---|---|---|
| APMPPE | Vascularite cérébrale (MCAT) · Infection streptococcique · Virus EB | Céphalées · Symptômes neurologiques → IRM cérébrale en urgence |
| Birdshot | HLA-A29 (80–98 % chez les Caucasiens) · Similaire à la sarcoïdose | Test HLA comme aide diagnostique (faible sensibilité chez les Japonais) |
| Choroïdite serpigineuse | Tuberculose (SLC) · HLA-B7/A2 | IGRA positif → traitement antituberculeux en priorité |
| PIC | Sarcoïdose · HLA-DRB1*15 | Envisager scanner thoracique et dosage de l’ACE |
| MFC | Haplotype IL-10·EBV·sarcoïdose | Réévaluation du bilan systémique en cas de récidive chronique |
| MEWDS | Infection à COVID-19·post-vaccination·HLA-B51 | L’infection par le SARS-CoV-2 agit comme déclencheur immunitaire |
| AZOOR | Maladie de Hashimoto, sclérose en plaques, maladies auto-immunes | Envisager un bilan thyroïdien et des auto-anticorps |
7. Points particuliers et connaissances récentes pour chaque maladie
Section intitulée « 7. Points particuliers et connaissances récentes pour chaque maladie »APMPPE et le spectre de la choriorétinite en plaques
Section intitulée « APMPPE et le spectre de la choriorétinite en plaques »L’APMPPE est désormais comprise de manière intégrée comme faisant partie du « spectre de la choriorétinite placoidienne » avec la maculopathie placoidienne persistante (PPM) et la choriorétinite placoidienne implacable (RPC). Dans ces trois maladies, l’OCT-A montre un motif commun de « flow void » de la choriocapillaire, indiquant que l’ischémie de la choriocapillaire est un substrat pathologique commun5).
Klufas et al. (2017) ont rapporté que l’OCT-A détecte les flow voids choriocapillaires avec une concordance élevée avec l’angiographie à la fluorescéine et l’angiographie au vert d’indocyanine dans trois maladies : APMPPE, PPM et RPC, soutenant ainsi le concept de spectre de choroïdite en plaques5).
MEWDS et granularité fovéale
Section intitulée « MEWDS et granularité fovéale »Le changement granulaire fovéolaire (foveal granularity) est un signe diagnostique observé dans 74 à 96 % des cas de MEWDS et peut rester la seule manifestation après la disparition des points blancs. L’autofluorescence proche infrarouge (NIR-FAF) révèle un motif granulaire fovéolaire caractéristique9).
Spectre de maladies du PIC et du MFC
Section intitulée « Spectre de maladies du PIC et du MFC »Le PIC et le MFC (MFCwP) partagent un fond génétique commun (haplotype IL-10, HLA-DRB1*15) et sont considérés comme des phénotypes différents d’un même spectre de maladies. Les principaux points de différenciation sont la présence ou l’absence de vitréite et d’inflammation de la chambre antérieure, ainsi que la distribution des lésions1, 3).
| Point de différenciation | PIC | MFC (MFCwP) |
|---|---|---|
| Vitréite | Absente | Présente (point de différenciation important) |
| Inflammation de la chambre antérieure | Absente | Légère |
| Distribution des lésions | Limitée au pôle postérieur | Pôle postérieur + périphérie moyenne |
| Taille de la lésion | 100–300 μm | 45–350 μm |
| Taux de CNV associé | 40–76 % | Jusqu’à 60 % |
Birdshot et HLA-A29
Section intitulée « Birdshot et HLA-A29 »L’association entre Birdshot et HLA-A29 est l’une des plus fortes associations génétiques connues dans toute maladie, avec un risque relatif multiplié par 50 à 224 chez les patients blancs4). Cependant, chez les Japonais, la faible prévalence des porteurs de HLA-A29 limite la sensibilité de la positivité HLA-A29 dans le diagnostic. Il est important de se concentrer sur les critères cliniques de la classification SUN 2021 (observations du fond d’œil, inflammation antérieure minime, hyalite) pour le diagnostic10).
Complexe AZOOR et déclencheur viral
Section intitulée « Complexe AZOOR et déclencheur viral »On pense que l’AZOOR se développe lorsqu’un déclencheur environnemental (infection virale, vaccin, médicament, etc.) s’ajoute à une prédisposition génétique (haplotype IL-10, etc.), et il est compris comme faisant partie du complexe AZOOR avec MEWDS, PIC, AMN et AIBSE3). Les cas de MEWDS après infection par le COVID-19 ou vaccination augmentent dans le monde entier, suggérant que le SARS-CoV-2 pourrait agir comme un déclencheur immunitaire11).
Oui. Plusieurs cas d’apparition ou de récidive de MEWDS, PIC et choriorétinite serpigineuse après une infection par le COVID-19 ont été rapportés, suggérant que l’infection par le SARS-CoV-2 pourrait agir comme un déclencheur immunitaire11, 12). Pour le MEWDS, une revue systématique de 27 cas après vaccination contre le COVID-19 a été réalisée, le vaccin à ARNm (Pfizer-BioNTech) étant le plus fréquent. Les personnes ayant des antécédents devraient consulter un ophtalmologiste pour un suivi avant et après la vaccination.
L’ordre de priorité recommandé pour les examens en cas de suspicion initiale de syndrome des points blancs est le suivant : ① FAF + OCT (non invasif, permet une évaluation initiale de presque toutes les maladies ; visualisation de l’hyper-AF du MEWDS, de l’évaluation de la zone ellipsoïde, et de l’élévation sous-EPR du PIC) → ② OCT-A (détection précoce de la CNV, évaluation du flow void choriocapillaire) → ③ FA + ICGA (si un diagnostic définitif ou une évaluation de l’activité est nécessaire). En cas de suspicion de choriorétinite serpigineuse, IGRA (exclusion de la tuberculose) doit être prioritaire avant la FA. En cas de suspicion d’AZOOR, l’ERG (ERG multifocal) est indispensable1, 2).
8. Articles connexes
Section intitulée « 8. Articles connexes »9. Références
Section intitulée « 9. Références »- Testi I, Modugno RL, Pavesio C. Multimodal imaging supporting the pathophysiology of white dot syndromes. J Ophthalmic Inflamm Infect. 2021;11:32.
- 日本眼炎症学会・日本眼科学会. ぶどう膜炎診療ガイドライン(13〜18節:APMPPE・MEWDS・PIC・多発性脈絡膜炎・バードショット・蛇行状脈絡膜炎・AZOOR). 日本眼科学会雑誌. 2019;123(6):635-696.
- Jampol LM, Becker KG. White spot syndromes of the retina: a hypothesis based on the common genetic hypothesis of autoimmune/inflammatory disease. Am J Ophthalmol. 2003;135(3):376-379.
- Agrawal R, et al. The role of HLA-A29 in birdshot chorioretinopathy and immune checkpoint inhibitor-related uveitis. Am J Ophthalmol. 2025. doi:10.1016/j.ajo.2024.01.007
- Klufas MA, Phasukkijwatana N, Iafe NA, et al. Optical coherence tomography angiography reveals choriocapillaris flow reduction in placoid chorioretinitis. Ophthalmol Retina. 2017;1(1):77-91.
- Stattin M, Forster J, Ahmed D, Krepler K, Ansari-Shahrezaei S. Swept Source-Optical Coherence Tomography Angiography for Management of Secondary Choroidal Neovascularization in Punctate Inner Choroidopathy. Case Rep Ophthalmol. 2021;12:232-238.
- Spaide RF, Goldberg N, Freund KB. Redefining multifocal choroiditis and panuveitis and punctate inner choroidopathy through multimodal imaging. Retina. 2013;33(7):1315-1324.
- Leclaire MD, Clemens CR, Eter N, Mihailovic N. Choroidale Neovaskularisation infolge einer “punctate inner choroidopathy”, dargestellt mittels optischer Kohärenztomographie-Angiographie. Ophthalmologe. 2021;118:842-846.
- Mantovani A, Invernizzi A, Staurenghi G, Herbort CP Jr. Multiple evanescent white dot syndrome: a multimodal imaging study of foveal granularity. Ocul Immunol Inflamm. 2019;27(1):141-147.
- Standardization of Uveitis Nomenclature (SUN) Working Group. Classification criteria for birdshot chorioretinitis. Am J Ophthalmol. 2021;228:65-71.
- Chen N, Mandell M, Arjmand P. Multimodal imaging findings of multiple evanescent white dot syndrome in COVID-19 patients. IDCases. 2024;38:e02110.
- Seddigh S, Pinto A, Zaki AM, Gupta RR. Serpiginous choroiditis after COVID-19 infection. J Vitreoretinal Dis. 2025;9(2):246-252.
- Pakzad-Vaezi K, Khaksari K, Chu Z, Van Gelder RN, Wang RK, Pepple KL. Swept-source OCT angiography of serpiginous choroiditis. Ophthalmol Retina. 2018;2(7):712-719.
- Pepple KL, Chu Z, Weinstein J, Munk MR, Van Gelder RN, Wang RK. Use of en face swept-source optical coherence tomography angiography in identifying choroidal flow voids in 3 patients with birdshot chorioretinopathy. JAMA Ophthalmol. 2018;136(11):1288-1292. doi:10.1001/jamaophthalmol.2018.3474. PMID:30128478. PMCID:PMC6248174
- Khochtali S, Dridi T, Abroug N, et al. Swept-source optical coherence tomography angiography shows choriocapillaris flow reduction in multiple evanescent white dot syndrome. J Curr Ophthalmol. 2020;32(2):211-215.
- Yeh S, Forooghian F, Wong WT, et al. Fundus autofluorescence imaging of the white dot syndromes. Arch Ophthalmol. 2010;128(1):46-56.
- Minos E, Barry RJ, Southworth S, et al. Birdshot chorioretinopathy: current knowledge and new concepts in pathophysiology, diagnosis, monitoring and treatment. Orphanet J Rare Dis. 2016;11(1):61.
- Maleki A, Maldonado Cerda A, Garcia CM, et al. Chlorambucil combination therapy in refractory serpiginous choroiditis: a cure? Am J Ophthalmol Case Rep. 2021;21:101014.
- Niederer RL, Al-Janabi A, Engelbrecht C, et al. Immunomodulatory therapy prescribing practices for non-infectious uveitis: a survey of international experts. Br J Ophthalmol. 2024;108:482-489.
- Tomkins-Netzer O, et al. Treatment of non-infectious uveitis with biologics: a survey of the International Ocular Inflammation Society. Br J Ophthalmol. 2022;106:482-488.
