نوع عمدتاً درگیرکننده شبکیه خارجی

سندرم لکههای سفید
نکات کلیدی در یک نگاه
Section titled “نکات کلیدی در یک نگاه”1. سندرم لکههای سفید چیست؟
Section titled “1. سندرم لکههای سفید چیست؟”سندرم لکههای سفید (white dot syndromes) مفهومی است که در سال ۱۹۷۷ توسط گاس نامگذاری شد و به گروهی از بیماریهای التهابی اطلاق میشود که با ضایعات لکهای سفید یا زرد-سفید متعدد در فوندوس مشخص میشوند. تعریف بیماریهای هدف بسته به محققان متفاوت است، اما امروزه به طور گسترده به عنوان گروهی از بیماریهای التهابی ایدیوپاتیک غیرعفونی که عمدتاً شبکیه خارجی، RPE، لایه مویرگی کوروئید و کوروئید را درگیر میکنند، استفاده میشود 1).
در راهنمای بالینی یووئیت (مجله چشمپزشکی ژاپن ۲۰۱۹؛۱۲۳(۶):۶۳۵-۶۹۶)، APMPPE، MEWDS، PIC، کوروئیدیت چندکانونی، کوریورتینوپاتی بردشات، کوروئیدیت سرپانتینی و AZOOR به عنوان بیماریهای مستقل در طبقهبندی یووئیت خلفی ذکر شدهاند و هنگامی که از نام کلی «سندرم لکههای سفید» استفاده میشود، به عنوان مفهومی جامع برای این موارد در نظر گرفته میشود 2).
رویکرد طبقهبندی
Section titled “رویکرد طبقهبندی”با پیشرفتهای اخیر در تصویربرداری چندوجهی (از جمله OCT-A)، سندرم نقاط سفید بر اساس لایهای که ضایعه عمدتاً در آن قرار دارد به سه گروه زیر طبقهبندی میشود1).
نوع عمدتاً درگیر در مویرگهای کوروئید
نوع عمدتاً درگیر در استرومای کوروئید
کوریورتینیت پرندهای (Birdshot)
- نفوذ لنفوسیتی به استرومای مشیمیه به عنوان ضایعه اولیه
- در OCT-A، فقدان جریان در لایه هالر و در مراحل اولیه، حفظ مویرگهای مشیمیه
- پیشرونده مزمن با ارتباط قوی با HLA-A29
علاوه بر این، مفهوم کمپلکس AZOOR نیز مطرح شده است که شامل MEWDS، AZOOR، PIC، MFC، AMN، AIBSE و AAOR به عنوان یک پیوستار با زمینه مشترک خودایمنی/التهابی ژنتیکی است3).
اپیدمیولوژی در ژاپن
Section titled “اپیدمیولوژی در ژاپن”بر اساس آمار انجمن التهاب چشم ژاپن، نسبت هر یک از بیماریهای سندرم لکههای سفید به کل یووئیت به شرح زیر است2).
| بیماری | نسبت به کل یووئیت |
|---|---|
| MEWDS | حدود ۱-۲٪ (گزارشهای داخلی) |
| APMPPE | نادر (آمار سالانه دقیقی وجود ندارد) |
| PIC | نادر |
| کوریورتینیت مارپیچی | حدود 0.3% |
| کوریورتینوپاتی بردشات | نادر (در سفیدپوستان شایع، در ژاپن بسیار نادر) |
| AZOOR | نادر (تعداد گزارشها در سالهای اخیر افزایش یافته است) |
2. تصویر بالینی مشترک
Section titled “2. تصویر بالینی مشترک”اگرچه علائم هر بیماری متفاوت است، ویژگیهای بالینی زیر در گروه سندرم نقاط سفید مشترک است1, 2).
الگوی مشترک علائم ذهنی
Section titled “الگوی مشترک علائم ذهنی”- کاهش بینایی: شدت آن از خفیف (MEWDS، AZOOR) تا شدید (کوروئیدیت مارپیچی، PIC همراه با CNV) متغیر است.
- فوتوپسی (فوتوپسیا): شایعترین علامت منعکسکننده آسیب شبکیه خارجی و سلولهای گیرنده نور
- نقاط کور و نقص میدان بینایی: اغلب نقاط کور پارامرکزی یا مرکزی متناظر با محل ضایعه
- دگرگونبینی (متامورفوپسی): در ضایعات ماکولا یا همراه با CNV رخ میدهد
وجود یا عدم وجود التهاب بخش قدامی چشم
Section titled “وجود یا عدم وجود التهاب بخش قدامی چشم”| گروه بیماری | التهاب اتاق قدامی و زجاجیه |
|---|---|
| MEWDS، APMPPE، PIC | معمولاً بدون (APMPPE ممکن است خفیف باشد) |
| MFC (MFCwP) | التهاب اتاق قدامی + ویتریت وجود دارد (نقطه تمایز با PIC) |
| Birdshot | التهاب اتاق قدامی بدون تا خفیف، ویتریت وجود دارد |
| کوریورتینیت مارپیچی | التهاب اتاق قدامی و زجاجیه معمولاً خفیف است |
| AZOOR | معمولاً وجود ندارد |
3. نحوه تفکیک تشخیصی
Section titled “3. نحوه تفکیک تشخیصی”سن، جنسیت، یکطرفه در مقابل دوطرفه، و عودکنندگی
Section titled “سن، جنسیت، یکطرفه در مقابل دوطرفه، و عودکنندگی”زن جوان، یکطرفه، بهبود خودبهخودی
زنان جوان تا میانسال، دوطرفه، خطر CNV
جوان تا میانسال، دوطرفه، شروع حاد
- شایع در دهه ۲۰ تا ۳۰ (میانگین ۲۵ سال)، بدون تفاوت جنسیتی
- دوطرفه، حاد، تمایل به بهبود خودبهخودی
- توجه به همراهی واسکولیت مغزی (در صورت بروز علائم عصبی، بررسی فوری)
میانسال و مسن · دوطرفه · مزمن و پیشرونده
بیردشات · کوروئیدیت سرپانتینی
- بیردشات: دهه ۴۰ تا ۶۰، کمی بیشتر در زنان
- کوروئیدیت سرپانتینی: دهه ۳۰ تا ۵۰، کمی بیشتر در مردان
- هر دو بیماری مزمن، عودکننده و نیازمند سرکوب طولانیمدت ایمنی هستند
- میزان مثبت بودن HLA-A29 در بیردشات (سفیدپوستان): ۸۰ تا ۹۸٪
نمودار جریان تشخیص افتراقی
Section titled “نمودار جریان تشخیص افتراقی”眼底に白点状病変 │ ├─ 片眼性? │ ├─ YES → MEWDS・AZOOR・AMN を考慮 │ │ ↳ FA で初期過蛍光 → MEWDS │ │ ↳ 眼底ほぼ正常・ERG 異常 → AZOOR │ └─ NO(両眼性) │ ├─ 急性発症・後極部大型白斑? │ └─ YES → APMPPE(FA 蛍光逆転現象を確認) │ ├─ 後極部小病変・近視女性・硝子体炎なし? │ └─ YES → PIC を考慮(CNV 検索:OCTA 必須) │ ├─ 小病変・硝子体炎あり・周辺部にも病変? │ └─ YES → MFC(MFCwP)を考慮 │ ├─ 乳頭周囲から蛇行状に進展・男性多め? │ └─ YES → 蛇行状脈絡膜炎(結核除外が最優先) │ └─ 後極部散弾状病変・中高年・HLA-A29? └─ YES → Birdshot 網脈絡膜症4. مقایسه بیماریهای اصلی
Section titled “4. مقایسه بیماریهای اصلی”جدول مقایسه اصلی: ماتریس ۷ بیماری
Section titled “جدول مقایسه اصلی: ماتریس ۷ بیماری”| مورد | APMPPE | MEWDS | PIC | MFC (MFCwP) | Birdshot | کوریورتینیت مارپیچی | AZOOR |
|---|---|---|---|---|---|---|---|
| سن شایع | دهه ۲۰ تا ۳۰ (میانگین ۲۵ سال) | دهه ۲۰ تا ۵۰ | دهه ۱۸ تا ۴۰ (میانگین ۳۶ سال) | میانگین ۳۰ سال | دهه ۴۰ تا ۶۰ | دهه ۳۰ تا ۵۰ | عمدتاً اواسط دهه ۳۰ |
| جنسیت | بدون تفاوت جنسیتی | غلبه زنان (1:4) | غلبه زنان (حدود 90%) | غلبه زنان (بیشتر در زنان سفیدپوست) | کمی بیشتر در زنان | کمی بیشتر در مردان | غلبه زنان (حدود 75%) |
| یکچشمی/دوچشمی | اغلب دوچشمی | یکچشمی (بیش از 95%) | اغلب دوچشمی (80%) | دوچشمی | دوچشمی | دوچشمی | یکچشمی → پیشرفت به دوچشمی (نهایتاً 76% دوچشمی) |
| علائم اصلی | کاهش بینایی، اسکوتوم مرکزی، دگرگونبینی | کاهش بینایی، فوتوپسی، تاربینی | اسکوتوم، کاهش بینایی، دگرگونبینی | مگسپران، کاهش بینایی، فوتوپسی | کاهش بینایی، شبکوری، اختلال رنگبینی | کاهش بینایی، اسکوتوم پاراسنترال | فوتوپسی، نقص میدان بینایی (فوندوس تقریباً طبیعی) |
| ویژگی لکههای سفید فوندوس | لکههای سفید کرمی بزرگ (یکچهارم تا یکدوم قطر دیسک بینایی) در قطب خلفی | لکههای کوچک متعدد خاکستری-سفید کمرنگ (۱۰۰-۲۰۰ میکرومتر) از قطب خلفی تا ناحیه استوایی | لکههای کوچک زرد-سفید (۱۰۰-۳۰۰ میکرومتر)، ۱۲-۲۵ عدد، در قطب خلفی | لکههای خاکستری-زرد (۴۵-۳۵۰ میکرومتر) از قطب خلفی تا محیط، همراه با التهاب زجاجیه | لکههای کرمی رنگ شلیکمانند (یکچهارم تا یکدوم قطر دیسک بینایی) از قطب خلفی تا ناحیه استوایی | ضایعات خاکستری-زرد نقشهمانند که از اطراف دیسک بینایی به صورت مارپیچ گسترش مییابند | فوندوس تقریباً طبیعی (مرحله حاد)، آتروفی لایههای خارجی در مراحل بعدی |
| یافتههای OCT | اختلال در ناحیه ellipsoid + هایپررفلکتیویته شبکیه خارجی، پس از بهبودی آتروفی جزئی باقی میماند | اختلال شدید و ناپدید شدن ناحیه ellipsoid (فاز حاد) → بهبودی | برجستگی هایپررفلکتیو زیر RPE + پارگی EZ (پیشرفت ۵ مرحلهای) | هایپررفلکتیویته زیر RPE + پارگی EZ (مشابه PIC) | ضایعات مشیمیه، ادم ماکولار کیستیک، ناپدید شدن EZ با پیشآگهی بد | فاز فعال: هایپررفلکتیویته شبکیه خارجی و مایع زیرشبکیه. فاز اسکار: آتروفی RPE | ناپدید شدن EZ (IS/OS) مهمترین یافته (مطابق با نقص میدان بینایی) |
| یافتههای FA | هیپوفلورسانس اولیه → هیپرفلورسانس دیررس (پدیده معکوس فلورسانس) | هیپرفلورسانس مداوم به شکل تاج گل (wreath-like) از ابتدا | فاز فعال: هیپرفلورسانس اولیه در فاز شریانی → نشت دیررس | فاز فعال: هیپوفلورسانس اولیه → نشت دیررس | هیپرفلورسانس ضایعه (بدون نشت) + نشت عروقی و هیپرفلورسانس دیسک بینایی | فاز فعال: هیپوفلورسانس اولیه → هیپرفلورسانس دیررس (نشت) | معمولاً طبیعی یا ناهنجاری خفیف |
| یافتههای ICGA | هیپوفلورسانس در تمام فازها (بازتاب مستقیم ایسکمی لایه مویرگی کوروئید) | هیپوفلورسانس دیررس (گستردهتر از نقاط سفید) | هیپوفلورسانس میانی، مفید برای تشخیص ضایعات زیربالینی | هیپوفلورسانس از فاز اولیه تا تمام فازها | هیپوفلورسانس اولیه و میانی → ایزوفلورسانس دیررس (مرحله اولیه) → مرحله پیشرفته: هیپوفلورسانس در تمام فازها | هیپوفلورسانس در تمام فازها (بازتاب اختلال گردش خون کوروئید) | معمولاً طبیعی |
| یافتههای FAF | فاز حاد: فلورسانس خودکار کم یا زیاد. فاز بهبودی: فلورسانس خودکار کم | فاز حاد: فلورسانس خودکار زیاد (هیپرفلورسانس متعدد). پس از بهبودی: نرمال | فاز فعال: فلورسانس خودکار کم (hypoAF)، هاله فلورسانس خودکار زیاد در حاشیه | فاز فعال: فلورسانس خودکار کم | فلورسانس خودکار کم و همجوار اطراف دیسک بینایی (در 73٪ موارد) | فاز فعال: حاشیه فلورسانس خودکار زیاد + هاله فلورسانس خودکار کم. فاز غیرفعال: فلورسانس خودکار کم | ناهنجاری فلورسانس خودکار نواری از زیاد تا کم |
| یافتههای OCT-A | نقص جریان در کوریوکاپیلاریس (همخوانی بالا با FA/ICGA) | کوریوکاپیلاریس عمدتاً حفظ شده (نقص جریان گذرا در برخی موارد) | نقص جریان در کوریوکاپیلاریس (در محل ضایعه التهابی) | نقص جریان در کوریوکاپیلاریس | نقص جریان در لایه هالر (مرحله اولیه) → در مرحله پیشرفته: نقص جریان در تمام لایهها | نقص جریان شدید در کوریوکاپیلاریس | کوریوکاپیلاریس عمدتاً حفظ شده |
| عودکننده | نادر (اساساً یکبار) | حدود ۱۰٪ عود | بالا (مزمن-عودکننده) | بالا (اپیزودهای التهابی مکرر) | بالا (مزمن با عود و بهبودی مکرر) | بالا (تکرار با فاصله ۳ ماه تا ۴ سال) | بیشتر در ۶ ماه پایدار میشود. برخی پیشرفت میکنند |
| میزان همراهی CNV | نادر | نادر | 40-76% (پرریسک) | حداکثر 60% | CNV زیرشبکیه: نادر | حداکثر 35% | تقریباً هیچ |
| مرتبط با HLA | هیچ | HLA-B51 (گزارش اولیه) | HLA-DR2 · HLA-DRB1*15 | مرتبط با هاپلوتیپ IL-10 | HLA-A29 (80-98% در سفیدپوستان) | HLA-B7 · HLA-A2 (گزارش مرتبط) | هیچ (استعداد ایمونولوژیک) |
| رویکرد درمانی | پیگیری (بهبود خودبهخودی)، موارد شدید: کورتیکواستروئید | پیگیری، موارد شدید: کورتیکواستروئید کوتاهمدت، CNV: ضد VEGF | پیگیری (بدون CNV)، CNV: ضد VEGF + کورتیکواستروئید، داروهای سرکوبکننده ایمنی | کورتیکواستروئید + درمان تعدیلکننده ایمنی، CNV: ضد VEGF | کورتیکواستروئید + مایکوفنولات موفتیل/آدالیموماب (طولانیمدت) | کورتیکواستروئید + داروهای سرکوبکننده ایمنی (شامل عوامل آلکیلهکننده)، CNV: ضد VEGF | پیگیری، موارد شدید: پالس کورتیکواستروئید |
| پیشآگهی بینایی | خوب (بهبود خودبهخودی شایع) | خوب (در عود و CNV احتیاط لازم است) | با CNV خطر پیشآگهی بد بالا | با CNV و ادم ماکولا خطر پیشآگهی بد | بدون درمان، 16-22% در 10 سال به دید 0.1 یا کمتر میرسند | اگر درگیر فووئا شود غیرقابل برگشت، در حداکثر 25% چشمها دید نهایی کمتر از 20/200 | بیشتر پایدار است. در موارد پیشرفت آسیب لایه خارجی، پیشآگهی بد |
کوروئیدیت مارپیچی و کوریورتینوپاتی بردشات بدترین پیشآگهی بینایی را دارند. در کوروئیدیت مارپیچی، حداکثر ۲۵٪ چشمها به دید نهایی کمتر از ۲۰/۲۰۰ میرسند و در بیماری بردشات بدون درمان، ۱۶ تا ۲۲٪ بیماران در طی ۱۰ سال به دید ۰٫۱ یا کمتر میرسند2, 4). PIC و MFC در موارد همراه با CNV خطر پیشآگهی بد را افزایش میدهند. APMPPE و MEWDS تمایل شدید به بهبود خودبهخودی دارند و پیشآگهی خوب است.
تصویر بالینی دقیق هر بیماری
Section titled “تصویر بالینی دقیق هر بیماری”APMPPE (اپیتلیوپاتی پلیمورفیک حاد خلفی)
Section titled “APMPPE (اپیتلیوپاتی پلیمورفیک حاد خلفی)”APMPPE بیشتر در دهه ۲۰ تا ۳۰ سالگی (میانگین ۲۵ سال) رخ میدهد و تفاوت جنسیتی ندارد. علت اصلی آن واسکولیت انسدادی در شریانهای آوران لایه مویرگی کوروئید در نظر گرفته میشود و عفونتهای ویروسی به عنوان عوامل محرک احتمالی مطرح هستند1, 2).
علائم پیشدرآمدی و سیر بیماری
- علائم شبهسرماخوردگی (آنفولانزا، ویروس اپشتین-بار، آبله مرغان، عفونت استرپتوکوکی و غیره) در حدود نیمی از بیماران مشاهده میشود.
- لکههای سفید دیسکوئید کرمرنگ به اندازه ۱/۴ تا ۱/۲ قطر دیسک بینایی به طور متعدد در قطب خلفی هر دو چشم ظاهر میشوند.
- لکههای سفید طی چند روز از مرکز شروع به محو شدن میکنند و پس از ۷ تا ۱۲ روز با دپیگمانتاسیون خفیف ناپدید میشوند.
- معمولاً با یک دوره منفرد به طور خودبهخود بهبود مییابد (عود نادر است)
- پیشآگهی بینایی معمولاً خوب است، اما در موارد شدید یا مواردی که به کوریورتینیت نقشهای تبدیل میشوند، ممکن است نامطلوب باشد.
عارضه خاص: واسکولیت مغزی (MCAT)
ترکیب APMPPE با واسکولیت سیستم عصبی مرکزی (MCAT: multiple cerebral arterial thrombosis) یک عارضه جدی است و در صورت بروز سردرد، تب و علائم عصبی، انجام فوری MRI و MRA مغز ضروری است. در موارد همراه با واسکولیت مغزی، نیاز به درمان با پالس متیلپردنیزولون و همکاری با متخصص مغز و اعصاب وجود دارد2).
ارتباط با طیف کوریورتینیت پلاکوئید
APMPPE همراه با PPM (persistent placoid maculopathy) و RPC (relentless placoid chorioretinitis) طیف «کوریورتینیت پلاکوئید» را تشکیل میدهند که زمینه پاتولوژیک مشترک ایسکمی لایه مویرگی کوروئید را دارند5).
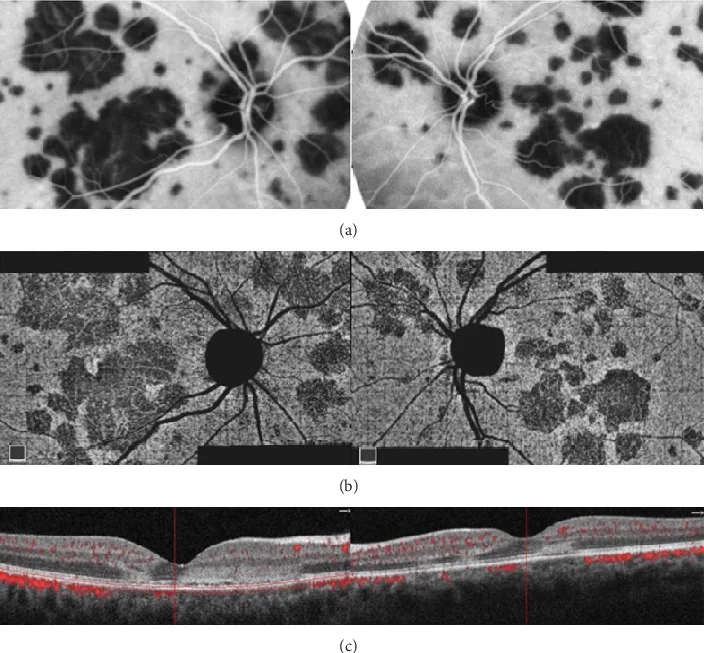
MEWDS (سندرم لکههای سفید متعدد ناپدیدشونده)
Section titled “MEWDS (سندرم لکههای سفید متعدد ناپدیدشونده)”MEWDS معمولاً در زنان ۲۰ تا ۵۰ ساله (نسبت زن به مرد ۴:۱) رخ میدهد و با ویژگیهای یکطرفه، حاد و بهبود خودبهخودی مشخص میشود.
تصویر بالینی مشخص
- لکههای کوچک متعدد خاکستری-سفید (۱۰۰-۲۰۰ میکرومتر) در لایه عمیق شبکیه تا سطح RPE از قطب خلفی تا ناحیه استوا
- دانهبندی فووئال (تغییرات دانهای در مرکز شبکیه): در ۷۴ تا ۹۶٪ از بیماران دیده میشود و ممکن است پس از ناپدید شدن لکههای سفید تنها یافته باقیمانده باشد. الگوی مشخصی را در تصویربرداری خودفلورسانس نزدیک به فروسرخ (NIR-FAF) نشان میدهد9)
- ظاهر نارنجی-نقطهای (orange-dot appearance): یافته مشخص در عکسبرداری از فوندوس و عکسبرداری با نور نزدیک به مادون قرمز
- ضایعه عاجی (ivory lesion) : تغییر رنگ سفید ملایم و محو در قطب خلفی چشم
- علائم پیشدرآمدی شبیه سرماخوردگی در حدود ۵۰٪ موارد قبل از بیماری رخ میدهد
- بروز سالانه حدود ۰٫۲۲ مورد در هر ۱۰۰٬۰۰۰ نفر، و در ۱۰٪ موارد عود مشاهده میشود
هایپرفلورسانس تاجگلمانند (wreath-like) در FA
هایپرفلورسانس تاجگلمانند مشخص از مراحل اولیه FA نکته کلیدی در تشخیص MEWDS است. ضایعات نقطهای سفید از مراحل اولیه FA هایپرفلورسانس میشوند و در مراحل بعدی گسترش نمییابند. این هایپرفلورسانس اولیه یک نکته افتراقی مهم از هیپوفلورسانس اولیه (پدیده معکوس فلورسانس) در APMPPE است1, 9).
تداوم با کمپلکس AZOOR
MEWDS عمدتاً با تخریب گذرای ناحیه ellipsoid (خط IS/OS) سلولهای بینایی مشخص میشود و به عنوان بیماری متعلق به کمپلکس AZOOR درک میگردد. در OCT در مرحله حاد، اختلال و ناپدید شدن ناحیه ellipsoid قابل مشاهده است که با بهبود بینایی بهبود مییابد3).
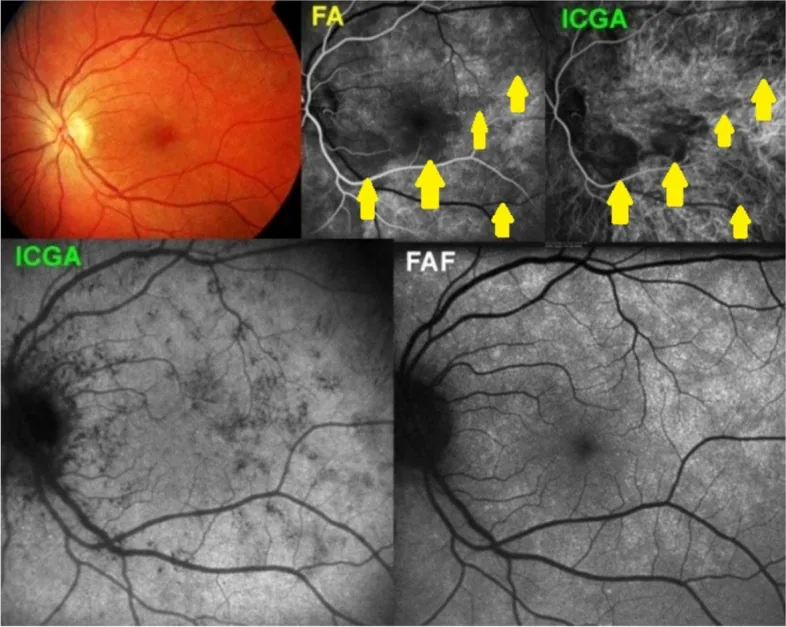
PIC (کوریوپاتی نقطهای داخلی)
Section titled “PIC (کوریوپاتی نقطهای داخلی)”PIC در زنان جوان (حدود 90%) 18 تا 40 ساله که نزدیکبینی دارند (میانگین حدود 5- دیوپتر) شایع است.
تصویر بالینی مشخص
- لکههای کوچک زرد-سفید به اندازه ۱۰۰ تا ۳۰۰ میکرومتر، محدود به قطب خلفی، معمولاً ۱۲ تا ۲۵ عدد
- بدون التهاب اتاق قدامی یا زجاجیه (این مهمترین نکته افتراقی از MFC است)
- ضایعات فعال به صورت برجستگیهای با بازتاب بالا در زیر RPE در OCT قابل مشاهده هستند
- پس از ایجاد اسکار، ضایعات آتروفیک کوچک باقی میمانند
عارضه CNV (۴۰ تا ۷۶٪) بزرگترین مشکل بالینی است
مهمترین عارضه PIC، CNV است که میزان بروز آن ۴۰ تا ۷۶٪ گزارش شده است7, 8). CNV به دلایل زیر راحتتر ایجاد میشود:
- شکنندگی غشای بروخ به دلیل نازک شدن مشیمیه در نزدیکبینی
- تخریب غشای بروخ به دلیل التهاب زیر RPE
- افزایش تولید موضعی سایتوکاینهای التهابی (مانند VEGF)
نشان داده شده است که OCT-A نسبت به FA برای غربالگری CNV حساسیت بیشتری دارد و پایش منظم با OCT-A توصیه میشود. بدتر شدن ناگهانی دگرسانی نشانه شروع CNV است و نیاز به بررسی فوری دارد.
ارتباط با بیماریهای سیستمیک
همچنین مواردی از همراهی PIC با سارکوئیدوز گزارش شده است و در بیماران با ضایعات متعدد ریوی، انجام سیتی قفسه سینه، اندازهگیری ACE سرم و لیزوزیم توصیه میشود. ارتباط با HLA-DR2 و HLA-DRB1*15 نیز گزارش شده است3).
MFC (کوریورتینیت چندکانونی، MFCwP)
Section titled “MFC (کوریورتینیت چندکانونی، MFCwP)”MFC (کوریورتینیت چندکانونی همراه با پانیووئیت؛ MFCwP) در طیف مشابهی با PIC قرار دارد، اما مهمترین وجه تمایز آن وجود ویتریت و التهاب اتاق قدامی است7).
یافتههای بالینی اختصاصی
- لکههای زرد-خاکستری به اندازه ۴۵ تا ۳۵۰ میکرومتر، نه تنها در قطب خلفی بلکه در ناحیه محیطی میانی نیز به صورت متعدد دیده میشوند.
- سیر مزمن عودکننده (اپیزودهای التهابی مکرر) مشخصه آن است
- غشای اپیرتینال (ERM) با فراوانی بالایی (تا ۳۵٪) همراه است و پیشآگهی طولانیمدت بینایی را تحت تأثیر قرار میدهد.
- در برخی موارد، التهاب بدون درمان سرکوبکننده ایمنی قابل کنترل نیست.
نکات مهم در درمان
MFC به ندرت خودبهخود بهبود مییابد و در بسیاری از موارد نیاز به درمان طولانیمدت با داروهای تعدیلکننده ایمنی دارد. در صورت ناکافی بودن استروئیدها، از متوترکسات (MTX)، آزاتیوپرین (AZA) و مایکوفنولات موفتیل (MMF) استفاده میشود. در صورت وجود CNV، رویکرد دوگانه درمان ضد VEGF و درمان تعدیلکننده ایمنی مهم است7, 8).
بیماری بردشات کوریورتینیت (کوریورتینیت ساچمهای)
Section titled “بیماری بردشات کوریورتینیت (کوریورتینیت ساچمهای)”بیماری بردشات (Birdshot) در افراد میانسال تا مسن (میانگین سنی ۵۰ سال) شایعتر است و در زنان کمی بیشتر دیده میشود (نسبت ۱.۵ به ۱). در سفیدپوستان شایعتر است و یکی از قویترین ارتباطات ژنتیکی شناخته شده با HLA-A29 است (در سفیدپوستان خطر نسبی ۵۰ تا ۲۲۴ برابر)4).
یافتههای مشخص در فوندوس
- لکههای کرمرنگ شبیه به آثار ساچمه (به اندازه ۱/۴ تا ۱/۲ قطر دیسک بینایی) به صورت متقارن در دو چشم از قطب خلفی تا ناحیه استوایی ظاهر میشوند.
- این لکهها به ضایعات اسکاری بدون رسوب رنگدانه تبدیل میشوند.
- ممکن است با واسکولیت شبکیه و تورم دیسک بینایی همراه باشد.
تغییرات عملکردی مشخص
- شبکوری و اختلال رنگبینی: از مراحل اولیه ظاهر میشوند و ممکن است قبل از کاهش دید رخ دهند
- نوع منفی در ERG میدان کامل: در مراحل اولیه دیده میشود و با پیشرفت، دامنه موج a کاهش مییابد
- تأخیر در ERG فلکر 30 هرتز: حساسترین شاخص برای پایش فعالیت بیماری است و میتواند ناهنجاری را زودتر از کاهش دید تشخیص دهد17)
نکات قابل توجه در ژاپنیها
از آنجایی که فراوانی HLA-A29 در ژاپنیها پایین است، حساسیت تشخیصی HLA-A29 محدود میشود. تشخیص باید بر اساس یافتههای بالینی معیارهای طبقهبندی SUN 2021 (ضایعات شاتگانی فوندوس، التهاب خفیف بخش قدامی، وجود ویتریت) تأکید کند10).
عوارض طولانیمدت
- ادم ماکولار کیستیک (CME): علت اصلی کاهش بینایی
- تورم دیسک بینایی و آتروفی عصب بینایی
- در موارد استفاده از ایمپلنت استروئیدی (فلوئوسینولون)، افزایش فشار چشم تا ۴۰٪ مشاهده میشود و ممکن است نیاز به ترابکولکتومی باشد
کوروئیدوپاتی سرپجینوس (Serpiginous choroidopathy)
Section titled “کوروئیدوپاتی سرپجینوس (Serpiginous choroidopathy)”کوریورتینیت سرپجینوز یک التهاب مزمن دوطرفه کوروئید است که در دهه ۳۰ تا ۵۰ سالگی (کمی بیشتر در مردان) رخ میدهد و با ضایعات زرد-خاکستری نقشهمانندی که از اطراف دیسک بینایی به صورت مارپیچ پیشرفت میکنند مشخص میشود.
الگوی پیشرفت مشخص
- از ناحیه اطراف دیسک بینایی (peripapillary) به صورت گریز از مرکز شروع شده و لبه ضایعه به تدریج به صورت مارپیچ گسترش مییابد.
- فاز فعال: یک حاشیه سفید-خاکستری در لبه ضایعه ظاهر میشود.
- فاز اسکار: به صورت ضایعه آتروفیک کوریورتینال تثبیت میشود.
- در عود، التهاب جدید همیشه از لبه اسکار موجود شروع میشود (که مشخصه آن است).
- فاصله عود بین ۳ ماه تا ۴ سال متغیر است و تفاوت فردی زیادی دارد
مهمترین نکته: افتراق از نوع مرتبط با سل (SLC)
کوروئیدیت مارپیچیشکل سلی (serpiginous-like choroiditis; SLC) از نظر تصویربرداری بسیار شبیه کوروئیدوپاتی مارپیچی است، اما رویکرد درمانی کاملاً متفاوت دارد:
| نکات افتراقی | کوروئیدوپاتی مارپیچی | نوع مرتبط با سل (SLC) |
|---|---|---|
| توزیع ضایعه | مرکزی اطراف پاپیلا، گریز از مرکز | قطب خلفی تا محیطی، چندگانه |
| IGRA/TST | منفی | مثبت |
| شکل ضایعه | نقرهای و پیوسته | ضایعات کوچک متعدد و ناپیوسته |
| درمان | استروئید + داروی سرکوبکننده ایمنی | داروی ضد سل ضروری است |
از آنجایی که استفاده از داروهای سرکوبکننده ایمنی در SLC باعث تشدید قابل توجه سل میشود، انجام آزمایش IGRA (کوانتیفرون) قبل از درمان کاملاً ضروری است2).
مدیریت CNV همراه (حداکثر ۳۵٪)
در کوروئیدیت سرپجینوس، CNV در حداکثر ۳۵٪ موارد همراه است و در صورت درگیری فووآ، باعث کاهش بینایی غیرقابل برگشت میشود. تزریق داخل زجاجیهای داروهای ضد VEGF (بواسیزوماب، رانیبیزوماب) مؤثر است18).
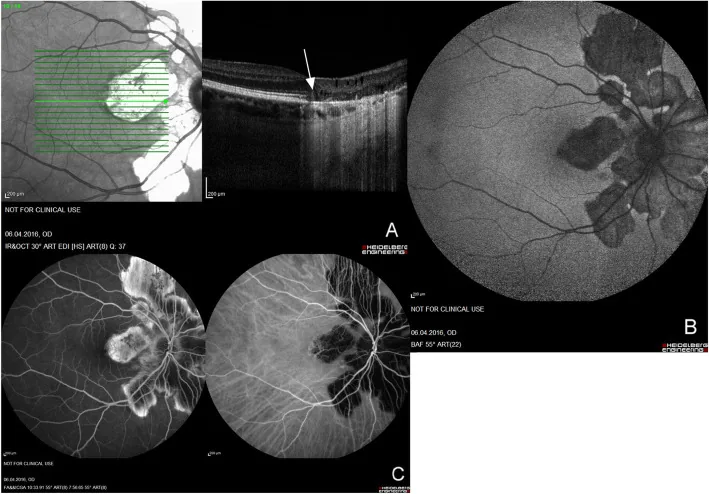
AZOOR (آکروپاتی حاد ناحیهای نهفته لایه خارجی شبکیه)
Section titled “AZOOR (آکروپاتی حاد ناحیهای نهفته لایه خارجی شبکیه)”AZOOR یک مفهوم بیماری است که توسط گاس در سال 1992 مطرح شد و یک رتینوپاتی خارجی است که با وجود تقریباً طبیعی بودن فوندوس، به طور ناگهانی باعث کاهش بینایی، نقص میدان بینایی و فوتوپسیا میشود3).
مفهوم کمپلکس AZOOR
کمپلکس AZOOR که توسط جامپول و همکاران مطرح شد، مفهومی است که MEWDS، AZOOR، PIC، MFC، AMN (نورورتینوپاتی حاد ماکولا)، AIBSE و AAOR را به عنوان یک پیوستار با زمینه مشترک خودایمنی/التهابی ژنتیکی درک میکند3).
تصویر بالینی مشخص
- شایع در زنان جوان 20 تا 50 ساله با نزدیکبینی
- فوتوپسی (دیدن نور) اغلب در مراحل اولیه بیماری ظاهر میشود (بهویژه نوری که بهصورت نواری یا کمانی دیده میشود)
- بیماری یکطرفه شروع میشود و در نهایت در ۷۶٪ موارد دوطرفه میشود
- در مرحله حاد، فوندوس تقریباً طبیعی است (افت بینایی با یافتههای فوندوس همخوانی ندارد)
- نقص میدان بینایی بهصورت الگوی نواری نامنظم (اغلب متصل به نقطه کور)
- ممکن است با بیماریهای خودایمنی (تیروئیدیت هاشیموتو، مولتیپل اسکلروزیس) همراه باشد
OCT و ERG کلید تشخیص هستند
- در OCT، از بین رفتن یا نامشخص شدن ناحیه ellipsoid (خط IS/OS) مهمترین یافته است
- در OCT، بهبود عملکرد در نواحی که لایه خارجی از بین رفته است، قابل انتظار نیست (برای پیشآگهی نیز مفید است)
- کاهش دامنه در ERG چندکانونی حتی در صورت نرمال بودن فوندوس قابل تشخیص است (حساسیت ERG چندکانونی بیشتر از ERG تمام میدان است)
- در FAF مادون قرمز، گاهی مرز بین ناحیه آسیبدیده و نرمال مشخص میشود
درمان و پیشآگهی
برای AZOOR درمان قطعی وجود ندارد. موارد خفیف فقط نیاز به پیگیری دارند، اما در موارد شدید (کاهش دید یا نقص میدان بینایی گسترده) از پالس درمانی با متیلپردنیزولون (۱۰۰۰ میلیگرم به مدت ۳ روز) و به دنبال آن پردنیزولون خوراکی استفاده میشود2). اکثر موارد در عرض ۶ ماه پایدار میشوند، اما میدان بینایی در نواحی با آسیب پایدار لایه خارجی بهبود نمییابد.
AZOOR و نوریت اپتیک رتروبولبار هر دو با فوندوس تقریباً طبیعی و کاهش بینایی و میدان بینایی تظاهر میکنند، بنابراین افتراق آنها ضروری است. نکات افتراقی عبارتند از: ① در AZOOR دامنه ERG چندکانونی کاهش مییابد اما در نوریت اپتیک رتروبولبار ERG طبیعی است. ② در AZOOR نقص میدان بینایی به صورت نواری یا قوسی نامنظم است در حالی که در نوریت اپتیک رتروبولبار اسکوتوم مرکزی شایعتر است. ③ در AZOOR RAPD معمولاً خفیف است اما در نوریت اپتیک رتروبولبار RAPD قابل توجه است. ④ در OCT، AZOOR با از بین رفتن ناحیه ellipsoid و نوریت اپتیک رتروبولبار با تورم دیسک اپتیک و نازک شدن RNFL مشخص میشود که به افتراق کمک میکند2, 3).
5. نحوه استفاده از تصویربرداری
Section titled “5. نحوه استفاده از تصویربرداری”تقسیم نقش بر اساس روش تصویربرداری
Section titled “تقسیم نقش بر اساس روش تصویربرداری”درک واضح نقش هر روش تصویربرداری برای تشخیص دقیق و ارزیابی فعالیت سندرمهای نقطه سفید ضروری است1, 5).
| مدالیته | قویترین اندیکاسیون/نقش |
|---|---|
| FA (آنژیوگرافی فلورسین) | ارزیابی نشت عروق شبکیه، RPE و کوریوکاپیلاریس. تأیید پدیده وارونگی فلورسانس در APMPPE. تأیید هیپرفلورسانس حلقوی در MEWDS. ارزیابی واسکولیت (Birdshot) |
| ICGA (آنژیوگرافی سبز ایندوسیانین) | ارزیابی مستقیم اختلال گردش خون مشیمیه. تشخیص زودهنگام ضایعات نسبت به FA (بهویژه Birdshot، APMPPE و سرپجینوس). تشخیص ضایعات گستردهتر از یافتههای بالینی (MEWDS، PIC). حساسترین روش برای تشخیص ضایعات فعال |
| FAF (فلورسانس خودبخودی فوندوس) | ارزیابی غیرتهاجمی آسیب RPE. تعیین فعالیت (APMPPE، سرپانتین). تشخیص MEWDS (نقاط سفید اولیه با فلورسانس خودبخودی بالا). ارزیابی مزمن شدن Birdshot (فلورسانس خودبخودی پایین اطراف پاپی در 73%) |
| OCT (توموگرافی انسجام نوری) | ارزیابی ناحیه بیضوی (یافته تشخیصی MEWDS و AZOOR). ارزیابی تکامل 5 مرحلهای ضایعه (PIC). ارزیابی CNV و ادم ماکولا. پیشآگهی (از بین رفتن EZ → پیشآگهی بد بینایی) |
| OCT-A | تشخیص غیرتهاجمی فقدان جریان در کوریوکاپیلاریس (APMPPE، سرپانتین، PIC). تشخیص زودهنگام و حساس CNV (در PIC و MFC حساستر از FA). ارزیابی جریان خون لایهای کوروئید در Birdshot. پایش پاسخ درمانی |
| ERG چندکانونی / ERG تمام میدان | تشخیص AZOOR (کاهش دامنه ERG حتی با فوندوس تقریباً طبیعی). پایش فعالیت Birdshot (تأخیر فلیکر 30Hz حساسترین). ارزیابی پاسخ درمان |
راهنمای «ابتدا کدام آزمایش» بر اساس بیماری
Section titled “راهنمای «ابتدا کدام آزمایش» بر اساس بیماری”هنگام شک به MEWDS
زمانی که APMPPE مشکوک است
- FA (تأیید پدیده معکوس فلورسانس)
- ICGA (ارزیابی مستقیم ایسکمی choriocapillaris)
- OCT-A (ارزیابی flow void)
- اگر علائم عصبی وجود دارد: MRI و MRA مغز (برای رد واسکولیت)
زمانی که PIC/MFC مشکوک است
زمانی که به کوریورتینوپاتی سرپانتینی (SC) مشکوک هستیم
استراتژی بسته به بیماری متفاوت است. در APMPPE و کوروئیدیت مارپیچی، ICGA اختلال گردش خون کوروئید را مستقیمتر نشان میدهد، بنابراین انجام ICGA همزمان یا پس از FA درک پاتوفیزیولوژی را عمیقتر میکند. در MEWDS، هیپرفلورسانس تاجمانند (wreath-like) در FA از نظر تشخیصی مهم است. با این حال، از آنجایی که این آزمایشها تهاجمی هستند، اکنون اطلاعات زیادی را میتوان با OCT-A جایگزین کرد و ترکیب FAF و OCT-A به عنوان ارزیابی اولیه استفاده میشود1, 5).
معنی ضایعات هیپوفلورسنت در ICGA
Section titled “معنی ضایعات هیپوفلورسنت در ICGA”هیپوفلورسانس ضایعات سندرم نقاط سفید در ICGA بازتاب مستقیم اختلال جریان خون کوروئید (انسداد کوریوکاپیلاریس) است1). ICGA به عنوان یک روش تصویربرداری برای ارزیابی گردش خون کوروئید حساسیت بیشتری نسبت به FA دارد و ویژگیهای زیر را داراست:
- هیپوفلورسانس در تمام فازها: در APMPPE، کوروئیدیت مارپیچی، PIC و MFC دیده میشود. نشاندهنده انسداد شدید ایسکمی کوریوکاپیلاریس است.
- هیپوفلورسانس دیررس (بدون ناهنجاری در FA): هیپوفلورسانس دیررس ICGA در MEWDS بهعنوان تغییر در جذب ICG ناشی از ناهنجاری RPE بهجای درگیری اولیه کوریوکاپیلاریس توضیح داده میشود (در OCT-A، کوریوکاپیلاریس عمدتاً حفظ میشود)1).
- flow void لایه Haller → flow void تمام لایه در مرحله پیشرفته: الگوی پیشرفت دو مرحلهای مخصوص Birdshot از استرومای مشیمیه به کوریوکاپیلاریس14).
ICGA نسبت به FA و OCT-A در تشخیص ضایعات پنهان بالینی (subclinical lesions) برتری دارد و بهویژه در MEWDS و PIC، ضایعات مشیمیهای گستردهتری را نسبت به نقاط سفید نشان میدهد1, 15).
نقشه بیماری بر اساس الگوهای هیپوفلورسانس و هیپرفلورسانس در FAF
Section titled “نقشه بیماری بر اساس الگوهای هیپوفلورسانس و هیپرفلورسانس در FAF”الگوی FAF (فلورسانس خودبخودی فوندوس) وضعیت متابولیک RPE را منعکس میکند و برای تشخیص و ارزیابی فعالیت سندرمهای نقاط سفید مفید است16).
| الگوی FAF | بیماری/مرحله | معنی |
|---|---|---|
| خودفلورسانس بالا (بیشفلورسانس) | فاز حاد MEWDS · لبه فعال سرپجینوس | تجمع محصولات تخریب سلولهای بینایی (مانند A2E) در RPE |
| خودفلورسانس پایین (کمفلورسانس) | فاز اسکار APMPPE · ضایعه فعال PIC · اطراف پاپیلای بردشات | از بین رفتن یا عدم عملکرد RPE |
| هالهای با AF مرکزی کم و AF حاشیهای زیاد | لبه فعال سرپجینوس و PIC | الگوی آسیب RPE در لبه فعال |
| AF غیرعادی نواری | AZOOR | مطابق با توزیع آسیب لایه خارجی فوتورسپتورها |
| هیپرفلورسانس گرانولار فووئال | MEWDS (NIR-FAF) | تصویربرداری غیرتهاجمی از دانهبندی فووئال |
در بیماری Birdshot، هیپوفلورسانس همجوار پاپیلاری در ۷۳٪ موارد دیده میشود و به عنوان شاخص مزمن شدن مفید است17).
الگوی نقص ناحیه بیضوی (EZ) در OCT
Section titled “الگوی نقص ناحیه بیضوی (EZ) در OCT”ارزیابی ناحیه بیضوی (EZ، خط IS/OS قدیمی) نقش محوری در پیشبینی فعالیت و پیشآگهی سندرم نقاط سفید دارد1).
| یافته EZ | بیماری/مرحله | پیشآگهی |
|---|---|---|
| اختلال شدید EZ → بهبود | MEWDS فاز حاد → فاز بهبودی | خوب (بهبود EZ و بهبود بینایی هماهنگ) |
| از بین رفتن EZ (مطابق با ناحیه ضایعه) | فاز فعال AZOOR | بدون بهبود عملکرد در ناحیه از دست رفته |
| اختلال EZ + بازتاب بالای شبکیه خارجی | فاز حاد APMPPE | پس از بهبود، مقداری آتروفی باقی میماند |
| برجستگی با بازتاب بالا زیر RPE + پارگی EZ | PIC/MFC (پنج مرحله تکامل) | پیشآگهی بد با همراهی CNV |
| از بین رفتن EZ (همراه با ادم ماکولای کیستی) | مرحله پیشرفته Birdshot | عامل خطر برای پیشآگهی بد بینایی |
نقص جریان خون در مویرگهای کوروئید (choriocapillaris flow void) در OCT-A همبستگی بالایی با یافتههای FA و ICGA نشان میدهد (به ویژه در APMPPE و کوروئیدیت مارپیچی مفید است)5, 13).
الگوهای فلورسانس در FA: تأخیر در پر شدن vs هیپرفلورسانس vs نشت
Section titled “الگوهای فلورسانس در FA: تأخیر در پر شدن vs هیپرفلورسانس vs نشت”| الگوی FA | بیماری | اهمیت بالینی |
|---|---|---|
| هیپوفلورسانس اولیه → هیپرفلورسانس دیررس (پدیده معکوس فلورسانس) | APMPPE | ایسکمی لایه مویرگی کوروئید. اختلال در پر شدن اولیه → نشت تأخیری رنگ از بافت اطراف |
| هایپرفلورسانس اولیه تاجمانند (wreath-like) | MEWDS | بهطور مستقیم آسیب RPE/سلولهای بینایی را نشان میدهد. نکته افتراقی: در مراحل بعدی بزرگ نمیشود |
| هیپوفلورسانس اولیه → نشت در مراحل بعدی | فاز فعال سرپجینوس و MFC | شواهد کوریوئیدیت فعال |
| هیپرفلورسانس اولیه فاز شریانی → نشت دیررس | فاز فعال PIC | مشکوک به وجود CNV التهابی |
| نشت عروقی + هیپرفلورسانس پاپیلاری (بدون نشت) | Birdshot | شواهد مستقیم واسکولیت شبکیه |
| معمولاً طبیعی تا خفیف | AZOOR | ویژگی آن عدم تطابق است: حتی اگر FA منفی باشد، نقص میدان بینایی و ناهنجاری ERG مشاهده میشود |
6. اصول کلی درمان
Section titled “6. اصول کلی درمان”انتخاب استراتژی درمان
Section titled “انتخاب استراتژی درمان”درمان سندرم لکههای سفید بسته به سیر طبیعی بیماری، شدت و وجود CNV تفاوت زیادی دارد.
بیماریهایی که اساساً نیاز به پیگیری (بدون درمان) دارند
Section titled “بیماریهایی که اساساً نیاز به پیگیری (بدون درمان) دارند”- تمایل شدید به بهبود خودبهخودی دارند و اغلب بدون درمان خاصی بهبود مییابند2)
- MEWDS: لکههای سفید در عرض چند هفته ناپدید شده و بینایی بهبود مییابد. در موارد شدید یا همراه با ادم پاپی، استروئید خوراکی تجویز میشود.
- APMPPE: لکههای سفید در ۷ تا ۱۲ روز پسرفت کرده و پیشآگهی بینایی معمولاً خوب است.
بیماریهایی که درمان اصلی آنها استروئید درمانی است
Section titled “بیماریهایی که درمان اصلی آنها استروئید درمانی است”APMPPE (شدید، همراه با پاپیلیت) • PIC (ضایعه فعال نزدیک فووهآ) • AZOOR (موارد شدید)
- شروع با پردنیزولون ۳۰ تا ۶۰ میلیگرم در روز و سپس کاهش تدریجی
- در APMPPE همراه با واسکولیت مغزی، نیاز به پالس متیلپردنیزولون و همکاری با نورولوژیست
- معیار شدت AZOOR: بهترین دید اصلاحشده چشم با دید خوب < ۰.۳ (بر اساس راهنمای تشخیصی انجمن چشمپزشکی ژاپن)
بیماریهایی که نیاز به درمان طولانیمدت با سرکوبکنندههای ایمنی دارند
Section titled “بیماریهایی که نیاز به درمان طولانیمدت با سرکوبکنندههای ایمنی دارند”کوریورتینیت بردشات، کوروئیدیت مارپیچی، MFC
بردشات (مدیریت طولانیمدت)
- شروع با پردنیزولون 0.5 تا 1 میلیگرم/کیلوگرم/روز
- میکوفنولات موفتیل (MMF) 2 تا 3 گرم/روز (داروی سرکوبکننده ایمنی خط اول)
- متوترکسات (MTX) 10 تا 25 میلیگرم/هفته
- آزاتیوپرین (AZA) 1 تا 3 میلیگرم/کیلوگرم/روز
- موارد مقاوم: آدالیموماب (93.2% به عنوان اولین داروی بیولوژیک استفاده میشود)
- بدون درمان، 16 تا 22% در 10 سال به دید 0.1 یا کمتر میرسند
کوروئیدیت مارپیچی (مدیریت طولانیمدت)
- پردنیزولون 40 تا 80 میلیگرم در روز شروع (کاهش تدریجی)
- آزاتیوپرین 1 تا 2.5 میلیگرم/کیلوگرم/روز (درمان نگهدارنده خط اول)
- میکوفنولات موفتیل و متوترکسات (جایگزین)
- موارد مقاوم: کلرامبوسیل (قویترین؛ حداکثر 0.2 میلیگرم/کیلوگرم/روز، آزمایش خون هفتگی الزامی)
- داروهای بیولوژیک: آدالیموماب (91.0% به عنوان گزینه اول توصیه میشود)
- پس از رد سل (در صورت مثبت بودن IGRA، ابتدا داروی ضد سل) و تأیید، داروی سرکوبکننده ایمنی شروع شود
درمان تعدیلکننده ایمنی MFC
Section titled “درمان تعدیلکننده ایمنی MFC”از آنجایی که MFC سیر مزمن عودکننده دارد، در بسیاری از موارد پس از کاهش تدریجی استروئید، نیاز به داروهای تعدیلکننده ایمنی به عنوان درمان نگهدارنده وجود دارد.
| دارو | دوز تقریبی | نکات ویژه |
|---|---|---|
| متوترکسات (MTX) | 10 تا 25 میلیگرم در هفته | همراه با فولیک اسید 1 میلیگرم در روز. پایش سمیت کبدی |
| آزاتیوپرین (AZA) | 1 تا 3 میلیگرم به ازای هر کیلوگرم در روز | توصیه به بررسی فعالیت TPMT. احتیاط در مورد سرکوب سلولهای خونی |
| میکوفنولات موفتیل (MMF) | ۱ تا ۳ گرم در روز | علائم گوارشی شایعترین عوارض جانبی هستند |
| سیکلوسپورین (CsA) | ۳ تا ۵ میلیگرم به ازای هر کیلوگرم وزن بدن در روز | پایش عملکرد کلیه و فشار خون ضروری است |
| آدالیموماب | 40 میلیگرم هر ۲ هفته (تزریق زیرجلدی) | موارد مقاوم یا وابسته به استروئید. غربالگری سل الزامی است |
مدیریت CNV همزمان
Section titled “مدیریت CNV همزمان”CNV مهمترین عارضه مؤثر بر پیشآگهی بینایی است و در PIC، MFC و کوروئیدیت مارپیچی به ویژه شایع است.
| بیماری | میزان همراهی CNV | درمان |
|---|---|---|
| PIC | 40-76% | تزریق داخل زجاجیهای ضد VEGF (بواسیزوماب، رانیبیزوماب، آفلیبرسپت) + استروئید. استراتژی PRN با OCTA |
| MFC | حداکثر 60% | تزریق داخل زجاجیهای ضد VEGF + درمان تعدیلکننده ایمنی |
| کوروئیدیت مارپیچی | حداکثر 35% | تزریق داخل زجاجیهای ضد VEGF (بواسیزوماب، رانیبیزوماب) |
| MEWDS·APMPPE | نادر | ضد VEGF (در صورت تأیید CNV همزمان) |
| Birdshot | نادر | درمان سرکوبکننده سیستم ایمنی + ضد VEGF در صورت CNV همزمان |
نکات احتیاطی در درمان
Section titled “نکات احتیاطی در درمان”| نکته | بیماری مربوطه |
|---|---|
| اولویت اول رد سل (قبل از سرکوب ایمنی) | کوروئیدیت مارپیچی شکل / MFC |
| در نظر گرفتن HLA-A29 (تشخیص) | شات پرنده (حساسیت پایین در ژاپنیها) |
| خطر افزایش فشار چشم با ایمپلنت استروئیدی | شات پرنده (حداکثر 40% نیاز به ترابکولکتومی) |
| خطر سرکوب مغز استخوان و بدخیمی با کلرامبوسیل | کوروئیدیت مارپیچی (آزمایش خون هفتگی ضروری) |
| COVID-19 感染・ワクチン後の再燃 | PIC・MEWDS(再燃報告あり) |
| 脳血管炎合併時の緊急対応 | APMPPE(頭痛・神経症状→脳 MRI 緊急施行) |
白点症候群に対して免疫抑制薬を開始する前に確認すべき必須検査は以下のとおりです。①IGRA(クォンティフェロン)による結核除外(蛇行状脈絡膜炎では最優先)、②HBs 抗原・HBc 抗体・HCV 抗体によるウイルス性肝炎スクリーニング(免疫抑制による再活性化防止)、③胸部 X 線・CT(結核・サルコイドーシスの除外)、④全血算・肝腎機能検査(ベースライン値の確認)。アダリムマブ等の生物学的製剤では結核スクリーニングが薬剤添付文書上も必須となっています19, 20)。
برخلاف دژنراسیون ماکولای وابسته به سن، در CNV التهابی (iCNVM) ممکن است با کنترل التهاب، CNV به طور خودبهخود پسرفت کند. معمولاً از استراتژی PRN (تجویز در صورت نیاز) استفاده میشود و هر بار که CNV فعال در OCT-A تأیید شود، تزریق انجام میشود. گاهی دوزهای بارگیری اولیه (سه تزریق متوالی) نیز انجام میشود، اما ترکیب با درمان سرکوبکننده ایمنی ممکن است تعداد تزریقات مورد نیاز را کاهش دهد. خطر عود با درمان ضد VEGF به تنهایی بالا است و رویکرد دوگانه با کنترل التهاب زمینهای اهمیت دارد7, 8).
6.5 ارتباط با بیماریهای سیستمیک
Section titled “6.5 ارتباط با بیماریهای سیستمیک”بیماریهای مختلف سندرم نقاط سفید با بیماریها و عفونتهای سیستمیک خاصی مرتبط هستند و جستجوی سیستماتیک برای رد این موارد قبل از درمان اهمیت دارد.
| بیماری | بیماری یا وضعیت سیستمیک مرتبط | اهمیت بالینی |
|---|---|---|
| APMPPE | واسکولیت مغزی (MCAT) · عفونت استرپتوکوکی · ویروس اپشتین-بار | سردرد · علائم عصبی → MRI فوری مغز |
| Birdshot | HLA-A29 (۸۰-۹۸٪ در سفیدپوستان) · مشابه سارکوئیدوز | آزمایش HLA به تشخیص کمک میکند (حساسیت پایین در ژاپنیها) |
| کوروئیدیت مارپیچی | سل (SLC) · HLA-B7/A2 | IGRA مثبت → اصولاً درمان ضد سل اولویت دارد |
| PIC | سارکوئیدوز · HLA-DRB1*15 | در نظر گرفتن CT قفسه سینه و اندازهگیری ACE |
| MFC | هاپلوتیپ IL-10 · EBV · سارکوئیدوز | در موارد عودکننده مزمن، ارزیابی مجدد سیستمیک انجام شود |
| MEWDS | عفونت COVID-19 · پس از واکسیناسیون · HLA-B51 | عفونت SARS-CoV-2 به عنوان محرک ایمنی عمل میکند |
| AZOOR | بیماری هاشیموتو، مولتیپل اسکلروزیس، بیماریهای خودایمنی | در نظر گرفتن آزمایش عملکرد تیروئید و آنتیبادیهای خودایمنی |
7. نکات ویژه و یافتههای جدید در بیماریهای مختلف
Section titled “7. نکات ویژه و یافتههای جدید در بیماریهای مختلف”APMPPE و طیف کوریورتینیت پلاکوئید
Section titled “APMPPE و طیف کوریورتینیت پلاکوئید”APMPPE همراه با ماکولوپاتی پلاکوئید پایدار (PPM) و کوریورتینیت پلاکوئید بیامان (RPC) به عنوان «طیف کوریورتینیت پلاکوئید» به طور یکپارچه درک میشود. در این سه بیماری، OCT-A یک الگوی مشترک از فقدان جریان کوریوکاپیلاریس را نشان میدهد که نشاندهنده ایسکمی صفحه مویرگی مشیمیه به عنوان زمینه پاتولوژیک مشترک است 5).
Klufas و همکاران (2017) گزارش کردند که OCT-A در سه بیماری APMPPE، PPM و RPC فقدان جریان کوریوکاپیلاریس را با تطابق بالایی با FA و ICGA تشخیص میدهد و از مفهوم طیف کوریورتینیت پلاکوئید حمایت میکند 5).
MEWDS و دانهدانه شدن فووئال
Section titled “MEWDS و دانهدانه شدن فووئال”تغییرات دانهدانه فووئال (foveal granularity) یک یافته تشخیصی است که در 74 تا 96 درصد موارد MEWDS دیده میشود و ممکن است پس از ناپدید شدن نقاط سفید به عنوان تنها یافته باقی بماند. NIR-FAF یک الگوی دانهدانه فووئال مشخص را نشان میدهد 9).
طیف بیماری PIC و MFC
Section titled “طیف بیماری PIC و MFC”PIC و MFC (MFCwP) زمینه ژنتیکی مشترکی (هاپلوتیپ IL-10 و HLA-DRB1*15) دارند و به عنوان فنوتیپهای متفاوت از یک طیف بیماری واحد در نظر گرفته میشوند. تفاوتهای اصلی شامل وجود یا عدم وجود ویتریت و التهاب اتاق قدامی و توزیع ضایعات است1, 3).
| نقطه افتراق | PIC | MFC (MFCwP) |
|---|---|---|
| ویتریت | ندارد | دارد (نقطه افتراق مهم) |
| التهاب اتاق قدامی | ندارد | خفیف دارد |
| توزیع ضایعات | محدود به قطب خلفی | قطب خلفی + محیط میانی |
| اندازه ضایعه | 100-300 میکرومتر | 45-350 میکرومتر |
| میزان همراهی با CNV | 40-76% | حداکثر 60% |
Birdshot و HLA-A29
Section titled “Birdshot و HLA-A29”ارتباط بین Birdshot و HLA-A29 یکی از قویترین ارتباطات ژنتیکی در میان تمام بیماریهای شناخته شده است و در بیماران سفیدپوست خطر نسبی را ۵۰ تا ۲۲۴ برابر افزایش میدهد4). با این حال، در ژاپنیها به دلیل شیوع کم HLA-A29، حساسیت تست HLA-A29 در تشخیص محدود است. تشخیص بر اساس معیارهای بالینی SUN 2021 (یافتههای فوندوس، التهاب خفیف اتاق قدامی، ویتریت) اهمیت دارد10).
کمپلکس AZOOR و محرک ویروسی
Section titled “کمپلکس AZOOR و محرک ویروسی”تصور میشود AZOOR در نتیجه استعداد ژنتیکی (مانند هاپلوتیپ IL-10) همراه با محرکهای محیطی مانند عفونت ویروسی، واکسن یا دارو ایجاد شود و همراه با MEWDS، PIC، AMN و AIBSE به عنوان کمپلکس AZOOR درک میشود3). موارد MEWDS پس از عفونت COVID-19 یا واکسیناسیون در سراسر جهان افزایش یافته است که نشان میدهد SARS-CoV-2 ممکن است به عنوان یک محرک ایمنی عمل کند11).
بله. موارد متعددی از شروع یا عود MEWDS، PIC و کوروئیدیت مارپیچی پس از عفونت COVID-19 گزارش شده است که نشان میدهد عفونت SARS-CoV-2 ممکن است به عنوان یک محرک ایمنی عمل کند11, 12). در MEWDS، یک مرور سیستماتیک روی ۲۷ مورد پس از واکسیناسیون COVID-19 انجام شده که واکسن mRNA (Pfizer-BioNTech) شایعترین بود. افرادی که سابقه این بیماری را دارند بهتر است در مورد پیگیری قبل و بعد از واکسیناسیون با چشمپزشک خود مشورت کنند.
اولویت آزمایشها در شک اولیه به سندرم لکههای سفید به شرح زیر توصیه میشود: ① FAF + OCT (غیرتهاجمی و امکان ارزیابی اولیه تقریباً همه بیماریها؛ AF بالای MEWDS، ارزیابی ناحیه ellipsoid و برجستگی زیر RPE در PIC قابل مشاهده است) → ② OCT-A (تشخیص زودهنگام CNV و ارزیابی flow void کوریوکاپیلاریس) → ③ FA + ICGA (در صورت نیاز به تشخیص قطعی و ارزیابی فعالیت). در صورت شک به کوروئیدیت مارپیچی، IGRA (رد سل) قبل از FA اولویت دارد. در شک به AZOOR، ERG (multi-focal ERG) ضروری است1, 2).
۸. مقالات مرتبط
Section titled “۸. مقالات مرتبط”9. منابع
Section titled “9. منابع”- Testi I, Modugno RL, Pavesio C. Multimodal imaging supporting the pathophysiology of white dot syndromes. J Ophthalmic Inflamm Infect. 2021;11:32.
- 日本眼炎症学会・日本眼科学会. ぶどう膜炎診療ガイドライン(13〜18節:APMPPE・MEWDS・PIC・多発性脈絡膜炎・バードショット・蛇行状脈絡膜炎・AZOOR). 日本眼科学会雑誌. 2019;123(6):635-696.
- Jampol LM, Becker KG. White spot syndromes of the retina: a hypothesis based on the common genetic hypothesis of autoimmune/inflammatory disease. Am J Ophthalmol. 2003;135(3):376-379.
- Agrawal R, et al. The role of HLA-A29 in birdshot chorioretinopathy and immune checkpoint inhibitor-related uveitis. Am J Ophthalmol. 2025. doi:10.1016/j.ajo.2024.01.007
- Klufas MA, Phasukkijwatana N, Iafe NA, et al. Optical coherence tomography angiography reveals choriocapillaris flow reduction in placoid chorioretinitis. Ophthalmol Retina. 2017;1(1):77-91.
- Stattin M, Forster J, Ahmed D, Krepler K, Ansari-Shahrezaei S. Swept Source-Optical Coherence Tomography Angiography for Management of Secondary Choroidal Neovascularization in Punctate Inner Choroidopathy. Case Rep Ophthalmol. 2021;12:232-238.
- Spaide RF, Goldberg N, Freund KB. Redefining multifocal choroiditis and panuveitis and punctate inner choroidopathy through multimodal imaging. Retina. 2013;33(7):1315-1324.
- Leclaire MD, Clemens CR, Eter N, Mihailovic N. Choroidale Neovaskularisation infolge einer “punctate inner choroidopathy”, dargestellt mittels optischer Kohärenztomographie-Angiographie. Ophthalmologe. 2021;118:842-846.
- Mantovani A, Invernizzi A, Staurenghi G, Herbort CP Jr. Multiple evanescent white dot syndrome: a multimodal imaging study of foveal granularity. Ocul Immunol Inflamm. 2019;27(1):141-147.
- Standardization of Uveitis Nomenclature (SUN) Working Group. Classification criteria for birdshot chorioretinitis. Am J Ophthalmol. 2021;228:65-71.
- Chen N, Mandell M, Arjmand P. Multimodal imaging findings of multiple evanescent white dot syndrome in COVID-19 patients. IDCases. 2024;38:e02110.
- Seddigh S, Pinto A, Zaki AM, Gupta RR. Serpiginous choroiditis after COVID-19 infection. J Vitreoretinal Dis. 2025;9(2):246-252.
- Pakzad-Vaezi K, Khaksari K, Chu Z, Van Gelder RN, Wang RK, Pepple KL. Swept-source OCT angiography of serpiginous choroiditis. Ophthalmol Retina. 2018;2(7):712-719.
- Pepple KL, Chu Z, Weinstein J, Munk MR, Van Gelder RN, Wang RK. Use of en face swept-source optical coherence tomography angiography in identifying choroidal flow voids in 3 patients with birdshot chorioretinopathy. JAMA Ophthalmol. 2018;136(11):1288-1292. doi:10.1001/jamaophthalmol.2018.3474. PMID:30128478. PMCID:PMC6248174
- Khochtali S, Dridi T, Abroug N, et al. Swept-source optical coherence tomography angiography shows choriocapillaris flow reduction in multiple evanescent white dot syndrome. J Curr Ophthalmol. 2020;32(2):211-215.
- Yeh S, Forooghian F, Wong WT, et al. Fundus autofluorescence imaging of the white dot syndromes. Arch Ophthalmol. 2010;128(1):46-56.
- Minos E, Barry RJ, Southworth S, et al. Birdshot chorioretinopathy: current knowledge and new concepts in pathophysiology, diagnosis, monitoring and treatment. Orphanet J Rare Dis. 2016;11(1):61.
- Maleki A, Maldonado Cerda A, Garcia CM, et al. Chlorambucil combination therapy in refractory serpiginous choroiditis: a cure? Am J Ophthalmol Case Rep. 2021;21:101014.
- Niederer RL, Al-Janabi A, Engelbrecht C, et al. Immunomodulatory therapy prescribing practices for non-infectious uveitis: a survey of international experts. Br J Ophthalmol. 2024;108:482-489.
- Tomkins-Netzer O, et al. Treatment of non-infectious uveitis with biologics: a survey of the International Ocular Inflammation Society. Br J Ophthalmol. 2022;106:482-488.
