外视网膜为主型
MEWDS・AZOOR
- 主要病变为椭圆体带(感光细胞内节/外节连接处)的短暂破坏
- 脉络膜毛细血管通常不受累(OCT-A上无或仅有轻微血流空区)
- 可逆性高,有很强的自然缓解倾向

白点综合征(white dot syndromes)是1977年由Gass命名的概念,指眼底出现多个白色或黄白色斑点状病变的一组炎症性疾病。虽然研究者对目标疾病的定义有所不同,但目前广泛将其视为主要累及外视网膜、RPE、脉络膜毛细血管层和脉络膜的非感染性特发性炎症性疾病群1)。
在葡萄膜炎诊疗指南(日眼会志 2019;123(6):635-696)中,APMPPE、MEWDS、PIC、多灶性脉络膜炎、鸟枪弹样视网膜脉络膜病变、蛇行状脉络膜炎和AZOOR被列为后葡萄膜炎的独立疾病类型,当使用“白点综合征”这一统称时,则涵盖这些疾病2)。
随着多模态成像(包括OCT-A)的进步,白点综合征现在根据病变主要累及的层次分为以下三组1)。
外视网膜为主型
MEWDS・AZOOR
脉络膜毛细血管板主导型
脉络膜间质主导型
此外,还提出了AZOOR复合体的概念,将MEWDS、AZOOR、PIC、MFC、AMN、AIBSE和AAOR视为具有共同遗传性自身免疫/炎症机制的连续体3)。
根据日本眼炎症学会统计,白点综合征各疾病在全部葡萄膜炎中所占比例见下2)。
| 疾病 | 占全部葡萄膜炎的比例 |
|---|---|
| MEWDS | 约1-2%(国内报告) |
| APMPPE | 罕见(无明确年发病率统计) |
| PIC | 罕见 |
| 匍行性脉络膜炎 | 约0.3% |
| 鸟枪弹样视网膜脉络膜病变 | 罕见(白种人多见,日本极为罕见) |
| AZOOR | 罕见(近年报告数量增加) |
各疾病的症状虽不同,但以下临床特征为白点综合征群所共有1, 2)。
| 疾病组 | 前房/玻璃体炎症 |
|---|---|
| MEWDS、APMPPE、PIC | 通常无(APMPPE 可有轻度) |
| MFC(MFCwP) | 前房炎症 + 玻璃体炎(与 PIC 鉴别点) |
| Birdshot | 无至轻微前房炎症,有玻璃体炎 |
| 匐行性脉络膜炎 | 前房炎症和玻璃体炎通常轻微 |
| AZOOR | 通常无 |
年轻女性、单眼、自然缓解
年轻至中年女性、双眼、CNV风险
青年至中年、双眼、急性发作
中老年、双眼、慢性进行性
鸟枪弹样脉络膜视网膜病变・匍行性脉络膜炎
眼底に白点状病変 │ ├─ 片眼性? │ ├─ YES → MEWDS・AZOOR・AMN を考慮 │ │ ↳ FA で初期過蛍光 → MEWDS │ │ ↳ 眼底ほぼ正常・ERG 異常 → AZOOR │ └─ NO(両眼性) │ ├─ 急性発症・後極部大型白斑? │ └─ YES → APMPPE(FA 蛍光逆転現象を確認) │ ├─ 後極部小病変・近視女性・硝子体炎なし? │ └─ YES → PIC を考慮(CNV 検索:OCTA 必須) │ ├─ 小病変・硝子体炎あり・周辺部にも病変? │ └─ YES → MFC(MFCwP)を考慮 │ ├─ 乳頭周囲から蛇行状に進展・男性多め? │ └─ YES → 蛇行状脈絡膜炎(結核除外が最優先) │ └─ 後極部散弾状病変・中高年・HLA-A29? └─ YES → Birdshot 網脈絡膜症| 项目 | APMPPE | MEWDS | PIC | MFC(MFCwP) | Birdshot | 匐行性脉络膜炎 | AZOOR |
|---|---|---|---|---|---|---|---|
| 好发年龄 | 20~30岁(平均25岁) | 20~50岁 | 18~40岁(平均36岁) | 平均30岁 | 40~60岁 | 30~50岁 | 以35岁左右为中心 |
| 性别 | 无性别差异 | 女性优势(1:4) | 女性优势(约90%) | 女性优势(白人女性多见) | 女性略多 | 男性略多 | 女性优势(约75%) |
| 单眼/双眼 | 多为双眼 | 单眼(≥95%) | 多为双眼(80%) | 双眼 | 双眼 | 双眼 | 单眼→双眼进展(最终76%双眼) |
| 主要症状 | 视力下降、中心暗点、视物变形 | 视力下降、闪光感、视物模糊 | 暗点、视力下降、视物变形 | 飞蚊症、视力下降、闪光感 | 视力下降、夜盲、色觉异常 | 视力下降、旁中心暗点 | 闪光感、视野缺损(眼底基本正常) |
| 眼底白斑的特征 | 后极部大型奶油色白斑(1/4~1/2 视盘直径) | 后极部至赤道部淡灰白色多发性小斑(100~200μm) | 后极部黄白色小斑(100~300μm),12~25个 | 后极部至周边黄灰色斑(45~350μm),伴玻璃体炎 | 后极部至赤道部散弹状奶油色斑(1/4~1/2 视盘直径) | 视盘周围蜿蜒状扩展的地图状灰黄色病变 | 眼底基本正常(急性期),后期外层萎缩 |
| OCT 表现 | 椭圆体带紊乱 + 外层视网膜高反射,恢复后部分萎缩残留 | 椭圆体带明显紊乱/消失(急性期)→ 恢复 | RPE 下高反射隆起 + EZ 断裂(5 阶段演变) | RPE 下高反射 + EZ 断裂(类似 PIC) | 脉络膜病变、囊样黄斑水肿,EZ 消失提示预后不良 | 活动期:外层视网膜高反射、视网膜下液。瘢痕期:RPE 萎缩 | EZ(IS/OS)消失是最重要表现(与视野缺损部位一致) |
| FA 表现 | 早期低荧光→晚期高荧光(荧光逆转现象) | 早期开始持续的花环状高荧光 | 活动期:动脉期早期高荧光→晚期渗漏 | 活动期:早期低荧光→晚期渗漏 | 病灶高荧光(无渗漏)+ 血管渗漏及视盘高荧光 | 活动期:早期低荧光→晚期高荧光(渗漏) | 通常正常或轻微异常 |
| ICGA 表现 | 各期低荧光(直接反映脉络膜毛细血管板缺血) | 晚期低荧光(范围比白点更广) | 中期低荧光,有助于检测亚临床病变 | 早期至各期低荧光 | 早期/中期低荧光→晚期等荧光(初期)→进展期:各期低荧光 | 各期低荧光(反映脉络膜循环障碍) | 通常正常 |
| FAF 表现 | 急性期:低或高自发荧光。缓解期:低自发荧光 | 急性期:高自发荧光(多发高荧光点)。恢复后:正常化 | 活动期:低自发荧光(hypoAF),边缘高自发荧光晕 | 活动期:低自发荧光 | 视乳头周围融合性低自发荧光(73%可见) | 活动期:高自发荧光边缘+低自发荧光晕。静止期:低自发荧光 | 带状高至低自发荧光异常 |
| OCT-A 表现 | 脉络膜毛细血管层血流缺失(与FA/ICGA高度一致) | 脉络膜毛细血管层基本保留(部分一过性血流缺失) | 脉络膜毛细血管层血流缺失(炎症病变部位) | 脉络膜毛细血管层血流缺失 | Haller层血流缺失(早期)→进展期:全层血流缺失 | 脉络膜毛细血管层血流缺失(重度) | 脉络膜毛细血管层基本保留 |
| 复发性 | 罕见(基本单次发作) | 约10%复发 | 高(慢性复发性) | 高(反复炎症发作) | 高(慢性,反复复发缓解) | 高(每3个月至4年间隔反复) | 多数6个月内稳定,部分进展 |
| CNV 合并率 | 罕见 | 罕见 | 40–76%(高风险) | 高达 60% | 视网膜下 CNV:罕见 | 高达 35% | 几乎没有 |
| HLA 相关 | 无 | HLA-B51(初步报告) | HLA-DR2、HLA-DRB1*15 | IL-10 单倍型相关 | HLA-A29(白人中80-98%) | HLA-B7、HLA-A2(相关报告) | 无(免疫学易感性) |
| 治疗方案 | 观察(自然缓解),重症:类固醇 | 观察,重症:短期类固醇,CNV:抗VEGF | 观察(无CNV),CNV:抗VEGF+类固醇,免疫抑制剂 | 类固醇+免疫调节治疗,CNV:抗VEGF | 类固醇+霉酚酸酯/阿达木单抗(长期) | 类固醇+免疫抑制剂(包括烷化剂),CNV:抗VEGF | 观察,重症:类固醇冲击 |
| 视力预后 | 良好(多可自然缓解) | 良好(注意复发和CNV) | 合并CNV时预后不良风险高 | CNV和黄斑水肿导致预后不良风险 | 未经治疗,10年内16%~22%视力≤0.1 | 累及中心凹则不可逆,最多25%的眼最终视力<20/200 | 多数稳定。外层进行性损害者预后不良 |
APMPPE好发于20~30岁(平均25岁),无性别差异。其本质被认为是脉络膜毛细血管板输入小动脉的闭塞性血管炎,病毒感染等可能为诱因1, 2)。
前驱症状与病程
特殊并发症:脑血管炎(MCAT)
APMPPE合并中枢神经系统血管炎(MCAT:多发性脑动脉血栓形成)是一种严重的并发症。如果出现头痛、发热或神经症状,需要紧急进行脑部MRI和MRA检查。合并脑血管炎的病例需要进行甲泼尼龙脉冲治疗并与神经内科协作2)。
与placoid脉络膜视网膜炎谱系的关系
APMPPE与PPM(持续性placoid黄斑病变)和RPC(顽固性placoid脉络膜视网膜炎)共同构成“placoid脉络膜视网膜炎谱系”,其共同病理基础是脉络膜毛细血管板缺血5)。
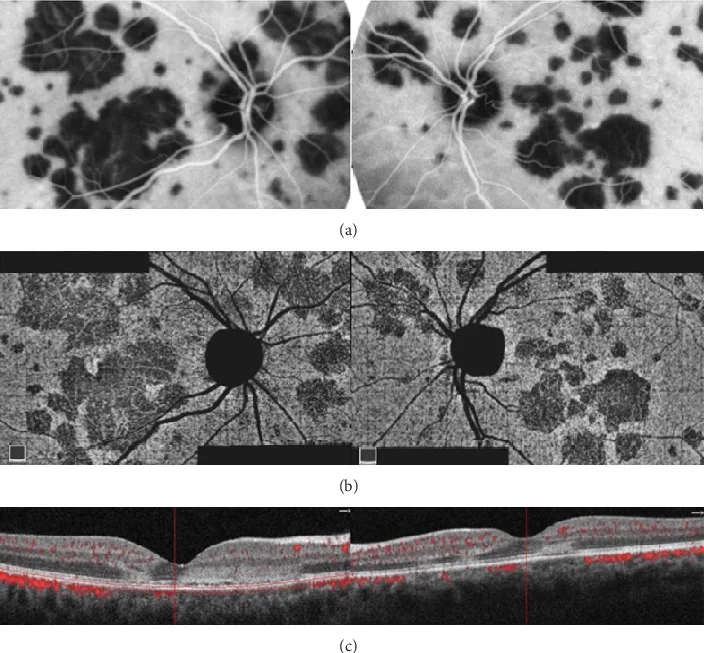
MEWDS好发于20~50岁女性(男女比例1:4),特征为单眼、急性、自然缓解。
特有的临床表现
FA上的花冠状高荧光
FA早期特征性的花冠状高荧光是诊断MEWDS的关键。白点病变在FA早期即出现高荧光,晚期不扩大。这种早期高荧光是与APMPPE早期低荧光(荧光逆转现象)的重要鉴别点1, 9)。
与AZOOR复合体的连续性
MEWDS 主要涉及光感受器椭圆体带(IS/OS 线)的短暂破坏,被理解为属于 AZOOR 复合体的疾病。OCT 可在急性期确认椭圆体带的紊乱或消失,并随视力恢复而改善3)。
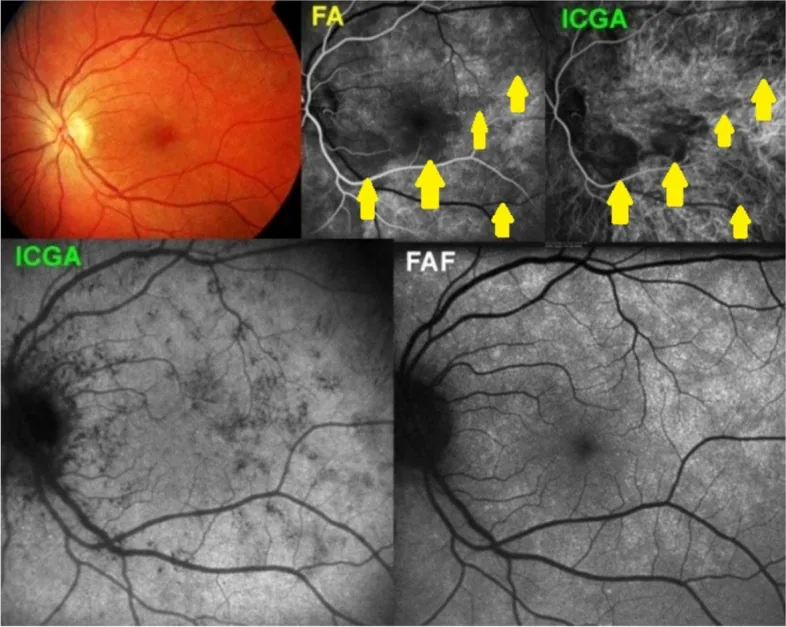
PIC 好发于 18-40 岁患有近视(平均约 -5 D)的年轻女性(约 90%)。
特有的临床表现
CNV合并(40%~76%)是最大的临床问题
PIC最重要的并发症是CNV,其发生率据报道为40–76%7, 8)。CNV易由以下因素引起:
OCT-A已被证明在CNV筛查中比FA更敏感,建议定期进行OCT-A监测。视物变形的突然恶化是CNV发生的征兆,需要及时检查。
与全身疾病的关系
已有报道PIC与结节病合并存在;对于有多发性肺部病变的病例,应进行胸部CT、血清ACE和溶菌酶检查。也有报道与HLA-DR2和HLA-DRB1*15相关3)。
MFC(全葡萄膜炎伴多灶性脉络膜炎;MFCwP)与PIC属于同一疾病谱,但最大的鉴别点是伴有玻璃体炎和前房炎症7)。
特有的临床表现
治疗注意事项
MFC不易自然缓解,许多病例需要长期免疫调节治疗。单用类固醇不足时,可使用甲氨蝶呤(MTX)、硫唑嘌呤(AZA)或吗替麦考酚酯(MMF)。合并CNV时,抗VEGF治疗与免疫调节治疗的双向方法至关重要7, 8)。
鸟枪弹样病变好发于4060岁的中老年人(平均50多岁),女性略多(1.5:1)。在白人中更常见,是与HLA-A29关联最强的已知疾病之一(白人相对风险为50224倍)4)。
特征性眼底表现
特有的功能变化
日本患者的注意事项
日本人HLA-A29携带频率低,因此HLA-A29的诊断敏感性受限。诊断需重视SUN 2021分类标准中的临床所见(眼底散弹状病变、前房炎症轻微、玻璃体炎存在)10)。
长期并发症
蛇行状脉络膜炎是一种30~50岁(男性略多)的双侧慢性脉络膜炎,特征为从视乳头周围呈蛇行状扩展的地图状灰黄色病变。
特有的进展模式
最重要:与结核相关型(SLC)的鉴别
结核性蛇行样脉络膜炎(SLC)与蛇行状脉络膜炎在影像学表现上非常相似,但治疗原则根本不同:
| 鉴别点 | 蛇行状脉络膜炎 | 结核相关型(SLC) |
|---|---|---|
| 病变分布 | 视乳头周围、向心性 | 后极部至周边部、多发性 |
| IGRA/TST | 阴性 | 阳性 |
| 病变形态 | 地图状、连续性 | 多发不连续的小病灶常见 |
| 治疗 | 类固醇+免疫抑制剂 | 抗结核药物必不可少 |
由于使用免疫抑制剂会导致结核病显著恶化,因此治疗前的IGRA(QuantiFERON)检查绝对不能省略2)。
CNV合并(最高35%)的处理
蛇行状脉络膜炎中CNV合并率高达35%,累及中心凹时可导致不可逆的视力障碍。抗VEGF疗法(贝伐珠单抗、雷珠单抗)的玻璃体内注射有效18)。
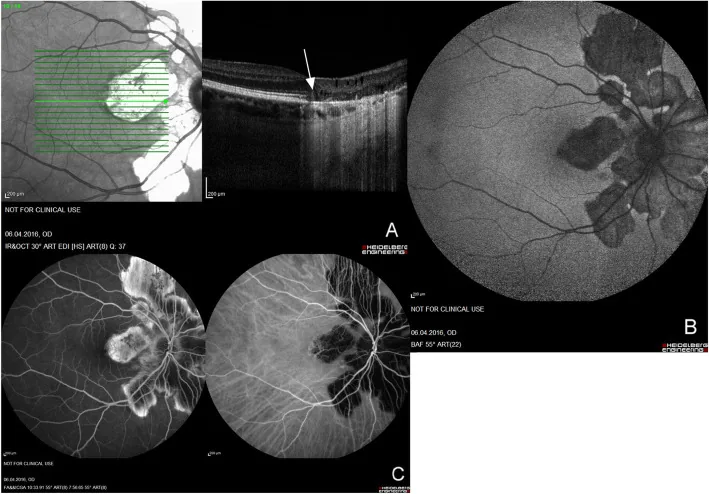
AZOOR 是 Gass 于 1992 年提出的疾病概念,是一种眼底基本正常但突然出现视力下降、视野缺损和闪光感的外层视网膜病变3)。
AZOOR 复合体的概念
Jampol 等人提出的 AZOOR 复合体概念将 MEWDS、AZOOR、PIC、MFC、AMN(急性黄斑神经视网膜病变)、AIBSE 和 AAOR 理解为具有共同遗传性自身免疫/炎症机制的连续体3)。
特有的临床表现
OCT和ERG是诊断关键
治疗与预后
AZOOR尚无确立的治疗方法。轻症病例仅需观察,但重症病例(视力下降或广泛视野缺损)需进行甲泼尼龙冲击疗法(1000 mg × 3天)后口服泼尼松龙2)。多数病例在6个月内稳定,但外层损伤残留部位的视野不会恢复。
明确了解每种影像学检查的作用对于准确诊断和评估白点综合征的活动性至关重要1, 5)。
| 检查方式 | 最强适应症/作用 |
|---|---|
| FA(荧光素眼底血管造影) | 评估视网膜血管、RPE和脉络膜毛细血管的渗漏。确认APMPPE的荧光逆转现象。确认MEWDS的花环样高荧光。评估血管炎(Birdshot)。 |
| ICGA(吲哚青绿血管造影) | 直接评估脉络膜循环障碍。比FA更早发现病变(尤其是Birdshot、APMPPE、匍行性)。发现比临床所见更广泛的病变(MEWDS、PIC)。对活动性病变的检测最敏感。 |
| FAF(眼底自发荧光) | RPE损伤的无创评估。活动性判断(APMPPE、匍行性)。MEWDS的诊断(早期白点处高自发荧光)。Birdshot的慢性化评估(视乳头周围低自发荧光73%) |
| OCT(光学相干断层扫描) | 椭圆体带评估(MEWDS、AZOOR的诊断性表现)。病变5阶段进展评估(PIC)。CNV、黄斑水肿的评估。预后预测(EZ消失→视力预后不良) |
| OCT-A | 脉络膜毛细血管血流空洞的无创检测(APMPPE、匍行性、PIC)。CNV的早期、灵敏检测(PIC、MFC中比FA更敏感)。Birdshot的脉络膜分层血流评估。治疗效果监测 |
| 多焦ERG / 全视野ERG | AZOOR的诊断(即使眼底基本正常,ERG振幅也降低)。Birdshot的活动性监测(30Hz闪烁延迟最敏感)。治疗效果评估。 |
怀疑MEWDS时
怀疑APMPPE时
当怀疑PIC/MFC时
怀疑蛇行状脉络膜炎时
ICGA 上白点综合征病变的低荧光是**脉络膜血流中断(脉络膜毛细血管闭塞)**的直接反映1)。ICGA 作为评估脉络膜循环的模态,比 FA 更敏感,具有以下特征:
ICGA相比FA和OCT-A在检测临床不可见的亚临床病变方面更具优势,尤其在MEWDS和PIC中,能显示比白点更广泛的脉络膜病变1, 15)。
FAF(眼底自发荧光)模式反映RPE的代谢状态,对白点综合征的诊断和活动性评估有用16)。
| FAF模式 | 疾病/分期 | 意义 |
|---|---|---|
| 高自发荧光(高AF) | MEWDS急性期、匍行性脉络膜炎活动边缘 | 光感受器变性产物(如A2E)在RPE中的积累 |
| 低自发荧光(低AF) | APMPPE瘢痕期、PIC活动病变、Birdshot视乳头周围 | RPE消失或功能丧失 |
| 中心低荧光伴周边高荧光晕 | 匍行性活动边缘、PIC | 活动边缘的RPE损伤模式 |
| 带状异常荧光 | AZOOR | 与感光细胞外层损伤分布一致 |
| 中心凹颗粒状高自发荧光 | MEWDS(近红外自发荧光) | 中心凹颗粒状改变的无创显示 |
在Birdshot病中,73%的患者可见视盘周围融合性低自发荧光,可作为慢性化的指标17)。
椭圆体带(EZ,原IS/OS线)的评估在白点综合征的活动性和预后预测中起核心作用1)。
| EZ 表现 | 疾病/分期 | 预后 |
|---|---|---|
| EZ 明显紊乱 → 恢复 | MEWDS 急性期 → 恢复期 | 良好(EZ 恢复与视力恢复相关) |
| EZ消失(与病变一致) | AZOOR活动期 | 消失部位无功能恢复 |
| EZ紊乱+外层视网膜高反射 | APMPPE急性期 | 恢复后部分萎缩残留 |
| RPE下高反射隆起+EZ断裂 | PIC/MFC(5阶段演变) | 合并CNV预后不良 |
| EZ消失(合并囊样黄斑水肿) | Birdshot进展期 | 视力预后不良的危险因素 |
OCT-A 上的 脉络膜毛细血管血流缺失 与 FA 和 ICGA 表现高度一致(在 APMPPE 和匍行性脉络膜炎中尤其有用)5, 13)。
| FA 模式 | 疾病 | 临床意义 |
|---|---|---|
| 早期低荧光 → 晚期高荧光(荧光逆转现象) | APMPPE | 脉络膜毛细血管缺血。早期充盈缺损 → 周围组织延迟染料渗漏。 |
| 早期花环状高荧光 | MEWDS | 直接反映RPE/感光细胞损伤。鉴别点:晚期不扩大 |
| 早期低荧光→晚期渗漏 | 活动性匍行性/MFC | 活动性脉络膜炎的证据 |
| 动脉早期高荧光→晚期渗漏 | PIC活动期 | 提示炎症性CNV |
| 血管渗漏+视盘高荧光(无渗漏) | Birdshot | 视网膜血管炎的直接证据 |
| 通常正常至轻微 | AZOOR | 特征为分离现象:FA阴性但存在视野缺损和ERG异常 |
白点综合征的治疗因疾病的自然病程、严重程度以及是否合并CNV而有很大差异。
APMPPE(重症、合并视乳头炎)· PIC(中心凹附近活动性病变)· AZOOR(重症病例)
鸟枪弹样视网膜脉络膜病变、匍行性脉络膜炎、MFC
鸟枪弹样(长期管理)
匐行性脉络膜炎(长期管理)
由于MFC呈慢性复发性病程,在激素减量后常需免疫调节药物作为维持治疗。
| 药物 | 剂量参考 | 备注 |
|---|---|---|
| 甲氨蝶呤(MTX) | 10~25 mg/周 | 联合叶酸1 mg/日。监测肝毒性。 |
| 硫唑嘌呤(AZA) | 1~3 mg/kg/日 | 建议检测TPMT活性。注意骨髓抑制。 |
| 吗替麦考酚酯(MMF) | 1~3克/日 | 消化系统症状是常见副作用 |
| 环孢素(CsA) | 3~5毫克/千克/日 | 必须监测肾功能和血压 |
| 阿达木单抗 | 40 mg/2周(皮下注射) | 难治性/激素依赖性病例。必须进行结核筛查。 |
CNV是影响视力预后的最重要并发症,在PIC、MFC和匐行性脉络膜炎中尤其常见。
| 疾病 | CNV合并率 | 治疗 |
|---|---|---|
| PIC | 40~76% | 抗VEGF玻璃体内注射(贝伐珠单抗、雷珠单抗、阿柏西普)+类固醇。OCTA PRN策略。 |
| MFC | 最高60% | 抗VEGF玻璃体内注射+免疫调节治疗 |
| 匐行性脉络膜炎 | 最高35% | 抗VEGF(贝伐珠单抗、雷珠单抗)玻璃体内注射 |
| MEWDS/APMPPE | 罕见 | 抗VEGF(确认合并CNV时) |
| Birdshot | 罕见 | 全身免疫抑制治疗+合并CNV时抗VEGF |
| 注意事项 | 相关疾病 |
|---|---|
| 优先排除结核(免疫抑制前) | 蛇行状脉络膜炎、MFC |
| 考虑HLA-A29(诊断) | 鸟枪弹样脉络膜视网膜病变(日本人敏感性低) |
| 类固醇植入物的眼压升高风险 | 鸟枪弹样脉络膜视网膜病变(最多40%需要小梁切除术) |
| 苯丁酸氮芥的骨髓抑制和恶性肿瘤风险 | 匍行性脉络膜炎(必须每周进行血液检查) |
| COVID-19感染或疫苗接种后复发 | PIC・MEWDS(有复发报告) |
| 合并脑血管炎时的紧急处理 | APMPPE(头痛、神经症状→紧急脑MRI) |
白点综合征的每种疾病都与特定的全身疾病或感染相关,治疗前进行系统的排除性检查很重要。
| 疾病 | 相关全身疾病/状态 | 临床意义 |
|---|---|---|
| APMPPE | 脑血管炎(MCAT)、链球菌感染、EB病毒 | 头痛、神经症状→紧急脑MRI |
| Birdshot | HLA-A29(白人80~98%)、类似结节病 | HLA检查辅助诊断(日本人敏感性低) |
| 匐行性脉络膜炎 | 结核(SLC)·HLA-B7/A2 | IGRA阳性→原则上先使用抗结核药物 |
| PIC | 结节病·HLA-DRB1*15 | 考虑胸部CT和ACE检测 |
| MFC | IL-10 单倍型、EB病毒、结节病 | 慢性复发者需重新评估全身检查 |
| MEWDS | COVID-19感染、疫苗接种后、HLA-B51 | SARS-CoV-2感染作为免疫触发因素 |
| AZOOR | 桥本病、多发性硬化症、自身免疫性疾病 | 考虑甲状腺功能和自身抗体检查 |
APMPPE 现与持续性斑块状黄斑病变(PPM)和顽固性斑块状脉络膜视网膜炎(RPC)一起被统称为“placoid chorioretinitis 谱系”。这三种疾病在 OCT-A 上均显示脉络膜毛细血管层血流缺失的共同模式,表明脉络膜毛细血管缺血是其共同的病理基础 5)。
Klufas 等人(2017)报告,在 APMPPE、PPM 和 RPC 中,OCT-A 检测脉络膜毛细血管层血流缺失与 FA 和 ICGA 具有高度一致性,支持了 placoid chorioretinitis 谱系的概念 5)。
中心凹颗粒状改变(foveal granularity)是 MEWDS 中 74%–96% 病例可见的诊断性表现,在白点消失后可能仍作为唯一体征存在。近红外 FAF(NIR-FAF)可显示特征性的中心凹颗粒状模式 9)。
PIC和MFC(MFCwP)具有共同的遗传背景(IL-10单倍型、HLA-DRB1*15),被认为是同一疾病谱的不同表型。主要鉴别点是玻璃体炎和前房炎症的有无以及病变分布区域1, 3)。
| 鉴别点 | PIC | MFC(MFCwP) |
|---|---|---|
| 玻璃体炎 | 无 | 有(重要鉴别点) |
| 前房炎症 | 无 | 轻度 |
| 病变分布 | 局限于后极部 | 后极部+中周边部 |
| 病变大小 | 100~300μm | 45~350μm |
| CNV合并率 | 40~76% | 最高60% |
Birdshot与HLA-A29的关联是已知所有疾病中最强的遗传关联之一,在白人患者中相对风险升高50~224倍4)。但日本人中HLA-A29携带者较少,因此诊断中HLA-A29阳性率的敏感性有限。应重视SUN 2021分类标准的临床所见项目(眼底所见、前房炎症轻微、玻璃体炎)进行诊断10)。
AZOOR被认为是在遗传易感性(如IL-10单倍型等)基础上,加上病毒感染、疫苗、药物等环境触发因素而发病,与MEWDS、PIC、AMN、AIBSE一起被理解为AZOOR复合体3)。COVID-19感染或疫苗接种后的MEWDS发病例在全球增加,提示SARS-CoV-2可能作为免疫触发因素发挥作用11)。