Tipo predominante de retina externa

Síndromes de puntos blancos
Puntos clave de un vistazo
Sección titulada «Puntos clave de un vistazo»1. ¿Qué son los síndromes de puntos blancos?
Sección titulada «1. ¿Qué son los síndromes de puntos blancos?»Los síndromes de puntos blancos, un concepto nombrado por Gass en 1977, se refieren a un grupo de enfermedades inflamatorias caracterizadas por múltiples lesiones puntiformes blancas o blanco-amarillentas en el fondo de ojo. Aunque la definición de las enfermedades objetivo varía entre investigadores, actualmente se utiliza ampliamente como un grupo de enfermedades inflamatorias idiopáticas no infecciosas que afectan principalmente la retina externa, el EPR, la coriocapilar y la coroides 1).
En las Guías de Práctica Clínica de Uveítis (Jpn J Ophthalmol 2019;123(6):635-696), APMPPE, MEWDS, PIC, coroiditis multifocal, retinochoroidopatía en perdigonada, coroiditis serpiginosa y AZOOR se enumeran como enfermedades independientes dentro de la clasificación de uveítis posterior, y cuando se utiliza el término inclusivo “síndromes de puntos blancos”, abarca estas enfermedades 2).
Conceptos de clasificación
Sección titulada «Conceptos de clasificación»Con los avances recientes en imágenes multimodales (incluyendo OCT-A), los síndromes de puntos blancos ahora se clasifican en los siguientes tres grupos según la capa principal de afectación1).
Tipo de capilar coroideo dominante
APMPPE, coroiditis serpiginosa, PIC
- La vasculitis oclusiva de la coriocapilar es central en la patología
- La OCT-A muestra ausencia de flujo en la coriocapilar
- Los cambios en la retina externa y el EPR son secundarios
Tipo de estroma coroideo dominante
Coriorretinopatía en perdigones
- La lesión primaria es la infiltración linfocítica del estroma coroideo
- OCT-A muestra vacío de flujo en la capa de Haller, con preservación inicial de la coriocapilar
- Curso crónico progresivo con fuerte asociación con HLA-A29
Además, se ha propuesto el concepto de complejo AZOOR, que integra MEWDS, AZOOR, PIC, MFC, AMN, AIBSE y AAOR como un continuo con una base genética autoinmune/inflamatoria común3).
Epidemiología en Japón
Sección titulada «Epidemiología en Japón»Según las estadísticas de la Sociedad Japonesa de Inflamación Ocular, la proporción de cada enfermedad del síndrome de puntos blancos en el total de uveítis es la siguiente2).
| Enfermedad | Proporción del total de uveítis |
|---|---|
| MEWDS | Aproximadamente 1–2% (informes nacionales) |
| APMPPE | Rara (sin estadísticas claras de incidencia anual) |
| PIC | Raro |
| Coroiditis serpiginosa | Aproximadamente 0.3% |
| Retinocoroidopatía en perdigonada | Raro (más común en caucásicos, extremadamente raro en Japón) |
| AZOOR | Raro (aumento de informes en los últimos años) |
2. Características clínicas comunes
Sección titulada «2. Características clínicas comunes»Aunque los síntomas varían según la enfermedad, las siguientes características clínicas son comunes en los síndromes de puntos blancos1, 2).
Patrones comunes de síntomas subjetivos
Sección titulada «Patrones comunes de síntomas subjetivos»- Disminución de la agudeza visual: varía de leve (MEWDS, AZOOR) a grave (coroiditis serpiginosa, PIC con CNV)
- Fotopsia: el síntoma más común que refleja daño en la retina externa/fotorreceptores
- Escotoma/defecto del campo visual: a menudo escotomas paracentrales o centrales correspondientes a la ubicación de la lesión
- Metamorfopsia: ocurre con lesiones maculares o CNV
Presencia de inflamación del segmento anterior
Sección titulada «Presencia de inflamación del segmento anterior»| Grupo de enfermedades | Inflamación de cámara anterior/vítreo |
|---|---|
| MEWDS, APMPPE, PIC | Generalmente ninguna (APMPPE puede tener leve) |
| MFC (MFCwP) | Inflamación de cámara anterior + vitritis presente (punto de diferenciación con PIC) |
| Birdshot | Inflamación de cámara anterior ausente a mínima, vitritis presente |
| Coroiditis serpiginosa | La inflamación de la cámara anterior y la vitritis suelen ser leves |
| AZOOR | Generalmente ninguna |
3. Enfoque del diagnóstico diferencial
Sección titulada «3. Enfoque del diagnóstico diferencial»Clasificación por edad, sexo, unilateral vs bilateral y recurrencia
Sección titulada «Clasificación por edad, sexo, unilateral vs bilateral y recurrencia»Mujer joven, unilateral, resolución espontánea
Mujeres jóvenes a mediana edad, bilateral, riesgo de CNV
Jóvenes a mediana edad, bilateral, inicio agudo
- Predomina en los 20–30 años (media 25 años), sin diferencia de sexo
- Bilateral, agudo, tendencia a la resolución espontánea
- Vigilar vasculitis cerebral (evaluación urgente si aparecen síntomas neurológicos)
Adultos mayores, bilateral, crónico progresivo
Birdshot・Coroiditis serpiginosa
- Birdshot: 40–60 años, ligeramente más frecuente en mujeres
- Serpiginosa: 30–50 años, ligeramente más frecuente en hombres
- Ambas enfermedades son crónicas, recurrentes y requieren inmunosupresión a largo plazo
- Tasa de positividad de HLA-A29 en Birdshot (caucásicos): 80–98%
Diagrama de flujo de diagnóstico diferencial
Sección titulada «Diagrama de flujo de diagnóstico diferencial»眼底に白点状病変 │ ├─ 片眼性? │ ├─ YES → MEWDS・AZOOR・AMN を考慮 │ │ ↳ FA で初期過蛍光 → MEWDS │ │ ↳ 眼底ほぼ正常・ERG 異常 → AZOOR │ └─ NO(両眼性) │ ├─ 急性発症・後極部大型白斑? │ └─ YES → APMPPE(FA 蛍光逆転現象を確認) │ ├─ 後極部小病変・近視女性・硝子体炎なし? │ └─ YES → PIC を考慮(CNV 検索:OCTA 必須) │ ├─ 小病変・硝子体炎あり・周辺部にも病変? │ └─ YES → MFC(MFCwP)を考慮 │ ├─ 乳頭周囲から蛇行状に進展・男性多め? │ └─ YES → 蛇行状脈絡膜炎(結核除外が最優先) │ └─ 後極部散弾状病変・中高年・HLA-A29? └─ YES → Birdshot 網脈絡膜症4. Comparación de las principales enfermedades
Sección titulada «4. Comparación de las principales enfermedades»Tabla comparativa principal: Matriz de 7 enfermedades
Sección titulada «Tabla comparativa principal: Matriz de 7 enfermedades»| Ítem | APMPPE | MEWDS | PIC | MFC (MFCwP) | Birdshot | Coroiditis serpiginosa | AZOOR |
|---|---|---|---|---|---|---|---|
| Edad típica de inicio | 20–30 años (promedio 25 años) | 20–50 años | 18–40 años (promedio 36 años) | Promedio 30 años | 40–60 años | 30–50 años | Principalmente mediados de los 30 |
| Sexo | Sin diferencia de sexo | Predominio femenino (1:4) | Predominio femenino (aproximadamente 90%) | Predominio femenino (más común en mujeres blancas) | Ligeramente más mujeres | Ligeramente más hombres | Predominio femenino (aproximadamente 75%) |
| Unilateral/Bilateral | Mayormente bilateral | Unilateral (≥95%) | Mayormente bilateral (80%) | Bilateral | Bilateral | Bilateral | Unilateral → progresión bilateral (finalmente 76% bilateral) |
| Síntomas principales | Disminución de la visión, escotoma central, metamorfopsia | Disminución de la visión, fotopsia, visión borrosa | Escotoma, disminución de la visión, metamorfopsia | Moscas volantes, disminución de la visión, fotopsia | Disminución de la visión, ceguera nocturna, anomalía de la visión cromática | Disminución de la visión, escotoma paracentral | Fotopsia, defecto del campo visual (fondo de ojo casi normal) |
| Características de las manchas blancas del fondo de ojo | Grandes manchas blancas cremosas en el polo posterior (1/4 a 1/2 del diámetro del disco) | Múltiples manchas pequeñas de color grisáceo pálido desde el polo posterior hasta el ecuador (100–200 μm) | Pequeñas manchas amarillentas en el polo posterior (100–300 μm), de 12 a 25 | Manchas grisáceas amarillentas desde el polo posterior hasta la periferia (45–350 μm), con vitritis | Manchas cremosas en perdigonada desde el polo posterior hasta el ecuador (1/4 a 1/2 del diámetro del disco) | Lesiones geográficas grisáceas amarillentas que se extienden tortuosamente desde la zona peripapilar | Fondo de ojo casi normal (fase aguda), atrofia de la capa externa en fase tardía |
| Hallazgos de OCT | Disrupción de la zona elipsoide + hiperreflectividad retiniana externa, atrofia parcial residual tras recuperación | Disrupción/desaparición marcada de la zona elipsoide (fase aguda) → recuperación | Elevación hiperreflectiva sub-RPE + rotura de EZ (evolución en 5 etapas) | Hiperreflectividad sub-RPE + rotura de EZ (similar a PIC) | Lesiones coroideas, edema macular quístico, desaparición de EZ como mal pronóstico | Fase activa: hiperreflectividad retiniana externa, líquido subretiniano. Fase cicatricial: atrofia del RPE | La desaparición de EZ (IS/OS) es el hallazgo más importante (corresponde al defecto del campo visual) |
| Hallazgos de FA | Hipofluorescencia temprana → hiperfluorescencia tardía (inversión de fluorescencia) | Hiperfluorescencia persistente en forma de corona desde la fase temprana | Activa: hiperfluorescencia arterial temprana → fuga tardía | Activa: hipofluorescencia temprana → fuga tardía | Hiperfluorescencia de la lesión (sin fuga) + fuga vascular e hiperfluorescencia del disco óptico | Activa: hipofluorescencia temprana → hiperfluorescencia tardía (fuga) | Generalmente normal o anomalías mínimas |
| Hallazgos de ICGA | Hipofluorescencia en todas las fases (refleja directamente isquemia de la coriocapilar) | Hipofluorescencia tardía (más extensa que los puntos blancos) | Hipofluorescencia en fase media, útil para detectar lesiones subclínicas | Hipofluorescencia temprana a todas las fases | Hipofluorescencia temprana/media → isofluorescencia tardía (inicial) → avanzada: hipofluorescencia en todas las fases | Hipofluorescencia en todas las fases (refleja trastorno circulatorio coroideo) | Normalmente normal |
| Hallazgos de FAF | Aguda: hipo o hiperautofluorescencia. Remisión: hipoautofluorescencia | Aguda: hiperautofluorescencia (múltiples puntos hiperfluorescentes). Tras recuperación: normalización | Activa: hipoautofluorescencia (hipoAF), halo marginal de hiperautofluorescencia | Activa: hipoautofluorescencia | Hipoautofluorescencia confluente peripapilar (observada en el 73%) | Activa: margen de hiperautofluorescencia + halo de hipoautofluorescencia. Inactiva: hipoautofluorescencia | Anomalías zonales de hiper a hipoautofluorescencia |
| Hallazgos de OCT-A | Vacío de flujo en coriocapilar (alta concordancia con FA/ICGA) | Coriocapilar generalmente preservado (vacío de flujo transitorio en algunos casos) | Vacío de flujo en coriocapilar (en sitios de lesiones inflamatorias) | Vacío de flujo en coriocapilar | Vacío de flujo en capa de Haller (temprano) → avanzado: vacío de flujo de espesor completo | Vacío de flujo en coriocapilar (grave) | Coriocapilar generalmente preservado |
| Recurrencia | Rara (básicamente episodio único) | Recurrencia en aproximadamente el 10% | Alta (crónica recurrente) | Alta (episodios inflamatorios recurrentes) | Alta (crónica con recaídas y remisiones repetidas) | Alta (se repite a intervalos de 3 meses a 4 años) | La mayoría se estabiliza en 6 meses; algunos progresan |
| Tasa de complicación de CNV | Rara | Rara | 40–76% (alto riesgo) | Hasta 60% | CNV subretiniana: Rara | Hasta 35% | Casi ninguna |
| Asociado a HLA | Ninguno | HLA-B51 (informes preliminares) | HLA-DR2, HLA-DRB1*15 | Asociación con haplotipo IL-10 | HLA-A29 (80-98% en caucásicos) | HLA-B7, HLA-A2 (asociaciones reportadas) | Ninguno (predisposición inmunológica) |
| Estrategia de tratamiento | Observación (resolución espontánea), grave: esteroides | Observación, grave: esteroides a corto plazo, CNV: anti-VEGF | Observación (sin CNV), CNV: anti-VEGF + esteroides, inmunosupresores | Esteroides + terapia inmunomoduladora, CNV: anti-VEGF | Esteroides + micofenolato de mofetilo / adalimumab (a largo plazo) | Esteroides + inmunosupresores (incluyentes agentes alquilantes), CNV: anti-VEGF | Observación, grave: pulso de esteroides |
| Pronóstico visual | Bueno (a menudo resolución espontánea) | Bueno (precaución por recurrencia y CNV) | Alto riesgo de mal pronóstico si se asocia a CNV | Riesgo de mal pronóstico por CNV y edema macular | Sin tratamiento, 16–22% tienen agudeza visual ≤0.1 a los 10 años | Irreversible si afecta la fóvea; hasta 25% de ojos tienen agudeza visual final <20/200 | Mayoría estable. Mal pronóstico en casos con daño progresivo de capas externas |
La coroiditis serpiginosa y la retinochoroidopatía en perdigonada tienen el peor pronóstico visual. En la coroiditis serpiginosa, hasta el 25% de los ojos tienen una agudeza visual final inferior a 20/200, y en la enfermedad en perdigonada, sin tratamiento, entre el 16% y el 22% de los pacientes tienen una agudeza visual de 0.1 o menos en 10 años2, 4). La PIC y la MFC tienen un mayor riesgo de mal pronóstico cuando se complican con CNV. La APMPPE y la MEWDS tienen una fuerte tendencia a la resolución espontánea y un buen pronóstico.
Características clínicas detalladas de cada enfermedad
Sección titulada «Características clínicas detalladas de cada enfermedad»APMPPE (Epiteliopatía pigmentaria placoidal multifocal posterior aguda)
Sección titulada «APMPPE (Epiteliopatía pigmentaria placoidal multifocal posterior aguda)»La APMPPE se presenta con frecuencia en personas de 20 a 30 años (promedio 25 años) sin predilección de género. Se cree que es causada por vasculitis oclusiva de las arteriolas aferentes de la coriocapilar, y se sospecha que las infecciones virales son desencadenantes1, 2).
Síntomas prodrómicos y evolución
- Aproximadamente la mitad de los pacientes presentan síntomas similares a los de un resfriado (influenza, virus de Epstein-Barr, varicela, infección estreptocócica, etc.)
- Múltiples manchas blancas discoides de color crema, de 1/4 a 1/2 del diámetro del disco óptico, aparecen en el polo posterior de ambos ojos
- Las manchas blancas comienzan a desaparecer desde el centro en unos pocos días y desaparecen después de 7 a 12 días, dejando una leve despigmentación
- Por lo general, un solo episodio se resuelve espontáneamente (la recurrencia es rara)
- El pronóstico visual generalmente es bueno, pero puede ser malo en casos graves o aquellos que progresan a coroiditis geográfica
Complicación específica: Vasculitis cerebral (MCAT)
La APMPPE complicada con vasculitis del sistema nervioso central (MCAT: trombosis arterial cerebral múltiple) es una complicación grave. Si aparecen cefalea, fiebre o síntomas neurológicos, se debe realizar una RM y ARM cerebral de emergencia. En casos con vasculitis cerebral, se requiere terapia de pulso con metilprednisolona y colaboración con neurología2).
Relación con el espectro de coriorretinitis placoides
La APMPPE, junto con la PPM (maculopatía placoides persistente) y la RPC (coriorretinitis placoides implacable), forma el “espectro de coriorretinitis placoides”, con isquemia de la capa coriocapilar como base patológica común5).
MEWDS (Síndrome de Puntos Blancos Evanescentes Múltiples)
Sección titulada «MEWDS (Síndrome de Puntos Blancos Evanescentes Múltiples)»El MEWDS afecta predominantemente a mujeres de 20 a 50 años (proporción hombre:mujer 1:4) y se caracteriza por aparición unilateral, aguda y resolución espontánea.
Características clínicas distintivas
- Múltiples manchas pequeñas de color blanco grisáceo pálido (100–200 μm) en la retina profunda hasta el nivel del EPR, desde el polo posterior hasta el ecuador
- Granularidad foveal: observada en el 74–96% de los pacientes, puede ser el único hallazgo residual después de que desaparezcan los puntos blancos. La FAF de infrarrojo cercano (NIR-FAF) muestra un patrón característico9)
- Apariencia de punto naranja: hallazgo característico en la fotografía de fondo de ojo y en la imagen de fondo de ojo con infrarrojo cercano
- Lesión de marfil: un cambio blanco tenue y borroso en el polo posterior del fondo de ojo
- Aproximadamente el 50% de los casos presentan síntomas prodrómicos similares a un resfriado
- La incidencia anual es de aproximadamente 0,22 por cada 100.000 personas, con recurrencia en el 10% de los casos
Hiperfluorescencia en forma de corona en la FA
La hiperfluorescencia característica en forma de corona desde la fase temprana de la FA es un punto clave para el diagnóstico de MEWDS. Las lesiones de puntos blancos muestran hiperfluorescencia desde la fase temprana de la FA y no se agrandan en la fase tardía. Esta hiperfluorescencia temprana es un importante rasgo distintivo de la hipofluorescencia temprana (fenómeno de inversión de fluorescencia) de la APMPPE1, 9).
Continuidad con el complejo AZOOR
MEWDS implica principalmente la destrucción transitoria de la zona elipsoide (línea IS/OS) de los fotorreceptores y se entiende como una enfermedad perteneciente al complejo AZOOR. La OCT puede confirmar la alteración o desaparición de la zona elipsoide en la fase aguda, que mejora con la recuperación visual3).
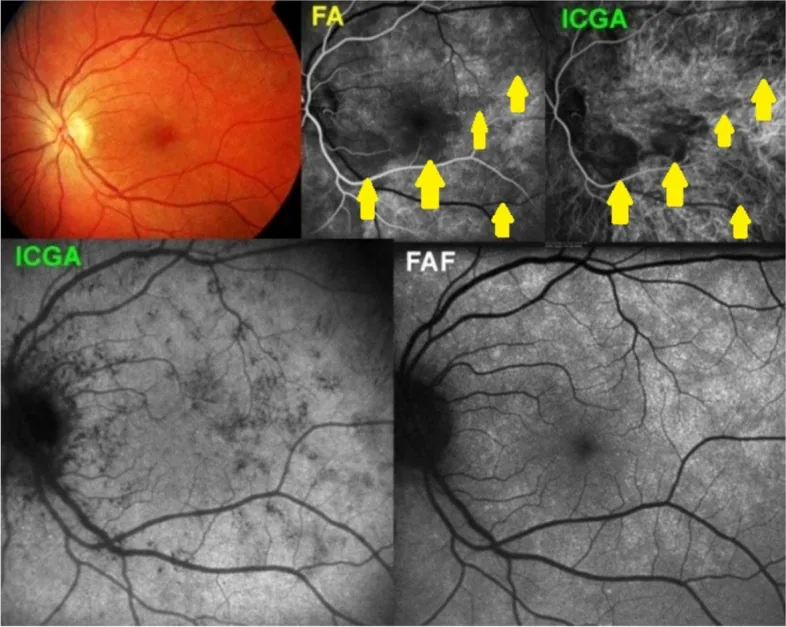
PIC (Coroidopatía Interna Punteada)
Sección titulada «PIC (Coroidopatía Interna Punteada)»La PIC ocurre predominantemente en mujeres jóvenes (aproximadamente 90%) de 18 a 40 años con miopía (promedio alrededor de -5 D).
Características clínicas distintivas
- Pequeñas manchas amarillentas de 100–300 μm limitadas al polo posterior, generalmente de 12 a 25
- Sin inflamación de cámara anterior ni vitritis (este es el punto de diferenciación más importante con MFC)
- Las lesiones activas se pueden observar en OCT como elevaciones hiperreflectivas debajo del EPR
- La cicatrización deja pequeñas lesiones atróficas
La complicación con CNV (40–76%) es el principal problema clínico
La complicación más importante de la PIC es la CNV, con tasas reportadas del 40–76%7, 8). La CNV es más probable que ocurra debido a los siguientes factores:
- Fragilidad de la membrana de Bruch debido al adelgazamiento coroideo miópico
- Ruptura de la membrana de Bruch debido a inflamación sub-RPE
- Aumento de la producción local de citocinas inflamatorias (p. ej., VEGF)
Se ha demostrado que la OCT-A es más sensible que la FA para la detección de CNV, y se recomienda la monitorización periódica con OCT-A. El empeoramiento repentino de la metamorfopsia es un signo de desarrollo de CNV y requiere una evaluación inmediata.
Asociación con enfermedades sistémicas
Se ha reportado la coexistencia de PIC y sarcoidosis; en casos con lesiones pulmonares múltiples, realizar TC de tórax, ACE sérico y pruebas de lisozima. También se ha reportado asociación con HLA-DR2 y HLA-DRB1*153).
MFC (Coroiditis Multifocal, MFCwP)
Sección titulada «MFC (Coroiditis Multifocal, MFCwP)»La MFC (coroiditis multifocal con panuveítis; MFCwP) está en el mismo espectro que la PIC, pero el punto clave de diferenciación es la presencia de vitritis e inflamación de la cámara anterior7).
Características clínicas distintivas
- Múltiples manchas gris-amarillentas de 45 a 350 μm aparecen no solo en el polo posterior sino también en la periferia media.
- Caracterizado por un curso crónico recurrente (episodios inflamatorios repetidos)
- Membrana epirretiniana (ERM) se asocia con frecuencia (hasta un 35%), afectando el pronóstico visual a largo plazo
- En algunos casos, la inflamación no se puede controlar sin terapia inmunosupresora
Consideraciones sobre el tratamiento
La MFC tiende a no resolverse espontáneamente, y muchos casos requieren terapia inmunomoduladora a largo plazo. Cuando los esteroides solos son insuficientes, se usan metotrexato (MTX), azatioprina (AZA) o micofenolato de mofetilo (MMF). Cuando hay CNV, es importante un enfoque bidireccional con terapia anti-VEGF e inmunomoduladora7, 8).
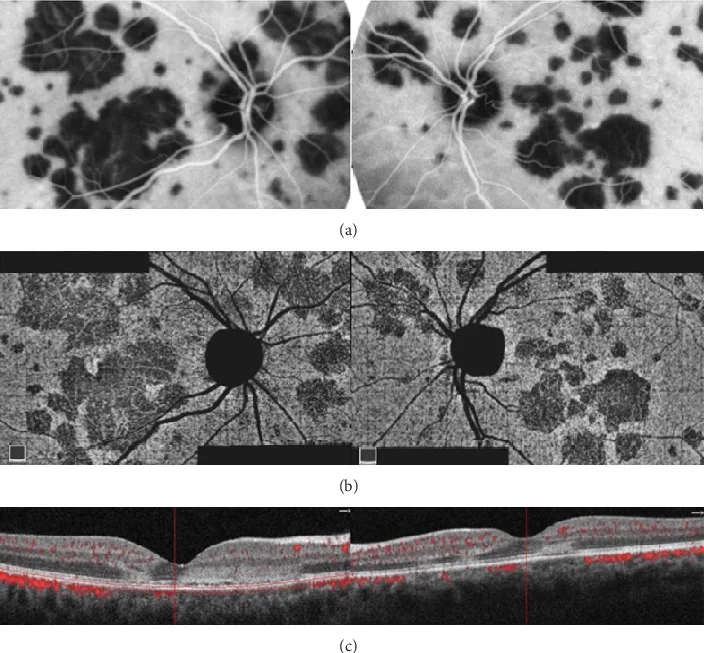
Coriorretinopatía en perdigonada (Retinocoroidopatía en perdigonada)
Sección titulada «Coriorretinopatía en perdigonada (Retinocoroidopatía en perdigonada)»La enfermedad en perdigonada ocurre típicamente en adultos de mediana edad y mayores de 40 a 60 años (promedio 50 años), con un ligero predominio femenino (1.5:1). Es más común en caucásicos y tiene una de las asociaciones genéticas más fuertes entre las enfermedades conocidas, vinculada al HLA-A29 (riesgo relativo 50–224 veces en caucásicos)4).
Hallazgos característicos del fondo de ojo
- Múltiples manchas color crema (1/4 a 1/2 del diámetro del disco óptico) que asemejan perdigones, distribuidas simétricamente desde el polo posterior hasta el ecuador
- Las manchas evolucionan a lesiones cicatriciales sin pigmentación
- Puede acompañarse de vasculitis retiniana e hinchazón del disco óptico
Cambios funcionales característicos
- Ceguera nocturna y anomalías de la visión cromática: Aparecen temprano y pueden preceder a la pérdida de agudeza visual
- ERG de campo completo de tipo negativo: Se observa temprano y la amplitud de la onda a disminuye a medida que la enfermedad progresa
- Retraso del ERG de parpadeo de 30 Hz: El indicador más sensible para monitorear la actividad; puede detectar anomalías antes que la pérdida de agudeza visual17)
Precauciones en pacientes japoneses
Debido a que la frecuencia de HLA-A29 es baja en los japoneses, la sensibilidad diagnóstica de HLA-A29 es limitada. El diagnóstico debe enfatizar los hallazgos clínicos de los criterios de clasificación SUN 2021 (lesiones de perdigonada en el fondo de ojo, inflamación mínima de la cámara anterior y presencia de vitritis)10).
Complicaciones a largo plazo
- Edema macular quístico (EMQ): causa principal de pérdida de visión
- Edema del disco óptico y atrofia óptica
- Con implantes de esteroides (fluocinolona), la elevación de la presión intraocular ocurre hasta en un 40% de los casos, requiriendo a veces trabeculectomía
Coroidopatía serpiginosa
Sección titulada «Coroidopatía serpiginosa»La coroidopatía serpiginosa es una coroiditis crónica bilateral que ocurre entre los 30 y 50 años (ligeramente más frecuente en hombres), caracterizada por lesiones geográficas de color gris-amarillo que se extienden en forma serpiginosa desde el área peripapilar.
Patrón de progresión característico
- Comienza centrípetamente desde el área peripapilar, con el margen de la lesión expandiéndose gradualmente en forma serpiginosa
- Fase activa: aparece un borde gris-blanquecino en el margen de la lesión
- Fase cicatricial: se fija como lesiones atróficas coriorretinianas
- Durante la recurrencia, la nueva inflamación siempre aparece desde el margen de la cicatriz existente (esto es característico)
- El intervalo de recurrencia varía mucho entre individuos, de 3 meses a 4 años.
Lo más importante: Diferenciación del tipo asociado a tuberculosis (SLC)
La coroiditis serpiginosa-like tuberculosa (SLC) se asemeja mucho a la coroidopatía serpiginosa en las imágenes, pero el enfoque del tratamiento es fundamentalmente diferente:
| Punto de diferenciación | Coroidopatía serpiginosa | Tipo asociado a tuberculosis (SLC) |
|---|---|---|
| Distribución de las lesiones | Peripapilar, centrípeta | Polo posterior a periferia, multifocal |
| IGRA/TST | Negativo | Positivo |
| Forma de la lesión | Geográfica, continua | Múltiples lesiones pequeñas discontinuas frecuentes |
| Tratamiento | Esteroides + inmunosupresores | Los fármacos antituberculosos son esenciales |
Dado que el uso de fármacos inmunosupresores puede empeorar notablemente la tuberculosis en la SLC, la prueba IGRA (QuantiFERON) antes del tratamiento es absolutamente indispensable2).
Manejo de la CNV (hasta un 35%)
En la coroidopatía serpiginosa, la CNV ocurre hasta en un 35% de los casos y puede causar pérdida irreversible de la visión si afecta la fóvea. La inyección intravítrea de terapia anti-VEGF (bevacizumab, ranibizumab) es efectiva18).
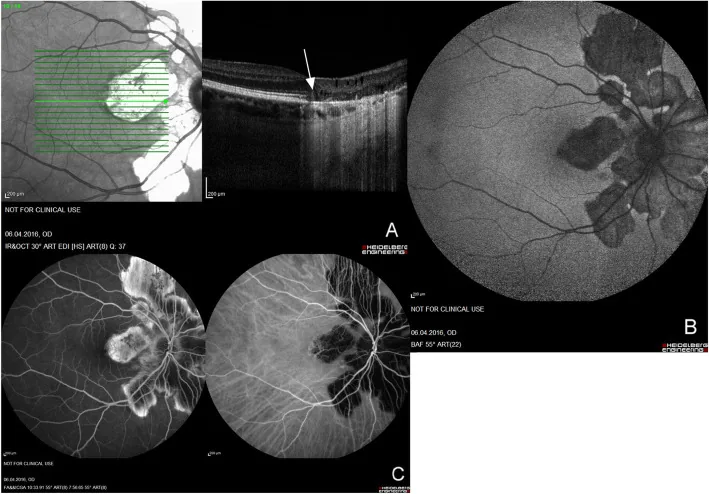
AZOOR (Retinopatía externa zonal oculta aguda)
Sección titulada «AZOOR (Retinopatía externa zonal oculta aguda)»AZOOR es un concepto de enfermedad propuesto por Gass en 1992. Es una retinopatía externa que causa pérdida repentina de la visión, defectos del campo visual y fotopsia a pesar de un fondo de ojo casi normal3).
Concepto del complejo AZOOR
El complejo AZOOR, propuesto por Jampol et al., es un concepto que entiende MEWDS, AZOOR, PIC, MFC, AMN (neuroretinopatía macular aguda), AIBSE y AAOR como un continuo con una base genética autoinmune/inflamatoria común3).
Características clínicas distintivas
- Ocurre con frecuencia en mujeres jóvenes de 20 a 50 años con miopía.
- Fotopsia (percepción de luz) aparece con frecuencia en la etapa inicial (especialmente luz en forma de banda o arco)
- Comienza unilateralmente y finalmente se vuelve bilateral en el 76% de los casos
- El fondo de ojo es casi normal en la fase aguda (caracterizado por la discrepancia entre la pérdida de agudeza visual y los hallazgos del fondo)
- Los defectos del campo visual muestran patrones irregulares en forma de banda (a menudo continuos con los puntos ciegos)
- Puede asociarse con enfermedades autoinmunes (enfermedad de Hashimoto, esclerosis múltiple)
La OCT y el ERG son clave para el diagnóstico
- El hallazgo más importante en la OCT es la desaparición o falta de claridad de la zona elipsoide (línea IS/OS).
- No se puede esperar recuperación funcional en las áreas donde la capa externa ha desaparecido en la OCT (también útil para el pronóstico).
- El ERG multifocal puede detectar una reducción de amplitud incluso cuando el fondo de ojo es normal (el ERG multifocal es más sensible que el ERG de campo completo).
- La FAF infrarroja puede delinear el borde entre la lesión y el área normal.
Tratamiento y pronóstico
No existe un tratamiento establecido para AZOOR. Los casos leves solo requieren observación, pero los casos graves (con disminución de la agudeza visual o defectos extensos del campo visual) se tratan con terapia de pulso de metilprednisolona (1,000 mg × 3 días) seguida de prednisolona oral2). La mayoría de los casos se estabilizan en 6 meses, pero los defectos del campo visual en áreas con daño residual de la capa externa no se recuperan.
Tanto la AZOOR como la neuritis óptica retrobulbar presentan fondo de ojo casi normal y disminución de la agudeza visual y del campo visual, por lo que es necesario diferenciarlas. Los puntos clave para la diferenciación son: ① En la AZOOR hay una reducción de la amplitud del ERG multifocal, mientras que en la neuritis óptica retrobulbar el ERG es normal; ② En la AZOOR los defectos del campo visual muestran un patrón irregular en banda o arco, mientras que en la neuritis óptica retrobulbar predominan los escotomas centrales; ③ En la AZOOR el RAPD suele ser leve, mientras que en la neuritis óptica retrobulbar se observa un RAPD marcado; ④ En la OCT, la AZOOR muestra pérdida de la zona elipsoide, mientras que la neuritis óptica retrobulbar muestra edema del disco óptico o adelgazamiento de la RNFL, lo que ayuda en la diferenciación2, 3).
5. Uso de pruebas de imagen
Sección titulada «5. Uso de pruebas de imagen»Asignación de roles por modalidad
Sección titulada «Asignación de roles por modalidad»Comprender claramente el papel de cada prueba de imagen es esencial para el diagnóstico preciso y la evaluación de la actividad de los síndromes de puntos blancos1, 5).
| Modalidad | Indicación/rol más fuerte |
|---|---|
| AFG (angiografía con fluoresceína) | Evaluación de la fuga de los vasos retinianos, EPR y coriocapilar. Confirmación del fenómeno de inversión de fluorescencia en APMPPE. Confirmación de hiperfluorescencia en forma de corona en MEWDS. Evaluación de vasculitis (Birdshot). |
| ICG (angiografía con verde de indocianina) | Evaluación directa de los trastornos de la circulación coroidea. Detección de lesiones más temprano que la AFG (especialmente Birdshot, APMPPE, serpiginosa). Detección de lesiones más extensas que los hallazgos clínicos (MEWDS, PIC). Más sensible para detectar lesiones activas. |
| FAF (Autofluorescencia de Fondo) | Evaluación no invasiva del daño del EPR. Determinación de actividad (APMPPE, serpiginosa). Diagnóstico de MEWDS (puntos blancos tempranos con hiperautofluorescencia). Evaluación de cronicidad en Birdshot (hipoautofluorescencia peripapilar 73%) |
| OCT (Tomografía de Coherencia Óptica) | Evaluación de la zona elipsoide (hallazgo diagnóstico en MEWDS, AZOOR). Evaluación de la evolución en 5 etapas de las lesiones (PIC). Evaluación de CNV y edema macular. Predicción pronóstica (pérdida de EZ → mal pronóstico visual) |
| OCT-A | Detección no invasiva de vacío de flujo en coriocapilar (APMPPE, serpiginosa, PIC). Detección temprana y sensible de CNV (mayor sensibilidad que FA en PIC, MFC). Evaluación del flujo sanguíneo coroideo por capas en Birdshot. Monitoreo del efecto del tratamiento |
| ERG multifocal / ERG de campo completo | Diagnóstico de AZOOR (disminución de la amplitud del ERG incluso con fondo de ojo casi normal). Monitoreo de actividad de Birdshot (el retraso del flicker de 30 Hz es el más sensible). Evaluación de la eficacia del tratamiento. |
Guía por enfermedad: “¿Qué prueba primero?”
Sección titulada «Guía por enfermedad: “¿Qué prueba primero?”»Cuando se sospecha MEWDS
Cuando se sospecha APMPPE
Cuando se sospecha PIC/MFC
Cuando se sospecha coroiditis serpiginosa
La estrategia difiere según la enfermedad. En la APMPPE y la coroiditis serpiginosa, la ICGA representa más directamente los trastornos de la circulación coroidea, por lo que realizar la ICGA simultáneamente o después de la FA profundiza la comprensión de la patología. En la MEWDS, la hiperfluencia en forma de corona de la FA es diagnósticamente importante. Sin embargo, dado que son pruebas invasivas, muchos hallazgos ahora pueden ser reemplazados por la OCT-A, y la combinación de FAF y OCT-A se utiliza para la evaluación inicial1, 5).
Significado de las lesiones hipofluorescentes en la ICGA
Sección titulada «Significado de las lesiones hipofluorescentes en la ICGA»La hipofluencia de las lesiones del síndrome de puntos blancos en la ICGA es un reflejo directo de la interrupción del flujo sanguíneo coroideo (oclusión de la coriocapilaris)1). La ICGA es más sensible que la FA para evaluar la circulación coroidea y tiene las siguientes características:
- Hipofluencia en todas las fases: Se observa en APMPPE, coroiditis serpiginosa, PIC y MFC. Refleja una oclusión grave de la isquemia de la coriocapilaris.
- Hipofluorescencia tardía (FA normal): La hipofluorescencia tardía en ICGA en MEWDS se explica por cambios en la captación de ICG debidos a una anomalía del EPR, no por afectación de la coriocapilar (la coriocapilar generalmente se conserva en OCT-A)1).
- Vacío de flujo en la capa de Haller → vacío de flujo de espesor completo en etapa avanzada: Un patrón de progresión en dos etapas característico de Birdshot, que comienza en el estroma coroideo y se extiende a la coriocapilar14).
La ICGA es superior a la FA y la OCT-A para detectar lesiones subclínicas clínicamente invisibles, y en particular en MEWDS y PIC, revela lesiones coroideas más extensas que los puntos blancos1, 15).
Mapa de enfermedades según el patrón de hipo e hiperautofluorescencia en FAF
Sección titulada «Mapa de enfermedades según el patrón de hipo e hiperautofluorescencia en FAF»Los patrones de FAF (autofluorescencia del fondo de ojo) reflejan el estado metabólico del EPR y son útiles para el diagnóstico de los síndromes de puntos blancos y la evaluación de la actividad de la enfermedad16).
| Patrón de FAF | Enfermedad/estadio | Significado |
|---|---|---|
| Alta autofluorescencia (hiper-AF) | Fase aguda de MEWDS, borde activo de Serpiginosa | Acumulación de productos de degeneración fotorreceptora (p. ej., A2E) en el EPR |
| Baja autofluorescencia (hipo-AF) | Fase cicatricial de APMPPE, lesión activa de PIC, peripapilar de Birdshot | Pérdida o disfunción del EPR |
| Hipo-AF central con halo hiper-AF periférico | Borde activo serpiginoso, PIC | Patrón de daño del EPR en el borde activo |
| AF anormal zonal | AZOOR | Corresponde a la distribución del daño de la capa externa de los fotorreceptores |
| Hiperautofluorescencia granular foveal | MEWDS (NIR-FAF) | Visualización no invasiva de la granularidad foveal |
En la enfermedad de Birdshot, se observa hipoautofluorescencia confluente peripapilar en el 73% de los casos, útil como indicador de cronicidad17).
Patrones de defecto de la zona elipsoide (EZ) en OCT
Sección titulada «Patrones de defecto de la zona elipsoide (EZ) en OCT»La evaluación de la zona elipsoide (EZ, anteriormente línea IS/OS) desempeña un papel central en la evaluación de la actividad y la predicción del pronóstico en los síndromes de puntos blancos1).
| Hallazgos de EZ | Enfermedad/etapa | Pronóstico |
|---|---|---|
| Alteración marcada de EZ → recuperación | MEWDS fase aguda → fase de recuperación | Bueno (la recuperación de EZ se relaciona con la recuperación de la agudeza visual) |
| Pérdida de EZ (correspondiente a la lesión) | Fase activa de AZOOR | Sin recuperación funcional en el área perdida |
| Alteración de EZ + hiperreflectividad retiniana externa | Fase aguda de APMPPE | Atrofia residual parcial después de la recuperación |
| Elevación hiperreflectiva sub-RPE + rotura de EZ | PIC/MFC (evolución en 5 etapas) | Mal pronóstico con complicación de CNV |
| Pérdida de EZ (con edema macular quístico) | Etapa avanzada de Birdshot | Factor de riesgo de mal pronóstico visual |
El vacío de flujo coriocapilar en OCT-A muestra una alta concordancia con los hallazgos de FA e ICGA (particularmente útil en APMPPE y coroiditis serpiginosa) 5, 13).
Patrones de fluorescencia en FA: retraso de llenado vs hiperfluorescencia vs fuga
Sección titulada «Patrones de fluorescencia en FA: retraso de llenado vs hiperfluorescencia vs fuga»| Patrón en FA | Enfermedad | Significado clínico |
|---|---|---|
| Hipofluorescencia temprana → hiperfluorescencia tardía (fenómeno de inversión de fluorescencia) | APMPPE | Isquemia coriocapilar. Defecto de llenado temprano → fuga tardía de colorante desde el tejido circundante. |
| Hiperfluencia temprana en forma de corona | MEWDS | Refleja directamente daño del EPR/fotorreceptores. Punto diferencial: no se expande en fase tardía |
| Hipofluencia temprana → fuga tardía | Serpiginoso/MFC activo | Evidencia de coroiditis activa |
| Hiperfluencia arterial temprana → fuga tardía | PIC activo | Sugiere CNV inflamatoria |
| Fuga vascular + hiperfluencia del disco óptico (sin fuga) | Birdshot | Evidencia directa de vasculitis retiniana |
| Normal a leve | AZOOR | Caracterizado por disociación: defectos del campo visual y anomalías en el ERG a pesar de FA negativa |
6. Tratamiento general
Sección titulada «6. Tratamiento general»Selección de la estrategia de tratamiento
Sección titulada «Selección de la estrategia de tratamiento»El tratamiento de los síndromes de puntos blancos varía considerablemente según la evolución natural de la enfermedad, la gravedad y la presencia de CNV.
Observación (sin necesidad de tratamiento) como principio
Sección titulada «Observación (sin necesidad de tratamiento) como principio»- Fuerte tendencia a la resolución espontánea; a menudo se recupera sin tratamiento específico2)
- MEWDS: los puntos blancos desaparecen y la visión se recupera en semanas. Esteroides orales solo en casos graves o con edema del disco óptico.
- APMPPE: las manchas blancas se resuelven en 7–12 días; el pronóstico visual suele ser bueno.
Enfermedades donde la terapia con esteroides es el pilar
Sección titulada «Enfermedades donde la terapia con esteroides es el pilar»APMPPE (casos graves, con papilitis) · PIC (lesiones foveales activas) · AZOOR (casos graves)
- Iniciar con prednisolona 30–60 mg/día y reducir gradualmente
- Si APMPPE se complica con vasculitis cerebral, se requiere pulsos de metilprednisolona y colaboración con neurología
- Criterios de gravedad para AZOOR: agudeza visual corregida en el ojo mejor < 0.3 (guía diagnóstica de la Sociedad Japonesa de Oftalmología)
Enfermedades que requieren terapia inmunosupresora a largo plazo
Sección titulada «Enfermedades que requieren terapia inmunosupresora a largo plazo»Coriorretinopatía en perdigonada, coroiditis serpiginosa, MFC
Perdigonada (manejo a largo plazo)
- Iniciar prednisolona 0.5–1 mg/kg/día
- Micofenolato de mofetilo (MMF) 2–3 g/día (inmunosupresor de primera línea)
- Metotrexato (MTX) 10–25 mg/semana
- Azatioprina (AZA) 1–3 mg/kg/día
- Casos refractarios: adalimumab (93,2% usado como agente biológico de primera línea)
- Sin tratamiento, 16–22% tienen agudeza visual ≤0,1 a los 10 años
Coroiditis serpiginosa (manejo a largo plazo)
- Prednisolona 40–80 mg/día inicial (reducción gradual)
- Azatioprina 1–2,5 mg/kg/día (terapia de mantenimiento de primera línea)
- Micofenolato de mofetilo / metotrexato (alternativas)
- Casos refractarios: clorambucilo (más potente; ≤0.2 mg/kg/día, análisis de sangre semanales obligatorios)
- Agentes biológicos: adalimumab (91.0% lo recomiendan como primera línea)
- Excluir tuberculosis (si IGRA positivo, iniciar tratamiento antituberculoso primero) antes de introducir inmunosupresores
Terapia inmunomoduladora para MFC
Sección titulada «Terapia inmunomoduladora para MFC»Dado que la MFC sigue un curso crónico recidivante, a menudo se necesitan fármacos inmunomoduladores como terapia de mantenimiento tras la reducción gradual de esteroides.
| Fármaco | Dosis orientativa | Notas |
|---|---|---|
| Metotrexato (MTX) | 10–25 mg/semana | Ácido fólico concomitante 1 mg/día. Monitorizar hepatotoxicidad. |
| Azatioprina (AZA) | 1–3 mg/kg/día | Se recomienda verificar actividad de TPMT. Vigilar mielosupresión. |
| Micofenolato de mofetilo (MMF) | 1–3 g/día | Los síntomas gastrointestinales son efectos secundarios comunes |
| Ciclosporina (CsA) | 3–5 mg/kg/día | Monitorización de la función renal y la presión arterial obligatoria |
| Adalimumab | 40 mg cada 2 semanas (inyección subcutánea) | Casos refractarios/dependientes de esteroides. Cribado de tuberculosis obligatorio. |
Manejo de la complicación por CNV
Sección titulada «Manejo de la complicación por CNV»La CNV es la complicación más importante que afecta el pronóstico visual y ocurre con especial frecuencia en PIC, MFC y coroiditis serpiginosa.
| Enfermedad | Tasa de complicación de CNV | Tratamiento |
|---|---|---|
| PIC | 40–76% | Inyección intravítrea anti-VEGF (bevacizumab, ranibizumab, aflibercept) + esteroides. Estrategia OCTA PRN. |
| MFC | Hasta un 60% | Inyección intravítrea anti-VEGF + terapia inmunomoduladora |
| Coroiditis serpiginosa | Hasta un 35% | Inyección intravítrea anti-VEGF (bevacizumab, ranibizumab) |
| MEWDS/APMPPE | Raro | Anti-VEGF (si se confirma CNV) |
| Birdshot | Raro | Inmunosupresión sistémica + anti-VEGF si hay CNV |
La CNV inflamatoria (iCNVM) difiere de la CNV en la degeneración macular relacionada con la edad; controlar la inflamación subyacente también es importante para prevenir la recurrencia de la CNV. Para PIC y MFC, se considera efectivo un enfoque bidireccional con anti-VEGF y esteroides (o inmunosupresores), y la monoterapia anti-VEGF deja un riesgo de recurrencia7, 8).
Precauciones en el tratamiento
Sección titulada «Precauciones en el tratamiento»| Precaución | Enfermedad relevante |
|---|---|
| Priorizar la exclusión de tuberculosis (antes de la inmunosupresión) | Coroiditis serpiginosa, MFC |
| Considerar HLA-A29 (diagnóstico) | Coroiditis en perdigones (baja sensibilidad en japoneses) |
| Riesgo de elevación de la presión intraocular con implantes de esteroides | Coroiditis en perdigones (hasta un 40% requiere trabeculectomía) |
| Riesgo de supresión de médula ósea y neoplasias malignas con clorambucilo | Coroiditis serpiginosa (análisis de sangre semanales obligatorios) |
| Reactivación tras infección o vacunación por COVID-19 | PIC・MEWDS (se ha reportado reactivación) |
| Manejo de emergencia cuando se complica con vasculitis cerebral | APMPPE (cefalea, síntomas neurológicos → resonancia magnética cerebral urgente) |
Las pruebas esenciales que se deben verificar antes de iniciar fármacos inmunosupresores para los síndromes de puntos blancos son las siguientes: ① Exclusión de tuberculosis mediante IGRA (QuantiFERON) (máxima prioridad en coroiditis serpiginosa), ② Cribado de hepatitis viral mediante antígeno HBs, anticuerpo HBc y anticuerpo HCV (para prevenir reactivación por inmunosupresión), ③ Radiografía de tórax/TC (para excluir tuberculosis y sarcoidosis), ④ Hemograma completo y pruebas de función hepática y renal (para confirmar valores basales). Para agentes biológicos como adalimumab, el cribado de tuberculosis también es obligatorio según el prospecto del medicamento 19, 20).
La CNV inflamatoria (iCNVM) difiere de la degeneración macular asociada a la edad en que la CNV puede regresar espontáneamente cuando se controla la inflamación. Generalmente se utiliza una estrategia PRN (pro re nata), administrando cada vez que se confirma CNV activa en OCT-A. Pueden administrarse dosis de carga inicial (3 inyecciones consecutivas), pero combinarla con terapia inmunosupresora puede reducir el número de administraciones necesarias. El anti-VEGF solo conlleva un alto riesgo de recurrencia, y es importante un enfoque bidireccional que aborde tanto el control de la inflamación subyacente como el anti-VEGF 7, 8).
6.5 Asociación con enfermedades sistémicas
Sección titulada «6.5 Asociación con enfermedades sistémicas»Cada enfermedad de los síndromes de puntos blancos se asocia con enfermedades sistémicas o infecciones específicas, y es importante realizar una búsqueda sistemática de exclusión antes del tratamiento.
| Enfermedad | Enfermedad/condición sistémica asociada | Significado clínico |
|---|---|---|
| APMPPE | Vasculitis cerebral (MCAT), infección estreptocócica, virus EB | Cefalea, síntomas neurológicos → RM cerebral urgente |
| Birdshot | HLA-A29 (80–98% en caucásicos), similar a sarcoidosis | Prueba de HLA ayuda al diagnóstico (baja sensibilidad en japoneses) |
| Coroiditis serpiginosa | Tuberculosis (SLC) · HLA-B7/A2 | IGRA positivo → Fármacos antituberculosos primero en principio |
| PIC | Sarcoidosis · HLA-DRB1*15 | Considerar TC de tórax y medición de ACE |
| MFC | Haplotipo IL-10, VEB, sarcoidosis | Reevaluar estudio sistémico en casos crónicos recurrentes |
| MEWDS | Infección por COVID-19, post-vacunación, HLA-B51 | La infección por SARS-CoV-2 actúa como desencadenante inmunitario |
| AZOOR | Enfermedad de Hashimoto, esclerosis múltiple, enfermedades autoinmunes | Considerar pruebas de función tiroidea y autoanticuerpos |
7. Notas especiales y hallazgos recientes para cada enfermedad
Sección titulada «7. Notas especiales y hallazgos recientes para cada enfermedad»APMPPE y el espectro de coriorretinitis placoides
Sección titulada «APMPPE y el espectro de coriorretinitis placoides»La APMPPE ahora se entiende como parte del “espectro de coriorretinitis placoides” junto con la maculopatía placoides persistente (PPM) y la coriorretinitis placoides implacable (RPC). En estas tres enfermedades, la OCT-A muestra un patrón común de vacío de flujo en la coriocapilar, lo que indica que la isquemia de la coriocapilar es una base patológica compartida 5).
Klufas et al. (2017) informaron que la OCT-A detecta el vacío de flujo de la coriocapilar con alta concordancia con la FA y la ICGA en APMPPE, PPM y RPC, apoyando el concepto del espectro de coriorretinitis placoides 5).
MEWDS y granularidad foveal
Sección titulada «MEWDS y granularidad foveal»La granularidad foveal es un hallazgo diagnóstico presente en el 74–96% de los casos de MEWDS y puede permanecer como el único signo después de que desaparecen los puntos blancos. La FAF de infrarrojo cercano (NIR-FAF) revela un patrón granular foveal característico 9).
Espectro de enfermedades de PIC y MFC
Sección titulada «Espectro de enfermedades de PIC y MFC»PIC y MFC (MFCwP) comparten un trasfondo genético común (haplotipo IL-10, HLA-DRB1*15) y se consideran diferentes fenotipos del mismo espectro de enfermedad. Los principales puntos de diferenciación son la presencia o ausencia de vitritis e inflamación de la cámara anterior, así como la distribución de las lesiones1, 3).
| Punto de diferenciación | PIC | MFC (MFCwP) |
|---|---|---|
| Vitritis | Ausente | Presente (punto de diferenciación importante) |
| Inflamación de la cámara anterior | Ninguna | Leve |
| Distribución de las lesiones | Limitado al polo posterior | Polo posterior + periferia media |
| Tamaño de la lesión | 100–300 μm | 45–350 μm |
| Tasa de complicación de CNV | 40–76% | Hasta 60% |
Birdshot y HLA-A29
Sección titulada «Birdshot y HLA-A29»La asociación entre Birdshot y HLA-A29 es una de las asociaciones genéticas más fuertes de todas las enfermedades conocidas, con un riesgo relativo de 50 a 224 veces en pacientes blancos4). Sin embargo, dado que los portadores de HLA-A29 son raros en japoneses, la sensibilidad de la positividad de HLA-A29 en el diagnóstico es limitada. El diagnóstico debe enfatizar los hallazgos clínicos de los criterios de clasificación SUN 2021 (hallazgos de fondo de ojo, inflamación mínima de la cámara anterior, vitritis)10).
Complejo AZOOR y desencadenantes virales
Sección titulada «Complejo AZOOR y desencadenantes virales»Se cree que AZOOR se desarrolla cuando se añaden desencadenantes ambientales como infección viral, vacunación o fármacos a una predisposición genética (p. ej., haplotipos de IL-10), y se entiende como parte del complejo AZOOR junto con MEWDS, PIC, AMN y AIBSE3). Los casos de MEWDS tras infección por COVID-19 o vacunación han aumentado en todo el mundo, lo que sugiere que el SARS-CoV-2 puede actuar como desencadenante inmunitario11).
Sí. Se han reportado múltiples casos de inicio o recurrencia de MEWDS, PIC y coroiditis serpiginosa después de la infección por COVID-19, lo que sugiere que la infección por SARS-CoV-2 podría actuar como un desencadenante inmunológico11, 12). Para MEWDS, una revisión sistemática de 27 casos después de la vacunación contra COVID-19 encontró que las vacunas de ARNm (Pfizer-BioNTech) fueron las más comunes. Los pacientes con antecedentes de estas afecciones deben consultar a un oftalmólogo sobre el seguimiento antes y después de la vacunación.
El orden de prioridad recomendado para las pruebas iniciales cuando se sospecha un síndrome de puntos blancos es el siguiente: ① FAF + OCT (no invasivo, permite la evaluación inicial de casi todas las enfermedades; puede detectar alta autofluorescencia en MEWDS, evaluación de la zona elipsoide y elevación del EPR en PIC) → ② OCT-A (detección temprana de CNV, evaluación del vacío de flujo de la coriocapilar) → ③ FA + ICGA (para diagnóstico definitivo y evaluación de actividad cuando sea necesario). Si se sospecha coroiditis serpiginosa, se debe priorizar IGRA (para descartar tuberculosis) antes de la FA. Ante la sospecha de AZOOR, el ERG (ERG multifocal) es esencial1, 2).
8. Artículos relacionados
Sección titulada «8. Artículos relacionados»9. Referencias
Sección titulada «9. Referencias»- Testi I, Modugno RL, Pavesio C. Multimodal imaging supporting the pathophysiology of white dot syndromes. J Ophthalmic Inflamm Infect. 2021;11:32.
- 日本眼炎症学会・日本眼科学会. ぶどう膜炎診療ガイドライン(13〜18節:APMPPE・MEWDS・PIC・多発性脈絡膜炎・バードショット・蛇行状脈絡膜炎・AZOOR). 日本眼科学会雑誌. 2019;123(6):635-696.
- Jampol LM, Becker KG. White spot syndromes of the retina: a hypothesis based on the common genetic hypothesis of autoimmune/inflammatory disease. Am J Ophthalmol. 2003;135(3):376-379.
- Agrawal R, et al. The role of HLA-A29 in birdshot chorioretinopathy and immune checkpoint inhibitor-related uveitis. Am J Ophthalmol. 2025. doi:10.1016/j.ajo.2024.01.007
- Klufas MA, Phasukkijwatana N, Iafe NA, et al. Optical coherence tomography angiography reveals choriocapillaris flow reduction in placoid chorioretinitis. Ophthalmol Retina. 2017;1(1):77-91.
- Stattin M, Forster J, Ahmed D, Krepler K, Ansari-Shahrezaei S. Swept Source-Optical Coherence Tomography Angiography for Management of Secondary Choroidal Neovascularization in Punctate Inner Choroidopathy. Case Rep Ophthalmol. 2021;12:232-238.
- Spaide RF, Goldberg N, Freund KB. Redefining multifocal choroiditis and panuveitis and punctate inner choroidopathy through multimodal imaging. Retina. 2013;33(7):1315-1324.
- Leclaire MD, Clemens CR, Eter N, Mihailovic N. Choroidale Neovaskularisation infolge einer “punctate inner choroidopathy”, dargestellt mittels optischer Kohärenztomographie-Angiographie. Ophthalmologe. 2021;118:842-846.
- Mantovani A, Invernizzi A, Staurenghi G, Herbort CP Jr. Multiple evanescent white dot syndrome: a multimodal imaging study of foveal granularity. Ocul Immunol Inflamm. 2019;27(1):141-147.
- Standardization of Uveitis Nomenclature (SUN) Working Group. Classification criteria for birdshot chorioretinitis. Am J Ophthalmol. 2021;228:65-71.
- Chen N, Mandell M, Arjmand P. Multimodal imaging findings of multiple evanescent white dot syndrome in COVID-19 patients. IDCases. 2024;38:e02110.
- Seddigh S, Pinto A, Zaki AM, Gupta RR. Serpiginous choroiditis after COVID-19 infection. J Vitreoretinal Dis. 2025;9(2):246-252.
- Pakzad-Vaezi K, Khaksari K, Chu Z, Van Gelder RN, Wang RK, Pepple KL. Swept-source OCT angiography of serpiginous choroiditis. Ophthalmol Retina. 2018;2(7):712-719.
- Pepple KL, Chu Z, Weinstein J, Munk MR, Van Gelder RN, Wang RK. Use of en face swept-source optical coherence tomography angiography in identifying choroidal flow voids in 3 patients with birdshot chorioretinopathy. JAMA Ophthalmol. 2018;136(11):1288-1292. doi:10.1001/jamaophthalmol.2018.3474. PMID:30128478. PMCID:PMC6248174
- Khochtali S, Dridi T, Abroug N, et al. Swept-source optical coherence tomography angiography shows choriocapillaris flow reduction in multiple evanescent white dot syndrome. J Curr Ophthalmol. 2020;32(2):211-215.
- Yeh S, Forooghian F, Wong WT, et al. Fundus autofluorescence imaging of the white dot syndromes. Arch Ophthalmol. 2010;128(1):46-56.
- Minos E, Barry RJ, Southworth S, et al. Birdshot chorioretinopathy: current knowledge and new concepts in pathophysiology, diagnosis, monitoring and treatment. Orphanet J Rare Dis. 2016;11(1):61.
- Maleki A, Maldonado Cerda A, Garcia CM, et al. Chlorambucil combination therapy in refractory serpiginous choroiditis: a cure? Am J Ophthalmol Case Rep. 2021;21:101014.
- Niederer RL, Al-Janabi A, Engelbrecht C, et al. Immunomodulatory therapy prescribing practices for non-infectious uveitis: a survey of international experts. Br J Ophthalmol. 2024;108:482-489.
- Tomkins-Netzer O, et al. Treatment of non-infectious uveitis with biologics: a survey of the International Ocular Inflammation Society. Br J Ophthalmol. 2022;106:482-488.
