Neuropatía óptica isquémica anterior no arterítica (NAION)

Neuropatía óptica
1. ¿Qué es la neuropatía óptica?
Sección titulada «1. ¿Qué es la neuropatía óptica?»La neuropatía óptica es un término general para un grupo de enfermedades en las que se produce algún daño en el nervio óptico, lo que lleva a una disminución de la función visual. Se presenta con uno o más de los siguientes: disminución de la agudeza visual, defectos del campo visual, anomalías de la visión cromática y reducción de la sensibilidad al contraste 2).
El nervio óptico está compuesto por aproximadamente 1.2 millones de axones de células ganglionares de la retina (CGR). Dentro del ojo, se agrupan como el disco óptico, pasan a través del canal óptico y llegan al quiasma óptico. El daño desde el disco óptico hasta la parte anterior del quiasma se denomina “trastorno de la vía visual anterior”, y la mayoría de las neuropatías ópticas clínicamente significativas corresponden a esta región 2). El daño más allá del quiasma (cintilla óptica, radiación óptica, lóbulo occipital) se denomina “trastorno de la vía visual posterior” y se trata como un trastorno de la vía visual, no como una neuropatía óptica.
El nervio óptico se divide en cuatro segmentos. El segmento intraocular (disco óptico, aproximadamente 1 mm) es propenso a neuropatías ópticas isquémicas e inflamatorias. El segmento intraorbitario (aproximadamente 25 mm) a menudo se ve afectado por condiciones compresivas e inflamatorias. El segmento intracanalicular (canal óptico, aproximadamente 5–8 mm) es susceptible a compresión traumática y ósea. El segmento intracraneal (aproximadamente 10 mm) es frecuentemente comprimido por adenomas hipofisarios y craneofaringiomas. También es importante distinguir entre “neuropatía óptica anterior”, donde el disco óptico se puede observar directamente, y “neuropatía óptica retrobulbar”, donde el fondo de ojo parece normal. En la neuropatía óptica retrobulbar, la ausencia de cambios en el disco hace que sea fácil pasarla por alto como causa de pérdida de visión.
El flujo sanguíneo al disco óptico es proporcionado principalmente por las arterias ciliares posteriores cortas (arterias SPC). Las arterias SPC son ramas terminales de la arteria oftálmica y suministran sangre a las regiones prelaminar, laminar y retrolaminar del disco óptico. Las alteraciones circulatorias en esta área son la base patológica principal de la NAION y la AAION 3). El interior del nervio óptico está protegido por la barrera hematoencefálica, pero este mecanismo de protección se rompe en la neuritis óptica inflamatoria y las enfermedades autoinmunes 2).
Vía Patológica Común y Atrofia Óptica
Sección titulada «Vía Patológica Común y Atrofia Óptica»Independientemente de la causa, la vía final común implica daño a las células ganglionares de la retina y los axones del nervio óptico, seguido de apoptosis y finalmente atrofia óptica. La atrofia óptica es la etapa terminal de la neuropatía óptica y se reconoce como palidez del disco óptico. Una vez establecida la atrofia, la recuperación de la función visual es severamente limitada 2).
Los axones del nervio óptico son una mezcla de fibras mielinizadas y amielínicas con diámetros de 0.2–10 μm, clasificadas ampliamente en células P (responsables de la luminancia y el contraste) y células M (responsables del movimiento y el contorno). En las neuropatías ópticas, las células P, que tienen un alto consumo de ATP, son más susceptibles al daño, lo que se relaciona con el mecanismo del escotoma central en las neuropatías ópticas tóxicas y nutricionales 2).
Resumen de Epidemiología
Sección titulada «Resumen de Epidemiología»Se resumen las tasas de incidencia anual de las principales neuropatías ópticas (por cada 100,000 adultos). La NAION es la más común, con tasas de 2.3 a 10.2 en Estados Unidos3). La neuritis óptica idiopática tiene una incidencia de 1.6 en adultos japoneses13), y la LHON (neuropatía óptica hereditaria de Leber) tiene aproximadamente 117 casos nuevos por año en Japón (encuesta de 2014), considerándose una enfermedad rara14). La incidencia anual estimada de AAION/GCA es de 0.36 por cada 100,000 en personas mayores de 50 años, y es más común en caucásicos del norte de Europa (aproximadamente 30 por cada 100,000 en Noruega). Las complicaciones visuales de la GCA ocurren en el 10–30% (hasta un 70% en algunos informes), y la AAION representa el 60–90% de estas1). La incidencia anual de MOGAD se estima en 1.6 a 4.8 por cada 1,000,0006).
Clasificación de las Neuropatías Ópticas
Sección titulada «Clasificación de las Neuropatías Ópticas»Las neuropatías ópticas se pueden clasificar desde múltiples perspectivas. La clasificación más útil clínicamente se muestra a continuación.
Clasificación según el patrón de inicio
- Agudo (horas a días): NAION, AAION, traumática
- Subagudo (días a semanas): Neuritis óptica idiopática, LHON, compresivo (algunos)
- Crónico (meses a años): ADOA, compresivo crónico, radioterapia (tardío)
Clasificación por causa
- Isquémico: NAION, AAION, PION
- Inflamatorio (neuritis óptica): Idiopática, relacionada con EM, relacionada con NMOSD, relacionada con MOGAD, infecciosa
- Compresivo: Tumor, quiste, aneurisma, oftalmopatía tiroidea
- Tóxico: etambutol, amiodarona, alcohol, etc.
- Nutricional: deficiencia de vitamina B12/B1/folato/cobre
- Hereditario: LHON, ADOA, síndrome de Wolfram
- Traumático: fractura del conducto óptico, lesión directa
- Por radiación: degeneración isquémica tardía
Clasificación por localización
- Neuropatía óptica anterior (con cambios en el disco): NAION, AAION, neuritis óptica anterior
- Neuropatía óptica retrobulbar (disco normal): tóxica, hereditaria, neuritis óptica relacionada con EM (la mayoría)
- Lesiones quiasmáticas: adenoma hipofisario, craneofaringioma (hemianopsia bitemporal)
Marco diagnóstico de la neuropatía óptica
Sección titulada «Marco diagnóstico de la neuropatía óptica»El diagnóstico de la neuropatía óptica se realiza en cinco pasos.
Paso 1: Confirmar la disfunción del nervio óptico Confirme objetivamente la disfunción del nervio óptico mediante RAPD, agudeza visual, visión cromática y campo visual.
Paso 2: Localización de la lesión Anterior (con cambios en el disco óptico) o retrobulbar (disco óptico normal), intraorbitario, intracanalicular o intracraneal. Estimar la localización según el patrón de defecto del campo visual.
Paso 3: Unilateral o bilateral, agudo o crónico Esto permite reducir significativamente el diagnóstico diferencial.
Paso 4: Exclusión de tipos peligrosos Priorizar la exclusión de GCA (VSG, PCR), compresivo (RM) e infeccioso (sífilis, hongos).
Paso 5: Pruebas específicas Agregar anticuerpos anti-AQP4, anticuerpos anti-MOG, prueba de mtDNA y pruebas nutricionales según el tipo.
2. Diferencias con la neuritis óptica (aclaración conceptual)
Sección titulada «2. Diferencias con la neuritis óptica (aclaración conceptual)»La “neuritis óptica” y la “neuropatía óptica” a menudo se confunden en la práctica clínica, pero tienen una relación de concepto subordinado y superordinado.
Confundir neuropatías ópticas no inflamatorias (isquémica, compresiva, tóxica, hereditaria) con neuritis óptica puede llevar a la administración errónea de esteroides. En particular, la aspergilosis invasiva contraindica los esteroides 2), y administrar esteroides en la fase aguda de LHON no solo es ineficaz, sino que retrasa el diagnóstico definitivo.
Principales características clínicas de la neuritis óptica
Sección titulada «Principales características clínicas de la neuritis óptica»La neuritis óptica (inflamatoria) tiene las siguientes características que ayudan a diferenciarla de las causas no inflamatorias.
- Inicio agudo: progresa en días a 2 semanas, luego muestra tendencia a recuperarse en 5 semanas.
- Dolor con el movimiento ocular: presente en aproximadamente el 50% de los casos. Generalmente ausente en causas isquémicas, compresivas o tóxicas.
- Edad típica: 15–45 años (la isquémica suele ser mayor de 50 años).
- Hallazgos en RM: realce típico del nervio óptico (T1 con gadolinio).
- Recuperación espontánea: en casos idiopáticos o relacionados con EM, más del 90% recupera una agudeza visual de 0.5 o mejor después de 1 año (estudio ONTT)4).
- Riesgo de conversión a EM: 15 años después del primer episodio, el 25% sin lesiones en RM cerebral y el 78% con lesiones progresan a EM4).
Situaciones en las que el diagnóstico diferencial es difícil
Sección titulada «Situaciones en las que el diagnóstico diferencial es difícil»A continuación, se vuelve difícil diferenciar entre neuritis óptica y neuropatía óptica no inflamatoria.
- Pérdida visual unilateral aguda en mujeres mayores de 50 años: NAION vs. neuritis óptica con anticuerpos AQP4 positivos (NMOSD)
- Pérdida visual bilateral aguda en adultos jóvenes: LHON vs. neuritis óptica bilateral simultánea vs. neuropatía óptica tóxica
- Pérdida visual unilateral con edema de papila: NAION vs. neuritis óptica anterior vs. vasculitis papilar
La neuritis óptica con anticuerpos AQP4 positivos representa aproximadamente el 10% de las neuritis ópticas idiopáticas, es una enfermedad refractaria resistente a los esteroides, con una edad de inicio más avanzada que la neuritis óptica típica y predominio femenino (proporción mujer:hombre 9:1) 5). El anticuerpo AQP4 se dirige a los canales de acuaporina 4 expresados en los astrocitos del nervio óptico, causando citotoxicidad dependiente del complemento 5). Dado que las estrategias de tratamiento difieren fundamentalmente entre los casos positivos y negativos para anticuerpos AQP4, se debe solicitar la prueba de anticuerpos antes de la pulsoterapia con esteroides. El método de ensayo basado en células (CBA) tiene mayor sensibilidad y especificidad que el ELISA y se recomienda su uso 5).
Antes de realizar la pulsoterapia con esteroides en la neuritis óptica, se deben descartar infecciones (hepatitis B, sífilis, VIH, hongos) 2). La administración de altas dosis de esteroides en portadores del virus de la hepatitis B puede causar hepatitis fulminante. En la neuritis óptica sifilítica, se deben priorizar los antibióticos sobre los esteroides.
3. Formas de alta urgencia
Sección titulada «3. Formas de alta urgencia»La siguiente tabla muestra los tipos de neuropatía óptica que requieren manejo urgente.
| Forma | Urgencia | Consecuencias si se pasa por alto |
|---|---|---|
| Neuropatía óptica isquémica anterior arterítica (AAION/GCA) | Muy urgente | Ceguera del ojo contralateral (65% la desarrollan en 10 días sin tratamiento) 1) |
| Neuropatía óptica compresiva aguda (tumor, quiste, hematoma) | Urgente | Atrofia óptica progresiva y pérdida irreversible de la visión |
| Neuropatía óptica nasal (aspergilosis invasiva) | Emergencia | Mortalidad reportada del 94%2) |
| Neuropatía óptica traumática (fractura del conducto óptico) | Emergencia | El tratamiento temprano puede preservar la función visual |
| Neuropatía óptica isquémica posterior (PION) | Emergencia | Ocurre después de cirugía o pérdida masiva de sangre; a menudo irreversible |
Flujo de respuesta de emergencia para GCA
Sección titulada «Flujo de respuesta de emergencia para GCA»La amaurosis fugax aparece como síntoma prodrómico en aproximadamente el 30% de los casos de pérdida visual permanente, ocurriendo en promedio 8.5 días antes 1). En este punto, es extremadamente importante sospechar GCA e iniciar esteroides de forma proactiva como prevención secundaria.
4. Punto de entrada para el diagnóstico diferencial
Sección titulada «4. Punto de entrada para el diagnóstico diferencial»El diagnóstico diferencial de la neuropatía óptica se organiza sistemáticamente en cuatro ejes: agudo vs. crónico, unilateral vs. bilateral, presencia o ausencia de dolor, y hallazgos en el disco óptico.
Agudo vs. Crónico
Sección titulada «Agudo vs. Crónico»Agudo (alcanza el déficit máximo en horas a días)
- NAION: típicamente se presenta con pérdida repentina de la visión al despertar
- AAION: pérdida visual unilateral rápida, grave (visión <20/200 en >60%) 1)
- Traumático: inmediatamente o dentro de horas después del traumatismo
Subagudo (días a semanas)
- Neuritis óptica idiopática: progresa durante 2 semanas, luego comienza la recuperación
- LHON: Pérdida visual subaguda indolora unilateral, que se vuelve bilateral en semanas a meses
- Compresivo: Puede progresar subagudamente por crecimiento tumoral rápido o hemorragia
Crónico (progresión lenta durante meses a años)
- ADOA (atrofia óptica autosómica dominante): Progresión lenta bilateral de inicio en edad escolar
- Compresivo crónico: Debido a adenoma hipofisario, tumor orbitario, etc.
- Tóxico/nutricional: Progresión subaguda a crónica por exposición prolongada o desnutrición
Un ojo o ambos ojos
Sección titulada «Un ojo o ambos ojos»Enfermedades que tienden a ser unilaterales
- NAION: Generalmente unilateral (la aparición bilateral simultánea es extremadamente rara)
- AAION: Comienza unilateralmente; sin tratamiento, el 65% se extiende al ojo contralateral en 10 días1)
- Neuritis óptica idiopática / relacionada con EM: Típicamente unilateral
- Compresiva, traumática, por radiación: A menudo unilateral
Enfermedades que tienden a ser bilaterales
- LHON: inicialmente unilateral, se vuelve bilateral en semanas a meses (finalmente casi 100% bilateral)
- ADOA: inicio bilateral simétrico
- Tóxico/nutricional: principalmente bilateral (si un ojo es completamente normal, considere excluir causa tóxica) 2)
- NMOSD/AQP4-IgG positivo: grave, bilateral, recidivante. 60–69% tienen pérdida visual permanente de 20/200 o peor en al menos un ojo 5)
- MOGAD: inicio bilateral frecuente (extremadamente raro en casos relacionados con EM o idiopáticos) 6)
Presencia o ausencia de dolor
Sección titulada «Presencia o ausencia de dolor»| Dolor presente | Sin dolor (indoloro) |
|---|---|
| Neuritis óptica idiopática (dolor con movimiento ocular ~50%)13) | NAION (sin dolor ocular; cefalea, claudicación mandibular son síntomas sistémicos de GCA) |
| Neuritis óptica relacionada con EM | AAION (sin dolor ocular; presencia de claudicación mandibular y cefalea) |
| Relacionado con NMOSD (dolor periorbitario) | LHON/ADOA (indoloro) 14) |
| MOGAD (a menudo con cefalea) 6) | Tóxico/nutricional (sin dolor con el movimiento ocular) |
| Traumático (dolor por lesión) | Compresivo (generalmente indoloro pero puede tener dolor orbitario) |
Clasificación según los hallazgos papilares
Sección titulada «Clasificación según los hallazgos papilares»5. Examen y pruebas
Sección titulada «5. Examen y pruebas»Evaluación oftalmológica esencial
Sección titulada «Evaluación oftalmológica esencial»Cuando se sospecha neuropatía óptica, realizar las siguientes evaluaciones de forma sistemática.
Agudeza visual y visión cromática La agudeza visual corregida es fundamental para evaluar el grado de deterioro y el seguimiento de la evolución. La visión cromática (Ishihara, Farnsworth-Munsell 100 hue) suele afectarse tempranamente en la neuropatía óptica, y las anomalías cromáticas pueden preceder a la pérdida de agudeza visual incluso cuando esta está relativamente conservada. En las neuropatías ópticas tóxicas y nutricionales, la desaturación del rojo es un signo temprano 2). En la ADOA (atrofia óptica autosómica dominante), es característica la tritanopía adquirida (defecto cromático azul-amarillo), que muestra un eje tritán en el test de Farnsworth-Munsell 100 hue 2).
RAPD (defecto pupilar aferente relativo)
El RAPD se evalúa mediante la prueba de la luz oscilante y constituye un indicador objetivo de disfunción del nervio óptico. También es útil para el diagnóstico diferencial con simulación y trastornos visuales funcionales 2).
OCT (Tomografía de Coherencia Óptica)
Sección titulada «OCT (Tomografía de Coherencia Óptica)»La OCT es una prueba esencial para la estadificación y el seguimiento de la neuropatía óptica.
| Parámetro de evaluación | Hallazgos en fase aguda | Hallazgos en fase crónica |
|---|---|---|
| pRNFL (grosor de la capa de fibras nerviosas peripapilar) | Engrosado en edema de papila (precaución por falsos positivos) | Adelgazado en atrofia óptica |
| GCL-IPL (grosor de la capa de células ganglionares + plexiforme interna) | Poco cambio | Adelgazado reflejando daño de células ganglionares de la retina |
| Forma de la papila óptica | La excavación desaparece o se reduce | Se fija después de la atrofia |
Patrón de adelgazamiento de pRNFL y diagnóstico diferencial
El patrón de adelgazamiento de pRNFL en la OCT es útil para el diagnóstico diferencial desde varias semanas hasta meses después del inicio.
- Adelgazamiento circunferencial severo: NMOSD (tipo positivo para anticuerpos AQP4) es el más grave. Se adelgaza severamente en toda la circunferencia.
- Adelgazamiento temporal (haz papilomacular): Tóxico, nutricional, LHON, ADOA. Corresponde a escotoma central.
- Adelgazamiento sectorial superior o inferior: NAION. Corresponde a defecto fascicular superior o inferior.
- MOGAD vs. relacionado con EM: El adelgazamiento de pRNFL después de MOG-ON es más severo que el relacionado con EM 6).
- Diferenciación del glaucoma: En el glaucoma, los cambios en la forma del disco (agrandamiento de la excavación) preceden, y el patrón de adelgazamiento de GCL también difiere.
Prueba de campo visual (Campímetro de Humphrey)
Sección titulada «Prueba de campo visual (Campímetro de Humphrey)»Los patrones de defecto del campo visual se relacionan directamente con la estimación anatómica del sitio de la lesión.
| Patrón de defecto del campo visual | Enfermedad sospechada principalmente | Correlación anatómica |
|---|---|---|
| Escotoma central, escotoma cecocentral | Tóxico/nutricional, LHON, ADOA, neuritis óptica idiopática2) | Daño del haz papilomacular (PMB) |
| Defecto horizontal (temporal inferior a inferior) | NAION (defecto fascicular)3) | Isquemia de la mitad superior o inferior del disco óptico |
| Hemianopsia bitemporal | Compresión del quiasma óptico (adenoma hipofisario, craneofaringioma) | Fibras de cruce central del quiasma óptico |
| Hemianopsia homónima (mismo lado) | Lesión postquiasmática (tracto óptico, radiación óptica, lóbulo occipital) | Vía visual central |
| Escotoma yuxtaquiasmático | Lesión del quiasma anterior, un tipo de neuropatía óptica nasal | Haz papilomacular + temporal superior contralateral |
| Disminución general de la sensibilidad | Relacionado con NMOSD / después de neuritis óptica grave5) | Daño extenso de las fibras del nervio óptico |
| Agrandamiento del punto ciego de Mariotte (agudeza visual normal) | Drusas del disco óptico, vasculitis del disco óptico, neuritis perióptica | Solo alrededor del disco óptico |

Análisis de sangre y líquido cefalorraquídeo
Sección titulada «Análisis de sangre y líquido cefalorraquídeo»Se muestran las pruebas recomendadas para la evaluación inicial de la neuropatía óptica aguda.
| Ítem de prueba | Propósito | Significado clínico |
|---|---|---|
| VSG, PCR, plaquetas | Excluir GCA (AAION) | Máxima prioridad. La PCR tiene mayor especificidad que la VSG1) |
| Anticuerpo anti-AQP4 (ensayo basado en células) | Diagnóstico de NMOSD | ELISA tiene menor sensibilidad y especificidad que CBA5) |
| Anticuerpo anti-MOG (ensayo basado en células) | Diagnóstico de MOGAD | CBA que reconoce la molécula MOG nativa es esencial6) |
| Serología de sífilis (TPHA/RPR) y VIH | Exclusión de neuritis óptica infecciosa | Debe verificarse antes de los esteroides |
| Vitamina B12, B1, ácido fólico, cobre | Evaluación de neuropatía óptica nutricional | Especialmente importante después de cirugía bariátrica o dieta vegana |
| Genes mitocondriales (mt11778, mt14484, mt3460) | Diagnóstico de LHON | Estas tres mutaciones cubren más del 95% de todos los casos14) |
| β-D-glucano y cultivo de hongos | Sospecha de aspergilosis invasiva | Tiende a elevarse en el tipo invasivo2) |
| ACE, lisozima, TC de tórax | Descartar sarcoidosis | — |
| ANA, dsDNA, ANCA | Enfermedades autoinmunes sistémicas (LES, vasculitis) | — |
Indicaciones para el examen de LCR Sospecha de meningitis/encefalitis infecciosa, ayuda diagnóstica para NMOSD/MOGAD (pleocitosis en LCR, elevación del índice de IgG), ayuda diagnóstica para EM (bandas oligoclonales en LCR). La NMOSD puede presentar pleocitosis marcada de hasta 50 células/μL o más6).
Pruebas de imagen
Sección titulada «Pruebas de imagen»| Prueba | Principales elementos de evaluación | Notas |
|---|---|---|
| RMN orbitaria (T2 con supresión grasa/T1 con contraste) | Inflamación, edema, masa, realce del nervio óptico | Neuritis óptica con realce. LHON aguda sin realce14) |
| RMN craneal (FLAIR) | Lesiones desmielinizantes (EM, NMOSD), lesiones intracraneales | Usado en criterios McDonald para diagnóstico de EM |
| TC (ventana ósea) | Fractura del conducto óptico (traumatismo), lesiones de senos paranasales, calcificación (drusas) | Esencial en traumatismos y enfermedades nasales |
| Ecografía craneal (Doppler color) | Signo de halo para diagnóstico de GCA | Sensibilidad 68%, especificidad 91% (100% si bilateral positivo)1) |
| PET-TC (FDG) | Evaluación de afectación de grandes vasos en GCA | Sensibilidad 92%, especificidad 85% (estudio GAPS)1) |
| Ecografía orbitaria | Confirmación de calcificación en drusas del disco óptico | — |
En la neuropatía óptica aguda, generalmente se requiere una resonancia magnética orbitaria. La prioridad es descartar lesiones compresivas, y el enfoque del tratamiento varía significativamente según se observe realce con contraste (inflamatorio) o compresión/deformación (compresivo) en el nervio óptico 2). Si la resonancia magnética con contraste no muestra hallazgos inflamatorios en el nervio óptico, se deben considerar causas tóxicas, hereditarias o nutricionales. En la fase aguda de la LHON, no hay hallazgos inflamatorios, y la angiografía fluoresceínica no muestra fuga de fluoresceína desde el disco óptico, lo que es un punto de diferenciación importante con la neuritis óptica inflamatoria 14). Si la resonancia magnética está contraindicada, se utiliza una tomografía computarizada para evaluar los senos paranasales, la órbita y el conducto óptico.
Uso de los potenciales evocados visuales (PEV)
Sección titulada «Uso de los potenciales evocados visuales (PEV)»Los potenciales evocados visuales (PEV) son útiles como marcador de neuritis óptica desmielinizante. La prolongación de la latencia de P100 (normal dentro de 130 ms) sugiere desmielinización, y en la neuritis óptica relacionada con esclerosis múltiple e idiopática, la prolongación a menudo persiste incluso después de la recuperación 13). La reducción de la amplitud es prominente en el daño axonal (tóxico, isquémico). En la neuropatía óptica tóxica, no hay retraso en la latencia de P100, solo se reduce la amplitud, lo que ayuda a diferenciarla de la enfermedad desmielinizante 13). Una disminución de la frecuencia crítica de fusión (FCF) también refleja la disfunción en la neuropatía óptica, y se reduce notablemente en la neuritis óptica relacionada con NMOSD 13).
6. Características según la causa
Sección titulada «6. Características según la causa»Las neuropatías ópticas principales se clasifican según su causa y se resumen las características de cada tipo.
6-1. Neuropatía óptica isquémica
Sección titulada «6-1. Neuropatía óptica isquémica»Neuropatía óptica isquémica anterior no arterítica (NAION)
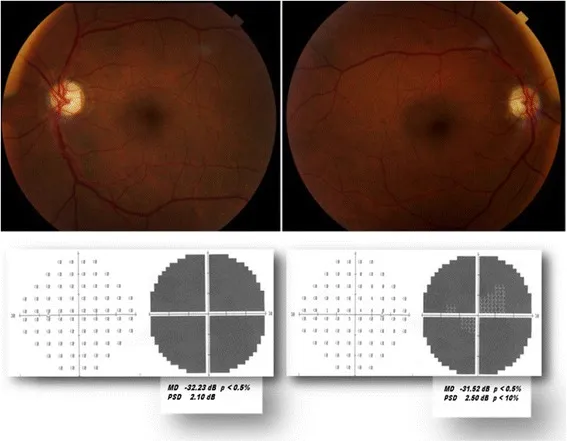
Sección titulada «Neuropatía óptica isquémica anterior no arterítica (NAION)»La NAION es el tipo más común de neuropatía óptica aguda en adultos y ocurre con mayor frecuencia en personas de 50 años o más 3). Se produce un infarto isquémico de la cabeza del nervio óptico debido a una insuficiencia circulatoria aguda de las arterias ciliares posteriores cortas (arterias SPC).
- Epidemiología: La incidencia anual en Estados Unidos es de 2.3 a 10.2 por cada 100,000 3). La mayoría ocurre en personas de 50 años o más, pero la incidencia en menores de 50 años también está aumentando.
- Factores de riesgo: Hipertensión, diabetes, hiperlipidemia, síndrome de apnea del sueño y disco en riesgo (disco óptico pequeño con relación copa-disco <0.2). El disco en riesgo está presente en aproximadamente el 80% de los ojos contralaterales 3).
- Síntomas: Pérdida visual unilateral aguda e indolora, a menudo notada al despertar. RAPD positivo en el lado afectado.
- Hallazgos papilares: Hiperemia e hinchazón (patrón sectorial inferior). Puede acompañarse de hemorragias.
- Campo visual: Defecto altitudinal (defecto temporal inferior típico).
- Tratamiento: No hay tratamiento efectivo establecido en la fase aguda. El manejo de los factores de riesgo vascular y el tratamiento de la apnea del sueño son fundamentales para prevenir la recurrencia.
- Atención reciente: Un estudio observacional de 2024 reportó un mayor riesgo de NAION en usuarios de semaglutida (agonista del receptor GLP-1). Sin embargo, no se ha establecido causalidad, y los beneficios para el tratamiento de la diabetes y la obesidad deben sopesarse al prescribir7).
Neuropatía Óptica Isquémica Anterior Arterítica (AAION/GCA)
Sección titulada «Neuropatía Óptica Isquémica Anterior Arterítica (AAION/GCA)»La AAION representa del 5 al 10% de todas las neuropatías ópticas isquémicas anteriores, pero es la neuropatía óptica más urgente 1). Su esencia es la vasculitis de las arterias ciliares posteriores cortas que irrigan la cabeza del nervio óptico, y más del 90% de los casos se deben a arteritis de células gigantes (GCA).
- Epidemiología: Más frecuente en mujeres mayores de 50 años (especialmente mayores de 75 años), con una proporción mujer:hombre de 3:1 1). La incidencia en Japón es de 1.47 por 100,000 personas, mucho menor que en Occidente.
- Síntomas: Pérdida visual unilateral aguda y grave (visión <20/200 en más del 60%, sin percepción de luz en más del 20%) 1). Alrededor del 30% experimenta amaurosis fugaz previa.
- Síntomas sistémicos: Cefalea (65–90%), claudicación mandibular (11–45%), dolor a la palpación del cuero cabelludo, fiebre y síntomas similares a la polimialgia reumática.
- Hallazgos papilares: Hinchazón pálida como tiza (pallid swelling) es característica.
- Pruebas: VSG y PCR elevadas (elevadas en >80% de los casos)1). Biopsia de arteria temporal (sensibilidad y especificidad >95%)1).
- Tratamiento: Esteroides en dosis altas (mPSL 500–1000 mg IV durante 3 días, luego prednisolona oral en reducción gradual)1). Tocilizumab (antagonista del receptor de IL-6) es efectivo para ahorrar esteroides (ensayo GiACTA, evidencia de ECA)1).
- Pronóstico: La recuperación visual en el ojo afectado rara vez se espera, pero el tratamiento con esteroides es efectivo para prevenir la aparición en el ojo contralateral.
6-2. Neuritis Óptica Inflamatoria
Sección titulada «6-2. Neuritis Óptica Inflamatoria»Neuritis Óptica Idiopática
Sección titulada «Neuritis Óptica Idiopática»Enfermedad inflamatoria del nervio óptico por mecanismo autoinmune, que constituye la mayoría de las neuritis ópticas 13). La edad de presentación típica es de 15 a 45 años, con aproximadamente un 70% de mujeres. La incidencia anual en Japón es de 1,6 por cada 100.000 adultos 13).
- Síntomas: Pérdida visual aguda unilateral y dolor con el movimiento ocular (aproximadamente 50%). Progresión en días a 2 semanas, con tendencia a la recuperación espontánea en 5 semanas.
- Campo visual: Escotoma central o escotoma cecocentral frecuentes.
- RM: Realce con contraste (gadolinio) concordante con el nervio óptico.
- Pronóstico: Más del 90% recupera una agudeza visual de 0,5 o mejor al año (estudio ONTT) 4).
- Tratamiento: La pulsoterapia con metilprednisolona 1.000 mg/día durante 3 días acelera la recuperación. No se realiza monoterapia oral con esteroides porque aumenta la tasa de recurrencia (estudio ONTT) 4).
- Riesgo de conversión a EM: Incidencia acumulada del 50% a los 15 años del primer episodio. Sin lesiones en RM cerebral: 25%, con lesiones: 78%4).
Neuritis óptica asociada a EM
Sección titulada «Neuritis óptica asociada a EM»La neuritis óptica aparece como síntoma inicial en aproximadamente el 30% de los casos de EM, y hasta el 75% de los pacientes con EM experimentan al menos un episodio de neuritis óptica durante su vida8). Generalmente es unilateral, con dolor al movimiento ocular y a menudo retrobulbar (fondo de ojo normal en el 65%). La RM cerebral que muestra lesiones desmielinizantes (hiperintensidad en T2/FLAIR) es clave para el diagnóstico. Tras el diagnóstico según los criterios de McDonald (versión 2017, revisada en 2024), se utilizan terapias modificadoras de la enfermedad (TME: interferón beta, natalizumab, fingolimod, fármacos anti-CD20, etc.) para prevenir recaídas.
Neuritis óptica asociada a NMOSD (trastorno del espectro de neuromielitis óptica)
Sección titulada «Neuritis óptica asociada a NMOSD (trastorno del espectro de neuromielitis óptica)»AQP4-IgG positivo. Predomina en mujeres (proporción mujer:hombre 9:1), de mediana edad y de ascendencia asiática. Es más grave, bilateral y recurrente que la neuritis óptica asociada a EM5). La discapacidad visual permanente de 20/200 o peor en al menos un ojo ocurre en el 60–69% de los casos5). La RM orbitaria muestra lesiones largas del nervio óptico (a menudo afectan el quiasma). El tratamiento incluye pulsos de esteroides en fase aguda, seguidos de plasmaféresis y luego inmunoterapia para prevención de recaídas (eculizumab, rituximab, satralizumab)5).
Neuritis óptica asociada a MOGAD (enfermedad asociada a anticuerpos MOG)
Sección titulada «Neuritis óptica asociada a MOGAD (enfermedad asociada a anticuerpos MOG)»MOG-IgG positivo. La incidencia anual es de 1.6 a 4.8 por millón de personas 6). Es frecuente la afectación bilateral con edema de papila marcado y predominio de la lesión anterior. La RM muestra edema de papila, lesiones del nervio óptico de segmento largo y perineuritis óptica 6). La comparación de la proporción de sexos entre MS-ON, AQP4-ON y MOG-ON muestra relaciones hombre:mujer de 3:1, 7-9:1 y 1:1, respectivamente 6). Responde a esteroides, pero es propenso a recaer con la reducción temprana de la dosis; se requiere una reducción gradual cuidadosa 6).
6-3. Neuropatía óptica compresiva
Sección titulada «6-3. Neuropatía óptica compresiva»Causada por la compresión del nervio óptico por tumores, aneurismas, hematomas, abscesos, quistes o músculos extraoculares agrandados. Los síntomas y los patrones de defecto del campo visual varían mucho según el sitio de compresión.
- Ápex orbitario: Enfermedad tiroidea ocular (la neuropatía óptica tiroidea complica del 3 al 8.6% de la enfermedad tiroidea ocular, 70% bilateral), tumores orbitarios (benignos: inflamación orbitaria idiopática 20%, adenoma pleomórfico 13%, hemangioma 13%; malignos: linfoma maligno más común) 9).
- Quiasma óptico: Adenoma hipofisario (más común en adultos, hemianopsia bitemporal), craneofaringioma (más común en niños).
- Neuropatía óptica nasal (nota especial): El tipo infiltrante de micosis de senos paranasales (Aspergillus, Mucor) tiene una tasa de mortalidad reportada del 94% 2). Puede diagnosticarse erróneamente como neuritis óptica retrobulbar porque los esteroides proporcionan una mejoría temporal, y continuar con esteroides sin saberlo puede ser fatal. Los hallazgos de destrucción ósea en TC/RM son clave para el diagnóstico, y es necesaria la colaboración urgente con un otorrinolaringólogo.
El principio del tratamiento es la extirpación quirúrgica de la lesión causal. Cuanto más temprana sea la descompresión, mejor será la recuperación de la función visual; una vez establecida la atrofia óptica, la recuperación es limitada.
6-4. Neuropatía Óptica Tóxica
Sección titulada «6-4. Neuropatía Óptica Tóxica»Es un grupo de enfermedades en las que la vía visual anterior se daña por la exposición a sustancias químicas2). Generalmente es bilateral e indolora; si un ojo está completamente normal, se debe excluir la neuropatía óptica tóxica2).
- Sustancias causantes: Tabaco, alcohol, disolvente (fármacos: etambutol [el más famoso], amiodarona, linezolid, cisplatino, inmunosupresores, etc.).
- Campo visual: Característicamente, un escotoma centrocecal o escotoma central (debido al daño predominante de las células P)2).
- Visión del color: La disminución de la percepción del color rojo es un signo temprano.
- Fondo de ojo: Inicialmente normal o enrojecimiento leve → en fase crónica, palidez temporal del disco óptico y pérdida del haz papilomacular.
- RAPD: Generalmente negativo debido a la simetría bilateral.
- VEP: Disminución de la amplitud sin retraso en la latencia de P100 (el retraso en la latencia es característico de la neuritis óptica desmielinizante) 13).
- Etambutol: Dosis dependiente (el riesgo aumenta por encima de 15 mg/kg). Son esenciales las pruebas de función visual basal antes de la administración y el monitoreo regular.
- Tratamiento: La suspensión del agente causal es fundamental. No existe un antídoto específico.
6-5. Neuropatía óptica nutricional
Sección titulada «6-5. Neuropatía óptica nutricional»Neuropatía óptica bilateral, simétrica y progresiva causada por deficiencia de vitaminas del grupo B (B12, B1, B2, B9) y cobre. Se encuentra en el mismo espectro que la neuropatía óptica tóxica, pero se distingue por tener como causa una deficiencia nutricional. Los factores de riesgo modernos incluyen cirugía bariátrica (requiere monitoreo de por vida), dieta vegana y alcoholismo. Los síntomas, el campo visual y los hallazgos de fondo de ojo son similares a los de la neuropatía óptica tóxica (escotoma central, indoloro, palidez temporal del disco óptico). La suplementación nutricional temprana puede permitir la recuperación, pero los casos crónicos pueden dejar daño irreversible.
6-6. Neuropatía óptica hereditaria
Sección titulada «6-6. Neuropatía óptica hereditaria»NOHL (Neuropatía óptica hereditaria de Leber)
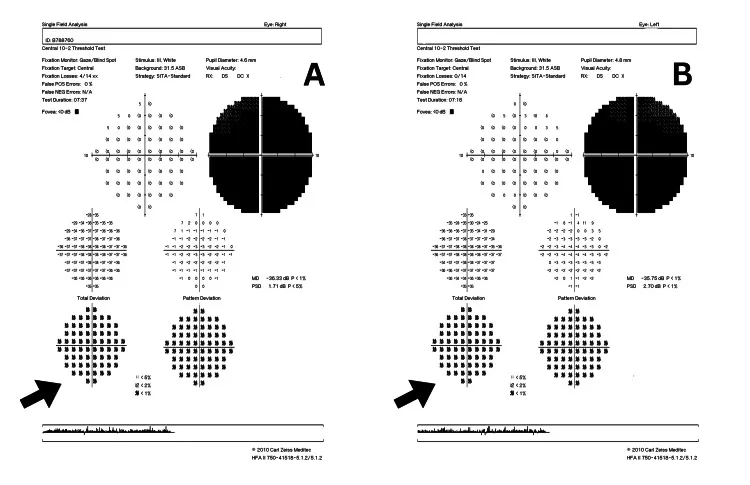
Sección titulada «NOHL (Neuropatía óptica hereditaria de Leber)»Neuropatía óptica aguda o subaguda causada por mutaciones puntuales en el ADN mitocondrial (ADNmt) con herencia materna 14). Tres mutaciones principales (mt3460, mt11778, mt14484) representan más del 95% de todos los casos, y mt11778 representa aproximadamente el 90% de todos los casos en Asia 14).
- Epidemiología: Prevalencia de 1/31,000 a 1/68,000. Penetrancia del 2,5 al 17,5%, la mayoría de los portadores no desarrollan la enfermedad 14). En Japón, aproximadamente 117 nuevos casos por año (encuesta de 2014). Designada como enfermedad intratable.
- Síntomas: Predomina en varones jóvenes (proporción hombre:mujer aproximadamente 93:7). Escotoma central bilateral subagudo e indoloro (un ojo afectado primero, luego ambos ojos en semanas a meses).
- Fondo de ojo en fase aguda: Hiperemia y edema del disco óptico, con dilatación y tortuosidad de los capilares peripapilares. La angiografía con fluoresceína no muestra fuga de fluoresceína del disco óptico (importante diferenciación de la neuritis óptica inflamatoria) 14).
- Reflejo pupilar a la luz: Relativamente conservado en comparación con otras enfermedades del nervio óptico, o solo levemente afectado 14).
- Agudeza visual final: Alrededor de 0.01 o menos en mt11778. mt14484 tiene la tasa más alta de recuperación espontánea 14).
- Tratamiento: Idebenona 900 mg/día (aprobado por la EMA). En el ensayo LEROS, la CRR (recuperación clínicamente relevante) fue del 46.0% (frente a placebo) 10). En el estudio de cohorte de Gales, la CRR alcanzó el 86% a los 27 meses 10). La terapia génica también ha mostrado eficacia en ensayos de fase III 11). La consejería para dejar de fumar es importante para prevenir la aparición y la progresión.
ADOA (Atrofia Óptica Autosómica Dominante)
Sección titulada «ADOA (Atrofia Óptica Autosómica Dominante)»La neuropatía óptica hereditaria más frecuente, causada principalmente por mutaciones en el gen OPA1. Se descubre en la edad escolar como un trastorno bilateral del desarrollo visual de causa desconocida. Es característica la deficiencia adquirida de la tercera visión cromática (discromatopsia azul-amarilla). La OCT muestra adelgazamiento de la capa de fibras nerviosas de la retina (RNFL) predominante en los cuadrantes temporal e inferior 2). Actualmente no existe un tratamiento eficaz, y el manejo se centra en la rehabilitación visual y el asesoramiento genético.
6-7. Neuropatía Óptica Traumática
Sección titulada «6-7. Neuropatía Óptica Traumática»Daño del nervio óptico que ocurre después de un traumatismo cerrado en la cabeza u órbita, con frecuencia debido a una fuerza indirecta dentro del conducto óptico. Se produce una pérdida aguda de la visión inmediatamente después de la lesión. La TC con ventana ósea confirma la fractura del conducto óptico. Se puede considerar el uso de corticosteroides en dosis altas o la descompresión del conducto óptico, pero la evidencia para ambos es limitada.
6-8. Neuropatía Óptica por Radiación
Sección titulada «6-8. Neuropatía Óptica por Radiación»Trastorno isquémico tardío después de radioterapia para tumores de cabeza y cuello u orbitales. La función visual se pierde a través de mecanismos que implican principalmente daño endotelial vascular. La aparición ocurre entre 3 meses y 9 años después de la irradiación, con mayor frecuencia a los 10–20 meses, con un promedio de aproximadamente 18 meses 12). El riesgo aumenta con una dosis total >50 Gy o una dosis por fracción >10 Gy. Generalmente es indolora y tiene mal pronóstico. No existe un tratamiento establecido; los corticosteroides sistémicos, la anticoagulación y la oxigenoterapia hiperbárica tienen eficacia limitada 12). La RM muestra realce de contraste correspondiente al nervio óptico.
6-9. Otras neuropatías ópticas específicas
Sección titulada «6-9. Otras neuropatías ópticas específicas»Neuropatía óptica isquémica posterior (PION) Isquemia del nervio óptico en la parte posterior de la órbita o dentro del conducto óptico. La PION postoperatoria es típica, ocurriendo después de hemorragia masiva, hipotensión, cirugía espinal o cirugía cardíaca. El fondo de ojo es normal (sin cambios en el disco óptico), pero hay una pérdida aguda de la visión. El reflejo pupilar a la luz muestra un defecto pupilar aferente relativo (RAPD). No se ha establecido un tratamiento eficaz.
Neuroretinitis Síndrome caracterizado por edema del disco óptico y una estrella macular. Las causas incluyen Bartonella henselae (enfermedad por arañazo de gato), sífilis y neuroretinitis estrellada idiopática de Leber. La estrella macular se debe al depósito de exudado a lo largo de la capa de fibras de Henle en la mácula, que aparece varias semanas después de que el edema del disco se resuelve. Tiende a la resolución espontánea, pero se administra tratamiento específico para las causas infecciosas.
Papiloflebitis (papillophlebitis) Síndrome que ocurre en adultos jóvenes y de mediana edad, caracterizado por edema de papila unilateral sin disfunción visual y dilatación y tortuosidad de las venas retinianas. Se observa agrandamiento del punto ciego de Mariotte, pero la agudeza visual corregida es normal. La RMN orbitaria es normal. El pronóstico es bueno y no requiere tratamiento, pero es importante diferenciarlo del papiledema, la neuritis óptica y la neuropatía óptica isquémica2).
Neuropatía óptica relacionada con inhibidores de puntos de control inmunitario La neuropatía óptica ocurre raramente como un evento adverso relacionado con el sistema inmunitario (irAE) de la inmunoterapia contra el cáncer (p. ej., nivolumab, pembrolizumab). Se trata con terapia de pulsos de esteroides y se debe discutir con un oncólogo la continuación del tratamiento oncológico.
Tabla resumen de una línea de neuropatía óptica
Sección titulada «Tabla resumen de una línea de neuropatía óptica»| Enfermedad | Lateralidad | Dolor | Hallazgos papilares | Campo visual | Puntos clave |
|---|---|---|---|---|---|
| NAION | Unilateral | Ninguno | Enrojecimiento e hinchazón (inferior) | Defecto fascicular horizontal | Inicio al despertar, disco en riesgo3) |
| AAION/GCA | Unilateral → bilateral | Ninguno (cefalea, claudicación mandibular) | Hinchazón pálida | Variable (grave) | Máxima urgencia, elevación de VSG/PCR1) |
| Neuritis óptica idiopática | Unilateral | Presente (50%) | Edematoso o normal | Escotoma central | Mujeres jóvenes, riesgo de conversión a EM 13) |
| Relacionado con NMOSD | Tiende a bilateralizarse | Sí | Hinchado o normal | Variable (grave) | Anticuerpo AQP4 positivo, refractario5) |
| Relacionado con MOGAD | Frecuentemente bilateral | Presente (cefalea) | Hinchazón severa | Variable | Anticuerpo MOG, perineuritis6) |
| Compresiva | Unilateral/Bilateral | Ninguno | Normal o atrófico | Variable | RM obligatoria9) |
| Tóxico | Ambos ojos | Ninguno | Normal → palidez temporal | Escotoma centrocecal | Preguntar sobre la sustancia causante 2) |
| Nutricional | Ambos ojos | Ninguno | Normal → palidez temporal | Escotoma central | Deficiencia de B12/cobre |
| LHON | Ambos ojos (uno primero) | Ninguno | Enrojecimiento/telangiectasia | Escotoma central | Varón joven, sin fuga de fluoresceína14) |
| ADOA | Ambos ojos | Ninguno | Pálido | Escotoma central | Edad escolar, discromatopsia azul-amarilla2) |
| Traumática | Unilateral | Sí (trauma) | Normal | Variable | TC confirma fractura del conducto óptico |
| Radioterapia | Unilateral/bilateral | Ninguno | Normal → atrofia | Variado | Promedio 18 meses12) |
7. Principios del tratamiento
Sección titulada «7. Principios del tratamiento»El tratamiento de la neuropatía óptica depende de la causa y difiere fundamentalmente según el tipo de enfermedad. Los principios comunes se muestran a continuación.
Situaciones que requieren tratamiento de emergencia
Sección titulada «Situaciones que requieren tratamiento de emergencia»- GCA/AAION: Esteroides sistémicos en dosis altas (iniciar el mismo día). No esperar los resultados de las pruebas 1).
- Neuropatía óptica compresiva aguda: Descompresión quirúrgica (colaboración urgente con otorrinolaringología y neurocirugía). En aspergilosis invasiva, suspender los esteroides y cambiar a antifúngicos 2).
- Traumática: Consideración de la descompresión del conducto óptico.
Tratamiento de la inflamatoria (neuritis óptica)
Sección titulada «Tratamiento de la inflamatoria (neuritis óptica)»La terapia con pulsos de esteroides (mPSL 1,000 mg/día durante 3 días) acelera la velocidad de recuperación en la fase aguda 4). Los corticosteroides orales solos no se administran porque aumentan el riesgo de recaída en la neuritis óptica idiopática (estudio ONTT) 4). En la fase aguda de NMOSD, se realiza un tratamiento escalonado: pulso de esteroides → plasmaféresis si la respuesta es insuficiente → inmunoterapia para prevenir recaídas 5). La neuritis óptica por MOGAD responde a los esteroides, pero recae con la reducción temprana, por lo que se requiere una disminución gradual cuidadosa 6).
Tratamiento de la isquémica (NAION)
Sección titulada «Tratamiento de la isquémica (NAION)»No se ha establecido un tratamiento eficaz para la fase aguda. El manejo de los factores de riesgo vascular (hipertensión, diabetes, hiperlipidemia, síndrome de apnea del sueño) es el pilar, y la prevención de la aparición en el ojo contralateral es el objetivo del tratamiento. En cuanto a la semaglutida (agonista del receptor GLP-1), existen estudios observacionales que sugieren una asociación con NAION, por lo que se recomienda una explicación cuidadosa y seguimiento en pacientes con antecedentes o riesgo 7).
Tratamiento de la hereditaria (LHON)
Sección titulada «Tratamiento de la hereditaria (LHON)»La idebenona 900 mg/día está aprobada por la Agencia Europea de Medicamentos (EMA) y alcanzó una CRR del 46% en el ensayo LEROS (controlado con placebo) 10). La cohorte galesa reportó una CRR del 86% a los 27 meses, lo que indica resultados favorables en la práctica clínica real 10). La terapia génica (lenadogene nolparvovec) ha mostrado eficacia en un ensayo de fase III, y se espera una futura ampliación de indicaciones 11). El consejo para dejar de fumar (el tabaquismo es un factor de riesgo para la aparición) y la atención adecuada de baja visión son esenciales 14).
Tratamiento de la neuropatía óptica tóxica y nutricional
Sección titulada «Tratamiento de la neuropatía óptica tóxica y nutricional»El enfoque básico es la suspensión de la sustancia causal o la suplementación de nutrientes deficientes. La intervención temprana puede permitir la recuperación de la función visual, pero los casos crónicos pueden dejar daño irreversible. La neuropatía óptica por etambutol es dosis-dependiente, por lo que son esenciales las pruebas de función visual basal antes de la administración y el monitoreo regular (agudeza visual, visión cromática, campo visual).
Tratamiento de la neuropatía óptica compresiva
Sección titulada «Tratamiento de la neuropatía óptica compresiva»El principio es la extirpación quirúrgica de la lesión causal. En la neuropatía óptica tiroidea, se realiza descompresión orbitaria urgente o electiva. Dado que la recuperación visual después de la extirpación quirúrgica es limitada una vez que la atrofia óptica ha progresado, el diagnóstico y tratamiento tempranos son importantes.
Resumen del pronóstico
Sección titulada «Resumen del pronóstico»| Tipo de enfermedad | Pronóstico visual | Posibilidad de recuperación |
|---|---|---|
| Neuritis óptica idiopática | Más del 90% alcanza 0.5 o mejor al año4) | Buena recuperación |
| NAION | 1/3 mejora, 1/3 sin cambios, 1/3 empeora | Recuperación parcial |
| AAION/GCA | La recuperación del ojo afectado casi nunca se espera | El objetivo es la prevención en el ojo contralateral1) |
| Relacionado con NMOSD | Grave. Al menos un ojo con 20/200 o peor en 60–69%5) | La prevención de recaídas es importante |
| LHON (mt11778) | La agudeza visual final suele ser alrededor de 0.01 | La recuperación espontánea solo en algunos casos14) |
| LHON (mt14484) | Tipo de mutación con la tasa de recuperación espontánea más alta | Existen casos de recuperación14) |
| ADOA | Progresión lenta, a menudo no conduce a ceguera severa | Sin supresión de la progresión |
| Compresivo | Recuperable con eliminación temprana | Antes de que progrese la atrofia es crucial |
| Tóxico/nutricional | Recuperable con cese/suplementación temprana | Irreversible en casos crónicos |
| Radioterápica | Pérdida visual aguda, grave y a menudo irreversible 12) | Sin tratamiento establecido |
La identificación rápida de la causa subyacente. Si se sospecha GCA, iniciar esteroides el mismo día sin esperar los resultados de las pruebas para prevenir la pérdida visual en el ojo contralateral 1). En casos compresivos, la extirpación quirúrgica de la lesión causal es el único método para preservar la función visual, y el retraso en el diagnóstico conduce a atrofia óptica irreversible. En casos inflamatorios (neuritis óptica), la pulsoterapia con esteroides acelera la recuperación, pero las estrategias de tratamiento adicional varían mucho según el subtipo. En particular, en casos con anticuerpos anti-AQP4 positivos, la monoterapia con esteroides provoca recaídas repetidas, por lo que la introducción temprana de inmunoterapia preventiva de recaídas es clave para preservar la función visual 5).
Ambas afecciones presentan síntomas iniciales similares de “pérdida visual indolora aguda a subaguda” y se confunden fácilmente, especialmente durante la fase aguda de LHON cuando hay hinchazón del disco óptico. La característica distintiva más importante es la presencia o ausencia de fuga de fluoresceína del disco óptico en la angiografía con fluoresceína. La neuritis óptica inflamatoria muestra realce con contraste y fuga de fluoresceína, pero no hay fuga de fluoresceína en la fase aguda de LHON 14). Además, aproximadamente el 50% de los casos de neuritis óptica presentan dolor con el movimiento ocular, mientras que LHON es indolora. El diagnóstico definitivo se puede realizar mediante pruebas genéticas mitocondriales (mt11778, mt14484, mt3460), que se pueden realizar como prueba externa 14). La administración de esteroides no solo es ineficaz en pacientes con LHON, sino que también retrasa el diagnóstico definitivo; por lo tanto, es esencial incluir LHON en el diagnóstico diferencial de la pérdida visual bilateral aguda en hombres jóvenes.
8. Artículos relacionados (Neuropatía óptica)
Sección titulada «8. Artículos relacionados (Neuropatía óptica)»Neuropatía óptica isquémica anterior arterítica (AAION)
Neuropatía óptica compresiva
Neuropatía óptica tóxica
Neuropatía óptica por deficiencia nutricional
Neuropatía óptica hereditaria de Leber (LHON)
Atrofia óptica autosómica dominante (ADOA)
Neuropatía óptica por radiación
Enfermedades y tumores del nervio óptico a diferenciar
Sección titulada «Enfermedades y tumores del nervio óptico a diferenciar»Neuritis óptica idiopática
Neuritis óptica relacionada con EM
Trastorno del espectro de neuromielitis óptica (NMOSD)
Enfermedad asociada a anticuerpos MOG (MOGAD)
Referencias
Sección titulada «Referencias»- Piccus R, Hansen MS, Hamann S, et al. An update on the clinical approach to giant cell arteritis. Eye 2023.
- Biousse V, Newman NJ. Diagnosis and clinical features of common optic neuropathies. Lancet Neurol 2016;15:1355–67.
- Salvetat ML, Pellegrini F, Spadea L, et al. Non-Arteritic Anterior Ischemic Optic Neuropathy (NA-AION): A Comprehensive Overview. Vision 2023;7:72.
- Beck RW, Gal RL. The Optic Neuritis Treatment Trial: a report on the visual function at 15 years. Ophthalmology 2008;115:1079–82.
- Wingerchuk DM, Banwell B, Bennett JL, et al. International consensus diagnostic criteria for neuromyelitis optica spectrum disorders. Neurology 2015;85:177–89.
- Jeyakumar N, Lerch M, Dale RC, Ramanathan S. MOG antibody-associated optic neuritis. Eye 2024.
- Hathaway JT, Shah MP, Hathaway DB, et al. Risk of nonarteritic anterior ischemic optic neuropathy in patients prescribed semaglutide. JAMA Ophthalmol. 2024;142:740-741. PMID: 38958939. doi:10.1001/jamaophthalmol.2024.2514.
- Thompson AJ, Banwell BL, Barkhof F, et al. Diagnosis of multiple sclerosis: 2017 revisions of the McDonald criteria. Lancet Neurol 2018;17:162–73.
- Biousse V, Newman NJ. Compressive Optic Neuropathies. J Neuroophthalmol 2015;35 Suppl 1:S67–S74.
- Sanders FWB, Votruba M. Outcomes of idebenone therapy for Leber hereditary optic neuropathy in a cohort of patients from Wales. Eye 2025.
- Newman NJ, et al. Hereditary optic neuropathy: advances in treatment. Eye 2024.
- Danesh-Meyer HV. Radiation-induced optic neuropathy. J Clin Neurosci 2008;15:95–100.
- Toosy AT, Mason DF, Miller DH. Optic neuritis. Lancet Neurol 2014;13:83–99.
- Carelli V, Ross-Cisneros FN, Sadun AA. Mitochondrial dysfunction as a cause of optic neuropathies. Prog Retin Eye Res 2004;23:53–89.
