Neuropatia ottica ischemica anteriore non arteritica (NAION)

Neuropatia ottica
1. Cos’è la neuropatia ottica?
Sezione intitolata “1. Cos’è la neuropatia ottica?”La neuropatia ottica è un termine generico per un gruppo di malattie in cui il nervo ottico è danneggiato, con conseguente riduzione della funzione visiva. Si manifesta con diminuzione dell’acuità visiva, difetti del campo visivo, anomalie della visione dei colori e/o riduzione della sensibilità al contrasto 2).
視神経は網膜神経節細胞(RGC)の軸索約120万本から構成される。眼球内で視神経乳頭として束ねられ、視神経管を経て視交叉に至る。視神経乳頭から視交叉前までの障害が「前部視路障害」であり、臨床的に問題となる視神経症の大半がこの部位に相当する2)。視交叉以降(視索・視放線・後頭葉)の障害は「後部視路障害」であり、視神経症ではなく「視路障害」として扱われる。
視神経は4区分に分けられる。眼球内部(乳頭部、約1 mm)は虚血性・炎症性視神経症が好発する。眼窩内部(約25 mm)は圧迫性・炎症性が多い。管内部(視神経管、約5〜8 mm)は外傷性や骨性圧迫が起きやすい。頭蓋内部(約10 mm)は下垂体腺腫や頭蓋咽頭腫による圧迫が多い。視神経乳頭を直接観察できる「前部視神経症」と、眼底が正常に見える「球後視神経症」の区別も重要である。球後視神経症では眼底に乳頭変化がないため、視力低下の原因として見落とされやすい。
視神経乳頭の血流は短後毛様動脈(SPC動脈)が主として担っている。SPC動脈は眼動脈の終枝であり、視神経乳頭前層部・篩状板・篩状板後部に血流を供給する。この部分の循環障害がNAIONおよびAAIONの主要な病態基盤となる3)。視神経内部は血液脳関門によって保護されているが、この保護機構が炎症性視神経炎や自己免疫疾患では破綻する2)。
病態の共通経路と視神経萎縮
Sezione intitolata “病態の共通経路と視神経萎縮”原因が異なっても、最終的には網膜神経節細胞および視神経軸索のダメージ→アポトーシス→視神経萎縮という共通経路をたどる。視神経萎縮(optic atrophy)は視神経症の終末像であり、乳頭の蒼白化として認識される。萎縮が確立すると視機能の回復は著しく限定的となる2)。
視神経軸索は直径0.2〜10 μmの有髄・無髄線維の混合体であり、p細胞(輝度・コントラスト担当)とm細胞(動き・輪郭担当)に大別される。視神経症では特にATP消費の激しいp細胞が障害されやすく、中毒性・栄養性視神経症での中心暗点の発生機序と関連する2)。
Panoramica epidemiologica
Sezione intitolata “Panoramica epidemiologica”Panoramica dell’incidenza annuale delle principali neuropatie ottiche (per 100.000 adulti). La NAION è la più comune con 2,3–10,2 (USA)3). La neurite ottica idiopatica è stimata a 1,6 (adulti giapponesi)13), e la LHON (neuropatia ottica ereditaria di Leber) ha circa 117 nuovi casi all’anno in Giappone (indagine 2014), configurandosi come malattia rara14). L’incidenza annuale stimata di AAION/GCA negli over 50 è di 0,36 per 100.000, più comune nei bianchi nordici (circa 30 per 100.000 in Norvegia). Le complicanze visive della GCA si verificano nel 10–30% (fino al 70% in alcuni report) e l’AAION ne rappresenta il 60–90%1). L’incidenza annuale di MOGAD è stimata tra 1,6 e 4,8 per milione6).
Classificazione delle neuropatie ottiche
Sezione intitolata “Classificazione delle neuropatie ottiche”Le neuropatie ottiche sono classificate da diverse prospettive. La classificazione clinicamente più utile è mostrata di seguito.
Classificazione per modalità di insorgenza
- Acuta (da ore a giorni): NAION, AAION, traumatica
- Subacuto (giorni–settimane): neurite ottica idiopatica, LHON, compressivo (parziale)
- Cronico (mesi–anni): ADOA, compressivo cronico, da radiazioni (tardivo)
Classificazione per causa
- Ischemico: NAION, AAION, PION
- Infiammatorio (neurite ottica): idiopatico, associato a SM, associato a NMOSD, associato a MOGAD, infettivo
- Compressivo: tumore, cisti, aneurisma, oftalmopatia tiroidea
- Tossica: etambutolo, amiodarone, alcol, ecc.
- Nutrizionale: carenza di vitamina B12/B1, acido folico, rame
- Ereditaria: LHON, ADOA, sindrome di Wolfram
- Traumatica: frattura del canale ottico, lesione diretta
- Da radiazioni: degenerazione ischemica tardiva
Classificazione per localizzazione
- Neuropatia ottica anteriore (con alterazioni della papilla): NAION, AAION, neurite ottica anteriore
- Neuropatia ottica retrobulbare (papilla normale): tossica, ereditaria, neurite ottica associata a SM (la maggior parte)
- Lesione chiasmatica: adenoma ipofisario, craniofaringioma (emianopsia bitemporale)
Quadro diagnostico della neuropatia ottica
Sezione intitolata “Quadro diagnostico della neuropatia ottica”La diagnosi di neuropatia ottica si articola in 5 fasi.
Fase 1: Conferma della disfunzione del nervo ottico Utilizzare RAPD, acuità visiva, visione dei colori e campo visivo per confermare oggettivamente la disfunzione del nervo ottico.
Passaggio 2: Localizzazione della lesione Anteriore (con alterazione papillare) o retrobulbare (papilla normale), intraorbitaria, intracanalicolare o intracranica. Stimare la localizzazione in base al pattern del difetto del campo visivo.
Passaggio 3: Monoculare o bilaterale? Acuto o cronico? Ciò consente di restringere notevolmente la diagnosi differenziale.
Passaggio 4: Esclusione delle forme pericolose Escludere prioritariamente GCA (VES, PCR), cause compressive (RMN) e cause infettive (sifilide, funghi).
Passaggio 5: Esami specifici Aggiungere anticorpi anti-AQP4, anticorpi anti-MOG, test del mtDNA ed esami nutrizionali in base alla forma.
2. Differenza dalla neurite ottica (chiarimento concettuale)
Sezione intitolata “2. Differenza dalla neurite ottica (chiarimento concettuale)”La « neurite ottica » e la « neuropatia ottica » sono spesso confuse nella pratica clinica, ma sono in relazione di sotto-concetto e sovra-concetto.
Confondere una neuropatia ottica non infiammatoria (ischemica, compressiva, tossica, ereditaria) con una neurite ottica può portare a una somministrazione errata di steroidi. In particolare, l’aspergillosi infiltrativa è una controindicazione agli steroidi 2), e somministrare steroidi nella fase acuta della LHON non solo è inefficace, ma ritarda anche la diagnosi definitiva.
Principali caratteristiche cliniche della neurite ottica
Sezione intitolata “Principali caratteristiche cliniche della neurite ottica”La neurite ottica (infiammatoria) presenta le seguenti caratteristiche che aiutano a distinguerla da quella non infiammatoria.
- Esordio acuto : progressione in pochi giorni – 2 settimane, poi tendenza al recupero entro 5 settimane.
- Dolore oculare ai movimenti : presente in circa il 50% dei casi. Di solito assente nelle forme ischemiche, compressive o tossiche.
- Età di insorgenza : 15–45 anni (la forma ischemica di solito dopo i 50 anni).
- Risonanza magnetica : enhancement del nervo ottico (T1 con gadolinio) tipico.
- Recupero spontaneo : nelle forme idiopatiche o correlate a SM, oltre il 90% raggiunge un visus di 0,5 o superiore dopo un anno (studio ONTT)4).
- Rischio di conversione in SM: a 15 anni dal primo episodio, il 25% senza lesioni alla RM cerebrale e il 78% con lesioni sviluppano SM4).
Situazioni di diagnosi differenziale difficile
Sezione intitolata “Situazioni di diagnosi differenziale difficile”Di seguito, la diagnosi differenziale tra neurite ottica e neuropatia ottica non infiammatoria diventa difficile.
- Riduzione acuta monolaterale della vista in donna >50 anni: NAION vs. neurite ottica con anticorpi anti-AQP4 (NMOSD)
- Riduzione acuta bilaterale della vista in giovane: LHON vs. neurite ottica bilaterale simultanea vs. neuropatia ottica tossica
- Riduzione monolaterale della vista con edema papillare: NAION vs. neurite ottica anteriore vs. vasculite papillare
La neurite ottica con anticorpi anti-AQP4 è una malattia refrattaria agli steroidi che rappresenta circa il 10% delle neuriti ottiche idiopatiche, con un’età di insorgenza più avanzata rispetto alla neurite ottica tipica e una prevalenza nel sesso femminile (rapporto femmine:maschi 1:9) 5). Gli anticorpi anti-AQP4 prendono di mira i canali dell’acquaporina-4 espressi sugli astrociti del nervo ottico, causando un danno cellulare dipendente dal complemento 5). Le strategie terapeutiche differiscono sostanzialmente tra i casi positivi e negativi per gli anticorpi anti-AQP4, pertanto il test anticorpale deve essere richiesto prima della terapia pulsata con steroidi. Il saggio su cellule (CBA) ha una sensibilità e specificità superiori rispetto all’ELISA, e si raccomanda il CBA 5).
Prima di somministrare la terapia pulsata con steroidi per la neurite ottica, è obbligatorio escludere infezioni (epatite B, sifilide, HIV, infezioni fungine) 2). La somministrazione di alte dosi di steroidi a portatori del virus dell’epatite B può causare epatite fulminante. Nella neurite ottica sifilitica, gli antibiotici sono prioritari rispetto agli steroidi.
3. Forme cliniche ad alta urgenza
Sezione intitolata “3. Forme cliniche ad alta urgenza”La tabella seguente mostra le forme di neuropatia ottica che richiedono un trattamento particolarmente urgente.
| Forma clinica | Urgenza | Conseguenze in caso di omissione |
|---|---|---|
| Neuropatia ottica ischemica anteriore arteritica (AAION/GCA) | Massima urgenza | Cecità dell’occhio controlaterale (65% non trattati entro 10 giorni) 1) |
| Neuropatia ottica compressiva acuta (tumore, cisti, ematoma) | Urgente | Atrofia ottica progressiva e perdita visiva irreversibile |
| Neuropatia ottica nasale (aspergillosi infiltrativa) | Emergenza | Mortalità riportata del 94% 2) |
| Neuropatia ottica traumatica (frattura del canale ottico) | Emergenza | Il trattamento precoce può preservare la funzione visiva |
| Neuropatia ottica ischemica posteriore (PION) | Emergenza | Insorge dopo intervento chirurgico o grave perdita di sangue, spesso irreversibile |
Flusso di emergenza per GCA
Sezione intitolata “Flusso di emergenza per GCA”L’amaurosi fugace (amaurosis fugax) compare come sintomo prodromico in circa il 30% dei casi di perdita visiva permanente, in media 8,5 giorni prima 1). A questo punto, sospettare un’arterite a cellule giganti (GCA) e iniziare attivamente gli steroidi è estremamente importante per la prevenzione secondaria.
4. Porta d’ingresso per la diagnosi differenziale
Sezione intitolata “4. Porta d’ingresso per la diagnosi differenziale”La diagnosi differenziale delle neuropatie ottiche si sistematizza secondo quattro assi: acuto o cronico, monolaterale o bilaterale, presenza o assenza di dolore, e aspetto della papilla.
Acuto o cronico
Sezione intitolata “Acuto o cronico”Acuto (raggiungimento del danno massimo in ore–giorni)
- NAION: improvvisa riduzione della visione notata al risveglio, tipica
- AAION: rapida riduzione della visione monoculare, grave (acuità visiva inferiore a 20/200 in oltre il 60% dei casi) 1)
- Traumatico: immediatamente o entro poche ore dal trauma
Subacuto (da giorni a settimane)
- Neurite ottica idiopatica: progressione in 2 settimane, poi inizio del recupero
- LHON: riduzione visiva subacuta indolore unilaterale, poi bilaterale in settimane-mesi
- Compressivo: può progredire subacutamente per rapida crescita tumorale o emorragia
Cronico (lenta progressione in mesi-anni)
- ADOA (atrofia ottica autosomica dominante): esordio in età scolare, bilaterale lentamente progressiva
- Compressivo cronico: da adenoma ipofisario, tumore orbitario, ecc.
- Tossico/nutrizionale: progressione subacuta-cronica per esposizione prolungata o carenza nutrizionale
Un occhio o entrambi
Sezione intitolata “Un occhio o entrambi”Malattie a prevalenza monolaterale
- NAION: di solito monolaterale (bilaterale simultanea estremamente rara)
- AAION: inizia monolaterale, senza trattamento il 65% si estende all’altro occhio entro 10 giorni1)
- Neurite ottica idiopatica / correlata a SM: tipicamente monolaterale
- Compressiva, traumatica, da radiazioni: spesso monolaterale
Malattie a prevalenza bilaterale
- LHON: inizialmente monolaterale, poi bilaterale in settimane-mesi (alla fine quasi 100% bilaterale)
- ADOA: esordio bilaterale simmetrico
- Tossica/nutrizionale: di regola bilaterale (se un occhio è completamente normale, considerare l’esclusione di causa tossica) 2)
- NMOSD/AQP4-IgG positivo: grave, bilaterale, ricorrente. Il 60-69% presenta deficit permanente ≤ 20/200 in almeno un occhio 5)
- MOGAD: esordio bilaterale frequente (molto raro nella neurite ottica associata a SM/idiopatica) 6)
Presenza o assenza di dolore
Sezione intitolata “Presenza o assenza di dolore”| Con dolore | Senza dolore (indolore) |
|---|---|
| Neurite ottica idiopatica (dolore ai movimenti oculari in circa il 50% dei casi)13) | NAION (nessun dolore oculare, cefalea e claudicatio della mandibola sono sintomi sistemici di GCA) |
| Neurite ottica associata a SM | AAION (nessun dolore oculare, presenti claudicatio della mandibola e cefalea) |
| NMOSD correlato (dolore periorbitale) | LHON·ADOA (indolore) 14) |
| MOGAD (spesso con cefalea) 6) | tossica·nutrizionale (nessun dolore oculomotorio) |
| traumatica (dolore da lesione) | compressiva (di solito indolore ma può associarsi a dolore orbitario) |
Classificazione basata sui segni papillari
Sezione intitolata “Classificazione basata sui segni papillari”5. Visita ed esami
Sezione intitolata “5. Visita ed esami”Valutazione oculistica obbligatoria
Sezione intitolata “Valutazione oculistica obbligatoria”In caso di sospetta neuropatia ottica, eseguire sistematicamente le seguenti valutazioni.
Acuità visiva e visione dei colori L’acuità visiva corretta è fondamentale per valutare il grado di disabilità e l’evoluzione. La visione dei colori (Ishihara, Farnsworth-Munsell 100 hue) è spesso compromessa precocemente nelle neuropatie ottiche e le anomalie della visione dei colori possono precedere una riduzione dell’acuità visiva. Nelle neuropatie ottiche tossiche e nutrizionali, un’attenuazione della sensibilità al rosso è un segno precoce2). Nell’ADOA (atrofia ottica autosomica dominante), è caratteristica un’anomalia acquisita della visione dei colori del terzo tipo (anomalia blu-giallo), che mostra un asse di anomalia del terzo tipo al test di Farnsworth-Munsell 100 hue2).
RAPD (difetto pupillare afferente relativo)
Il RAPD viene valutato con il metodo della luce oscillante (test di illuminazione alternata) ed è un indicatore oggettivo di disfunzione del nervo ottico. È utile anche per la diagnosi differenziale tra simulazione e disturbi visivi funzionali2).
OCT (tomografia a coerenza ottica)
Sezione intitolata “OCT (tomografia a coerenza ottica)”L’OCT è un esame essenziale per la valutazione dello stadio e il follow-up della neuropatia ottica.
| Indicatore di valutazione | Reperti in fase acuta | Reperti in fase cronica |
|---|---|---|
| pRNFL (spessore RNFL peripapillare) | Ispessimento nell’edema papillare (attenzione ai falsi positivi) | Assottigliamento nell’atrofia ottica |
| GCL-IPL (spessore cellule gangliari + strato plessiforme interno) | Pochi cambiamenti | Assottigliamento che riflette il danno alle cellule gangliari retiniche |
| Forma della testa del nervo ottico | Scomparsa o riduzione dell’escavazione | Fissazione dopo atrofia |
Pattern di assottigliamento del pRNFL e diagnosi differenziale
Il pattern di assottigliamento del pRNFL all’OCT è utile per la diagnosi differenziale da alcune settimane ad alcuni mesi dopo l’esordio.
- Assottigliamento grave circonferenziale: La NMOSD (tipo con anticorpi anti-AQP4) è la più grave. Assottigliamento grave su tutta la circonferenza.
- Assottigliamento temporale predominante (fascio papillomaculare) : tossico, nutrizionale, LHON, ADOA. Corrisponde a scotoma centrale.
- Assottigliamento settoriale superiore o inferiore : NAION. Corrisponde a difetto fascicolare superiore o inferiore.
- MOGAD vs. correlato a SM : L’assottigliamento del pRNFL dopo MOG-ON è più grave rispetto a quello correlato a SM6).
- Diagnosi differenziale con il glaucoma : Nel glaucoma, le modificazioni della forma della testa del nervo ottico (aumento dell’escavazione) precedono e il pattern di assottigliamento del GCL è diverso.
Esame del campo visivo (perimetro di Humphrey)
Sezione intitolata “Esame del campo visivo (perimetro di Humphrey)”Il pattern del difetto del campo visivo è direttamente collegato alla stima anatomica del sito della lesione.
| Pattern di difetto del campo visivo | Malattia principalmente sospettata | Corrispondenza anatomica |
|---|---|---|
| Scotoma centrale, scotoma centro-cecale | Tossico, nutrizionale, LHON, ADOA, neurite ottica idiopatica2) | Danno del fascio papillomaculare (PMB) |
| Difetto orizzontale (infero-temporale a inferiore) | NAION (difetto fascicolare) 3) | Ischemia della metà superiore o inferiore della papilla |
| Emianopsia bitemporale | Compressione chiasmatica (adenoma ipofisario, craniofaringioma) | Fibre incrociate centrali del chiasma |
| Emianopsia omonima (stesso lato) | Lesione post-chiasmatica (tratto ottico, radiazioni ottiche, lobo occipitale) | Via visiva centrale |
| Scotoma giunzionale | Lesione della parte anteriore del chiasma, un tipo di neuropatia ottica nasale | Fascio papillomaculare + quadrante temporale superiore controlaterale |
| Riduzione generale della sensibilità | Correlato a NMOSD / dopo neurite ottica grave5) | Danno esteso delle fibre del nervo ottico |
| Allargamento della macchia cieca di Mariotte (acuità visiva normale) | Drusen della papilla, papillite, perineurite ottica | Solo intorno alla papilla |

Esami del sangue e del liquido cerebrospinale
Sezione intitolata “Esami del sangue e del liquido cerebrospinale”Test raccomandati per la valutazione iniziale della neuropatia ottica acuta.
| Parametro del test | Scopo | Significato clinico |
|---|---|---|
| VES, PCR, piastrine | Esclusione di GCA (AAION) | Massima priorità. La PCR ha una specificità maggiore della VES 1) |
| Anticorpi anti-AQP4 (saggio su cellule) | Diagnosi di NMOSD | Il metodo ELISA ha sensibilità e specificità inferiori rispetto al metodo CBA 5) |
| Anticorpi anti-MOG (saggio cell-based) | Diagnosi di MOGAD | È obbligatorio un CBA che riconosca la molecola MOG nativa6) |
| Sierologia per sifilide (TPHA, RPR) e HIV | Esclusione di neurite ottica infettiva | Da verificare obbligatoriamente prima degli steroidi |
| Vitamina B12, B1, acido folico, rame | Valutazione della neuropatia ottica nutrizionale | Particolarmente importante dopo chirurgia bariatrica o dieta vegana |
| Geni mitocondriali (mt11778, mt14484, mt3460) | Diagnosi di LHON | Queste 3 mutazioni coprono oltre il 95% dei casi14) |
| β-D-glucano e coltura fungina | Sospetta aspergillosi invasiva | Spesso elevato nella forma invasiva2) |
| ACE, lisozima, TC torace | Esclusione della sarcoidosi | — |
| ANA, dsDNA, ANCA | Malattie autoimmuni sistemiche (LES, vasculite) | — |
Indicazioni per l’esame del liquido cefalorachidiano Sospetto di meningite/encefalite infettiva, supporto diagnostico per NMOSD/MOGAD (pleiocitosi del LCR, aumento dell’indice IgG), supporto diagnostico per SM (bande oligoclonali nel LCR). Nella NMOSD può verificarsi una marcata pleiocitosi fino a 50 cellule/μL o più6).
Esami di imaging
Sezione intitolata “Esami di imaging”| Esame | Principali valutazioni | Note particolari |
|---|---|---|
| RMN orbitaria (T2 con soppressione del grasso / T1 con contrasto) | Infiammazione, edema, massa, enhancement del nervo ottico | Enhancement nella neurite ottica. Nessun enhancement nella fase acuta di LHON14) |
| RMN cerebrale (FLAIR) | Lesioni demielinizzanti (SM, NMOSD), lesioni intracraniche | Utilizzato nei criteri di McDonald per la diagnosi di SM |
| TC (osso) | Frattura del canale ottico (trauma), patologia dei seni paranasali, calcificazione (drusen) | Obbligatoria in caso di trauma o malattia nasale |
| Ecografia cranica (color Doppler) | Segno dell’alone per diagnosi di GCA | Sensibilità 68%, specificità 91% (100% se bilaterale positivo) 1) |
| PET-TC (FDG) | Valutazione delle lesioni dei grandi vasi nell’ACG | Sensibilità 92%, specificità 85% (studio GAPS)1) |
| Ecografia orbitaria | Conferma della calcificazione della drusen del disco ottico | — |
Nella neuropatia ottica acuta, in linea di principio è necessaria una RM orbitaria. L’esclusione di una lesione compressiva è prioritaria e la strategia terapeutica cambia notevolmente a seconda che si tratti di un potenziamento del contrasto (infiammatorio) corrispondente al nervo ottico o di una compressione/deformazione (compressivo) 2). Se la RM con contrasto non mostra segni infiammatori del nervo ottico, si considerano cause tossiche, ereditarie o nutrizionali. Nella fase acuta della LHON non ci sono segni infiammatori e anche all’angiografia retinica con fluoresceina non si osserva perdita di fluoresceina dalla papilla, un importante punto di differenziazione dalla neurite ottica infiammatoria 14). In caso di controindicazioni alla RM, si esegue una TC dei seni paranasali, dell’orbita e del canale ottico.
Utilizzo dei potenziali evocati visivi (PEV)
Sezione intitolata “Utilizzo dei potenziali evocati visivi (PEV)”I potenziali evocati visivi (PEV) sono utili come marker della neurite ottica demielinizzante. Un allungamento della latenza di P100 (normale ≤130 ms) suggerisce demielinizzazione, e nella neurite ottica associata a SM o idiopatica, questo allungamento spesso persiste dopo il recupero 13). Una riduzione dell’ampiezza è evidente nel danno assonale (tossico, ischemico). Nella neuropatia ottica tossica non c’è ritardo della latenza di P100, ma solo una riduzione dell’ampiezza, il che aiuta a differenziarla dalla neurite demielinizzante 13). Una riduzione della frequenza critica di fusione (CFF) riflette anche il danno funzionale della neuropatia ottica ed è particolarmente marcata nella neurite ottica associata a NMOSD 13).
6. Caratteristiche per causa
Sezione intitolata “6. Caratteristiche per causa”Classificazione delle principali neuropatie ottiche per causa e riepilogo delle caratteristiche di ciascun tipo.
6-1. Neuropatia ottica ischemica
Sezione intitolata “6-1. Neuropatia ottica ischemica”Neuropatia ottica ischemica anteriore non arteritica (NAION)
Sezione intitolata “Neuropatia ottica ischemica anteriore non arteritica (NAION)”La NAION è il tipo più comune di neuropatia ottica acuta negli adulti, che si verifica principalmente dopo i 50 anni3). Un infarto ischemico della testa del nervo ottico è causato da un’insufficienza circolatoria acuta delle arterie ciliari posteriori corte (arterie SPC).
- Epidemiologia : Incidenza annuale negli Stati Uniti di 2,3-10,2 per 100.000 persone3). La maggior parte dei casi si verifica dopo i 50 anni, ma l’incidenza prima dei 50 anni è in aumento.
- Fattori di rischio : Ipertensione, diabete, iperlipidemia, sindrome delle apnee notturne, disco a rischio (papilla piccola con rapporto C/D < 0,2). Il disco a rischio è presente in circa l’80% degli occhi controlaterali3).
- Sintomi : riduzione della vista unilaterale acuta e indolore, spesso notata al risveglio. RAPD positivo sul lato affetto.
- Aspetto della papilla : arrossamento e gonfiore (a ventaglio, prevalente in basso). Può essere accompagnato da emorragie.
- Campo visivo : difetto fascicolare orizzontale (tipicamente difetto inferotemporale).
- Trattamento: Non esiste una terapia efficace stabilita per la fase acuta. La gestione dei fattori di rischio vascolari e il trattamento della sindrome delle apnee notturne sono al centro della prevenzione delle recidive.
- Punto di attenzione recente: Uno studio osservazionale del 2024 ha riportato un aumento del rischio di NAION negli utilizzatori di semaglutide (agonista del recettore GLP-1). Tuttavia, il nesso causale non è stabilito e la decisione prescrittiva deve confrontare i benefici nel trattamento del diabete e dell’obesità7).
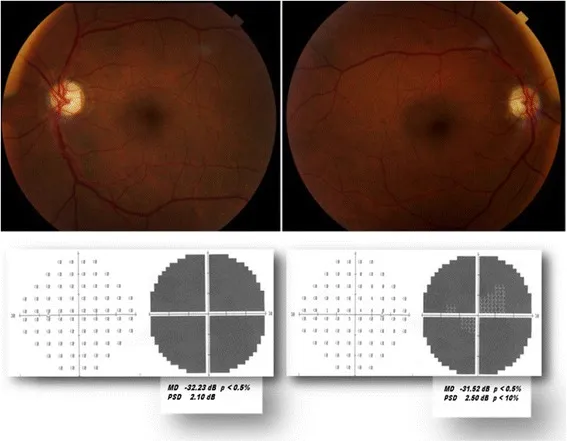
動脈炎性前部虚血性視神経症(AAION/GCA)
Sezione intitolata “動脈炎性前部虚血性視神経症(AAION/GCA)”AAIONは前部虚血性視神経症全体の5〜10%を占めるが、最緊急の視神経症である1)。視神経乳頭を栄養する短後毛様動脈の血管炎が本態であり、原疾患の90%以上が巨細胞性動脈炎(GCA)である。
- 疫学:50歳以上(特に75歳以上)の高齢女性に多い(男女比1:3)1)。日本での発症率は10万人あたり1.47人と欧米に比べて極めて低い。
- 症状:急激な片眼重度視力低下(60%以上で視力20/200未満、20%以上で光覚なし)1)。一過性黒内障を約30%が先行して経験する。
- 全身症状:頭痛(65〜90%)・顎跛行(11〜45%)・頭皮圧痛・発熱・PMR様症状。
- Reperti papillari : edema pallido gessoso (pallid swelling) caratteristico.
- Esami : VES e PCR elevati (aumentati in oltre l’80% dei casi)1). Biopsia dell’arteria temporale (sensibilità e specificità >95%)1).
- Trattamento : Steroidi ad alto dosaggio (mPSL 500-1000 mg ev per 3 giorni, poi prednisolone orale in riduzione graduale)1). Tocilizumab (antagonista del recettore dell’IL-6) efficace per ridurre gli steroidi (studio GiACTA, evidenza RCT)1).
- Prognosi : Il recupero visivo dell’occhio colpito è quasi impossibile, ma la terapia steroidea è efficace per prevenire il coinvolgimento dell’altro occhio.
6-2. Neurite ottica infiammatoria
Sezione intitolata “6-2. Neurite ottica infiammatoria”Neurite ottica idiopatica
Sezione intitolata “Neurite ottica idiopatica”Malattia infiammatoria del nervo ottico da meccanismo autoimmune, che costituisce la maggior parte delle neuriti ottiche 13). L’età di insorgenza è tra 15 e 45 anni, circa il 70% sono donne, e l’incidenza annuale in Giappone è di 1,6 per 100.000 adulti 13).
- Sintomi : Riduzione acuta unilaterale della vista e dolore oculare ai movimenti (circa 50%). Progressione in pochi giorni-2 settimane, con tendenza al recupero spontaneo entro 5 settimane.
- Campo visivo : Frequente scotoma centrale o scotoma centro-cecale.
- RMN : Enhancement contrastografico (gadolinio) corrispondente al nervo ottico.
- Prognosi : Oltre il 90% recupera un’acuità visiva ≥ 0,5 dopo 1 anno (studio ONTT) 4).
- Trattamento : La terapia pulsata con steroidi mPSL 1.000 mg/die × 3 giorni accelera il recupero. La monoterapia steroidea orale non viene eseguita per l’aumento del tasso di recidive (studio ONTT) 4).
- Rischio di conversione in SM: incidenza cumulativa del 50% a 15 anni dal primo episodio. Assenza di lesioni alla RM encefalo → 25%, presenza → 78%4).
Neurite ottica associata a SM
Sezione intitolata “Neurite ottica associata a SM”La neurite ottica si presenta come sintomo iniziale della SM in circa il 30% dei casi, e fino al 75% dei pazienti con SM sperimenta almeno un episodio di neurite ottica nel corso della vita 8). È spesso unilaterale, con dolore ai movimenti oculari, e frequentemente è retrobulbare (fondo oculare normale nel 65% dei casi). Le lesioni demielinizzanti alla RM encefalo (iperintensità T2/FLAIR) sono la chiave diagnostica. Dopo la conferma diagnostica secondo i criteri di McDonald (versione 2017, revisione 2024), si utilizza una terapia modificante la malattia (DMT: interferone beta, natalizumab, fingolimod, farmaci anti-CD20, ecc.) per prevenire le recidive.
Neurite ottica associata a NMOSD (disturbo dello spettro della neuromielite ottica)
Sezione intitolata “Neurite ottica associata a NMOSD (disturbo dello spettro della neuromielite ottica)”AQP4-IgG positivo. Si verifica prevalentemente nelle donne (rapporto maschi:femmine 1:9), di mezza età, di origine asiatica, ed è più grave, bilaterale e ricorrente rispetto alla neurite ottica associata a SM 5). Almeno il 60-69% dei pazienti sviluppa un deficit visivo permanente di 20/200 o inferiore in almeno un occhio 5). La RM orbitaria mostra una lesione lunga del nervo ottico (con frequente coinvolgimento del chiasma). Il trattamento prevede terapia pulsata con steroidi in fase acuta, seguita da plasmaferesi e quindi immunoterapia preventiva delle recidive (eculizumab, rituximab, satralizumab) 5).
Neurite ottica associata a MOGAD (malattia correlata agli anticorpi anti-MOG)
Sezione intitolata “Neurite ottica associata a MOGAD (malattia correlata agli anticorpi anti-MOG)”MOG-IgG positivo. Incidenza annuale di 1,6-4,8 per milione di abitanti6). Frequente esordio bilaterale con marcato edema papillare, predominanza anteriore. Alla RM, edema papillare, lesione ottica estesa e perineurite ottica sono caratteristici6). Confronto di genere: MS-ON 3:1, AQP4-ON 7-9:1, MOG-ON 1:16). Risponde agli steroidi ma recidiva facilmente con una riduzione precoce, richiedendo una graduale diminuzione6).
6-3. Neuropatia ottica compressiva
Sezione intitolata “6-3. Neuropatia ottica compressiva”Causata dalla compressione del nervo ottico da tumore, aneurisma, ematoma, ascesso, cisti o muscoli extraoculari ipertrofici. I sintomi e i pattern di difetto del campo visivo variano notevolmente in base al sito di compressione.
- Apice orbitario: Orbitopatia tiroidea (la neuropatia ottica tiroidea complica il 3-8,6% delle orbitopatie tiroidee, bilaterale nel 70%), tumori orbitari (benigni: infiammazione orbitaria idiopatica 20%, adenoma pleomorfo 13%, emangioma 13%; maligni: linfoma maligno più frequente)9).
- Chiasma ottico: Adenoma ipofisario (più frequente nell’adulto, emianopsia bitemporale), craniofaringioma (più frequente nel bambino).
- Neuropatia ottica nasale (menzione speciale): La forma invasiva della sinusite fungina (Aspergillus, Mucor) ha una mortalità riportata del 94%2). Gli steroidi sono temporaneamente efficaci, portando a una diagnosi errata di neurite ottica retrobulbare; la continuazione inconsapevole degli steroidi può essere fatale. I segni di distruzione ossea alla TC/RM sono fondamentali per la diagnosi, richiedendo un’urgente collaborazione con l’ORL.
Il principio del trattamento è la rimozione chirurgica della lesione causale. Quanto più precoce è la decompressione, tanto maggiore è la possibilità di recupero della funzione visiva; una volta stabilita l’atrofia ottica, il recupero è limitato.
6-4. Neuropatia ottica tossica
Sezione intitolata “6-4. Neuropatia ottica tossica”Si tratta di un gruppo di malattie in cui la via visiva anteriore viene danneggiata dall’esposizione a sostanze chimiche2). In linea di principio è bilaterale e indolore; se un occhio è completamente normale, la neuropatia ottica tossica dovrebbe essere esclusa2).
- Sostanze causali : tabacco, alcol, solventi (farmaci: etambutolo [il più noto], amiodarone, linezolid, cisplatino, immunosoppressori, ecc.).
- Campo visivo : caratteristicamente scotoma centro-cecale o scotoma centrale (danno predominante delle cellule p)2).
- Visione dei colori : un’attenuazione della percezione del rosso è un segno precoce.
- Fondo oculare: inizialmente normale o lieve arrossamento → in fase cronica pallore temporale della papilla e difetto del fascio papillomaculare.
- RAPD: di solito negativo a causa della simmetria bilaterale.
- VEP: riduzione dell’ampiezza senza ritardo della latenza di P100 (il ritardo della latenza è caratteristico della neurite ottica demielinizzante)13).
- Etambutolo: dose-dipendente (rischio aumentato oltre 15 mg/kg). Esame visivo di base prima del trattamento e monitoraggio regolare sono essenziali.
- Trattamento: la sospensione dell’agente causale è fondamentale. Non esiste un farmaco specifico.
6-5. Neuropatia ottica nutrizionale
Sezione intitolata “6-5. Neuropatia ottica nutrizionale”È una neuropatia ottica bilaterale simmetrica e progressiva causata da carenza di vitamine del gruppo B (B12, B1, B2, B9) e rame. Si colloca nello stesso spettro della neuropatia ottica tossica, ma se ne distingue per la causa nutrizionale. I rischi moderni includono la chirurgia bariatrica (monitoraggio obbligatorio per tutta la vita), la dieta vegana e l’alcolismo. Sintomi, campo visivo e reperti del fondo oculare sono simili a quelli della forma tossica (scotoma centrale, indolore, pallore temporale della papilla). La supplementazione nutrizionale precoce può portare a recupero, ma i casi cronici lasciano danni irreversibili.
6-6. Neuropatia ottica ereditaria
Sezione intitolata “6-6. Neuropatia ottica ereditaria”LHON (Neuropatia ottica ereditaria di Leber)
Sezione intitolata “LHON (Neuropatia ottica ereditaria di Leber)”È una neuropatia ottica acuta o subacuta causata da mutazioni puntiformi del DNA mitocondriale (mtDNA) e trasmessa per via materna14). Le tre mutazioni principali (mt3460, mt11778, mt14484) rappresentano oltre il 95% di tutti i casi, e mt11778 rappresenta circa il 90% di tutti i casi in Asia14).
- Epidemiologia: Prevalenza da 1/31.000 a 1/68.000. Penetranza dal 2,5% al 17,5%; la maggior parte dei portatori non sviluppa la malattia14). In Giappone circa 117 nuovi casi all’anno (indagine 2014). Malattia rara designata.
- Sintomi: Colpisce prevalentemente giovani maschi (rapporto maschi:femmine circa 93:7). Scotoma centrale bilaterale subacuto e indolore (un occhio prima, poi entrambi in poche settimane o mesi).
- 急性期眼底:視神経乳頭の発赤・腫脹と乳頭近傍毛細血管の拡張・蛇行。蛍光眼底造影で乳頭からの蛍光漏出を認めない(炎症性視神経炎との重要鑑別)14)。
- 対光反射:他の視神経疾患に比べて保たれるか、障害されても軽微14)。
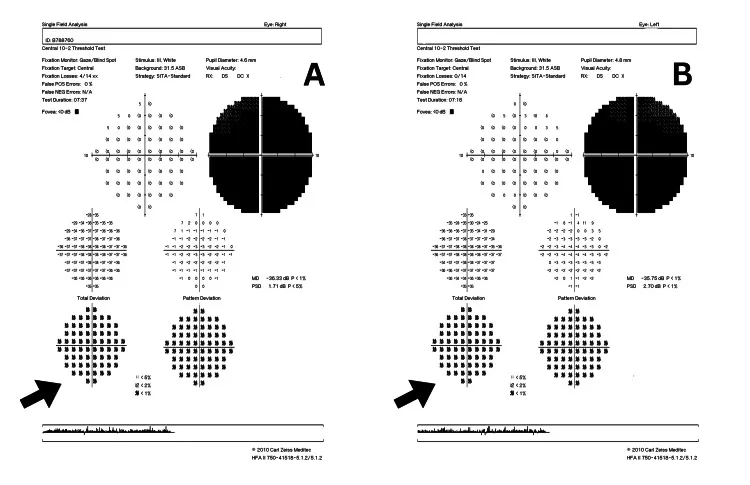
- 最終視力:mt11778では0.01前後が多い。mt14484は自然回復率が最も高い14)。
- 治療:イデベノン900 mg/日(欧州EMA承認)。LEROS試験ではCRR(有意義な視力回復)が46.0%(プラセボ対照)10)。ウェールズコホート試験では27カ月時点でCRR 86%を達成10)。遺伝子治療も第III相試験で有効性を示している11)。禁煙指導が発症・重症化予防に重要。
ADOA (atrofia ottica autosomica dominante)
Sezione intitolata “ADOA (atrofia ottica autosomica dominante)”Neuropatia ottica ereditaria più frequente, causata principalmente da mutazione del gene OPA1. Viene scoperta in età scolare come disturbo bilaterale dello sviluppo visivo di origine sconosciuta. Caratteristica è la tritanopia acquisita (cecità ai colori blu-giallo). All’OCT si osserva un assottigliamento dello strato delle fibre nervose retiniche (RNFL) prevalente nei quadranti temporale e inferiore 2). Attualmente non esiste una terapia efficace; la gestione si basa sulla riabilitazione visiva e sulla consulenza genetica.
6-7. Neuropatia ottica traumatica
Sezione intitolata “6-7. Neuropatia ottica traumatica”Lesione del nervo ottico che si verifica dopo un trauma contusivo della testa o dell’orbita, spesso dovuta a una forza indiretta all’interno del canale ottico. Un calo acuto della vista si manifesta immediatamente dopo la lesione. La frattura del canale ottico viene confermata dalla TC in finestra ossea. Si considera il trattamento con steroidi ad alto dosaggio o la decompressione del canale ottico, ma l’evidenza per entrambi è limitata.
6-8. Neuropatia ottica da radiazioni
Sezione intitolata “6-8. Neuropatia ottica da radiazioni”Si tratta di un danno ischemico tardivo dopo radioterapia per tumori della testa e del collo o dell’orbita. La funzione visiva viene persa attraverso un meccanismo principalmente dovuto a danno endoteliale vascolare. L’esordio avviene da 3 mesi a 9 anni dopo l’irradiazione, più frequentemente tra 10 e 20 mesi, con una media di circa 18 mesi 12). Il rischio aumenta con una dose totale superiore a 50 Gy o una dose singola superiore a 10 Gy. Di solito indolore e con prognosi infausta. Non esiste un trattamento consolidato; l’efficacia di steroidi sistemici, terapia anticoagulante e ossigenoterapia iperbarica è limitata 12). La RM mostra un potenziamento del contrasto corrispondente al nervo ottico.
6-9. その他の特殊な視神経症
Sezione intitolata “6-9. その他の特殊な視神経症”後部虚血性視神経症(PION) 眼窩内後部または管内部の視神経虚血。大量出血・低血圧・脊椎手術・心臓手術後に発症する術後PIGNが代表的である。眼底所見は正常(乳頭変化なし)で急激な視力低下をきたす。対光反射はRAPD陽性となる。有効な治療法は確立されていない。
視神経网膜炎(neuroretinitis) 視神経乳頭浮腫と網膜の星芒状白斑(star figure)が特徴的な症候群。Bartonella henselae(ネコひっかき病)・梅毒・Leber特発性星芒状視神経網膜症などが原因。星芒状白斑は浮腫液が黄斑部でHenle線維層に沿って沈着したものであり、乳頭浮腫が消退する数週間後に出現する。自然寛解傾向があるが、感染症は原因に対する特異的治療を行う。
乳頭血管炎(papillophlebitis) 若年〜壮年者に生じる、視機能障害を伴わない片眼性乳頭浮腫と網膜静脈拡張蛇行を示す症候群。Mariotte盲点の拡大を認めるが矯正視力は正常。眼窩MRIは正常。予後良好で治療不要であるが、うっ血乳頭・視神経炎・虚血性視神経症との鑑別が重要である2)。
免疫チェックポイント阻害薬関連視神経症 がん免疫療法(ニボルマブ・ペムブロリズマブ等)の免疫関連有害事象(irAE)として視神経症が稀に生じる。ステロイドパルス療法で治療し、がん治療との継続可否をオンコロジストと協議する。
視神経症ワンライナーまとめ表
Sezione intitolata “視神経症ワンライナーまとめ表”| Malattia | Lateralità | Dolore | Aspetto della papilla | Campo visivo | Punto chiave |
|---|---|---|---|---|---|
| NAION | Monoculare | Nessuno | Arrossamento e gonfiore (inferiore) | Difetto a fascio orizzontale | Insorgenza al risveglio, disco a rischio3) |
| AAION/GCA | Un occhio → entrambi gli occhi | Nessuno (cefalea, claudicatio mandibolare) | Edema pallido | Variabile (grave) | Massima urgenza, VES/PCR elevati1) |
| Neurite ottica idiopatica | Monoculare | Presente (50%) | Edema o normale | Scotoma centrale | Giovane donna, rischio di transizione verso SM 13) |
| Associato a NMOSD | Tendenza alla bilateralizzazione | Sì | Edema o normale | Variabile (grave) | Anticorpi AQP4 positivi, refrattario5) |
| Associato a MOGAD | Spesso bilaterale | Sì (cefalea) | Edema grave | Variabile | Anticorpi MOG, perineurite6) |
| Compressiva | Monoculare/Bilaterale | Nessuno | Normale o atrofico | Vari | Risonanza magnetica obbligatoria9) |
| Tossica | Entrambi gli occhi | Nessuno | Normale → pallore temporale | Scotoma centro-cecale | Anamnesi sulla sostanza causale2) |
| Nutrizionale | Entrambi gli occhi | Nessuna | Normale → pallore temporale | Scotoma centrale | Carenza di B12/rame |
| LHON | Bilaterale (un occhio prima) | Nessuno | Rossore/telangectasie | Scotoma centrale | Giovane uomo, nessuna perdita fluorescente14) |
| ADOA | Entrambi gli occhi | Nessuno | Pallido | Scotoma centrale | Età scolare, discromatopsia blu-giallo2) |
| Traumatica | Monoculare | Sì (trauma) | Normale | Vari | TC del canale ottico per confermare la frattura |
| Radioterapica | Monoculare/Bilaterale | Nessuno | Normale → Atrofia | Vari | Media 18 mesi12) |
7. Approccio terapeutico
Sezione intitolata “7. Approccio terapeutico”Il trattamento della neuropatia ottica dipende dalla causa e differisce fondamentalmente in base al tipo di malattia. I principi comuni sono indicati di seguito.
Situazioni che richiedono un trattamento di emergenza
Sezione intitolata “Situazioni che richiedono un trattamento di emergenza”- GCA/AAION : Somministrazione sistemica di steroidi ad alto dosaggio (iniziare lo stesso giorno). Non attendere i risultati degli esami 1).
- Compressione acuta : decompressione chirurgica (collaborazione urgente con ORL e neurochirurgia). Nell’aspergillosi invasiva, sospendere gli steroidi e passare agli antimicotici2).
- Traumatica : valutazione dell’indicazione alla decompressione del canale ottico.
Trattamento dell’infiammatoria (neurite ottica)
Sezione intitolata “Trattamento dell’infiammatoria (neurite ottica)”La terapia con boli di steroidi (mPSL 1.000 mg/die × 3 giorni) accelera la velocità di recupero nella fase acuta4). La sola terapia steroidea orale non viene eseguita nella neurite ottica idiopatica perché aumenta il rischio di recidiva (studio ONTT)4). Nella fase acuta di NMOSD si esegue un trattamento a tappe: bolo steroideo → plasmaferesi in caso di risposta insufficiente → immunoterapia di prevenzione delle recidive5). La neurite ottica MOGAD è sensibile agli steroidi, ma una riduzione precoce provoca recidive, pertanto è necessaria una cauta riduzione graduale6).
Trattamento dell’ischemica (NAION)
Sezione intitolata “Trattamento dell’ischemica (NAION)”Nella fase acuta non è stabilito alcun trattamento efficace. La gestione dei fattori di rischio vascolari (ipertensione, diabete, iperlipidemia, sindrome delle apnee notturne) è fondamentale e la prevenzione dell’interessamento dell’occhio controlaterale è l’obiettivo terapeutico. Per quanto riguarda il semaglutide (agonista del recettore GLP-1), esistono studi osservazionali che mostrano un’associazione con NAION; nei pazienti con anamnesi o rischio, sono auspicabili una spiegazione attenta e un follow-up7).
Trattamento dell’ereditaria (LHON)
Sezione intitolata “Trattamento dell’ereditaria (LHON)”L’idebenone 900 mg/die è approvato dall’EMA europea e ha raggiunto un CRR del 46% nello studio LEROS (confronto con placebo) 10). La coorte gallese ha riportato un CRR dell’86% a 27 mesi, mostrando buoni risultati nella pratica clinica 10). La terapia genica (lenadogene nolparvovec) ha mostrato efficacia in uno studio di fase III e ci si aspetta un’estensione delle indicazioni 11). La consulenza per la cessazione del fumo (il fumo è un fattore di rischio per l’insorgenza) e un’adeguata assistenza per l’ipovisione sono essenziali 14).
Trattamento delle neuropatie tossiche e nutrizionali
Sezione intitolata “Trattamento delle neuropatie tossiche e nutrizionali”Il trattamento di base consiste nell’interruzione della sostanza causale o nella supplementazione dei nutrienti carenti. Un intervento precoce può portare al recupero della funzione visiva, ma i casi cronici possono lasciare danni irreversibili. La neuropatia ottica da etambutolo è dose-dipendente, pertanto sono indispensabili un esame visivo di base prima del trattamento e un monitoraggio regolare (acuità visiva, visione dei colori, campo visivo).
Trattamento delle neuropatie compressive
Sezione intitolata “Trattamento delle neuropatie compressive”Il principio è la rimozione chirurgica della lesione causale. Nella neuropatia ottica tiroidea si esegue una decompressione orbitaria d’urgenza o elettiva. Dopo l’avanzamento dell’atrofia ottica, il recupero visivo dopo la rimozione chirurgica è limitato, quindi sono importanti una diagnosi e un trattamento precoci.
Panoramica della prognosi
Sezione intitolata “Panoramica della prognosi”| Tipo di malattia | Prognosi visiva | Possibilità di recupero |
|---|---|---|
| Neurite ottica idiopatica | Oltre il 90% ha un visus ≥ 0,5 dopo 1 anno4) | Buon recupero |
| NAION | 1/3 miglioramento, 1/3 invariato, 1/3 peggioramento | Recupero parziale |
| AAION/GCA | Il recupero dell’occhio colpito è quasi impossibile | La prevenzione dell’occhio controlaterale è l’obiettivo1) |
| NMOSD correlato | Grave. Almeno un occhio ≤ 20/200 nel 60-69%5) | Prevenzione delle recidive importante |
| LHON (mt11778) | Acuità visiva finale spesso intorno a 0.01 | Recupero spontaneo solo parziale14) |
| LHON (mt14484) | Tipo di mutazione con il più alto tasso di recupero spontaneo | Casi di recupero segnalati14) |
| ADOA | Progressione lenta, raramente porta a cecità grave | Nessuna inibizione della progressione |
| Da compressione | Recuperabile con rimozione precoce | Prima della progressione dell’atrofia |
| Tossica o nutrizionale | Recupero con sospensione precoce o supplementazione | Irreversibile nei casi cronici |
| Radioterapica | Spesso perdita visiva acuta, grave e irreversibile 12) | Nessuna terapia consolidata |
La rapida identificazione della malattia causale. In caso di sospetto di GCA, iniziare gli steroidi lo stesso giorno senza attendere i risultati degli esami per prevenire la cecità dell’altro occhio 1). In caso di compressione, la rimozione chirurgica della lesione causale è l’unico modo per preservare la funzione visiva, e un ritardo nella diagnosi porta ad atrofia ottica irreversibile. Nelle forme infiammatorie (neurite ottica), la terapia steroidea in bolo accelera il recupero, ma la strategia terapeutica aggiuntiva varia notevolmente a seconda del sottotipo. In particolare, in caso di positività agli anticorpi anti-AQP4, gli steroidi da soli portano a recidive ripetute, quindi l’introduzione precoce di una immunoterapia preventiva delle recidive è fondamentale per preservare la funzione visiva 5).
Entrambe presentano sintomi iniziali simili di ‘riduzione della vista indolore acuta-subacuta’ e sono facilmente confuse, specialmente nella fase acuta della LHON a causa del gonfiore papillare. Il punto di differenziazione più importante è la presenza o assenza di perdita di fluoresceina dalla papilla all’angiografia con fluoresceina. La neurite ottica infiammatoria mostra enhancement e perdita di fluoresceina, mentre nella fase acuta della LHON non c’è perdita di fluoresceina 14). Inoltre, nella neurite ottica si osserva dolore oculare al movimento in circa il 50% dei casi, mentre la LHON è indolore. La diagnosi definitiva può essere ottenuta tramite test genetico mitocondriale (mt11778, mt14484, mt3460), eseguibile come esame esterno 14). La somministrazione di steroidi ai pazienti con LHON non solo è inefficace, ma ritarda anche la diagnosi definitiva, pertanto nei giovani maschi con riduzione acuta bilaterale della vista è essenziale includere la LHON nella diagnosi differenziale.
8. Articoli correlati (neuropatie ottiche)
Sezione intitolata “8. Articoli correlati (neuropatie ottiche)”Neuropatia ottica ischemica anteriore arteritica (AAION)
Neuropatia ottica compressiva
Neuropatia ottica tossica
Neuropatia ottica da carenza nutrizionale
Neuropatia ottica ereditaria di Leber (LHON)
Atrofia ottica autosomica dominante (ADOA)
Neuropatia ottica da radiazioni
Malattie e tumori del nervo ottico da differenziare
Sezione intitolata “Malattie e tumori del nervo ottico da differenziare”Neurite ottica idiopatica
Neurite ottica associata a SM
Neuromielite ottica (NMOSD)
Malattia associata agli anticorpi MOG (MOGAD)
Riferimenti bibliografici
Sezione intitolata “Riferimenti bibliografici”- Piccus R, Hansen MS, Hamann S, et al. An update on the clinical approach to giant cell arteritis. Eye 2023.
- Biousse V, Newman NJ. Diagnosis and clinical features of common optic neuropathies. Lancet Neurol 2016;15:1355–67.
- Salvetat ML, Pellegrini F, Spadea L, et al. Non-Arteritic Anterior Ischemic Optic Neuropathy (NA-AION): A Comprehensive Overview. Vision 2023;7:72.
- Beck RW, Gal RL. The Optic Neuritis Treatment Trial: a report on the visual function at 15 years. Ophthalmology 2008;115:1079–82.
- Wingerchuk DM, Banwell B, Bennett JL, et al. International consensus diagnostic criteria for neuromyelitis optica spectrum disorders. Neurology 2015;85:177–89.
- Jeyakumar N, Lerch M, Dale RC, Ramanathan S. MOG antibody-associated optic neuritis. Eye 2024.
- Hathaway JT, Shah MP, Hathaway DB, et al. Risk of nonarteritic anterior ischemic optic neuropathy in patients prescribed semaglutide. JAMA Ophthalmol. 2024;142:740-741. PMID: 38958939. doi:10.1001/jamaophthalmol.2024.2514.
- Thompson AJ, Banwell BL, Barkhof F, et al. Diagnosis of multiple sclerosis: 2017 revisions of the McDonald criteria. Lancet Neurol 2018;17:162–73.
- Biousse V, Newman NJ. Compressive Optic Neuropathies. J Neuroophthalmol 2015;35 Suppl 1:S67–S74.
- Sanders FWB, Votruba M. Outcomes of idebenone therapy for Leber hereditary optic neuropathy in a cohort of patients from Wales. Eye 2025.
- Newman NJ, et al. Hereditary optic neuropathy: advances in treatment. Eye 2024.
- Danesh-Meyer HV. Radiation-induced optic neuropathy. J Clin Neurosci 2008;15:95–100.
- Toosy AT, Mason DF, Miller DH. Optic neuritis. Lancet Neurol 2014;13:83–99.
- Carelli V, Ross-Cisneros FN, Sadun AA. Mitochondrial dysfunction as a cause of optic neuropathies. Prog Retin Eye Res 2004;23:53–89.
