Nicht-arteriitische anteriore ischämische Optikusneuropathie (NAION)

Optikusneuropathie
1. Was ist eine Optikusneuropathie?
Abschnitt betitelt „1. Was ist eine Optikusneuropathie?“Die Optikusneuropathie ist ein Sammelbegriff für eine Gruppe von Erkrankungen, bei denen der Sehnerv geschädigt ist und die Sehfunktion beeinträchtigt wird. Sie äußert sich in einer verminderten Sehschärfe, Gesichtsfeldausfällen, Farbsehstörungen und/oder einer verminderten Kontrastempfindlichkeit 2).
視神経は網膜神経節細胞(RGC)の軸索約120万本から構成される。眼球内で視神経乳頭として束ねられ、視神経管を経て視交叉に至る。視神経乳頭から視交叉前までの障害が「前部視路障害」であり、臨床的に問題となる視神経症の大半がこの部位に相当する2)。視交叉以降(視索・視放線・後頭葉)の障害は「後部視路障害」であり、視神経症ではなく「視路障害」として扱われる。
視神経は4区分に分けられる。眼球内部(乳頭部、約1 mm)は虚血性・炎症性視神経症が好発する。眼窩内部(約25 mm)は圧迫性・炎症性が多い。管内部(視神経管、約5〜8 mm)は外傷性や骨性圧迫が起きやすい。頭蓋内部(約10 mm)は下垂体腺腫や頭蓋咽頭腫による圧迫が多い。視神経乳頭を直接観察できる「前部視神経症」と、眼底が正常に見える「球後視神経症」の区別も重要である。球後視神経症では眼底に乳頭変化がないため、視力低下の原因として見落とされやすい。
視神経乳頭の血流は短後毛様動脈(SPC動脈)が主として担っている。SPC動脈は眼動脈の終枝であり、視神経乳頭前層部・篩状板・篩状板後部に血流を供給する。この部分の循環障害がNAIONおよびAAIONの主要な病態基盤となる3)。視神経内部は血液脳関門によって保護されているが、この保護機構が炎症性視神経炎や自己免疫疾患では破綻する2)。
病態の共通経路と視神経萎縮
Abschnitt betitelt „病態の共通経路と視神経萎縮“原因が異なっても、最終的には網膜神経節細胞および視神経軸索のダメージ→アポトーシス→視神経萎縮という共通経路をたどる。視神経萎縮(optic atrophy)は視神経症の終末像であり、乳頭の蒼白化として認識される。萎縮が確立すると視機能の回復は著しく限定的となる2)。
視神経軸索は直径0.2〜10 μmの有髄・無髄線維の混合体であり、p細胞(輝度・コントラスト担当)とm細胞(動き・輪郭担当)に大別される。視神経症では特にATP消費の激しいp細胞が障害されやすく、中毒性・栄養性視神経症での中心暗点の発生機序と関連する2)。
Epidemiologischer Überblick
Abschnitt betitelt „Epidemiologischer Überblick“Überblick über die jährliche Inzidenz der wichtigsten Optikusneuropathien (pro 100.000 Erwachsene). NAION ist mit 2,3–10,2 (USA) am häufigsten3). Die idiopathische Optikusneuritis wird mit 1,6 (japanische Erwachsene) angegeben13), und LHON (Lebersche hereditäre Optikusneuropathie) hat in Japan etwa 117 Neuerkrankungen pro Jahr (Erhebung 2014) und gilt als seltene Erkrankung14). Die geschätzte jährliche Inzidenz von AAION/GCA beträgt bei über 50-Jährigen 0,36 pro 100.000, häufiger bei nordischen Weißen (in Norwegen etwa 30 pro 100.000). Visuelle Komplikationen der GCA treten bei 10–30 % (in einigen Berichten bis zu 70 %) auf, wobei AAION 60–90 % davon ausmacht1). Die jährliche Inzidenz von MOGAD wird auf 1,6–4,8 pro Million geschätzt6).
Klassifikation der Optikusneuropathien
Abschnitt betitelt „Klassifikation der Optikusneuropathien“Optikusneuropathien werden aus mehreren Perspektiven klassifiziert. Die klinisch nützlichste Klassifikation ist unten dargestellt.
Klassifikation nach Beginnmuster
- Akut (Stunden bis Tage): NAION, AAION, traumatisch
- Subakut (Tage bis Wochen): idiopathische Optikusneuritis, LHON, kompressiv (teilweise)
- Chronisch (Monate bis Jahre): ADOA, chronisch kompressiv, strahleninduziert (spät)
Klassifikation nach Ursache
- Ischämisch: NAION, AAION, PION
- Entzündlich (Optikusneuritis): idiopathisch, MS-assoziiert, NMOSD-assoziiert, MOGAD-assoziiert, infektiös
- Kompressiv: Tumor, Zyste, Aneurysma, endokrine Orbitopathie
- Toxisch: Ethambutol, Amiodaron, Alkohol usw.
- Nutritionell: Vitamin-B12/B1-, Folsäure-, Kupfermangel
- Hereditär: LHON, ADOA, Wolfram-Syndrom
- Traumatisch: Optikuskanalfraktur, direkte Verletzung
- Strahlenbedingt: verzögerte ischämische Degeneration
Klassifikation nach Lokalisation
- Vordere Optikusneuropathie (mit Papillenveränderungen): NAION, AAION, vordere Optikusneuritis
- Retrobulbäre Optikusneuropathie (normale Papille): toxisch, hereditär, MS-assoziierte Optikusneuritis (meistens)
- Chiasmaläsion: Hypophysenadenom, Kraniopharyngeom (bitemporale Hemianopsie)
Diagnostischer Rahmen der Optikusneuropathie
Abschnitt betitelt „Diagnostischer Rahmen der Optikusneuropathie“Die Diagnose einer Optikusneuropathie erfolgt in 5 Schritten.
Schritt 1: Bestätigung der Sehnervenfunktionsstörung Verwenden Sie RAPD, Sehschärfe, Farbsehen und Gesichtsfeld, um die Sehnervenfunktionsstörung objektiv zu bestätigen.
Schritt 2: Lokalisation der Läsion Vorderer Abschnitt (mit Papillenveränderung) oder retrobulbär (Papille normal), intraorbital, intrakanalikulär oder intrakraniell. Lokalisation anhand des Gesichtsfeldausfallmusters abschätzen.
Schritt 3: Ein- oder beidseitig? Akut oder chronisch? Dadurch kann die Differenzialdiagnose erheblich eingegrenzt werden.
Schritt 4: Ausschluss gefährlicher Formen Prioritär ausschließen: GCA (BSG, CRP), kompressive Ursachen (MRT), infektiöse Ursachen (Syphilis, Pilze).
Schritt 5: Spezifische Untersuchungen Je nach Form Anti-AQP4-Antikörper, Anti-MOG-Antikörper, mtDNA-Test und Ernährungstests hinzufügen.
2. Unterschied zur Optikusneuritis (Begriffsklärung)
Abschnitt betitelt „2. Unterschied zur Optikusneuritis (Begriffsklärung)“Die „Optikusneuritis“ und die „Optikusneuropathie“ werden im klinischen Alltag oft verwechselt, stehen jedoch in einem Verhältnis von Unter- und Oberbegriff.
Wenn eine nicht-entzündliche Optikusneuropathie (ischämisch, kompressiv, toxisch, hereditär) mit einer Optikusneuritis verwechselt wird, besteht die Gefahr einer falschen Steroidgabe. Insbesondere bei der infiltrativen Aspergillose sind Steroide kontraindiziert 2), und die Gabe von Steroiden in der akuten Phase der LHON ist nicht nur unwirksam, sondern führt auch zu einer verzögerten endgültigen Diagnose.
Wichtigste klinische Merkmale der Optikusneuritis
Abschnitt betitelt „Wichtigste klinische Merkmale der Optikusneuritis“Die Optikusneuritis (entzündlich) weist folgende Merkmale auf, die zur Abgrenzung von der nicht-entzündlichen Form beitragen.
- Akuter Beginn : Progression über einige Tage bis 2 Wochen, danach Erholungstendenz innerhalb von 5 Wochen.
- Bulbusschmerz bei Bewegung : bei etwa 50 % vorhanden. Bei ischämischer, kompressiver oder toxischer Genese fehlt er meist.
- Häufigkeitsgipfel : 15–45 Jahre (ischämische Form meist ab 50 Jahren).
- MRT-Befund : typisches Kontrastmittel-Enhancement des N. opticus (Gadolinium-verstärktes T1).
- Spontanerholung : Bei idiopathischer oder MS-assoziierter Optikusneuritis erreichen über 90 % nach einem Jahr einen Visus von 0,5 oder besser (ONTT-Studie)4).
- MS-Übergangsrisiko: 15 Jahre nach Erstmanifestation entwickeln 25 % ohne und 78 % mit Hirn-MRT-Läsionen eine MS4).
Schwierige Differenzialsituationen
Abschnitt betitelt „Schwierige Differenzialsituationen“Im Folgenden wird die Unterscheidung zwischen Optikusneuritis und nicht-entzündlicher Optikusneuropathie erschwert.
- Akute einseitige Sehverschlechterung bei Frauen über 50: NAION vs. AQP4-Antikörper-positive Optikusneuritis (NMOSD)
- Akute beidseitige Sehverschlechterung bei jungen Erwachsenen: LHON vs. simultane beidseitige Optikusneuritis vs. toxische Optikusneuropathie
- Einseitige Sehverschlechterung mit Papillenödem: NAION vs. anteriore Optikusneuritis vs. Papillenvaskulitis
Die AQP4-Antikörper-positive Optikusneuritis ist eine steroidresistente, schwer behandelbare Erkrankung, die etwa 10 % der idiopathischen Optikusneuritiden ausmacht, mit einem höheren Erkrankungsalter als bei der typischen Optikusneuritis und einem Überwiegen von Frauen (Frauen:Männer-Verhältnis 1:9) 5). AQP4-Antikörper richten sich gegen Aquaporin-4-Kanäle auf Astrozyten im Sehnerv und verursachen eine komplementabhängige Zellschädigung 5). Da sich die Behandlungsstrategien zwischen AQP4-Antikörper-positiven und -negativen Fällen grundlegend unterscheiden, sollte vor der Steroidpulstherapie ein Antikörpertest angefordert werden. Der zellbasierte Assay (CBA) hat eine höhere Sensitivität und Spezifität als der ELISA, und die CBA wird empfohlen 5).
Vor der Durchführung einer Steroidpulstherapie bei Optikusneuritis müssen Infektionen (Hepatitis B, Syphilis, HIV, Pilzinfektionen) zwingend ausgeschlossen werden 2). Die Gabe hoher Steroiddosen an Hepatitis-B-Virusträger kann eine fulminante Hepatitis auslösen. Bei syphilitischer Optikusneuritis werden Antibiotika vor Steroiden eingesetzt.
3. Dringliche Krankheitsformen
Abschnitt betitelt „3. Dringliche Krankheitsformen“Die folgende Tabelle zeigt die Krankheitsformen der Optikusneuropathie, die eine besonders dringende Behandlung erfordern.
| Krankheitsform | Dringlichkeit | Folgen bei Übersehen |
|---|---|---|
| Arteriitische anteriore ischämische Optikusneuropathie (AAION/GCA) | Höchste Dringlichkeit | Erblindung des Partnerauges (unbehandelt 65% innerhalb von 10 Tagen) 1) |
| Akute kompressive Optikusneuropathie (Tumor, Zyste, Hämatom) | Dringend | Progressive Optikusatrophie und irreversible Sehstörung |
| Nasale Optikusneuropathie (infiltrative Aspergillose) | Notfall | Berichtete Mortalität von 94% 2) |
| Traumatische Optikusneuropathie (Optikuskanalfraktur) | Notfall | Frühbehandlung kann Sehfunktion erhalten |
| Posteriore ischämische Optikusneuropathie (PION) | Notfall | Tritt nach Operation oder massivem Blutverlust auf, oft irreversibel |
GCA-Notfallablauf
Abschnitt betitelt „GCA-Notfallablauf“Eine Amaurosis fugax tritt bei etwa 30 % der Fälle von dauerhaftem Sehverlust als Prodromalsymptom auf, durchschnittlich 8,5 Tage zuvor 1). Zu diesem Zeitpunkt ist es äußerst wichtig, eine Riesenzellarteriitis (RZA) zu vermuten und aktiv mit Steroiden zu beginnen, um eine Sekundärprävention zu erreichen.
4. Einstieg in die Differenzialdiagnose
Abschnitt betitelt „4. Einstieg in die Differenzialdiagnose“Die Differenzialdiagnose der Optikusneuropathie wird systematisch anhand von vier Achsen geordnet: akut oder chronisch, ein- oder beidseitig, Vorhandensein von Schmerzen und Papillenbefund.
Akut oder chronisch
Abschnitt betitelt „Akut oder chronisch“Akut (Erreichen des maximalen Schadens innerhalb von Stunden bis Tagen)
- NAION: Plötzliche Sehverschlechterung beim Aufwachen, typisch
- AAION: Akute einseitige Sehverschlechterung, schwer (Sehschärfe unter 20/200 bei über 60 %) 1)
- Traumatisch: unmittelbar bis wenige Stunden nach dem Trauma
Subakut (Tage bis Wochen)
- Idiopathische Optikusneuritis: Progression über 2 Wochen, dann beginnende Erholung
- LHON: Schmerzlose subakute Sehverschlechterung eines Auges, nach Wochen bis Monaten beidseitig
- Kompression: Kann durch schnelles Tumorwachstum oder Blutung subakut fortschreiten
Chronisch (langsame Progression über Monate bis Jahre)
- ADOA (autosomal-dominante Optikusatrophie): Beginn im Schulalter, beidseitig langsam fortschreitend
- Chronische Kompression: durch Hypophysenadenom, Orbitatumor usw.
- Toxisch/ernährungsbedingt: subakuter bis chronischer Verlauf bei langer Exposition oder Mangelernährung
Ein Auge oder beide Augen
Abschnitt betitelt „Ein Auge oder beide Augen“Erkrankungen mit einseitiger Betonung
- NAION: in der Regel einseitig (gleichzeitiges Auftreten beidseits extrem selten)
- AAION: beginnt einseitig, unbehandelt breitet es sich bei 65 % innerhalb von 10 Tagen auf das andere Auge aus1)
- Idiopathische Optikusneuritis / MS-assoziiert: typischerweise einseitig
- Kompression, Trauma, Strahlung: meist einseitig
Erkrankungen mit Neigung zu beidseitigem Auftreten
- LHON: zunächst einseitig, nach Wochen bis Monaten beidseitig (letztlich fast 100 % beidseitig)
- ADOA: beidseitig symmetrischer Beginn
- Toxisch/ernährungsbedingt: grundsätzlich beidseitig (bei völlig normalem einem Auge sollte eine toxische Ursache in Betracht gezogen werden) 2)
- NMOSD/AQP4-IgG-positiv: schwer, beidseitig, rezidivierend. 60–69 % haben eine dauerhafte Sehbehinderung von ≤ 20/200 auf mindestens einem Auge 5)
- MOGAD: beidseitiger Beginn häufig (bei MS-assoziierter/idiopathischer Optikusneuritis äußerst selten) 6)
Vorhandensein oder Fehlen von Schmerzen
Abschnitt betitelt „Vorhandensein oder Fehlen von Schmerzen“| Mit Schmerzen | Schmerzfrei (schmerzlos) |
|---|---|
| Idiopathische Optikusneuritis (Augenbewegungsschmerz bei etwa 50 %)13) | NAION (keine Augenschmerzen, Kopfschmerzen und Kieferclaudication sind systemische Symptome der GCA) |
| MS-assoziierte Optikusneuritis | AAION (keine Augenschmerzen, Kieferclaudication und Kopfschmerzen vorhanden) |
| NMOSD-assoziiert (periorbitaler Schmerz) | LHON·ADOA (schmerzlos) 14) |
| MOGAD (häufig mit Kopfschmerzen) 6) | toxisch·ernährungsbedingt (kein Augenschmerz bei Bewegung) |
| traumatisch (Schmerz durch Verletzung) | kompressiv (meist schmerzlos, aber gelegentlich Orbitalschmerz) |
Klassifikation basierend auf Papillenbefunden
Abschnitt betitelt „Klassifikation basierend auf Papillenbefunden“5. Untersuchung und Tests
Abschnitt betitelt „5. Untersuchung und Tests“Obligate augenärztliche Beurteilung
Abschnitt betitelt „Obligate augenärztliche Beurteilung“Bei Verdacht auf Optikusneuropathie sind die folgenden Untersuchungen systematisch durchzuführen.
Sehschärfe und Farbsehen Die korrigierte Sehschärfe ist die Grundlage für die Beurteilung des Schweregrads und des Verlaufs der Beeinträchtigung. Das Farbsehen (Ishihara, Farnsworth-Munsell 100 Hue) ist bei Optikusneuropathien frühzeitig beeinträchtigt, und Farbsehstörungen können einer verminderten Sehschärfe vorausgehen. Bei toxischen und nutritiven Optikusneuropathien ist eine verminderte Rotempfindlichkeit ein frühes Zeichen2). Bei ADOA (autosomal-dominante Optikusatrophie) ist eine erworbene Tritanomalie (Blau-Gelb-Störung) charakteristisch, die im Farnsworth-Munsell 100-Hue-Test eine Tritan-Achse zeigt2).
RAPD (relativer afferenter Pupillendefekt)
Der RAPD wird mit der Swing-Flashlight-Methode (Wechselbelichtungstest) beurteilt und ist ein objektiver Indikator für eine Funktionsstörung des Sehnervs. Er hilft auch bei der Unterscheidung von Simulation und funktionellen Sehstörungen2).
OCT (optische Kohärenztomographie)
Abschnitt betitelt „OCT (optische Kohärenztomographie)“Die OCT ist eine unverzichtbare Untersuchung zur Stadienbeurteilung und Verlaufskontrolle der Optikusneuropathie.
| Bewertungsindikator | Akute Befunde | Chronische Befunde |
|---|---|---|
| pRNFL (peripapilläre RNFL-Dicke) | Verdickung bei Papillenödem (Achtung falsch positiv) | Ausdünnung bei Optikusatrophie |
| GCL-IPL (Ganglienzell- + innere plexiforme Schichtdicke) | Wenig Veränderung | Ausdünnung als Zeichen einer retinalen Ganglienzellschädigung |
| Form der Papille | Verschwinden oder Verkleinerung der Exkavation | Fixierung nach Atrophie |
Muster der pRNFL-Ausdünnung und Differentialdiagnose
Das Muster der pRNFL-Ausdünnung im OCT ist ab einigen Wochen bis Monaten nach Beginn für die Differentialdiagnose nützlich.
- Zirkuläre hochgradige Ausdünnung: NMOSD (AQP4-Antikörper-positiver Typ) ist am schwersten. Hochgradige Ausdünnung im gesamten Umfang.
- Temporal betonte Ausdünnung (papillomakuläres Bündel) : toxisch, nutritiv, LHON, ADOA. Korrespondiert mit Zentralskotom.
- Obere oder untere sektorförmige Ausdünnung : NAION. Korrespondiert mit oberem oder unterem Bündeldefekt.
- MOGAD vs. MS-assoziiert : Die pRNFL-Ausdünnung nach MOG-ON ist stärker ausgeprägt als bei MS6).
- Abgrenzung zum Glaukom : Beim Glaukom treten zuerst Veränderungen der Papillenform (Exkavationsvergrößerung) auf, und das GCL-Ausdünnungsmuster ist unterschiedlich.
Gesichtsfelduntersuchung (Humphrey-Perimeter)
Abschnitt betitelt „Gesichtsfelduntersuchung (Humphrey-Perimeter)“Das Muster des Gesichtsfeldausfalls steht in direktem Zusammenhang mit der anatomischen Lokalisation der Läsion.
| Gesichtsfeldausfallmuster | Hauptverdachtsdiagnose | Anatomische Korrelation |
|---|---|---|
| Zentralskotom, blindfleckzentriertes Skotom | Toxisch, ernährungsbedingt, LHON, ADOA, idiopathische Optikusneuritis2) | Schädigung des papillomakulären Bündels (PMB) |
| Horizontaler Ausfall (unter-temporal bis unten) | NAION (bündelförmiger Faserverlust) 3) | Ischämie der oberen oder unteren Papillenhälfte |
| Bitemporale Hemianopsie | Chiasma-Kompression (Hypophysenadenom, Kraniopharyngeom) | Zentrale Kreuzungsfasern des Chiasmas |
| Homonyme Hemianopsie (gleiche Seite) | Postchiasmatische Läsion (Sehbahn, Sehstrahlung, Hinterhauptslappen) | Zentrale Sehbahn |
| Junktionsskotom | Läsion des vorderen Chiasmaabschnitts, eine Form der nasalen Optikusneuropathie | Papillomakuläres Bündel + kontralateraler oberer temporalen Quadrant |
| Allgemeine Empfindlichkeitsminderung | NMOSD-assoziiert / nach schwerer Optikusneuritis5) | Ausgedehnte Schädigung der Sehnervenfasern |
| Vergrößerung des Mariotte-Blinden Flecks (normale Sehschärfe) | Papillendrusen, Papillitis, Perineuritis des Sehnervs | Nur um die Papille herum |

Blut- und Liquoruntersuchungen
Abschnitt betitelt „Blut- und Liquoruntersuchungen“Empfohlene Tests zur Erstbeurteilung einer akuten Optikusneuropathie.
| Testparameter | Zweck | Klinische Bedeutung |
|---|---|---|
| BSG, CRP, Thrombozyten | Ausschluss einer GCA (AAION) | Höchste Priorität. CRP hat eine höhere Spezifität als BSG 1) |
| Anti-AQP4-Antikörper (zellbasierter Assay) | NMOSD-Diagnose | Die ELISA-Methode hat eine geringere Sensitivität und Spezifität als die CBA-Methode 5) |
| Anti-MOG-Antikörper (zellbasierter Assay) | MOGAD-Diagnose | Ein CBA, der das native MOG-Molekül erkennt, ist obligatorisch6) |
| Syphilisserologie (TPHA, RPR) und HIV | Ausschluss einer infektiösen Optikusneuritis | Vor Steroiden unbedingt überprüfen |
| Vitamin B12, B1, Folsäure, Kupfer | Beurteilung der nutritionellen Optikusneuropathie | Besonders wichtig nach bariatrischer Operation oder veganer Ernährung |
| Mitochondriale Gene (mt11778, mt14484, mt3460) | LHON-Diagnose | Diese 3 Mutationen decken über 95% aller Fälle ab14) |
| β-D-Glucan und Pilzkultur | Verdacht auf invasive Aspergillose | Bei invasiver Form häufig erhöht2) |
| ACE, Lysozym, Thorax-CT | Ausschluss einer Sarkoidose | — |
| ANA, dsDNA, ANCA | Systemische Autoimmunerkrankungen (SLE, Vaskulitis) | — |
Indikationen für Liquoruntersuchung Verdacht auf infektiöse Meningitis/Enzephalitis, Diagnosehilfe bei NMOSD/MOGAD (Liquorpleozytose, erhöhter IgG-Index), Diagnosehilfe bei MS (oligoklonale Banden im Liquor). Bei NMOSD kann eine ausgeprägte Pleozytose von bis zu 50 Zellen/μL oder mehr auftreten6).
Bildgebende Untersuchungen
Abschnitt betitelt „Bildgebende Untersuchungen“| Untersuchung | Hauptbewertungsinhalte | Besondere Hinweise |
|---|---|---|
| Orbitale MRT (fettunterdrückte T2/Kontrast-T1) | Entzündung, Ödem, Raumforderung, Kontrastmittelanreicherung des Sehnervs | Kontrastmittelanreicherung bei Optikusneuritis. Keine Anreicherung in der akuten Phase der LHON14) |
| Kopf-MRT (FLAIR) | Demyelinisierende Läsionen (MS, NMOSD), intrakranielle Läsionen | Verwendung in den McDonald-Kriterien für die MS-Diagnose |
| CT (Knochenfenster) | Optikuskanalfraktur (Trauma), Nasennebenhöhlenerkrankung, Verkalkung (Drusen) | Bei Trauma oder nasalen Erkrankungen obligat |
| Kopfultraschall (Farbdoppler) | Halo-Zeichen zur GCA-Diagnose | Sensitivität 68%, Spezifität 91% (100% bei beidseitig positiv) 1) |
| PET-CT (FDG) | Beurteilung von Großgefäßläsionen bei GCA | Sensitivität 92%, Spezifität 85% (GAPS-Studie)1) |
| Orbitasonographie | Bestätigung der Verkalkung von Drusen der Papille | — |
Bei einer akuten Optikusneuropathie ist grundsätzlich eine MRT der Orbita erforderlich. Der Ausschluss einer raumfordernden Läsion hat höchste Priorität, und die Therapiestrategie unterscheidet sich erheblich, je nachdem, ob eine Kontrastmittelanreicherung (entzündlich) entsprechend des Sehnervs oder eine Kompression/Deformierung (kompressiv) vorliegt 2). Zeigt die kontrastmittelverstärkte MRT keine entzündlichen Veränderungen des Sehnervs, werden toxische, hereditäre oder nutritive Ursachen in Betracht gezogen. Im akuten Stadium der LHON gibt es keine entzündlichen Befunde, und auch in der Fluoreszenzangiographie zeigt sich keine Leckage aus der Papille, was ein wichtiges Unterscheidungsmerkmal zur entzündlichen Optikusneuritis darstellt 14). Bei Kontraindikationen für die MRT wird eine CT der Nasennebenhöhlen, der Orbita und des Sehnervenkanals durchgeführt.
Nutzung visuell evozierter Potenziale (VEP)
Abschnitt betitelt „Nutzung visuell evozierter Potenziale (VEP)“Visuell evozierte Potenziale (VEP) sind als Marker für eine demyelinisierende Optikusneuritis nützlich. Eine Verlängerung der P100-Latenz (normal ≤130 ms) deutet auf eine Demyelinisierung hin, und bei MS-assoziierter oder idiopathischer Optikusneuritis bleibt diese Verlängerung oft auch nach der Erholung bestehen 13). Eine Amplitudenminderung ist bei axonaler Schädigung (toxisch, ischämisch) deutlich ausgeprägt. Bei toxischer Optikusneuropathie gibt es keine Verzögerung der P100-Latenz, sondern nur eine Amplitudenminderung, was zur Unterscheidung von der demyelinisierenden Neuritis beiträgt 13). Eine Verminderung der kritischen Flimmerfrequenz (CFF) spiegelt ebenfalls die Funktionsstörung der Optikusneuropathie wider und zeigt sich bei NMOSD-assoziierter Optikusneuritis besonders deutlich 13).
6. Merkmale nach Ursache
Abschnitt betitelt „6. Merkmale nach Ursache“Klassifikation der wichtigsten Optikusneuropathien nach Ursache und Zusammenfassung der Merkmale jedes Typs.
6-1. Ischämische Optikusneuropathie
Abschnitt betitelt „6-1. Ischämische Optikusneuropathie“Nicht-arteriitische anteriore ischämische Optikusneuropathie (NAION)
Abschnitt betitelt „Nicht-arteriitische anteriore ischämische Optikusneuropathie (NAION)“Die NAION ist die häufigste Form der akuten Optikusneuropathie bei Erwachsenen und tritt meist nach dem 50. Lebensjahr auf3). Ein ischämischer Infarkt der Papille wird durch eine akute Kreislaufinsuffizienz der kurzen hinteren Ziliararterien (SPC-Arterien) verursacht.
- Epidemiologie : Jährliche Inzidenz in den USA von 2,3 bis 10,2 pro 100.000 Personen3). Die Mehrheit der Fälle tritt nach dem 50. Lebensjahr auf, aber die Inzidenz vor dem 50. Lebensjahr nimmt zu.
- Risikofaktoren : Hypertonie, Diabetes, Hyperlipidämie, Schlafapnoe-Syndrom, Risikopapille (kleine Papille mit C/D-Verhältnis < 0,2). Eine Risikopapille findet sich bei etwa 80 % der Partneraugen3).
- Symptome : Schmerzlose, akute einseitige Sehverschlechterung, die oft beim Aufwachen bemerkt wird. RAPD auf der betroffenen Seite positiv.
- Papillenbefund : Rötung und Schwellung (fächerförmig, unten betont). Kann mit Blutungen einhergehen.
- Gesichtsfeld : horizontales Faserbündeldefekt (typischerweise unterer temporaldefekt).
- Behandlung: In der akuten Phase ist keine wirksame Behandlung etabliert. Die Kontrolle vaskulärer Risikofaktoren und die Behandlung des Schlafapnoe-Syndroms stehen im Mittelpunkt der Rezidivprophylaxe.
- Aktueller Aufmerksamkeitspunkt: Eine Beobachtungsstudie aus dem Jahr 2024 berichtete über ein erhöhtes NAION-Risiko bei Anwendern von Semaglutid (GLP-1-Rezeptoragonist). Ein kausaler Zusammenhang ist jedoch nicht belegt, und bei der Verschreibungsentscheidung muss der Nutzen für die Behandlung von Diabetes und Adipositas abgewogen werden7).
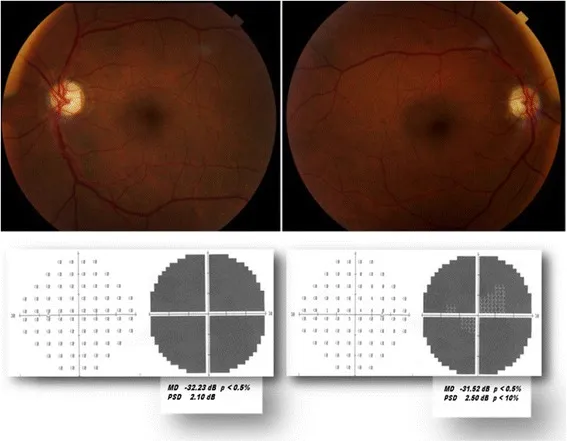
動脈炎性前部虚血性視神経症(AAION/GCA)
Abschnitt betitelt „動脈炎性前部虚血性視神経症(AAION/GCA)“AAIONは前部虚血性視神経症全体の5〜10%を占めるが、最緊急の視神経症である1)。視神経乳頭を栄養する短後毛様動脈の血管炎が本態であり、原疾患の90%以上が巨細胞性動脈炎(GCA)である。
- 疫学:50歳以上(特に75歳以上)の高齢女性に多い(男女比1:3)1)。日本での発症率は10万人あたり1.47人と欧米に比べて極めて低い。
- 症状:急激な片眼重度視力低下(60%以上で視力20/200未満、20%以上で光覚なし)1)。一過性黒内障を約30%が先行して経験する。
- 全身症状:頭痛(65〜90%)・顎跛行(11〜45%)・頭皮圧痛・発熱・PMR様症状。
- Papillenbefund : Kreideartige blasse Schwellung (pallid swelling) ist charakteristisch.
- Untersuchungen : BSG und CRP erhöht (bei über 80% gesteigert)1). Temporalarterienbiopsie (Sensitivität und Spezifität über 95%)1).
- Therapie : Hochdosierte Steroide (mPSL 500-1000 mg i.v. für 3 Tage, dann Prednisolon oral ausschleichend)1). Tocilizumab (IL-6-Rezeptor-Antagonist) ist wirksam zur Steroideinsparung (GiACTA-Studie, RCT-Evidenz)1).
- Prognose : Eine Visuserholung des betroffenen Auges ist kaum zu erwarten, aber die Steroidtherapie ist wirksam zur Verhinderung des Befalls des anderen Auges.
6-2. Entzündliche Optikusneuritis
Abschnitt betitelt „6-2. Entzündliche Optikusneuritis“Idiopathische Optikusneuritis
Abschnitt betitelt „Idiopathische Optikusneuritis“Entzündliche Erkrankung des Sehnervs durch einen Autoimmunmechanismus, die den Großteil der Optikusneuritis ausmacht 13). Das bevorzugte Alter liegt zwischen 15 und 45 Jahren, etwa 70 % sind Frauen, und die jährliche Inzidenz in Japan beträgt 1,6 pro 100.000 Erwachsene 13).
- Symptome : Akute einseitige Sehverschlechterung und Augenschmerzen bei Bewegung (ca. 50 %). Progression über einige Tage bis 2 Wochen, mit Tendenz zur spontanen Erholung innerhalb von 5 Wochen.
- Gesichtsfeld : Häufig zentrales Skotom oder zentrozäkales Skotom.
- MRT : Kontrastmittelanreicherung (Gadolinium) entsprechend dem Sehnerv.
- Prognose : Über 90 % erholen sich nach 1 Jahr auf eine Sehschärfe von ≥ 0,5 (ONTT-Studie) 4).
- Behandlung : Steroid-Pulstherapie mit mPSL 1.000 mg/Tag × 3 Tage beschleunigt die Erholung. Orale Steroid-Monotherapie wird aufgrund erhöhter Rezidivrate nicht durchgeführt (ONTT-Studie) 4).
- MS-Konversionsrisiko: kumulative Inzidenz von 50 % über 15 Jahre nach dem ersten Schub. Keine Läsionen im MRT des Gehirns → 25 %, Läsionen vorhanden → 78 %4).
MS-assoziierte Optikusneuritis
Abschnitt betitelt „MS-assoziierte Optikusneuritis“Als erstes Symptom einer MS tritt eine Optikusneuritis bei etwa 30 % der Patienten auf, und bis zu 75 % der MS-Patienten erleiden im Laufe ihres Lebens mindestens eine Episode einer Optikusneuritis 8). Sie ist meist einseitig, mit Schmerzen bei Augenbewegungen, und häufig liegt eine retrobulbäre Läsion vor (Fundus normal in 65 %). Die demyelinisierenden Läsionen im MRT des Gehirns (T2/FLAIR-Hyperintensität) sind der Schlüssel zur Diagnose. Nach Bestätigung der Diagnose gemäß den McDonald-Kriterien (Version 2017, überarbeitet 2024) wird eine krankheitsmodifizierende Therapie (DMT: Interferon beta, Natalizumab, Fingolimod, Anti-CD20-Medikamente usw.) zur Vorbeugung von Rückfällen eingesetzt.
NMOSD (Neuromyelitis-optica-Spektrum-Erkrankung)-assoziierte Optikusneuritis
Abschnitt betitelt „NMOSD (Neuromyelitis-optica-Spektrum-Erkrankung)-assoziierte Optikusneuritis“AQP4-IgG-positiv. Tritt bevorzugt bei Frauen (Geschlechterverhältnis 1:9), mittleren Alters und asiatischer Abstammung auf und ist schwerer, bilateraler und rezidivierender als MS-assoziierte Optikusneuritis 5). Mindestens 60–69 % entwickeln eine dauerhafte Sehbehinderung von 20/200 oder schlechter auf mindestens einem Auge 5). Die orbitale MRT zeigt eine lange Läsion des Sehnervs (häufig mit Chiasma-Beteiligung). Die Behandlung umfasst eine akute Steroid-Pulstherapie, gefolgt von Plasmaaustausch und dann einer rezidivpräventiven Immuntherapie (Eculizumab, Rituximab, Satralizumab) 5).
MOGAD (MOG-Antikörper-assoziierte Erkrankung) assoziierte Optikusneuritis
Abschnitt betitelt „MOGAD (MOG-Antikörper-assoziierte Erkrankung) assoziierte Optikusneuritis“MOG-IgG-positiv. Jährliche Inzidenz von 1,6 bis 4,8 pro 1 Million Einwohner6). Häufig bilaterales Auftreten mit ausgeprägter Papillenschwellung, überwiegend vorderer Abschnitt betroffen. MRT zeigt Papillenschwellung, langstreckige Sehnervenläsion und Optikusperineuritis6). Geschlechterverhältnis: MS-ON 3:1, AQP4-ON 7-9:1, MOG-ON 1:16). Ansprechbar auf Steroide, aber bei frühem Absetzen leicht rezidivierend, daher vorsichtige Dosisreduktion erforderlich6).
6-3. Kompressive Optikusneuropathie
Abschnitt betitelt „6-3. Kompressive Optikusneuropathie“Verursacht durch Kompression des Sehnervs durch Tumore, Aneurysmen, Hämatome, Abszesse, Zysten oder hypertrophierte äußere Augenmuskeln. Symptome und Gesichtsfeldausfälle variieren stark je nach Kompressionsort.
- Orbitaspitze: Thyreoide Orbitopathie (thyreoide Optikusneuropathie tritt bei 3-8,6 % der thyreoiden Orbitopathie auf, 70 % bilateral), Orbitatumoren (gutartig: idiopathische orbitale Entzündung 20 %, pleomorphes Adenom 13 %, Hämangiom 13 %; bösartig: malignes Lymphom am häufigsten)9).
- Chiasma opticum: Hypophysenadenom (häufigste Ursache bei Erwachsenen, bitemporale Hemianopsie), Kraniopharyngeom (häufigste Ursache bei Kindern).
- Nasale Optikusneuropathie (besondere Erwähnung): Die invasive Form der Pilzsinusitis (Aspergillus, Mucor) hat eine berichtete Mortalität von 94 %2). Steroide wirken vorübergehend, was zu einer Fehldiagnose als retrobulbäre Neuritis führt; eine unbemerkte Fortsetzung der Steroide kann tödlich sein. Knochendestruktion im CT/MRT ist der Schlüssel zur Diagnose, und eine dringende Zusammenarbeit mit HNO ist erforderlich.
Das Behandlungsprinzip ist die chirurgische Entfernung der ursächlichen Läsion. Je früher die Dekompression erfolgt, desto besser ist die Erholung der Sehfunktion; nach Etablierung der Optikusatrophie ist die Erholung begrenzt.
6-4. Toxische Optikusneuropathie
Abschnitt betitelt „6-4. Toxische Optikusneuropathie“Hierbei handelt es sich um eine Gruppe von Erkrankungen, bei denen die vordere Sehbahn durch Exposition gegenüber Chemikalien geschädigt wird2). Sie ist in der Regel beidseitig und schmerzlos; wenn ein Auge völlig normal ist, sollte eine toxische Optikusneuropathie ausgeschlossen werden2).
- Ursächliche Substanzen : Tabak, Alkohol, Lösungsmittel (Medikamente: Ethambutol [am bekanntesten], Amiodaron, Linezolid, Cisplatin, Immunsuppressiva usw.).
- Gesichtsfeld : charakteristischerweise ein zentrozökales Skotom oder Zentralskotom (überwiegende Schädigung der p-Zellen)2).
- Farbsehen : eine verminderte Rotempfindung ist ein frühes Zeichen.
- Fundus : initial normal oder leichte Rötung → in der chronischen Phase temporale Abblassung der Papille und Defekt des papillomakulären Bündels.
- RAPD : aufgrund der bilateralen Symmetrie in der Regel negativ.
- VEP : Amplitudenminderung ohne Verzögerung der P100-Latenz (Latenzverzögerung ist charakteristisch für demyelinisierende Optikusneuritis)13).
- Ethambutol : dosisabhängig (Risikoerhöhung bei >15 mg/kg). Vorbehandlung-Basis-Sehfunktionstest und regelmäßiges Monitoring sind unerlässlich.
- Therapie : Absetzen der verursachenden Substanz ist grundlegend. Es gibt kein spezifisches Medikament.
6-5. Ernährungbedingte Optikusneuropathie
Abschnitt betitelt „6-5. Ernährungbedingte Optikusneuropathie“Es handelt sich um eine beidseitige, symmetrische, fortschreitende Sehnervenschädigung durch Mangel an B-Vitaminen (B12, B1, B2, B9) und Kupfer. Sie liegt im gleichen Spektrum wie die toxische Optikusneuropathie, unterscheidet sich jedoch durch die Ursache des Nährstoffmangels. Moderne Risiken sind bariatrische Chirurgie (lebenslange Überwachung erforderlich), vegane Ernährung und Alkoholabhängigkeit. Symptome, Gesichtsfeld und Fundusbefunde ähneln denen der toxischen Form (zentrales Skotom, schmerzlos, temporale Papillenblässe). Frühe Nährstoffergänzung kann eine Erholung ermöglichen, aber chronische Fälle hinterlassen irreversible Schäden.
6-6. Hereditäre Optikusneuropathie
Abschnitt betitelt „6-6. Hereditäre Optikusneuropathie“LHON (Lebersche hereditäre Optikusneuropathie)
Abschnitt betitelt „LHON (Lebersche hereditäre Optikusneuropathie)“Es handelt sich um eine akute oder subakute Optikusneuropathie, die durch Punktmutationen der mitochondrialen DNA (mtDNA) verursacht wird und maternal vererbt wird14). Die drei Hauptmutationen (mt3460, mt11778, mt14484) machen über 95 % aller Fälle aus, und mt11778 macht in Asien etwa 90 % aller Fälle aus14).
- Epidemiologie: Prävalenz 1/31.000 bis 1/68.000. Penetranz 2,5–17,5 %, die meisten Träger erkranken nicht14). In Japan etwa 117 Neuerkrankungen pro Jahr (Erhebung 2014). Designierte seltene Krankheit.
- Symptome: Tritt vorwiegend bei jungen Männern auf (Geschlechterverhältnis etwa 93:7). Subakutes, schmerzloses beidseitiges zentrales Skotom (ein Auge zuerst, dann innerhalb von Wochen bis Monaten beide Augen).
- 急性期眼底:視神経乳頭の発赤・腫脹と乳頭近傍毛細血管の拡張・蛇行。蛍光眼底造影で乳頭からの蛍光漏出を認めない(炎症性視神経炎との重要鑑別)14)。
- 対光反射:他の視神経疾患に比べて保たれるか、障害されても軽微14)。
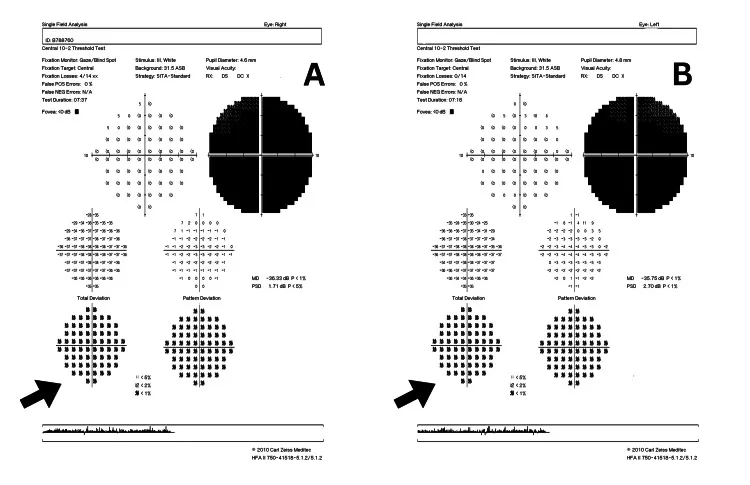
- 最終視力:mt11778では0.01前後が多い。mt14484は自然回復率が最も高い14)。
- 治療:イデベノン900 mg/日(欧州EMA承認)。LEROS試験ではCRR(有意義な視力回復)が46.0%(プラセボ対照)10)。ウェールズコホート試験では27カ月時点でCRR 86%を達成10)。遺伝子治療も第III相試験で有効性を示している11)。禁煙指導が発症・重症化予防に重要。
ADOA (autosomal-dominante Optikusatrophie)
Abschnitt betitelt „ADOA (autosomal-dominante Optikusatrophie)“Häufigste hereditäre Optikusneuropathie, hauptsächlich verursacht durch OPA1-Genmutation. Sie wird im Schulalter als beidseitige Sehentwicklungsstörung unklarer Ursache entdeckt. Erworbene Tritanomalie (Blau-Gelb-Sehstörung) ist charakteristisch. Im OCT zeigt sich eine temporale bis inferiore Quadranten betonende RNFL-Verdünnung 2). Derzeit gibt es keine wirksame Behandlung; die Betreuung umfasst Low-Vision-Versorgung und genetische Beratung.
6-7. Traumatische Optikusneuropathie
Abschnitt betitelt „6-7. Traumatische Optikusneuropathie“Schädigung des Sehnervs nach stumpfem Trauma des Kopfes oder der Augenhöhle, häufig durch indirekte Gewalteinwirkung im Sehnervenkanal. Unmittelbar nach der Verletzung kommt es zu einer akuten Sehverschlechterung. Eine Fraktur des Sehnervenkanals wird im CT-Knochenfenster bestätigt. Eine Behandlung mit hochdosierten Steroiden oder eine Dekompression des Sehnervenkanals wird in Betracht gezogen, jedoch ist die Evidenz für beide begrenzt.
6-8. Strahleninduzierte Optikusneuropathie
Abschnitt betitelt „6-8. Strahleninduzierte Optikusneuropathie“Es handelt sich um eine verzögerte ischämische Störung nach Strahlentherapie von Kopf-Hals-Tumoren oder Orbitatumoren. Der Sehverlust wird hauptsächlich durch eine Schädigung des Gefäßendothels verursacht. Der Beginn liegt zwischen 3 Monaten und 9 Jahren nach Bestrahlung, meist zwischen 10 und 20 Monaten, im Durchschnitt etwa 18 Monate 12). Das Risiko steigt bei einer Gesamtdosis über 50 Gy oder einer Einzeldosis über 10 Gy. In der Regel schmerzlos und mit schlechter Prognose. Es gibt keine etablierte Behandlung; die Wirksamkeit von systemischen Steroiden, Antikoagulation und hyperbarer Sauerstofftherapie ist begrenzt 12). In der MRT zeigt sich eine Kontrastmittelanreicherung entsprechend dem Sehnerv.
6-9. その他の特殊な視神経症
Abschnitt betitelt „6-9. その他の特殊な視神経症“後部虚血性視神経症(PION) 眼窩内後部または管内部の視神経虚血。大量出血・低血圧・脊椎手術・心臓手術後に発症する術後PIGNが代表的である。眼底所見は正常(乳頭変化なし)で急激な視力低下をきたす。対光反射はRAPD陽性となる。有効な治療法は確立されていない。
視神経网膜炎(neuroretinitis) 視神経乳頭浮腫と網膜の星芒状白斑(star figure)が特徴的な症候群。Bartonella henselae(ネコひっかき病)・梅毒・Leber特発性星芒状視神経網膜症などが原因。星芒状白斑は浮腫液が黄斑部でHenle線維層に沿って沈着したものであり、乳頭浮腫が消退する数週間後に出現する。自然寛解傾向があるが、感染症は原因に対する特異的治療を行う。
乳頭血管炎(papillophlebitis) 若年〜壮年者に生じる、視機能障害を伴わない片眼性乳頭浮腫と網膜静脈拡張蛇行を示す症候群。Mariotte盲点の拡大を認めるが矯正視力は正常。眼窩MRIは正常。予後良好で治療不要であるが、うっ血乳頭・視神経炎・虚血性視神経症との鑑別が重要である2)。
免疫チェックポイント阻害薬関連視神経症 がん免疫療法(ニボルマブ・ペムブロリズマブ等)の免疫関連有害事象(irAE)として視神経症が稀に生じる。ステロイドパルス療法で治療し、がん治療との継続可否をオンコロジストと協議する。
視神経症ワンライナーまとめ表
Abschnitt betitelt „視神経症ワンライナーまとめ表“| Erkrankung | Seitigkeit | Schmerz | Papillenbefund | Gesichtsfeld | Schlüsselpunkt |
|---|---|---|---|---|---|
| NAION | Einseitig | Keine | Rötung und Schwellung (unten) | Horizontales Bündeldefekt | Auftreten beim Aufwachen, Risikopapille3) |
| AAION/GCA | Ein Auge → beide Augen | Keine (Kopfschmerzen, Kieferclaudicatio) | Blasse Schwellung | Variabel (schwer) | Höchste Dringlichkeit, BSG/CRP erhöht1) |
| Idiopathische Optikusneuritis | Einseitig | Vorhanden (50%) | Geschwollen oder normal | Zentralskotom | Junge Frau, Risiko eines MS-Übergangs 13) |
| NMOSD-assoziiert | Neigung zur Beidseitigkeit | Ja | Schwellung oder normal | Variabel (schwer) | AQP4-Antikörper positiv, therapierefraktär5) |
| MOGAD-assoziiert | Häufig beidseitig | Ja (Kopfschmerz) | Starke Schwellung | Variabel | MOG-Antikörper, Perineuritis6) |
| Kompression | Ein-/beidseitig | Keine | Normal oder atrophisch | Vielfältig | MRT obligatorisch9) |
| Toxisch | Beide Augen | Keine | Normal → temporale Abblassung | Zentrozökales Skotom | Anamnese zur ursächlichen Substanz2) |
| Ernährungsbedingt | Beide Augen | Keine | Normal → temporale Abblassung | Zentralskotom | B12/Kupfermangel |
| LHON | Beidseitig (ein Auge zuerst) | Keine | Rötung/Telangiektasien | Zentralskotom | Junger Mann, keine Fluoreszenzleckage14) |
| ADOA | Beide Augen | Keine | Blass | Zentralskotom | Schulalter, Blau-Gelb-Farbsehstörung2) |
| Traumatisch | Einseitig | Ja (Trauma) | Normal | Variabel | CT des Sehnervenkanals zur Frakturbestätigung |
| Strahlenbedingt | Einseitig/Beidseitig | Keine | Normal → Atrophie | Vielfältig | Durchschnittlich 18 Monate12) |
7. Behandlungsansätze
Abschnitt betitelt „7. Behandlungsansätze“Die Behandlung der Optikusneuropathie hängt von der Ursache ab und unterscheidet sich grundlegend je nach Krankheitstyp. Die gemeinsamen Prinzipien sind unten aufgeführt.
Situationen, die eine Notfallbehandlung erfordern
Abschnitt betitelt „Situationen, die eine Notfallbehandlung erfordern“- GCA/AAION : Systemische Gabe von hochdosierten Steroiden (Beginn am selben Tag). Warten Sie nicht auf die Untersuchungsergebnisse 1).
- Akute Kompression : chirurgische Dekompression (Notfallkooperation mit HNO und Neurochirurgie). Bei invasiver Aspergillose Steroide absetzen und auf Antimykotika umstellen2).
- Traumatisch : Prüfung der Indikation für eine Dekompression des Sehnervenkanals.
Behandlung der entzündlichen (Optikusneuritis)
Abschnitt betitelt „Behandlung der entzündlichen (Optikusneuritis)“Die Steroid-Pulstherapie (mPSL 1.000 mg/Tag × 3 Tage) beschleunigt die Erholungsgeschwindigkeit in der akuten Phase4). Eine alleinige orale Steroidtherapie wird bei idiopathischer Optikusneuritis nicht durchgeführt, da sie das Rezidivrisiko erhöht (ONTT-Studie)4). In der akuten Phase der NMOSD erfolgt eine stufenweise Behandlung: Steroid-Puls → bei unzureichendem Ansprechen Plasmaaustausch → Rezidivprophylaxe-Immuntherapie5). Die MOGAD-Optikusneuritis spricht auf Steroide an, rezidiviert jedoch bei frühzeitiger Dosisreduktion, sodass eine vorsichtige Ausschleichung erforderlich ist6).
Behandlung der ischämischen (NAION)
Abschnitt betitelt „Behandlung der ischämischen (NAION)“In der akuten Phase ist keine wirksame Behandlung etabliert. Die Behandlung vaskulärer Risikofaktoren (Hypertonie, Diabetes, Hyperlipidämie, Schlafapnoe) steht im Vordergrund, und die Prävention des Befalls des anderen Auges ist das Therapieziel. Zu Semaglutid (GLP-1-Rezeptoragonist) gibt es Beobachtungsstudien, die einen Zusammenhang mit NAION zeigen; bei Patienten mit Vorgeschichte oder Risiko sind sorgfältige Aufklärung und Nachbeobachtung wünschenswert7).
Behandlung der hereditären (LHON)
Abschnitt betitelt „Behandlung der hereditären (LHON)“Idebenon 900 mg/Tag ist von der europäischen EMA zugelassen und erreichte in der LEROS-Studie eine CRR von 46 % (Placebo-kontrollierter Vergleich) 10). Die walisische Kohorte berichtete eine CRR von 86 % nach 27 Monaten, was gute Ergebnisse in der klinischen Praxis zeigt 10). Die Gentherapie (Lenadogen Nolparvovec) zeigte Wirksamkeit in einer Phase-III-Studie, und eine Erweiterung der Indikationen wird erwartet 11). Raucherentwöhnungsberatung (Rauchen ist ein Risikofaktor für die Erkrankung) und angemessene Sehbehindertenversorgung sind unerlässlich 14).
Behandlung toxischer und ernährungsbedingter Neuropathien
Abschnitt betitelt „Behandlung toxischer und ernährungsbedingter Neuropathien“Die Grundbehandlung besteht im Absetzen der verursachenden Substanz oder der Supplementierung fehlender Nährstoffe. Ein frühzeitiges Eingreifen kann eine Erholung der Sehfunktion ermöglichen, aber chronische Fälle können irreversible Schäden hinterlassen. Die Ethambutol-Optikusneuropathie ist dosisabhängig, daher sind eine visuelle Basisuntersuchung vor der Behandlung und regelmäßige Überwachung (Sehschärfe, Farbsehen, Gesichtsfeld) unerlässlich.
Behandlung kompressiver Neuropathien
Abschnitt betitelt „Behandlung kompressiver Neuropathien“Das Prinzip ist die chirurgische Entfernung der ursächlichen Läsion. Bei der thyreoidalen Optikusneuropathie wird eine notfallmäßige oder elektive orbitale Dekompression durchgeführt. Nach fortgeschrittener Optikusatrophie ist die visuelle Erholung nach chirurgischer Entfernung begrenzt, daher sind frühe Diagnose und Behandlung wichtig.
Überblick über die Prognose
Abschnitt betitelt „Überblick über die Prognose“| Krankheitstyp | Sehprognose | Erholungsmöglichkeit |
|---|---|---|
| Idiopathische Optikusneuritis | Über 90 % haben nach 1 Jahr einen Visus ≥ 0,54) | Gute Erholung |
| NAION | 1/3 Besserung, 1/3 unverändert, 1/3 Verschlechterung | Teilweise Erholung |
| AAION/GCA | Eine Erholung des betroffenen Auges ist kaum zu erwarten | Prävention des Partnerauges ist das Ziel1) |
| NMOSD-assoziiert | Schwerwiegend. Mindestens ein Auge ≤ 20/200 bei 60-69%5) | Rückfallprävention wichtig |
| LHON (mt11778) | Endvisus oft um 0.01 | Spontane Erholung nur teilweise14) |
| LHON (mt14484) | Mutationstyp mit der höchsten spontanen Erholungsrate | Erholungsfälle berichtet14) |
| ADOA | Langsame Progression, führt selten zu schwerer Blindheit | Keine Progressionshemmung |
| Druckbedingt | Erholung durch frühe Entfernung möglich | Vor Fortschreiten der Atrophie entscheidend |
| Toxisch oder ernährungsbedingt | Erholung durch frühes Absetzen oder Supplementierung | Bei chronischen Fällen irreversibel |
| Strahlungsbedingt | Häufig akuter, schwerer und irreversibler Sehverlust 12) | Keine etablierte Behandlung |
Die schnelle Identifizierung der Grunderkrankung. Bei Verdacht auf GCA noch am selben Tag mit Steroiden beginnen, ohne auf Testergebnisse zu warten, um eine Erblindung des anderen Auges zu verhindern 1). Bei kompressiver Ursache ist die chirurgische Entfernung der ursächlichen Läsion die einzige Möglichkeit, das Sehvermögen zu erhalten; eine Verzögerung der Diagnose führt zu irreversibler Optikusatrophie. Bei entzündlicher Ursache (Optikusneuritis) beschleunigt eine Steroid-Pulstherapie die Erholung, aber die zusätzliche Behandlungsstrategie variiert stark je nach Subtyp. Insbesondere bei Anti-AQP4-Antikörper-Positivität führen Steroide allein zu wiederholten Rückfällen, daher ist die frühzeitige Einführung einer rückfallpräventiven Immuntherapie der Schlüssel zum Erhalt des Sehvermögens 5).
Beide weisen ähnliche Anfangssymptome einer „akuten bis subakuten schmerzlosen Sehverschlechterung“ auf und werden insbesondere in der akuten Phase der LHON aufgrund einer Papillenschwellung leicht verwechselt. Das wichtigste Unterscheidungsmerkmal ist das Vorhandensein oder Fehlen einer Fluoreszenzleckage aus der Papille in der Fluoreszenzangiographie. Bei einer entzündlichen Optikusneuritis zeigen sich Kontrastmittelanreicherung und Fluoreszenzleckage, während in der akuten Phase der LHON keine Fluoreszenzleckage auftritt 14). Zudem tritt bei der Optikusneuritis in etwa 50 % der Fälle ein Augenschmerz bei Bewegung auf, während die LHON schmerzlos ist. Die definitive Diagnose kann durch einen mitochondrialen Gentest (mt11778, mt14484, mt3460) gestellt werden, der als externe Untersuchung durchgeführt werden kann 14). Die Gabe von Steroiden bei LHON-Patienten ist nicht nur unwirksam, sondern verzögert auch die definitive Diagnose. Daher ist es bei jungen Männern mit akuter beidseitiger Sehverschlechterung unerlässlich, die LHON in die Differenzialdiagnose einzubeziehen.
8. Verwandte Artikel (Optikusneuropathien)
Abschnitt betitelt „8. Verwandte Artikel (Optikusneuropathien)“Arteriitische anteriore ischämische Optikusneuropathie (AAION)
Druckbedingte Optikusneuropathie
Toxische Optikusneuropathie
Ernährungsbedingte Optikusneuropathie
Lebersche hereditäre Optikusneuropathie (LHON)
Autosomal-dominante Optikusatrophie (ADOA)
Strahlenoptikusneuropathie
Zu unterscheidende Sehnervenerkrankungen und -tumoren
Abschnitt betitelt „Zu unterscheidende Sehnervenerkrankungen und -tumoren“Idiopathische Optikusneuritis
MS-assoziierte Optikusneuritis
Neuromyelitis optica (NMOSD)
MOG-Antikörper-assoziierte Erkrankung (MOGAD)
Literaturverzeichnis
Abschnitt betitelt „Literaturverzeichnis“- Piccus R, Hansen MS, Hamann S, et al. An update on the clinical approach to giant cell arteritis. Eye 2023.
- Biousse V, Newman NJ. Diagnosis and clinical features of common optic neuropathies. Lancet Neurol 2016;15:1355–67.
- Salvetat ML, Pellegrini F, Spadea L, et al. Non-Arteritic Anterior Ischemic Optic Neuropathy (NA-AION): A Comprehensive Overview. Vision 2023;7:72.
- Beck RW, Gal RL. The Optic Neuritis Treatment Trial: a report on the visual function at 15 years. Ophthalmology 2008;115:1079–82.
- Wingerchuk DM, Banwell B, Bennett JL, et al. International consensus diagnostic criteria for neuromyelitis optica spectrum disorders. Neurology 2015;85:177–89.
- Jeyakumar N, Lerch M, Dale RC, Ramanathan S. MOG antibody-associated optic neuritis. Eye 2024.
- Hathaway JT, Shah MP, Hathaway DB, et al. Risk of nonarteritic anterior ischemic optic neuropathy in patients prescribed semaglutide. JAMA Ophthalmol. 2024;142:740-741. PMID: 38958939. doi:10.1001/jamaophthalmol.2024.2514.
- Thompson AJ, Banwell BL, Barkhof F, et al. Diagnosis of multiple sclerosis: 2017 revisions of the McDonald criteria. Lancet Neurol 2018;17:162–73.
- Biousse V, Newman NJ. Compressive Optic Neuropathies. J Neuroophthalmol 2015;35 Suppl 1:S67–S74.
- Sanders FWB, Votruba M. Outcomes of idebenone therapy for Leber hereditary optic neuropathy in a cohort of patients from Wales. Eye 2025.
- Newman NJ, et al. Hereditary optic neuropathy: advances in treatment. Eye 2024.
- Danesh-Meyer HV. Radiation-induced optic neuropathy. J Clin Neurosci 2008;15:95–100.
- Toosy AT, Mason DF, Miller DH. Optic neuritis. Lancet Neurol 2014;13:83–99.
- Carelli V, Ross-Cisneros FN, Sadun AA. Mitochondrial dysfunction as a cause of optic neuropathies. Prog Retin Eye Res 2004;23:53–89.
