非动脉炎性前部缺血性视神经病变(NAION)

视神经病变
1. 什么是视神经病变?
Section titled “1. 什么是视神经病变?”视神经病变(optic neuropathy)是指视神经发生某种损伤导致视功能下降的一组疾病的总称。表现为视力下降、视野缺损、色觉异常、对比敏感度下降中的一种或多种 2)。
视神经由约120万根视网膜神经节细胞(RGC)的轴突构成。在眼球内,它们汇聚成视神经乳头,经视神经管到达视交叉。从视神经乳头到视交叉前的损伤称为“前部视路障碍”,临床上大多数有意义的视神经病变都对应这一区域2)。视交叉之后(视束、视放射、枕叶)的损伤称为“后部视路障碍”,被视为视路障碍而非视神经病变。
视神经分为四个部分。眼球内部(乳头部分,约1毫米)好发缺血性和炎症性视神经病变。眼眶内部(约25毫米)常见压迫性和炎症性病变。管内部分(视神经管,约5-8毫米)易发生外伤性和骨性压迫。颅内部分(约10毫米)常受垂体腺瘤和颅咽管瘤压迫。区分可直接观察视神经乳头的“前部视神经病变”和眼底正常的“球后视神经病变”也很重要。球后视神经病变因眼底无乳头变化,易被忽视作为视力下降的原因。
视神经乳头的血流主要由短后睫状动脉(SPC动脉)供应。SPC动脉是眼动脉的终末支,为视神经乳头的前层、筛板及筛板后区域供血。该区域的循环障碍是NAION和AAION的主要病理基础3)。视神经内部受血脑屏障保护,但在炎症性视神经炎和自身免疫性疾病中,这种保护机制会失效2)。
病理共同通路与视神经萎缩
Section titled “病理共同通路与视神经萎缩”无论病因如何,最终都会经历视网膜神经节细胞和视神经轴突损伤→凋亡→视神经萎缩的共同通路。视神经萎缩是视神经病变的终末阶段,表现为视乳头苍白。一旦萎缩形成,视功能恢复极为有限2)。
视神经轴突是直径0.2-10微米的有髓和无髓纤维的混合体,大致分为P细胞(负责亮度和对比度)和M细胞(负责运动和轮廓)。在视神经病变中,ATP消耗高的P细胞更易受损,这与中毒性和营养性视神经病变中中心暗点的发生机制有关2)。
流行病学概述
Section titled “流行病学概述”概述主要视神经病变的年发病率(每10万成人)。NAION最常见,在美国为2.3~10.23)。特发性视神经炎在日本成人为1.613),LHON(Leber遗传性视神经病变)在日本每年新发病例约117人(2014年调查),属于罕见病14)。AAION/GCA的估计年发病率在50岁以上人群中为每10万0.36,在北欧白人中更常见(挪威每10万约30人)。GCA的视觉并发症发生率为10%~30%(有报告高达70%),其中AAION占60%~90%1)。MOGAD的年发病率估计为每100万1.6~4.86)。
视神经病变的分类体系
Section titled “视神经病变的分类体系”视神经病变可从多个角度进行分类。以下是最具临床实用性的分类。
按发病方式分类
按病因分类
- 缺血性:NAION、AAION、PION
- 炎症性(视神经炎):特发性、MS相关、NMOSD相关、MOGAD相关、感染性
- 压迫性:肿瘤、囊肿、动脉瘤、甲状腺眼病
- 中毒性:乙胺丁醇、胺碘酮、酒精等
- 营养性:维生素B12/B1/叶酸/铜缺乏
- 遗传性:LHON、ADOA、Wolfram综合征
- 外伤性:视神经管骨折、直接损伤
- 放射性:迟发性缺血变性
按部位分类
视神经病变的诊断框架
Section titled “视神经病变的诊断框架”视神经病变的诊断分五个步骤进行。
步骤1:确认视神经功能障碍 使用RAPD、视力、色觉和视野客观确认视神经功能障碍。
第2步:病变部位的定位 前部(有视乳头改变)还是球后(视乳头正常),眶内、管内还是颅内。根据视野缺损模式推断定位。
第3步:单眼还是双眼,急性还是慢性 可以大幅缩小鉴别诊断范围。
第4步:排除危险类型 优先排除GCA(ESR、CRP)、压迫性(MRI)和感染性(梅毒、真菌)。
第5步:特异性检查 根据类型追加抗AQP4抗体、抗MOG抗体、mtDNA检查和营养检查。
2. 与视神经炎的区别(概念整理)
Section titled “2. 与视神经炎的区别(概念整理)”“视神经炎”和“视神经病变”在临床上常被混淆,但两者是下位概念与上位概念的关系。
将非炎症性视神经病变(缺血性、压迫性、中毒性、遗传性)与视神经炎混淆,可能导致错误使用类固醇。特别是侵袭性曲霉病禁用类固醇2),而LHON急性期使用类固醇不仅无效,还会延误确诊。
视神经炎的主要临床特征
Section titled “视神经炎的主要临床特征”视神经炎(炎症性)具有以下特征,有助于与非炎症性病因鉴别。
- 急性起病:数天至2周内进展,随后5周内显示恢复趋势。
- 眼球运动痛:约50%的患者出现。缺血性、压迫性或中毒性病因通常无此症状。
- 好发年龄:15–45岁(缺血性通常50岁以上)。
- MRI表现:视神经一致的强化(钆增强T1)是典型特征。
- 自然恢复:特发性或多发性硬化相关病例中,90%以上在1年后视力恢复至0.5以上(ONTT研究)4)。
- MS转化风险:首次发作后15年,无脑MRI病变者25%进展为MS,有病变者78%进展为MS4)。
鉴别困难的情况
Section titled “鉴别困难的情况”以下情况中,视神经炎与非炎症性视神经病的鉴别变得困难。
- 50岁以上女性急性单眼视力下降:NAION vs. AQP4抗体阳性视神经炎(NMOSD)
- 年轻人急性双眼视力下降:LHON vs. 双眼同时发作的视神经炎 vs. 中毒性视神经病
- 伴有视盘水肿的单眼视力下降:NAION vs. 前部视神经炎 vs. 视盘血管炎
AQP4抗体阳性视神经炎约占特发性视神经炎的10%,是一种类固醇抵抗的难治性疾病,发病年龄较普通视神经炎偏高,女性多见(男女比例1:9)5)。AQP4抗体靶向视神经星形胶质细胞上表达的水通道蛋白4通道,引起补体依赖性细胞损伤5)。AQP4抗体阳性和阴性病例的治疗策略根本不同,因此应在类固醇冲击前进行抗体检测。检测方法中,基于细胞的检测(CBA)法比ELISA法具有更高的灵敏度和特异性,推荐使用CBA法5)。
在视神经炎进行类固醇冲击治疗前,必须排除感染性疾病(乙型肝炎、梅毒、HIV、真菌)2)。对乙型肝炎病毒携带者使用大剂量类固醇可能导致暴发性肝炎。梅毒性视神经炎应优先使用抗生素而非类固醇。
3. 紧急程度高的病型
Section titled “3. 紧急程度高的病型”下表列出了需要紧急处理的视神经病变类型。
| 病型 | 紧急程度 | 漏诊后果 |
|---|---|---|
| 动脉炎性前部缺血性视神经病变(AAION/GCA) | 最紧急 | 对侧眼失明(未治疗者65%在10天内发生)1) |
| 急性压迫性视神经病变(肿瘤、囊肿、血肿) | 紧急 | 进行性视神经萎缩和不可逆性视力损害 |
| 鼻源性视神经病变(侵袭性曲霉菌病) | 紧急 | 据报道死亡率为94%2) |
| 外伤性视神经病变(视神经管骨折) | 紧急 | 早期治疗可能保留视功能 |
| 后部缺血性视神经病变(PION) | 紧急 | 手术后或大量失血后发生,多为不可逆性 |
GCA紧急应对流程
Section titled “GCA紧急应对流程”一过性黑蒙(amaurosis fugax)作为永久性视力丧失的前驱症状出现在约30%的病例中,平均在发病前8.5天出现1)。此时怀疑GCA并积极开始使用类固醇作为二级预防极为重要。
4. 鉴别诊断的入口
Section titled “4. 鉴别诊断的入口”视神经病变的鉴别诊断按四个轴系统整理:急性或慢性、单眼或双眼、有无疼痛、以及视盘表现。
急性(数小时至数天内达到最大损害)
- NAION:典型表现为醒来时突然视力下降
- AAION:急剧的单眼视力下降,重度(视力低于20/200者超过60%)1)
- 外伤性:外伤后即刻至数小时内
亚急性(数天至数周)
慢性(数月到数年缓慢进展)
- ADOA(常染色体显性视神经萎缩):学龄期发病,双眼缓慢进展
- 慢性压迫性:由垂体腺瘤、眼眶肿瘤等引起
- 中毒性/营养性:长期暴露或营养不良导致亚急性至慢性进展
单眼还是双眼
Section titled “单眼还是双眼”倾向于单眼的疾病
倾向于双眼发病的疾病
- LHON:最初单眼,数周至数月内变为双眼(最终几乎100%双眼)
- ADOA:双眼对称性发病
- 中毒性/营养性:原则上双眼(若一眼完全正常,可考虑排除中毒性)2)
- NMOSD/AQP4-IgG阳性:重症、双眼、复发性。60~69%至少一眼有20/200以下的永久性视力损害5)
- MOGAD:双眼发病常见(MS相关或特发性中极为罕见)6)
| 有疼痛 | 无疼痛(无痛性) |
|---|---|
| 特发性视神经炎(眼球运动痛约50%)13) | NAION(无眼球痛;头痛、颌跛行为GCA全身症状) |
| MS相关性视神经炎 | AAION(无眼球痛;有颌跛行、头痛) |
| NMOSD相关(眼周疼痛) | LHON/ADOA(无痛性)14) |
| MOGAD(常合并头痛)6) | 中毒性/营养性(无眼球运动痛) |
| 外伤性(受伤引起的疼痛) | 压迫性(通常无痛但可合并眼窝痛) |
基于视乳头表现的分型
Section titled “基于视乳头表现的分型”5. 检查与检验
Section titled “5. 检查与检验”必要的眼科评估
Section titled “必要的眼科评估”当怀疑视神经病变时,应系统地进行以下评估。
视力和色觉 矫正视力是评估损伤程度和病程进展的基础。色觉(石原色盲检查图、Farnsworth-Munsell 100色相测试)在视神经病变早期容易受损,即使视力相对保留,色觉异常也可能先出现。中毒性和营养性视神经病变中,红色感觉减退是早期征兆2)。ADOA(常染色体显性视神经萎缩)的特征是获得性第三色觉异常(蓝黄色觉异常),在Farnsworth-Munsell 100色相测试中显示第三色觉异常轴2)。
RAPD通过摆动闪光灯法评估,是视神经功能障碍的客观指标。也有助于与诈病和功能性视觉障碍鉴别2)。
OCT(光学相干断层扫描)
Section titled “OCT(光学相干断层扫描)”OCT是评估视神经病变分期和随访的必要检查。
| 评估指标 | 急性期表现 | 慢性期表现 |
|---|---|---|
| pRNFL(视乳头周围RNFL厚度) | 视乳头水肿时增厚(注意假阳性) | 视神经萎缩时变薄 |
| GCL-IPL(神经节细胞+内丛状层厚度) | 变化不大 | 反映视网膜神经节细胞损伤而变薄 |
| 视盘形态 | 凹陷消失或缩小 | 萎缩后固定 |
pRNFL变薄模式与疾病类型鉴别
OCT的pRNFL变薄模式在发病后数周至数月后对疾病类型鉴别有用。
- 全周性高度变薄:NMOSD(AQP4抗体阳性型)最严重。全周高度变薄。
- 颞侧优势变薄(乳头黄斑束):中毒性、营养性、LHON、ADOA。对应中心暗点。
- 上方或下方扇形变薄:NAION。对应上方或下方束状缺损。
- MOGAD vs. MS相关:MOG-ON后pRNFL变薄比MS相关更严重6)。
- 与青光眼的鉴别:青光眼先出现视盘形态变化(凹陷扩大),GCL变薄模式也不同。
视野检查(Humphrey视野计)
Section titled “视野检查(Humphrey视野计)”视野缺损模式直接关联到病变部位的解剖学定位。
| 视野缺损模式 | 主要怀疑的疾病 | 解剖对应 |
|---|---|---|
| 中心暗点、盲点中心暗点 | 中毒性/营养性、LHON、ADOA、特发性视神经炎2) | 乳头黄斑束(PMB)损伤 |
| 水平缺损(下颞侧至下方) | NAION(束状纤维缺损)3) | 视盘上半或下半缺血 |
| 双颞侧偏盲 | 视交叉压迫(垂体腺瘤、颅咽管瘤) | 视交叉中央交叉纤维 |
| 同名偏盲(同侧) | 视交叉后(视束、视放射、枕叶)病变 | 中枢视路 |
| 交界性暗点 | 视交叉前端病变、鼻性视神经病的一种 | 乳头黄斑束 + 对侧上颞侧 |
| 整体敏感度下降 | NMOSD相关/重症视神经炎后5) | 广泛视神经纤维损伤 |
| Mariotte盲点扩大(视力正常) | 视盘玻璃疣、视盘血管炎、视神经周围炎 | 仅视盘周围 |

血液与脑脊液检查
Section titled “血液与脑脊液检查”显示急性视神经病变初始评估中推荐的检查。
| 检查项目 | 目的 | 临床意义 |
|---|---|---|
| ESR、CRP、血小板 | 排除GCA(AAION) | 最优先。CRP的特异性高于ESR1) |
| 抗AQP4抗体(基于细胞的检测) | NMOSD诊断 | ELISA法的敏感性和特异性低于CBA法5) |
| 抗MOG抗体(基于细胞的检测) | MOGAD诊断 | 识别天然MOG分子的CBA是必需的6) |
| 梅毒血清学(TPHA/RPR)和HIV | 排除感染性视神经炎 | 使用类固醇前必须确认 |
| 维生素B12、B1、叶酸、铜 | 营养性视神经病变的评估 | 肥胖外科手术后或纯素食饮食时尤其重要 |
| 线粒体基因(mt11778、mt14484、mt3460) | LHON诊断 | 这三种突变覆盖了95%以上的病例14) |
| β-D-葡聚糖和真菌培养 | 疑似侵袭性曲霉病 | 侵袭型中易升高2) |
| ACE、溶菌酶、胸部CT | 排除结节病 | — |
| ANA、dsDNA、ANCA | 全身性自身免疫性疾病(SLE、血管炎) | — |
脑脊液检查的适应证 疑似感染性脑膜炎/脑炎、NMOSD/MOGAD的诊断辅助(脑脊液细胞增多、IgG指数升高)、MS诊断辅助(脑脊液寡克隆区带)。NMOSD可出现高达50 cells/μL或以上的显著细胞增多6)。
| 检查 | 主要评估内容 | 备注 |
|---|---|---|
| 眼眶MRI(脂肪抑制T2/增强T1) | 视神经炎症、水肿、肿块、强化效应 | 视神经炎有强化效应。LHON急性期无强化14) |
| 头部MRI(FLAIR) | 脱髓鞘病变(MS、NMOSD)、颅内病变 | 用于MS诊断的McDonald标准 |
| CT(骨窗) | 视神经管骨折(外伤)、鼻窦病变、钙化(玻璃膜疣) | 外伤和鼻部疾病必需 |
| 头部超声(彩色多普勒) | GCA诊断的晕轮征 | 敏感性68%,特异性91%(双侧阳性时100%)1) |
| PET-CT(FDG) | GCA大血管病变的评估 | 敏感性92%,特异性85%(GAPS试验)1) |
| 眼眶超声 | 确认视盘玻璃膜疣的钙化 | — |
急性视神经病变原则上需要进行眼眶MRI。排除压迫性病变是首要任务,根据视神经是否出现对比增强(炎症性)或受压变形(压迫性),治疗方案会有很大不同2)。如果增强MRI未发现视神经炎症表现,则考虑中毒性、遗传性或营养性原因。LHON急性期无炎症表现,荧光眼底造影也未发现视盘荧光渗漏,这是与炎症性视神经炎的重要鉴别点14)。如果MRI禁忌,则进行CT评估鼻窦、眼眶和视神经管。
视觉诱发电位(VEP)的应用
Section titled “视觉诱发电位(VEP)的应用”视觉诱发电位(VEP)可作为脱髓鞘性视神经炎的标志物。P100潜伏期延长(正常在130 ms以内)提示脱髓鞘,在多发性硬化相关和特发性视神经炎中,恢复后潜伏期延长常持续存在13)。振幅降低在轴索损伤(中毒性、缺血性)中显著。中毒性视神经病变中,P100潜伏期无延迟,仅振幅降低,这有助于与脱髓鞘性疾病鉴别13)。临界闪烁频率(CFF)降低也反映视神经病变的功能障碍,在NMOSD相关视神经炎中显著降低13)。
6. 不同病因的特点
Section titled “6. 不同病因的特点”按病因对主要视神经病变进行分类,并总结各类型的特征。
6-1. 缺血性视神经病变
Section titled “6-1. 缺血性视神经病变”非动脉炎性前部缺血性视神经病变(NAION)
Section titled “非动脉炎性前部缺血性视神经病变(NAION)”NAION是成人急性视神经病变中最常见的类型,多发生于50岁以上人群3)。由于睫状后短动脉(SPC动脉)急性循环障碍,导致视盘发生缺血性梗死。
- 流行病学:美国年发病率为每10万人2.3~10.2例3)。50岁以上占大多数,但50岁以下发病也呈增加趋势。
- 危险因素:高血压、糖尿病、高脂血症、睡眠呼吸暂停综合征、视盘危险(杯盘比<0.2的小视盘)。约80%的对侧眼存在视盘危险3)。
- 症状:无痛性、急性单眼视力下降,常在起床时发现。患侧RAPD阳性。
- 视乳头表现:充血肿胀(下方为主的扇形)。可伴有出血。
- 视野:水平性纤维束缺损(典型为下颞侧缺损)。
- 治疗:急性期尚无确立的有效治疗方法。管理血管危险因素、治疗睡眠呼吸暂停综合征是预防复发的核心。
- 近年关注点:2024年的观察性研究报告称,使用司美格鲁肽(GLP-1受体激动剂)的患者NAION风险升高。但因果关系尚未确立,处方决策需权衡糖尿病和肥胖治疗的利益7)。
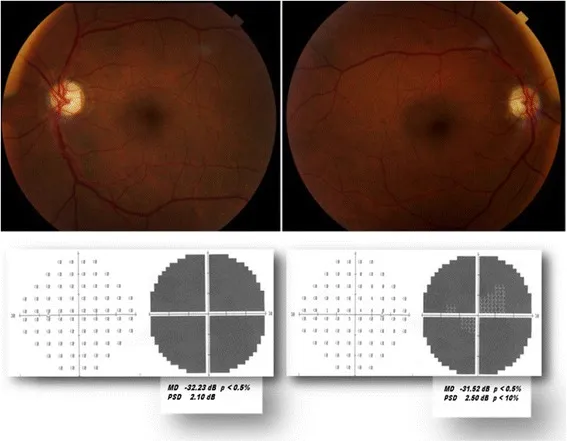
动脉炎性前部缺血性视神经病变(AAION/GCA)
Section titled “动脉炎性前部缺血性视神经病变(AAION/GCA)”AAION占所有前部缺血性视神经病变的5%~10%,但属于最紧急的视神经病变1)。其本质是供应视神经乳头的短后睫状动脉的血管炎,原发病90%以上为巨细胞动脉炎(GCA)。
- 流行病学:多见于50岁以上(尤其是75岁以上)的老年女性,男女比为1:31)。日本发病率为每10万人1.47例,远低于欧美。
- 症状:急性单眼重度视力下降(60%以上视力低于20/200,20%以上无光感)1)。约30%患者先出现一过性黑矇。
- 全身症状:头痛(65%~90%)、下颌跛行(11%~45%)、头皮压痛、发热、风湿性多肌痛样症状。
- 视盘表现:特征性表现为粉笔样苍白肿胀(pallid swelling)。
- 检查:ESR和CRP升高(>80%病例升高)1)。颞动脉活检(敏感性和特异性>95%)1)。
- 治疗:大剂量类固醇(甲泼尼龙500–1000 mg静脉滴注3天,随后口服泼尼松龙逐渐减量)1)。托珠单抗(IL-6受体拮抗剂)有助于减少类固醇用量(GiACTA试验,RCT证据)1)。
- 预后:患眼视力恢复几乎无望,但类固醇治疗可有效预防对侧眼发病。
6-2. 炎症性视神经炎
Section titled “6-2. 炎症性视神经炎”特发性视神经炎
Section titled “特发性视神经炎”一种由自身免疫机制引起的视神经炎症性疾病,占视神经炎的大多数13)。好发年龄为15~45岁,女性约占70%,日本年发病率为每10万成人1.6人13)。
- 症状:急性单眼视力下降和眼球运动痛(约50%)。数天至2周内进展,5周内呈自然恢复趋势。
- 视野:中心暗点或盲点中心暗点多见。
- MRI:与视神经一致的造影增强(钆)。
- 预后:90%以上在1年后视力恢复至0.5以上(ONTT研究)4)。
- 治疗:甲泼尼龙1000 mg/日×3天的类固醇冲击疗法可加速恢复。不进行口服类固醇单药治疗,因其会增加复发率(ONTT研究)4)。
- 转化为MS的风险:首次发作后15年累积发病率为50%。无脑MRI病变者:25%,有病变者:78%4)。
MS相关视神经炎
Section titled “MS相关视神经炎”约30%的MS患者以视神经炎为首发症状,MS患者一生中至少经历一次视神经炎的比例高达75%8)。通常为单眼、眼球运动痛、球后病变多见(眼底正常占65%)。脑MRI显示脱髓鞘病变(T2/FLAIR高信号)是诊断关键。根据McDonald标准(2017年版,2024年修订)确诊后,使用疾病修饰疗法(DMT:干扰素β、那他珠单抗、芬戈莫德、抗CD20药物等)预防复发。
NMOSD(视神经脊髓炎谱系障碍)相关视神经炎
Section titled “NMOSD(视神经脊髓炎谱系障碍)相关视神经炎”AQP4-IgG阳性。好发于女性(男女比1:9)、中年、亚洲人群。比MS相关视神经炎更严重、更常双眼受累、更易复发5)。至少一眼永久性视力障碍达20/200或以下的比例为60-69%5)。眼眶MRI显示视神经长节段病变(常累及视交叉)。治疗包括急性期类固醇冲击疗法,随后进行血浆置换,再使用预防复发的免疫疗法(依库珠单抗、利妥昔单抗、萨特利珠单抗)5)。
MOGAD(MOG抗体相关疾病)相关视神经炎
Section titled “MOGAD(MOG抗体相关疾病)相关视神经炎”MOG-IgG阳性。年发病率为每百万人1.6~4.8例6)。双眼发病常见,视乳头水肿明显,以前部病变为主。MRI特征为视乳头肿胀、长节段视神经病变和视神经周围炎6)。MS-ON、AQP4-ON和MOG-ON的性别比分别为3:1、7~9:1和1:16)。对类固醇有反应,但早期减量易复发,需谨慎逐渐减量6)。
6-3. 压迫性视神经病变
Section titled “6-3. 压迫性视神经病变”由肿瘤、动脉瘤、血肿、脓肿、囊肿或肥大的眼外肌压迫视神经引起。根据压迫部位不同,症状和视野缺损模式差异很大。
- 眶尖部:甲状腺眼病(甲状腺视神经病变合并甲状腺眼病的3%~8.6%,70%为双眼)、眼眶肿瘤(良性:特发性眼眶炎症20%、多形性腺瘤13%、血管瘤13%;恶性:恶性淋巴瘤最常见)9)。
- 视交叉部:垂体腺瘤(成人最常见,双颞侧偏盲)、颅咽管瘤(儿童最常见)。
- 鼻源性视神经病变(特别说明):侵袭性鼻窦真菌病(曲霉菌、毛霉菌)的死亡率据报道高达94%2)。因类固醇可暂时有效,易被误诊为球后视神经炎,若不知情继续使用类固醇可致命。CT/MRI显示骨质破坏是诊断关键,需与耳鼻喉科紧急协作。
治疗原则是手术切除病因病变。减压越早,视功能恢复的可能性越大;一旦视神经萎缩确立,恢复有限。
6-4. 中毒性视神经病变
Section titled “6-4. 中毒性视神经病变”这是一组因接触化学物质导致前部视路受损的疾病2)。通常为双眼性、无痛性;如果一只眼睛完全正常,则应排除中毒性视神经病变2)。
- 致病物质:烟草、酒精、稀释剂(药物:乙胺丁醇[最著名]、胺碘酮、利奈唑胺、顺铂、免疫抑制剂等)。
- 视野:特征性表现为中心盲点或中心暗点(由于P细胞优势损伤)2)。
- 色觉:红色感觉迟钝是早期征兆。
- 眼底:初期正常或轻度发红→慢性期视盘颞侧苍白、乳头黄斑束缺损。
- RAPD:因双眼对称,原则上阴性。
- VEP:振幅减小,P100潜伏期无延迟(潜伏期延迟是脱髓鞘性视神经炎的特征)13)。
- 乙胺丁醇:剂量依赖性(超过15 mg/kg时发病风险升高)。用药前基线视功能检查及定期监测必不可少。
- 治疗:基本措施是停用致病物质。无特效药。
6-5. 营养性视神经病变
Section titled “6-5. 营养性视神经病变”由B族维生素(B12、B1、B2、B9)和铜缺乏引起的双眼对称性、进行性视神经病变。与中毒性视神经病变属于同一谱系,但以营养缺乏为病因加以区分。现代风险因素包括减肥手术后(需终身监测)、纯素食和酒精依赖。症状、视野和眼底表现与中毒性视神经病变相似(中心暗点、无痛性、视盘颞侧苍白)。早期补充营养有望恢复,但慢性病例可能留下不可逆损伤。
6-6. 遗传性视神经病变
Section titled “6-6. 遗传性视神经病变”LHON(Leber遗传性视神经病变)
Section titled “LHON(Leber遗传性视神经病变)”由线粒体DNA(mtDNA)点突变引起、母系遗传的急性或亚急性视神经病变14)。三大突变(mt3460、mt11778、mt14484)占所有病例的95%以上,其中mt11778在亚洲占所有病例的约90%14)。
- 流行病学:患病率1/31,000至1/68,000。外显率2.5%至17.5%,大多数携带者不发病14)。日本每年新发病例约117人(2014年调查)。指定为疑难病。
- 症状:好发于年轻男性(男女比例约93:7)。亚急性、无痛性双眼中心暗点(一眼先发,数周至数月后双眼化)。
- 急性期眼底:视盘充血、肿胀,视盘周围毛细血管扩张、迂曲。荧光眼底造影未见视盘荧光渗漏(与炎性视神经炎的重要鉴别)14)。
- 对光反射:与其他视神经疾病相比相对保留,或仅轻度受损14)。
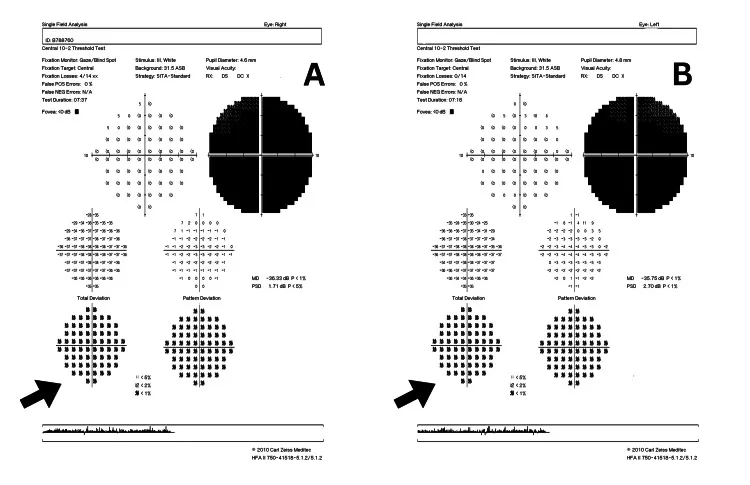
- 最终视力:mt11778 多在 0.01 左右。mt14484 自然恢复率最高14)。
- 治疗:艾地苯醌 900 mg/日(欧洲 EMA 批准)。LEROS 试验中 CRR(有意义的视力恢复)为 46.0%(安慰剂对照)10)。威尔士队列研究在 27 个月时 CRR 达到 86%10)。基因治疗在 III 期试验中也显示出有效性11)。戒烟指导对预防发病和重症化很重要。
ADOA(常染色体显性视神经萎缩症)
Section titled “ADOA(常染色体显性视神经萎缩症)”主要由OPA1基因突变引起的最常见的遗传性视神经病变。在学龄期被发现为双眼不明原因的视力发育障碍。特征性表现为后天性第三色觉异常(蓝黄色觉异常)。OCT显示颞侧至下侧象限为主的RNFL变薄2)。目前尚无有效治疗,主要以低视力护理和遗传咨询为主。
6-7. 外伤性视神经病变
Section titled “6-7. 外伤性视神经病变”头部或眼眶钝性外伤后发生的视神经损伤,多为视神经管内间接外力所致。受伤后立即出现急性视力下降。CT骨窗检查可确认视神经管骨折。可考虑大剂量类固醇或视神经管减压术,但两者的证据均有限。
6-8. 放射性视神经病变
Section titled “6-8. 放射性视神经病变”头颈部肿瘤或眼眶肿瘤放疗后发生的迟发性缺血性病变。主要通过血管内皮损伤机制导致视功能丧失。发病时间为放疗后3个月至9年,以10~20个月多见,平均约18个月12)。总剂量超过50Gy或单次剂量超过10Gy时风险增加。通常无痛,预后不良。尚无确定的治疗方法,全身类固醇、抗凝治疗和高压氧治疗效果有限12)。MRI显示与视神经一致的强化灶。
6-9. 其他特殊视神经病变
Section titled “6-9. 其他特殊视神经病变”后部缺血性视神经病变(PION) 眼眶后部或视神经管内的视神经缺血。典型的是术后PION,发生于大量出血、低血压、脊柱手术或心脏手术后。眼底检查正常(无视盘改变),但出现急剧视力下降。瞳孔对光反射表现为相对性传入性瞳孔缺陷(RAPD)。尚无有效的治疗方法。
视神经视网膜炎(neuroretinitis) 以视盘水肿和黄斑星芒状渗出为特征的综合征。病因包括汉塞巴尔通体(猫抓病)、梅毒和Leber特发性星芒状视神经视网膜炎。星芒状渗出是水肿液在黄斑区沿Henle纤维层沉积所致,常在视盘水肿消退数周后出现。有自然缓解倾向,但感染性疾病需针对病因进行特异性治疗。
乳头血管炎(papillophlebitis) 发生于青壮年的、无视力功能障碍的单眼视乳头水肿和视网膜静脉扩张迂曲的综合征。可见Mariotte盲点扩大,但矫正视力正常。眼眶MRI正常。预后良好,无需治疗,但需与视乳头水肿、视神经炎和缺血性视神经病变鉴别2)。
免疫检查点抑制剂相关视神经病变 癌症免疫治疗(如纳武利尤单抗、帕博利珠单抗等)的免疫相关不良事件(irAE)中,罕见发生视神经病变。采用类固醇冲击疗法治疗,并与肿瘤科医生协商是否继续癌症治疗。
视神经病变单行总结表
Section titled “视神经病变单行总结表”| 疾病 | 侧别 | 疼痛 | 视乳头所见 | 视野 | 关键点 |
|---|---|---|---|---|---|
| NAION | 单眼 | 无 | 发红肿胀(下方) | 水平束状缺损 | 起床时发病、disc at risk3) |
| AAION/GCA | 单眼→双眼 | 无(头痛、颌跛行) | 苍白肿胀 | 多样(重度) | 最紧急,ESR/CRP升高1) |
| 特发性视神经炎 | 单眼 | 有(50%) | 肿胀或正常 | 中心暗点 | 年轻女性,MS转化风险13) |
| NMOSD相关 | 易双眼化 | 有 | 肿胀或正常 | 多样(重度) | AQP4抗体阳性、难治性5) |
| MOGAD相关 | 多为双眼 | 有(头痛) | 高度肿胀 | 多样 | MOG抗体、视神经周围炎6) |
| 压迫性 | 单眼/双眼 | 无 | 正常或萎缩 | 多样 | 必须进行MRI检查9) |
| 中毒性 | 双眼 | 无 | 正常→颞侧苍白 | 中心盲点 | 询问致病物质2) |
| 营养性 | 双眼 | 无 | 正常→颞侧苍白 | 中心暗点 | B12/铜缺乏 |
| LHON | 双眼(一眼先发) | 无 | 发红/毛细血管扩张 | 中心暗点 | 年轻男性,无荧光渗漏14) |
| ADOA | 双眼 | 无 | 苍白 | 中心暗点 | 学龄期、蓝黄色觉异常2) |
| 外伤性 | 单眼 | 有(外伤) | 正常 | 多样 | CT确认视神经管骨折 |
| 放射性 | 单眼/双眼 | 无 | 正常→萎缩 | 多样 | 平均18个月12) |
7. 治疗原则
Section titled “7. 治疗原则”视神经病的治疗取决于病因,不同病型的治疗根本不同。共同原则如下所示。
需要紧急处理的情况
Section titled “需要紧急处理的情况”- GCA/AAION:大剂量全身性类固醇(当天开始)。不等检查结果1)。
- 急性压迫性视神经病:手术减压(与耳鼻喉科和神经外科紧急协作)。侵袭性曲霉病时停用类固醇,改用抗真菌药2)。
- 外伤性:考虑视神经管减压术的适应证。
炎症性(视神经炎)的治疗
Section titled “炎症性(视神经炎)的治疗”类固醇脉冲疗法(mPSL 1000 mg/日×3天)可加快急性期的恢复速度4)。单独口服类固醇会增加特发性视神经炎的复发风险,因此不施行(ONTT研究)4)。NMOSD急性期采用阶梯治疗:类固醇脉冲→反应不充分时行血浆置换→预防复发的免疫治疗5)。MOGAD视神经炎对类固醇有反应,但早期减量会导致复发,因此需要谨慎逐渐减量6)。
缺血性(NAION)的治疗
Section titled “缺血性(NAION)的治疗”急性期尚无有效的治疗方法。主要管理血管危险因素(高血压、糖尿病、高脂血症、睡眠呼吸暂停综合征),治疗目标是预防对侧眼发病。关于司美格鲁肽(GLP-1受体激动剂),有观察性研究显示其与NAION相关,对于有病史或风险的患者,应进行仔细说明和随访7)。
遗传性(LHON)的治疗
Section titled “遗传性(LHON)的治疗”艾地苯醌900毫克/日已获欧洲药品管理局(EMA)批准,在LEROS试验中达到46%的CRR(安慰剂对照)10)。威尔士队列报告27个月时CRR为86%,显示出良好的真实世界疗效10)。基因治疗(lenadogene nolparvovec)在III期试验中显示出有效性,未来有望扩大适应症11)。戒烟指导(吸烟是发病风险因素)和适当的低视力护理是必需的14)。
中毒性和营养性视神经病变的治疗
Section titled “中毒性和营养性视神经病变的治疗”基本原则是停用致病物质或补充缺乏的营养素。早期干预有望恢复视功能,但慢性病例可能留下不可逆损伤。乙胺丁醇视神经病变具有剂量依赖性,因此给药前进行基线视功能检查和定期监测(视力、色觉、视野)至关重要。
压迫性视神经病变的治疗
Section titled “压迫性视神经病变的治疗”原则是手术切除病因病变。对于甲状腺视神经病变,需进行紧急或择期眼眶减压术。一旦视神经萎缩进展,手术切除后的视力恢复有限,因此早期诊断和早期治疗至关重要。
| 病型 | 视力预后 | 恢复可能性 |
|---|---|---|
| 特发性视神经炎 | 90%以上1年后视力达0.5以上4) | 恢复良好 |
| NAION | 1/3改善、1/3不变、1/3恶化 | 部分恢复 |
| AAION/GCA | 患眼几乎无法恢复 | 目标是预防对侧眼1) |
| NMOSD相关 | 严重。至少一只眼视力20/200或以下占60~69%5) | 预防复发很重要 |
| LHON(mt11778) | 最终视力多在0.01左右 | 仅部分患者可自然恢复14) |
| LHON(mt14484) | 自然恢复率最高的突变类型 | 有恢复案例14) |
| ADOA | 缓慢进展,通常不会导致严重失明 | 无进展抑制 |
| 压迫性 | 早期解除可恢复 | 萎缩进展前是关键 |
| 中毒性/营养性 | 早期停止/补充可恢复 | 慢性病例不可逆 |
| 放射性 | 急性、重度、常为不可逆性视力下降12) | 无确立的治疗方法 |
快速确定病因。若怀疑GCA,应在当天开始使用类固醇,无需等待检查结果,以预防对侧眼失明1)。对于压迫性病变,手术切除病因是保留视功能的唯一方法,诊断延迟会导致不可逆的视神经萎缩。炎症性(视神经炎)可使用类固醇冲击疗法加速恢复,但根据亚型不同,附加治疗策略差异很大。特别是抗AQP4抗体阳性病例,单用类固醇会导致反复复发,因此早期引入预防复发的免疫治疗是保留视功能的关键5)。
8. 相关文章(视神经病变)
Section titled “8. 相关文章(视神经病变)”需要鉴别的视神经疾病和肿瘤
Section titled “需要鉴别的视神经疾病和肿瘤”- Piccus R, Hansen MS, Hamann S, et al. An update on the clinical approach to giant cell arteritis. Eye 2023.
- Biousse V, Newman NJ. Diagnosis and clinical features of common optic neuropathies. Lancet Neurol 2016;15:1355–67.
- Salvetat ML, Pellegrini F, Spadea L, et al. Non-Arteritic Anterior Ischemic Optic Neuropathy (NA-AION): A Comprehensive Overview. Vision 2023;7:72.
- Beck RW, Gal RL. The Optic Neuritis Treatment Trial: a report on the visual function at 15 years. Ophthalmology 2008;115:1079–82.
- Wingerchuk DM, Banwell B, Bennett JL, et al. International consensus diagnostic criteria for neuromyelitis optica spectrum disorders. Neurology 2015;85:177–89.
- Jeyakumar N, Lerch M, Dale RC, Ramanathan S. MOG antibody-associated optic neuritis. Eye 2024.
- Hathaway JT, Shah MP, Hathaway DB, et al. Risk of nonarteritic anterior ischemic optic neuropathy in patients prescribed semaglutide. JAMA Ophthalmol. 2024;142:740-741. PMID: 38958939. doi:10.1001/jamaophthalmol.2024.2514.
- Thompson AJ, Banwell BL, Barkhof F, et al. Diagnosis of multiple sclerosis: 2017 revisions of the McDonald criteria. Lancet Neurol 2018;17:162–73.
- Biousse V, Newman NJ. Compressive Optic Neuropathies. J Neuroophthalmol 2015;35 Suppl 1:S67–S74.
- Sanders FWB, Votruba M. Outcomes of idebenone therapy for Leber hereditary optic neuropathy in a cohort of patients from Wales. Eye 2025.
- Newman NJ, et al. Hereditary optic neuropathy: advances in treatment. Eye 2024.
- Danesh-Meyer HV. Radiation-induced optic neuropathy. J Clin Neurosci 2008;15:95–100.
- Toosy AT, Mason DF, Miller DH. Optic neuritis. Lancet Neurol 2014;13:83–99.
- Carelli V, Ross-Cisneros FN, Sadun AA. Mitochondrial dysfunction as a cause of optic neuropathies. Prog Retin Eye Res 2004;23:53–89.
