前部RON

放射性视神经病变
一目了然的要点
Section titled “一目了然的要点”1. 什么是放射性视神经病变?
Section titled “1. 什么是放射性视神经病变?”放射性视神经病变(RON)是视觉器官接受放射线照射后发生的迟发性缺血性变化导致的视神经损伤。视觉器官对放射线高度敏感,主要通过血管内皮损伤机制导致视功能丧失。
好发部位为视交叉或其前后,分为前部RON和后部RON。前部RON由眼眶、脉络膜、视网膜肿瘤的质子线治疗或敷贴治疗引起,后部RON由鼻窦或颅底肿瘤的治疗引起。
流行病学与安全剂量
Section titled “流行病学与安全剂量”发病风险与照射剂量密切相关。下表显示了剂量与发病风险的关系。
| 照射条件 | 发病风险 |
|---|---|
| 总剂量低于5,000 cGy | 罕见 |
| 总剂量5,000–6,000 cGy | 10年内最高5% |
| 单次剂量≤2 Gy,总剂量≤50 Gy | 相对安全 |
| 伽玛刀800–1,000 cGy单次(1–3次) | 相对安全 |
发病时间从照射后3个月到数年不等,大多数在3年内发病。高峰在照射后1.5年,最常见的发病时间为治疗后8–16个月。随着伽玛刀的普及,RON的发生率显著降低。
总剂量低于5,000 cGy(50 Gy)的分次照射,发病罕见。在5,000–6,000 cGy时,10年内发生率最高可达5%。单次剂量≤2 Gy且总剂量≤50 Gy被认为是相对安全的,这些值成为制定照射计划的标准。
2. 主要症状与临床所见
Section titled “2. 主要症状与临床所见”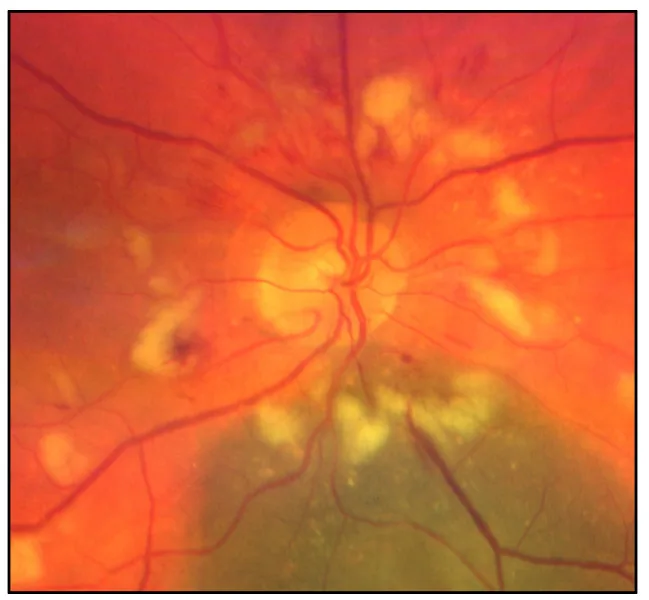
- 视力下降:表现为数周内进行性且快速的视力下降。可为单侧或双侧,通常无痛。
- 色觉障碍:色觉异常也常见。
- 发病方式:分为急性(治疗中)、早期迟发性(照射后3个月)、晚期迟发性(照射后6个月至10年)。
- 若为双眼:第二只眼的症状常在数周内出现。
后部RON
正常或苍白的视神经:后部RON眼底所见较少,视神经正常或苍白。
视野缺损模式:视交叉损伤导致双颞侧偏盲,视束损伤导致对侧同向偏盲伴带状萎缩。
42岁女性(乳腺癌脑转移接受50 Gy照射)病例,照射后1年右眼出现上方高度视野缺损、下方节段性视神经苍白和RAPD阳性。最终右眼仅存光感(黑矇性瞳孔)1)。
74岁女性(脑膜瘤切除后接受54 Gy照射)病例,照射后22个月时左眼视力20/20且无症状,但OCT检测到pRNFL和GCIPL变薄2)。
3. 原因和风险因素
Section titled “3. 原因和风险因素”辐射通过两种途径损伤细胞:直接破坏分子键和通过自由基产生间接损伤。如Bergonie-Tribondeau定律所示,细胞分裂频率高、分化程度低的细胞更容易受到辐射损伤。血管内皮细胞的损伤导致血管通透性增加和毛细血管闭塞,最终引起缺血性视神经病变。
- 照射剂量:总剂量、单次剂量和照射间隔均与风险相关。
- 糖尿病:增加缺血性血管疾病的风险,并提高RON的发生风险。
- 高血压和已有血管病变:已有血管病变的病例风险增加。
- 联合化疗:可能增强辐射损伤。
- 患者年龄:年龄也被视为风险因素之一。
糖尿病患者缺血性血管疾病的风险较高,因此认为RON的发生风险增加。高血压和已有血管病变同样是风险因素。联合化疗也可能增加风险。对于多重风险因素叠加的病例,需要特别谨慎的照射计划和随访观察。
4. 诊断和检查方法
Section titled “4. 诊断和检查方法”放射性视神经病变是一种排除性诊断,在排除类似疾病后进行诊断。
主要的鉴别诊断包括以下疾病:
可能需要进行腰椎穿刺脑脊液检查(排除癌性脑膜炎)和血清学检查(寻找副肿瘤综合征)。
- MRI(首选):MRI是视神经疾病的首选检查,STIR序列和Gd增强T1加权冠状位图像有用。推荐使用3T及3 mm以下的薄层扫描。可见受累视神经的强化。早期有时难以与肿瘤复发鉴别。在2)报告的病例中,T1增强MRI证实了左侧视交叉前视神经的肿胀和强化。
- OCT:可检测pRNFL和GCIPL的变薄,并可能在出现症状前捕捉到变化2)。其作为放疗后筛查工具的价值已被提出。
- OCT-A(光学相干断层扫描血管成像):基于视乳头周围放射状毛细血管网(RPCP)变化的0-4级分级量表已被提出,作为一种无创评估方法受到关注。
以下是OCT-A分级量表的概述:
| 分级 | 表现 |
|---|---|
| 0 | RPCP的规则放射状分布 |
| 1 | RPCP初始放射状模式消失 |
| 2 | 少于2个象限的视乳头周围低灌注 |
| 3 | 2个及以上象限的低灌注 |
| 4 | 全部4个象限的弥漫性低灌注 |
1~3级有“+”亚分类(乳头黄斑束受累),与视力下降相关。
通过OCT检测pRNFL和GCIPL变薄,可能在主观症状出现前捕捉到变化2)。MRI显示受累视神经的强化。放疗后的定期眼科监测有助于早期发现RON,有报告建议在外照射完成后10~20个月进行常规MRI监测2)。
5. 标准治疗方法
Section titled “5. 标准治疗方法”基本没有根治性治疗方法,预后通常不良。对于尚未发生视神经萎缩的早期病例,以下治疗有一定效果。
- 全身类固醇治疗:在发病初期进行。有病例报告使用泼尼松龙50 mg/天1)。也有病例使用泼尼松60 mg/天×4周治疗2)。但也有报告指出,类固醇和抗凝治疗对RON并未取得成功。
- 抗凝治疗:可能会使用肝素等抗凝药物。
- 高压氧治疗(HBOT):旨在促进血管新生并抑制缺血性坏死的进展。在症状出现后尽早(约72小时内)进行,给予2-3个大气压的近100%氧气,持续30-60分钟。副作用包括气压伤、支气管肺毒性、癫痫发作、干眼和可逆性近视。费用高昂,且停止后可能再次进展。
- 45%的患眼最终视力低于20/200至光感。
- 约半数病例最终无光感。
- 可能导致单侧或双侧永久性失明。
没有根治性治疗方法,预后通常不良。45%的患眼最终视力低于20/200至光感,约半数无光感。全身类固醇、高压氧治疗和抗凝治疗对近期发病的病例可能有一定效果,但都不能保证视功能恢复。
6. 病理生理学与详细发病机制
Section titled “6. 病理生理学与详细发病机制”RON的发病机制涉及血管损伤(放射性血管炎)和放射线对视器的直接损伤。初始损伤出现在血管系统还是神经实质尚不明确。
不同病期的变化
Section titled “不同病期的变化”早期阶段(数周内)
可逆性炎症和渗出性血管损伤:血管通透性增高是核心。此阶段的变化被认为是可逆的。
进展阶段(数月至数年)
血管闭塞和内皮细胞增殖:自由基损伤加入。
微血管功能不全:诱发伴有缺氧的微血管功能不全。细胞DNA和血脑屏障也发生直接损伤。
不可逆阶段
脱髓鞘和反应性星形胶质细胞增生:损伤扩散至周围神经,导致不可逆的视力丧失。
放射线引起的细胞损伤通过两条途径发生。第一条是通过分子键断裂的直接损伤,第二条是通过自由基产生的间接损伤。根据Bergonie-Tribondeau定律,细胞分裂频率高、分化程度低的细胞更容易受损。血管内皮细胞的损伤导致毛细血管通透性增高和闭塞,通过局部VEGF升高和炎症反应,形成缺血性视神经病变。
7. 最新研究与未来展望(研究阶段报告)
Section titled “7. 最新研究与未来展望(研究阶段报告)”抗VEGF治疗(贝伐珠单抗)
Section titled “抗VEGF治疗(贝伐珠单抗)”贝伐珠单抗作为针对内皮细胞损伤相关局部VEGF升高的治疗药物备受关注。已有报告采用全身给药(每3周一次,共4次)或玻璃体内给药(每6-8周至少2次),并有报告称在3年内稳定改善视力和色觉。
己酮可可碱(Trental)是一种甲基黄嘌呤衍生物,已被证明可改变血液粘度并可能有助于改善循环,有报告显示有希望的结果。在实际病例报告中,己酮可可碱1,200 mg/天已被处方2)。
有报告称,在放射照射后2周开始给予ACE抑制剂(雷米普利)约6个月,可减少炎症细胞因子的释放。然而,目前仅在老鼠模型中证实,尚未确立在人类中的应用。
维生素E在体外研究中显示出减少活性氧生成和抑制纤维化的作用,但临床证据有限。
OCT和OCT-A早期检测的前景
Section titled “OCT和OCT-A早期检测的前景”通过OCT检测pRNFL和GCIPL的变薄,可能能够在出现症状前诊断放射性视神经病变2)。基于OCT-A的分级量表也有望作为非侵入性随访工具在未来得到应用。国际注册数据库的建立将有助于进一步阐明临床特征。
8. 参考文献
Section titled “8. 参考文献”- Abduraman S, Mali B, Celebi ARC. Taxane-associated retinopathy and radiation-induced optic neuropathy in a young female patient with metastatic breast cancer. GMS Ophthalmol Cases. 2025;15:Doc07.
- Grosinger A, Chen JJ, Link MJ, Bhatti MT. Detection of asymptomatic radiation induced optic neuropathy with optical coherence tomography. Neuroophthalmology. 2021;45(5):339-342.
- Oakey Z, Yeşiltaş YS, Singh AD. Radiation Optic Neuropathy: Management Options. Ocul Oncol Pathol. 2023;9(5-6):166-171. PMID: 38089180.
