RON قدامی

نوروپاتی ناشی از پرتودرمانی
نکات کلیدی در یک نگاه
Section titled “نکات کلیدی در یک نگاه”1. نوروپاتی بینایی ناشی از پرتودرمانی چیست؟
Section titled “1. نوروپاتی بینایی ناشی از پرتودرمانی چیست؟”نوروپاتی بینایی ناشی از پرتودرمانی (radiation optic neuropathy: RON) یک اختلال عصب بینایی است که در اثر تغییرات ایسکمیک دیررس پس از پرتودرمانی به دستگاه بینایی (optic apparatus) ایجاد میشود. دستگاه بینایی حساسیت بالایی به پرتو دارد و عملکرد بینایی عمدتاً از طریق مکانیسم آسیب اندوتلیال عروقی از دست میرود.
محل شایع کیاسمای بینایی یا نواحی قبل و بعد از آن است و به دو نوع RON قدامی (anterior RON) و RON خلفی (posterior RON) تقسیم میشود. RON قدامی ناشی از پرتودرمانی پروتونی یا براکیتراپی پلاک برای تومورهای اربیت، کوروئید و رتین است، در حالی که RON خلفی ناشی از درمان تومورهای سینوس و قاعده جمجمه است.
اپیدمیولوژی و دوز ایمن
Section titled “اپیدمیولوژی و دوز ایمن”خطر بروز ارتباط نزدیکی با دوز پرتودرمانی دارد. در زیر راهنمایی برای دوز و خطر بروز ارائه شده است.
| شرایط پرتودرمانی | خطر بروز |
|---|---|
| کمتر از 5000 سانتیگری دوز کل | نادر |
| 5000 تا 6000 سانتیگری دوز کل | حداکثر 5% در 10 سال |
| دوز تکی ≤2 گری و دوز کل ≤50 گری | نسبتاً ایمن |
| گاما نایف 800 تا 1000 سانتیگری در یک جلسه (1 تا 3 جلسه) | نسبتاً ایمن |
زمان بروز از 3 ماه تا چند سال پس از پرتودرمانی متغیر است و بیشتر موارد در 3 سال اول رخ میدهد. اوج بروز 1.5 سال پس از پرتودرمانی و شایعترین زمان بروز 8 تا 16 ماه پس از درمان گزارش شده است. با گسترش استفاده از گاما نایف، فراوانی نوروپاتی بینایی ناشی از پرتو به طور قابل توجهی کاهش یافته است.
در پرتودرمانی تقسیمشده با دوز کل کمتر از 5000 سانتیگری (50 گری)، بروز نوروپاتی نادر است. با دوز 5000 تا 6000 سانتیگری، احتمال بروز تا 5% در 10 سال گزارش شده است. اگر دوز تکی ≤2 گری و دوز کل ≤50 گری باشد، نسبتاً ایمن در نظر گرفته میشود و این مقادیر به عنوان معیار در برنامهریزی پرتودرمانی استفاده میشوند.
2. علائم اصلی و یافتههای بالینی
Section titled “2. علائم اصلی و یافتههای بالینی”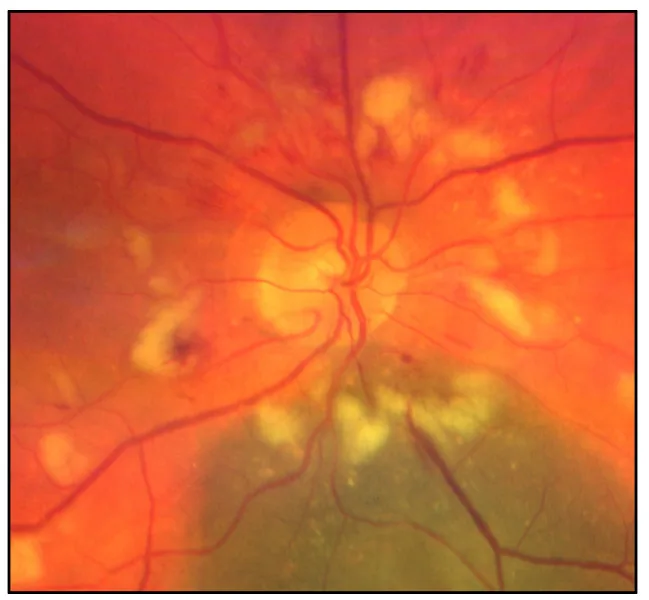
علائم ذهنی
Section titled “علائم ذهنی”- کاهش بینایی: به صورت کاهش پیشرونده و سریع بینایی طی چند هفته ظاهر میشود. ممکن است یکطرفه یا دوطرفه باشد و معمولاً بدون درد است.
- اختلال رنگبینی: اختلال در تشخیص رنگها نیز شایع است.
- الگوی شروع: به سه نوع حاد (در حین درمان)، زودرس دیررس (۳ ماه پس از پرتودرمانی) و دیررس دیررس (۶ ماه تا ۱۰ سال پس از پرتودرمانی) تقسیم میشود.
- در صورت درگیری دوطرفه: علائم چشم دوم معمولاً ظرف چند هفته ظاهر میشود.
یافتههای بالینی
Section titled “یافتههای بالینی”RON خلفی
عصب بینایی طبیعی یا رنگپریده: در RON خلفی، یافتههای فوندوسکوپی اندک است و عصب بینایی طبیعی یا رنگپریده به نظر میرسد.
الگوی نقص میدان بینایی: در آسیب کیاسم، همیانوپسی تمپورال و در آسیب مجرای بینایی، همیانوپسی همنام کنترال همراه با آتروفی نواری دیده میشود.
در یک بیمار ۴۲ ساله (تحت ۵۰ گری پرتودرمانی به دلیل متاستاز مغزی سرطان پستان)، یک سال پس از پرتودرمانی، نقص شدید میدان بینایی فوقانی، رنگپریدگی سگمنتال تحتانی عصب بینایی و RAPD مثبت در چشم راست مشاهده شد. در نهایت، چشم راست تنها درک نور داشت (مردمک آموروتیک) 1).
در یک بیمار ۷۴ ساله (تحت ۵۴ گری پرتودرمانی پس از برداشتن مننژیوم)، در ۲۲ ماه پس از پرتودرمانی، با وجود دید ۲۰/۲۰ و بدون علامت در چشم چپ، OCT نازک شدن pRNFL و GCIPL را نشان داد 2).
3. علل و عوامل خطر
Section titled “3. علل و عوامل خطر”مکانیسم بروز
Section titled “مکانیسم بروز”پرتو با دو مسیر به سلولها آسیب میزند: تخریب مستقیم پیوندهای مولکولی و آسیب غیرمستقیم از طریق تولید رادیکالهای آزاد. طبق قانون برگونی-تریبوندو، سلولهایی که تقسیم سریعتری دارند و تمایز نیافتهتر هستند، بیشتر در معرض آسیب پرتو قرار میگیرند. آسیب به سلولهای اندوتلیال عروق منجر به افزایش نفوذپذیری عروق و انسداد مویرگها میشود و در نهایت نوروپاتی ایسکمیک بینایی را ایجاد میکند.
عوامل خطر
Section titled “عوامل خطر”- دوز پرتو: دوز کل، دوز هر جلسه و فاصله بین جلسات همگی در خطر نقش دارند.
- دیابت: خطر بیماری عروقی ایسکمیک را افزایش میدهد و خطر بروز RON را بالا میبرد.
- فشار خون بالا و ضایعات عروقی موجود: در مواردی که از قبل ضایعات عروقی وجود دارد، خطر افزایش مییابد.
- شیمیدرمانی همزمان: ممکن است آسیب پرتوی را تشدید کند.
- سن بیمار: سن نیز یکی از عوامل خطر محسوب میشود.
بیماران دیابتی به دلیل خطر بالای بیماری عروقی ایسکمیک، خطر بروز RON در آنها افزایش مییابد. فشار خون بالا و ضایعات عروقی موجود نیز عوامل خطر مشابهی هستند. شیمیدرمانی همزمان نیز ممکن است خطر را افزایش دهد و در مواردی که این عوامل همپوشانی دارند، برنامهریزی دقیقتر پرتودرمانی و پیگیری لازم است.
4. تشخیص و روشهای آزمایش
Section titled “4. تشخیص و روشهای آزمایش”نوروپاتی بینایی ناشی از پرتو یک تشخیص افتراقی است و پس از رد بیماریهای مشابه تشخیص داده میشود.
تشخیص افتراقی
Section titled “تشخیص افتراقی”بیماریهای افتراقی اصلی عبارتند از:
- نوروپاتی فشاری عصب بینایی، فشردگی عصب بینایی ناشی از عود تومور
- نوروپاتی نفوذی عصب بینایی، مننژیت کارسینوماتوز
- نوروپاتی سمی عصب بینایی ناشی از شیمیدرمانی
- نوروپاتی پارانئوپلاستیک عصب بینایی، آراخنوئیدیت
- آرتریت سلول ژانت (تشخیص افتراقی در سالمندان)
ممکن است نیاز به بررسی مایع مغزی-نخاعی از طریق پونکسیون کمری (برای رد مننژیت کارسینوماتوز) و آزمایشهای سرولوژیک (برای جستجوی سندرم پارانئوپلاستیک) باشد.
آزمایشها
Section titled “آزمایشها”- MRI (انتخاب اول): MRI اولین انتخاب برای بیماریهای عصب بینایی است و تصاویر STIR و T1-weighted با گادولینیوم در برشهای کرونال مفید هستند. برشهای نازک 3 میلیمتر یا کمتر با دستگاه 3 تسلا توصیه میشود. افزایش کنتراست عصب بینایی مبتلا مشاهده میشود. در مراحل اولیه، تشخیص افتراقی از عود تومور ممکن است دشوار باشد. 2) در موارد گزارش شده، MRI T1 با کنتراست، برجستگی و افزایش کنتراست در عصب بینایی قدامی-کیاسمایی چپ را تأیید کرد.
- OCT: میتواند نازکشدن pRNFL و GCIPL را تشخیص دهد و ممکن است تغییرات را قبل از بروز علائم نشان دهد 2). به عنوان ابزار غربالگری پس از پرتودرمانی پیشنهاد شده است.
- OCT-A (آنژیوگرافی توموگرافی همدوسی نوری): یک مقیاس درجهبندی 0 تا 4 بر اساس تغییرات شبکه مویرگی شعاعی اطراف پاپیلا (RPCP) پیشنهاد شده است و به عنوان یک روش ارزیابی غیرتهاجمی مورد توجه است.
خلاصه مقیاس درجهبندی OCT-A در زیر آورده شده است:
| درجه | یافته |
|---|---|
| 0 | توزیع شعاعی منظم RPCP |
| 1 | از بین رفتن الگوی شعاعی اولیه RPCP |
| 2 | هیپوپرفیوژن پری پاپیلاری کمتر از دو ربع |
| 3 | هیپوپرفیوژن دو ربع یا بیشتر |
| 4 | هیپوپرفیوژن منتشر هر چهار ربع |
گریدهای 1 تا 3 دارای زیرطبقهبندی «+» (درگیری دسته پاپیلوماکولار) هستند که با کاهش بینایی همبستگی دارد.
تشخیص نازک شدن pRNFL و GCIPL توسط OCT ممکن است تغییرات را قبل از بروز علائم ذهنی نشان دهد2). MRI افزایش کنتراست عصب بینایی مبتلا را تأیید میکند. پایش منظم چشمپزشکی پس از پرتودرمانی منجر به تشخیص زودهنگام RON میشود و برخی گزارشها پایش روتین MRI را 10 تا 20 ماه پس از اتمام پرتودرمانی خارجی پیشنهاد میکنند2).
5. درمان استاندارد
Section titled “5. درمان استاندارد”اساساً درمان قطعی وجود ندارد و پیشآگهی معمولاً ضعیف است. در موارد تازه شروع شده که آتروفی عصب بینایی رخ نداده است، درمانهای زیر تا حدودی مفید تلقی میشوند.
- تجویز سیستمیک استروئیدها: در مراحل اولیه بیماری انجام میشود. مواردی از تجویز پردنیزولون ۵۰ میلیگرم در روز گزارش شده است1). همچنین مواردی با درمان پردنیزون ۶۰ میلیگرم در روز به مدت ۴ هفته وجود دارد2). با این حال، برخی گزارشها حاکی از عدم موفقیت استروئیدها و ضد انعقادها در درمان RON است.
- ضد انعقاد درمانی: ممکن است از داروهای ضد انعقاد مانند هپارین استفاده شود.
- اکسیژن درمانی با فشار بالا (HBOT): به منظور تحریک رگزایی و جلوگیری از پیشرفت نکروز ایسکمیک انجام میشود. در اسرع وقت پس از بروز علائم (حدود ۷۲ ساعت) با اکسیژن تقریباً ۱۰۰٪ در فشار ۲ تا ۳ اتمسفر به مدت ۳۰ تا ۶۰ دقیقه انجام میشود. عوارض جانبی شامل باروتروما، سمیت برونکوپولمونری، تشنج، خشکی چشم و نزدیکبینی برگشتپذیر است. هزینه بالا بوده و ممکن است پس از قطع درمان، پیشرفت مجدد رخ دهد.
پیشآگهی
Section titled “پیشآگهی”- در ۴۵٪ از چشمهای مبتلا، حدت بینایی نهایی کمتر از ۲۰/۲۰۰ تا درک نور میرسد.
- حدود نیمی از موارد به عدم درک نور منجر میشوند.
- احتمال نابینایی دائمی یکطرفه یا دوطرفه وجود دارد.
هیچ درمان قطعی وجود ندارد و پیشآگهی معمولاً ضعیف است. در ۴۵٪ از چشمهای مبتلا، حدت بینایی نهایی کمتر از ۲۰/۲۰۰ تا درک نور میرسد و حدود نیمی به عدم درک نور منجر میشوند. تجویز سیستمیک استروئیدها، اکسیژن درمانی با فشار بالا و ضد انعقاد درمانی ممکن است در موارد اولیه تا حدودی مفید باشند، اما هیچکدام بهبود عملکرد بینایی را تضمین نمیکنند.
۶. پاتوفیزیولوژی و مکانیسم دقیق بروز
Section titled “۶. پاتوفیزیولوژی و مکانیسم دقیق بروز”مکانیسم بروز RON شامل آسیب عروقی (واسکولیت پرتویی) و آسیب مستقیم پرتو به دستگاه بینایی است. اینکه آسیب اولیه در سیستم عروقی رخ میدهد یا در پارانشیم عصبی، هنوز به طور کامل مشخص نیست.
تغییرات بر اساس مرحله بیماری
Section titled “تغییرات بر اساس مرحله بیماری”مرحله اولیه (در عرض چند هفته)
التهاب برگشتپذیر و آسیب عروقی اگزوداتیو: افزایش نفوذپذیری عروق مرکزی است. تغییرات در این مرحله برگشتپذیر در نظر گرفته میشوند.
مرحله پیشرونده (چند ماه تا چند سال)
انسداد عروق و تکثیر سلولهای اندوتلیال: آسیب رادیکالهای آزاد اضافه میشود.
نارسایی میکروواسکولار: نارسایی میکروواسکولار همراه با هیپوکسی ایجاد میشود. آسیب مستقیم به DNA سلولها و سد خونی-مغزی نیز رخ میدهد.
مرحله غیرقابل برگشت
دمیلیناسیون و آستروسیتوز واکنشی: آسیب به اعصاب اطراف گسترش یافته و منجر به از دست دادن غیرقابل برگشت عملکرد بینایی میشود.
آسیب سلولی ناشی از پرتو از دو مسیر رخ میدهد. اولی آسیب مستقیم از طریق تخریب پیوندهای مولکولی و دومی آسیب غیرمستقیم از طریق تولید رادیکالهای آزاد است. بر اساس قانون برگونی-تریبوندو، سلولهایی با تقسیم سلولی بالا و تمایز نیافته بیشتر مستعد آسیب هستند. آسیب به سلولهای اندوتلیال عروقی منجر به افزایش نفوذپذیری مویرگی و انسداد میشود و از طریق افزایش VEGF موضعی و پاسخ التهابی، نوروپاتی ایسکمیک بینایی کامل میشود.
7. تحقیقات جدید و چشماندازهای آینده (گزارشهای مرحله تحقیقاتی)
Section titled “7. تحقیقات جدید و چشماندازهای آینده (گزارشهای مرحله تحقیقاتی)”درمان ضد VEGF (بواسیزوماب)
Section titled “درمان ضد VEGF (بواسیزوماب)”بواسیزوماب به عنوان درمانی با هدف افزایش VEGF موضعی ناشی از آسیب سلولهای اندوتلیال مورد توجه قرار گرفته است. تجویز سیستمیک (یک بار هر 3 هفته، مجموعاً 4 بار) یا تزریق داخل زجاجیهای (حداقل 2 بار هر 6 تا 8 هفته) گزارش شده است و گزارشهایی از بهبود پایدار بینایی و دید رنگی به مدت 3 سال وجود دارد.
پنتوکسی فیلین
Section titled “پنتوکسی فیلین”پنتوکسی فیلین (ترنتال)، یک مشتق متیل گزانتین، نشان داده است که ویسکوزیته خون را تعدیل کرده و به بهبود گردش خون کمک میکند و نتایج امیدوارکنندهای گزارش شده است. در یک گزارش موردی واقعی، پنتوکسی فیلین با دوز 1200 میلیگرم در روز تجویز شده است 2).
سایر تحقیقات
Section titled “سایر تحقیقات”گزارش شده است که تجویز مهارکننده ACE (رامیپریل) از دو هفته پس از پرتودرمانی به مدت حدود شش ماه، آزادسازی سیتوکینهای التهابی را کاهش میدهد. با این حال، در حال حاضر این موضوع فقط در مدلهای موش صحرایی نشان داده شده است و کاربرد آن در انسان هنوز اثبات نشده است.
ویتامین E در مطالعات آزمایشگاهی کاهش تولید گونههای فعال اکسیژن و مهار فیبروز را نشان داده است، اما شواهد بالینی محدود است.
چشمانداز تشخیص زودهنگام با OCT و OCT-A
Section titled “چشمانداز تشخیص زودهنگام با OCT و OCT-A”تشخیص نازک شدن pRNFL و GCIPL با OCT ممکن است امکان تشخیص نوروپاتی بینایی ناشی از پرتو را قبل از بروز علائم فراهم کند 2). مقیاس درجهبندی OCT-A نیز به عنوان یک ابزار غیرتهاجمی برای پیگیری در آینده مورد انتظار است. با ایجاد یک ثبت بینالمللی، انتظار میرود که درک بیشتری از مشخصات بالینی حاصل شود.
8. منابع
Section titled “8. منابع”- Abduraman S, Mali B, Celebi ARC. Taxane-associated retinopathy and radiation-induced optic neuropathy in a young female patient with metastatic breast cancer. GMS Ophthalmol Cases. 2025;15:Doc07.
- Grosinger A, Chen JJ, Link MJ, Bhatti MT. Detection of asymptomatic radiation induced optic neuropathy with optical coherence tomography. Neuroophthalmology. 2021;45(5):339-342.
- Oakey Z, Yeşiltaş YS, Singh AD. Radiation Optic Neuropathy: Management Options. Ocul Oncol Pathol. 2023;9(5-6):166-171. PMID: 38089180.
