โรคเส้นประสาทตาจากรังสี รักษา (RON) เป็นความผิดปกติของเส้นประสาทตา ที่เกิดจากการเปลี่ยนแปลงของภาวะขาดเลือดที่เกิดขึ้นช้าหลังการฉายรังสี โดยตำแหน่งที่พบบ่อยคือบริเวณออปติกไคแอซึมหรือบริเวณรอบๆการฉายรังสีแบบแบ่งครั้งโดยให้ขนาดครั้งละไม่เกิน 2 Gy และขนาดรวมไม่เกิน 50 Gy ถือว่าค่อนข้างปลอดภัย และการแพร่หลายของมีดแกมมาช่วยลดอุบัติการณ์ลงอย่างมาก
การเกิดโรคมีช่วงเวลาตั้งแต่ 3 เดือนถึงหลายปีหลังการฉายรังสี ส่วนใหญ่เกิดขึ้นภายใน 3 ปี โดยจุดสูงสุดอยู่ที่ประมาณ 1.5 ปีหลังการฉายรังสี
โดยทั่วไปจะเริ่มมีอาการแบบไม่เจ็บปวดและสูญเสียการมองเห็น อย่างกะทันหัน การพยากรณ์โรคไม่ดี โดยประมาณครึ่งหนึ่งของผู้ป่วยจะสูญเสียการรับรู้แสงในที่สุด
ไม่มีวิธีการรักษาที่จำเพาะเจาะจง สำหรับผู้ป่วยที่เพิ่งเริ่มมีอาการ การให้สเตียรอยด์ ทางระบบ การรักษาด้วยยาต้านการแข็งตัวของเลือด และการบำบัดด้วยออกซิเจนความดันสูง อาจมีประโยชน์ในระดับหนึ่ง
การตรวจพบการบางลงของ pRNFL และ GCI PL ด้วยเครื่องตรวจการเชื่อมโยงกันของแสง (OCT ) และการเพิ่มความเข้มของสารทึบรังสีด้วย MRI มีประโยชน์ในการวินิจฉัยระยะแรก และสามารถตรวจพบได้ในระยะที่ยังไม่มีอาการ
โรคเส้นประสาทตาจากรังสี รักษา (radiation optic neuropathy: RON) เป็นความผิดปกติของเส้นประสาทตา ที่เกิดจากการเปลี่ยนแปลงของภาวะขาดเลือดที่เกิดขึ้นช้าหลังการฉายรังสีบริเวณออปติกแอพพาราตัส ออปติกแอพพาราตัสมีความไวต่อรังสีสูง และการทำงานของการมองเห็น จะสูญเสียไปจากกลไกที่เกิดจากความเสียหายของเยื่อบุผนังหลอดเลือดเป็นหลัก
ตำแหน่งที่พบบ่อยคือบริเวณออปติกไคแอสม์หรือบริเวณใกล้เคียง แบ่งเป็น RON ส่วนหน้า (anterior RON) และ RON ส่วนหลัง (posterior RON) RON ส่วนหน้าเกิดจากการรักษาด้วยโปรตอนบีม หรือการฝังแร่สำหรับเนื้องอกในเบ้าตา คอรอยด์ และจอประสาทตา ส่วน RON ส่วนหลังเกิดจากการรักษาเนื้องอกในโพรงไซนัสและฐานกะโหลกศีรษะ
ความเสี่ยงในการเกิดโรคสัมพันธ์อย่างใกล้ชิดกับปริมาณรังสีที่ได้รับ ด้านล่างนี้แสดงปริมาณรังสีและความเสี่ยงโดยประมาณ
เงื่อนไขการฉายรังสี ความเสี่ยงในการเกิดโรค ปริมาณรังสีรวมน้อยกว่า 5,000 cGy พบได้น้อย ปริมาณรังสีรวม 5,000–6,000 cGy สูงสุด 5% ภายใน 10 ปี ขนาดยาต่อครั้ง ≤2 Gy · ขนาดยารวม ≤50 Gy ค่อนข้างปลอดภัย Gamma Knife 800–1,000 cGy ครั้งเดียว (1–3 ครั้ง) ค่อนข้างปลอดภัย
ระยะเวลาที่เริ่มมีอาการมีตั้งแต่ 3 เดือนถึงหลายปีหลังการฉายรังสี โดยส่วนใหญ่จะเกิดภายใน 3 ปี จุดสูงสุดคือ 1.5 ปีหลังการฉายรังสี และการเริ่มมีอาการที่พบบ่อยที่สุดคือ 8–16 เดือนหลังการรักษา การใช้ Gamma Knife อย่างแพร่หลายช่วยลดอุบัติการณ์ของ RON ลงอย่างมาก
Q
หากได้รับการฉายรังสี มีโอกาสเป็นโรคเส้นประสาทตาจากรังสีมากน้อยเพียงใด?
A
การฉายรังสีแบบแบ่งขนาดยารวมน้อยกว่า 5,000 cGy (50 Gy) มักไม่ค่อยทำให้เกิดโรค การฉายรังสี 5,000–6,000 cGy มีความเสี่ยงสูงถึง 5% ภายใน 10 ปี หากขนาดยาต่อครั้ง ≤2 Gy และขนาดยารวม ≤50 Gy ถือว่าค่อนข้างปลอดภัย และค่าเหล่านี้ใช้เป็นเกณฑ์ในการวางแผนการฉายรังสี
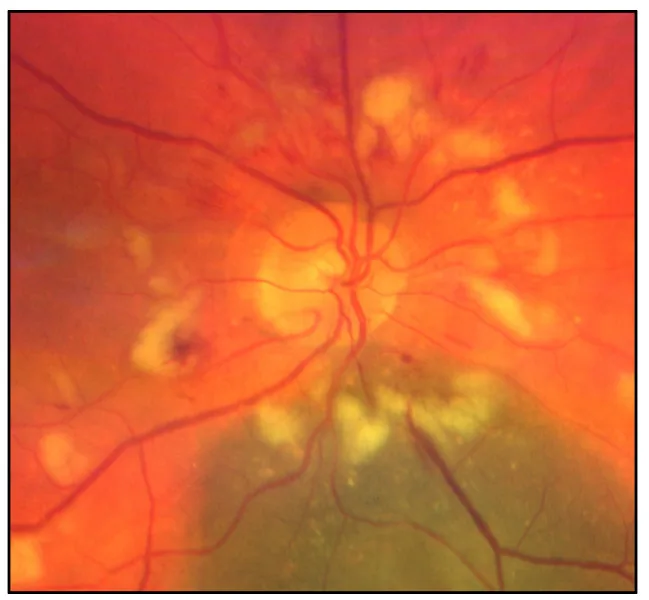
ภาพถ่ายจอประสาทตาของโรคเส้นประสาทตาจากรังสี แสดงอาการบวมของหัวประสาทตา และเลือดออกและสารหลั่งสีขาวรอบหัวประสาทตา Midena G, et al. Chorioretinal Side Effects of Therapeutic Ocular Irradiation: A Multimodal Imaging Approach. J Clin Med. 2020. Figure 3. PM
CI D: PMC7693915. License: CC BY.
ภาพถ่ายสี
จอประสาทตา ของโรค
จอประสาทตา และ
คอรอยด์ จากรังสีหลัง
การรักษาด้วยเลเซอร์ แสดงการฝ่อของ
คอรอยด์ และ
จอประสาทตา ภาวะขาดเลือด หลอดเลือดผี ฝ้าขาวนิ่ม ฝ้าขาวแข็ง และเลือดออกใน
จอประสาทตา ทั้งในบริเวณจุดรับภาพ (โรค
จอประสาทตา จากรังสี) และ
เส้นประสาทตา (
โรคเส้นประสาทตาจากรังสี ) ซึ่งสอดคล้องกับ
โรคเส้นประสาทตาจากรังสี ที่กล่าวถึงในหัวข้อ “2. อาการหลักและอาการแสดงทางคลินิก”
สายตาเลือนราง : เริ่มมีอาการสายตาเลือนรางที่แย่ลงอย่างรวดเร็วในช่วงหลายสัปดาห์ เกิดขึ้นข้างเดียวหรือสองข้าง มักไม่เจ็บปวดความผิดปกติของการมองเห็นสี ความผิดปกติของการมองเห็นสี ร่วมด้วยรูปแบบการเกิด : แบ่งเป็นชนิดเฉียบพลัน (ระหว่างการรักษา) ชนิดเกิดเร็วหลังการฉายรังสี (3 เดือนหลังฉายรังสี) และชนิดเกิดช้าหลังการฉายรังสี (6 เดือนถึง 10 ปีหลังฉายรังสี)กรณีเกิดในสองข้าง : อาการของตาข้างที่สองมักเกิดขึ้นภายในไม่กี่สัปดาห์
RON ส่วนหน้า
อาการบวมของหัวประสาทตา : ในชนิด anterior ischemic optic neuropathy จะมีอาการบวมของหัวประสาทตา ร่วมกับเลือดออก และความผิดปกติของหลอดเลือดขนาดเล็ก
หัวประสาทตาซีด : อาการบวมจะเปลี่ยนเป็นสีซีดของหัวประสาทตาภายใน 4-6 สัปดาห์
การเกิดร่วมกับจอประสาทตา ฉายรังสี : อาจพบร่วมกันได้
RON ส่วนหลัง
หัวประสาทตาปกติหรือซีด : ใน RON ส่วนหลังจะพบการเปลี่ยนแปลงของอวัยวะภายในตาได้น้อย หัวประสาทตาจะปกติหรือซีด
รูปแบบของลานสายตาบกพร่อง : การบาดเจ็บที่ optic chiasm จะทำให้เกิด hemianopsia ด้านขมับ ส่วนการบาดเจ็บที่ optic tract จะทำให้เกิด contralateral homonymous hemianopsia ร่วมกับ band atrophy
RAPD RAPD )
ผู้ป่วยหญิงอายุ 42 ปี (ได้รับรังสี 50 Gy สำหรับการแพร่กระจายของมะเร็งเต้านมไปยังสมอง) หนึ่งปีหลังการฉายรังสี พบว่าตาขวามีข้อบกพร่องของลานสายตาส่วนบนอย่างรุนแรง เส้นประสาทตา ซีดเป็นปล้องส่วนล่าง และ RAPD เป็นบวก ในที่สุดตาขวาเหลือเพียงการรับรู้แสง (amaurotic pupil) 1)
ผู้ป่วยหญิงอายุ 74 ปี (ได้รับรังสี 54 Gy หลังการผ่าเนื้องอกเยื่อหุ้มสมอง) ที่ 22 เดือนหลังการฉายรังสี แม้ตาซ้ายจะมีสายตา 20/20 และไม่มีอาการ แต่ OCT ตรวจพบการบางลงของ pRNFL และ GCI PL 2)
รังสีทำลายเซลล์ผ่านสองเส้นทาง: การทำลายพันธะโมเลกุลโดยตรง และการทำลายทางอ้อมผ่านการเกิดอนุมูลอิสระ ตามกฎของ Bergonie-Tribondeau เซลล์ที่มีการแบ่งตัวบ่อยและมีความแตกต่างน้อยจะไวต่อรังสีมากกว่า การทำลายเซลล์บุผนังหลอดเลือดทำให้การซึมผ่านของหลอดเลือดเพิ่มขึ้นและการอุดตันของเส้นเลือดฝอย นำไปสู่ภาวะเส้นประสาทตา ขาดเลือดในที่สุด
ปริมาณรังสี : ปริมาณรวม ปริมาณต่อครั้ง และช่วงเวลาระหว่างการฉายรังสี ล้วนมีผลต่อความเสี่ยงโรคเบาหวาน : เพิ่มความเสี่ยงของโรคหลอดเลือดขาดเลือด และเพิ่มความเสี่ยงในการเกิด RONความดันโลหิตสูงและโรคหลอดเลือดที่มีอยู่เดิม : ผู้ที่มีรอยโรคหลอดเลือดอยู่เดิมมีความเสี่ยงสูงขึ้นการใช้เคมีบำบัดร่วม : อาจเพิ่มความเสียหายจากรังสี อายุของผู้ป่วย : อายุถือเป็นปัจจัยเสี่ยงอย่างหนึ่ง
หากคุณมีปัจจัยเสี่ยงทางหลอดเลือด เช่น เบาหวานหรือความดันโลหิตสูง ควรแจ้งให้แพทย์ผู้รักษาทราบก่อนการฉายรังสี หลังการฉายรังสี การตรวจตาเป็นประจำเพื่อติดตามการทำงานของสายตาเป็นสิ่งสำคัญ หากสังเกตเห็นการเปลี่ยนแปลงของการมองเห็น หรือมีจุดบอดในลานสายตา ควรรีบไปพบแพทย์ทันที
Q
ผู้ป่วยเบาหวานมีแนวโน้มเป็นโรคเส้นประสาทตาจากรังสีได้ง่ายหรือไม่?
A
ผู้ป่วยเบาหวานมีความเสี่ยงสูงต่อโรคหลอดเลือดขาดเลือด จึงถือว่ามีความเสี่ยงเพิ่มขึ้นในการเกิด RON ความดันโลหิตสูงและรอยโรคหลอดเลือดที่มีอยู่เดิมก็เป็นปัจจัยเสี่ยงเช่นกัน การใช้เคมีบำบัดร่วมอาจเพิ่มความเสี่ยงได้ ในกรณีที่มีปัจจัยเหล่านี้ร่วมกัน จำเป็นต้องวางแผนการฉายรังสีและติดตามผลอย่างระมัดระวังเป็นพิเศษ
โรคเส้นประสาทตาจากรังสี รักษาเป็นการวินิจฉัยโดยการแยกโรค ซึ่งต้องวินิจฉัยหลังจากแยกโรคที่คล้ายคลึงกันออกแล้ว
โรคที่ต้องแยกออกได้แก่
โรคเส้นประสาทตาถูกกดทับ การกดทับเส้นประสาทตา จากการกลับเป็นซ้ำของเนื้องอกโรคเส้นประสาทตา ชนิดแทรกซึม เยื่อหุ้มสมองอักเสบจากมะเร็งโรคเส้นประสาทตาจากพิษ ที่เกิดตามหลังเคมีบำบัดโรคเส้นประสาทตา จากพารานีโอพลาสติก เยื่อหุ้มสมองชั้นกลางอักเสบหลอดเลือดแดงเซลล์ยักษ์ (การแยกโรคในผู้สูงอายุ)
อาจจำเป็นต้องตรวจน้ำไขสันหลังโดยการเจาะเอว (เพื่อแยกเยื่อหุ้มสมองอักเสบจากมะเร็ง) และการตรวจทางซีรั่มวิทยา (เพื่อค้นหากลุ่มอาการพารานีโอพลาสติก )
MRI (ทางเลือกแรก) : MRI เป็นทางเลือกแรกสำหรับโรคเส้นประสาทตา โดยภาพ STIR และภาพ T1-weighted ที่มีการเพิ่มความเข้มด้วย Gd ในแนว冠状ตัดมีประโยชน์ แนะนำให้ใช้เครื่อง 3T และความหนาชิ้น ≤3 มม. จะพบการเพิ่มความเข้มของเส้นประสาทตา ที่ได้รับผลกระทบ ในระยะแรกอาจแยกจากภาวะการกลับเป็นซ้ำของเนื้องอกได้ยาก ในรายงานที่ 2) พบว่าภาพ MRI T1-weighted ที่มีการเพิ่มความเข้มพบการโป่งและการเพิ่มความเข้มของเส้นประสาทตา ส่วนหน้าบริเวณจุดไขว้ประสาทตาซ้ายOCT RNFL และ GCI PL และอาจตรวจพบการเปลี่ยนแปลงก่อนที่จะมีอาการ 2) มีการแนะนำว่ามีประโยชน์เป็นเครื่องมือคัดกรองหลังการรักษาด้วยรังสีOCT -A (Optical Coherence Tomography Angiography)RPC P) ซึ่งเป็นวิธีการประเมินแบบไม่รุกล้ำที่ได้รับความสนใจ
ด้านล่างนี้คือภาพรวมของระดับคะแนน OCT -A
ระดับ ผลการตรวจ 0 การกระจายแบบรัศมีปกติของ RPC P 1 การหายไปของรูปแบบรัศมีเริ่มต้นของ RPC P 2 ภาวะเลือดไปเลี้ยงรอบหัวประสาทตาน้อยกว่า 2 ควอดแรนต์ 3 ภาวะเลือดไปเลี้ยงน้อยใน 2 ควอดแรนต์ขึ้นไป 4 ภาวะเลือดไหลเวียนน้อยแบบกระจายในทั้ง 4 ควอดแรนต์
เกรด 1 ถึง 3 มีการแบ่งย่อยด้วย ”+” (การมีส่วนร่วมของมัดเส้นใยประสาทจอประสาทตา ส่วน papilloma cular) ซึ่งสัมพันธ์กับการมองเห็น ที่ลดลง
Q
จะตรวจพบโรคเส้นประสาทตาจากรังสีได้ตั้งแต่ระยะเริ่มต้นได้อย่างไร?
A
การตรวจพบการบางลงของ pRNFL และ GCI PL ด้วย OCT อาจจับการเปลี่ยนแปลงก่อนที่อาการจะปรากฏ2) MRI แสดงการเพิ่มความเข้มของเส้นประสาทตา ที่ได้รับผลกระทบ การติดตามทางจักษุวิทยาอย่างสม่ำเสมอหลังการฉายรังสีช่วยในการตรวจพบ RON ตั้งแต่ระยะแรก และมีรายงานที่เสนอให้ติดตาม MRI เป็นประจำในช่วง 10-20 เดือนหลังการฉายรังสีภายนอก2)
โดยทั่วไปไม่มีการรักษาที่หายขาด และการพยากรณ์โรคมักไม่ดี ในกรณีที่เพิ่งเริ่มมีอาการและยังไม่เกิดการฝ่อของเส้นประสาทตา การรักษาต่อไปนี้อาจมีประโยชน์ในระดับหนึ่ง
การให้สเตียรอยด์ ทั่วร่างกาย : ทำในระยะเริ่มแรก มีรายงานผู้ป่วยที่ได้รับ prednisolone 50 มก./วัน1) และบางรายได้รับ prednisone 60 มก./วัน เป็นเวลา 4 สัปดาห์2) อย่างไรก็ตาม มีรายงานว่าสเตียรอยด์ และการรักษาด้วยยาต้านการแข็งตัวของเลือด ไม่ประสบความสำเร็จในการรักษา RONการรักษาด้วยยาต้านการแข็งตัวของเลือด การบำบัดด้วยออกซิเจนความดันสูง (HBOT)ตาแห้ง และสายตาสั้น แบบชั่วคราว มีค่าใช้จ่ายสูง และอาจเกิดการดำเนินโรคอีกครั้งหลังจากหยุดการรักษา
ร้อยละ 45 ของดวงตาที่ได้รับผลกระทบจะมีค่าสายตาสุดท้ายต่ำกว่า 20/200 ถึงเหลือเพียงการรับรู้แสง
ประมาณครึ่งหนึ่งของผู้ป่วยจะมีค่าสายตาสุดท้ายไม่มีการรับรู้แสง
อาจนำไปสู่การสูญเสียการมองเห็น ถาวรข้างเดียวหรือทั้งสองข้าง
Q
โรคเส้นประสาทตาจากรังสีรักษาสามารถฟื้นฟูการมองเห็นได้หรือไม่?
A
ไม่มีวิธีการรักษาที่เป็นสาเหตุ และการพยากรณ์โรคมักไม่ดี ผู้ป่วยร้อยละ 45 ของตาที่ได้รับผลกระทบจะมีระดับการมองเห็น สุดท้ายน้อยกว่า 20/200 ถึงแค่รับรู้แสง และประมาณครึ่งหนึ่งจะไม่มีการรับรู้แสงเลย การให้สเตียรอยด์ ทางระบบ การบำบัดด้วยออกซิเจนความดันสูง และการรักษาด้วยยาต้านการแข็งตัวของเลือด อาจมีประโยชน์บ้างในผู้ป่วยที่เพิ่งเริ่มมีอาการ แต่ไม่มีการรักษาใดที่รับประกันการฟื้นฟูการมองเห็น
กลไกการเกิดโรค RON เกี่ยวข้องทั้งความเสียหายของหลอดเลือด (หลอดเลือดอักเสบจากรังสี) และความเสียหายโดยตรงจากรังสีต่ออวัยวะรับภาพ ยังไม่ทราบแน่ชัดว่าความเสียหายเริ่มแรกเกิดขึ้นที่ระบบหลอดเลือดหรือเนื้อเยื่อประสาท
ระยะเริ่มแรก (ภายในไม่กี่สัปดาห์)
การอักเสบที่สามารถกลับคืนได้และความผิดปกติของหลอดเลือดที่มีการรั่วซึม : การเพิ่มขึ้นของการซึมผ่านของหลอดเลือดเป็นจุดศูนย์กลาง การเปลี่ยนแปลงในระยะนี้ถือว่าสามารถกลับคืนได้
ระยะลุกลาม (หลายเดือนถึงหลายปี)
การอุดตันของหลอดเลือดและการเพิ่มจำนวนของเซลล์บุผนังหลอดเลือด : เกิดความเสียหายจากอนุมูลอิสระ
ความล้มเหลวของหลอดเลือดขนาดเล็ก : เกิดความล้มเหลวของหลอดเลือดขนาดเล็กที่มาพร้อมกับภาวะขาดออกซิเจน นอกจากนี้ยังเกิดความเสียหายโดยตรงต่อดีเอ็นเอของเซลล์และอุปสรรคเลือด-สมอง
ระยะที่ไม่สามารถย้อนกลับได้
การสูญเสียปลอกไมอีลินและการเกิดปฏิกิริยาแอสโตรไซโทซิส : ความเสียหายลุกลามไปยังเส้นประสาทรอบข้าง นำไปสู่การสูญเสียการมองเห็น อย่างถาวร
ความเสียหายของเซลล์จากรังสีเกิดขึ้นผ่าน 2 เส้นทาง เส้นทางแรกคือความเสียหายโดยตรงจากการทำลายพันธะโมเลกุล เส้นทางที่สองคือความเสียหายทางอ้อมจากการเกิดอนุมูลอิสระ ตามกฎของ Bergonie-Tribondeau เซลล์ที่มีการแบ่งตัวบ่อยและมีความแตกต่างน้อยจะไวต่อความเสียหายมากกว่า ความเสียหายต่อเซลล์บุผนังหลอดเลือดทำให้เกิดการเพิ่มขึ้นของการซึมผ่านของเส้นเลือดฝอยและการอุดตัน ส่งผลให้ VEGF ในท้องถิ่นสูงขึ้นและเกิดปฏิกิริยาการอักเสบ นำไปสู่ภาวะเส้นประสาทตา ขาดเลือด
เนื้อหาต่อไปนี้อยู่ในขั้นตอนการวิจัยหรือการทดลองทางคลินิก และไม่ใช่การรักษามาตรฐานที่สามารถรับได้ในโรงพยาบาลทั่วไป เป็นข้อมูลอ้างอิงสำหรับผู้เชี่ยวชาญเกี่ยวกับการพัฒนาทางการแพทย์ในอนาคต
เบวาซิซูแมบ กำลังได้รับความสนใจในฐานะการรักษาที่มุ่งเป้าไปที่การเพิ่มขึ้นของ VEGF ในท้องถิ่นที่เกิดจากความเสียหายของเซลล์บุผนังหลอดเลือด มีรายงานการให้ยาแบบทั่วร่างกาย (ทุก 3 สัปดาห์ รวม 4 ครั้ง) หรือการฉีดเข้าแก้วตา (อย่างน้อย 2 ครั้ง ทุก 6-8 สัปดาห์) และมีรายงานว่าสามารถปรับปรุงการมองเห็น และการมองเห็น สีให้คงที่ได้นานถึง 3 ปี
เพนทอกซิฟิลลีน (Trental) ซึ่งเป็นอนุพันธ์ของเมทิลแซนทีน แสดงให้เห็นถึงศักยภาพในการปรับเปลี่ยนความหนืดของเลือดและช่วยปรับปรุงการไหลเวียน โดยมีรายงานผลลัพธ์ที่มีแนวโน้มดี ในรายงานผู้ป่วยจริง มีการสั่งจ่ายเพนทอกซิฟิลลีนในขนาด 1,200 มก./วัน2)
มีรายงานว่าการให้ยา ACE inhibitor (ramipril) ตั้งแต่ 2 สัปดาห์หลังการฉายรังสีเป็นเวลาประมาณ 6 เดือน สามารถลดการปล่อยไซโตไคน์ที่ก่อให้เกิดการอักเสบได้ อย่างไรก็ตาม ในปัจจุบันพบผลดังกล่าวเฉพาะในแบบจำลองหนูเท่านั้น ยังไม่มีการนำมาใช้ในมนุษย์อย่างเป็นทางการ
วิตามินอีแสดงให้เห็นในการศึกษาในหลอดทดลองว่าช่วยลดการสร้างอนุมูลอิสระและยับยั้งการเกิดพังผืด แต่หลักฐานทางคลินิกยังมีจำกัด
การตรวจพบการบางลงของ pRNFL และ GCI PL ด้วย OCT อาจช่วยวินิจฉัยโรคเส้นประสาทตาจากรังสี รักษาก่อนที่จะมีอาการ2) ระดับคะแนนจาก OCT -A ยังคาดว่าจะถูกนำมาใช้เป็นเครื่องมือติดตามผลแบบไม่รุกล้ำในอนาคต การจัดตั้งทะเบียนผู้ป่วยในระดับนานาชาติจะช่วยให้เข้าใจลักษณะทางคลินิกได้ดียิ่งขึ้น
Abduraman S, Mali B, Celebi ARC. Taxane-associated retinopathy and radiation-induced optic neuropathy in a young female patient with metastatic breast cancer. GMS Ophthalmol Cases. 2025;15:Doc07.
Grosinger A, Chen JJ, Link MJ, Bhatti MT. Detection of asymptomatic radiation induced optic neuropathy with optical coherence tomography. Neuroophthalmology. 2021;45(5):339-342.
Oakey Z, Yeşiltaş YS, Singh AD. Radiation Optic Neuropathy : Management Options. Ocul Oncol Pathol. 2023;9(5-6):166-171. PMID: 38089180.
ถาม AI เกี่ยวกับบทความนี้
คัดลอกข้อความบทความแล้ววางในผู้ช่วย AI ที่คุณต้องการใช้
เปิดผู้ช่วย AI ด้านล่าง แล้ววางข้อความที่คัดลอกลงในช่องแชต