Neuropathie optique ischémique antérieure non artéritique (NAION)

Neuropathie optique
1. Qu’est-ce que la neuropathie optique ?
Section intitulée « 1. Qu’est-ce que la neuropathie optique ? »La neuropathie optique est un terme générique désignant un groupe de maladies dans lesquelles le nerf optique est endommagé, entraînant une diminution de la fonction visuelle. Elle se manifeste par une baisse de l’acuité visuelle, un déficit du champ visuel, une dyschromatopsie et/ou une diminution de la sensibilité au contraste 2).
視神経は網膜神経節細胞(RGC)の軸索約120万本から構成される。眼球内で視神経乳頭として束ねられ、視神経管を経て視交叉に至る。視神経乳頭から視交叉前までの障害が「前部視路障害」であり、臨床的に問題となる視神経症の大半がこの部位に相当する2)。視交叉以降(視索・視放線・後頭葉)の障害は「後部視路障害」であり、視神経症ではなく「視路障害」として扱われる。
視神経は4区分に分けられる。眼球内部(乳頭部、約1 mm)は虚血性・炎症性視神経症が好発する。眼窩内部(約25 mm)は圧迫性・炎症性が多い。管内部(視神経管、約5〜8 mm)は外傷性や骨性圧迫が起きやすい。頭蓋内部(約10 mm)は下垂体腺腫や頭蓋咽頭腫による圧迫が多い。視神経乳頭を直接観察できる「前部視神経症」と、眼底が正常に見える「球後視神経症」の区別も重要である。球後視神経症では眼底に乳頭変化がないため、視力低下の原因として見落とされやすい。
視神経乳頭の血流は短後毛様動脈(SPC動脈)が主として担っている。SPC動脈は眼動脈の終枝であり、視神経乳頭前層部・篩状板・篩状板後部に血流を供給する。この部分の循環障害がNAIONおよびAAIONの主要な病態基盤となる3)。視神経内部は血液脳関門によって保護されているが、この保護機構が炎症性視神経炎や自己免疫疾患では破綻する2)。
病態の共通経路と視神経萎縮
Section intitulée « 病態の共通経路と視神経萎縮 »原因が異なっても、最終的には網膜神経節細胞および視神経軸索のダメージ→アポトーシス→視神経萎縮という共通経路をたどる。視神経萎縮(optic atrophy)は視神経症の終末像であり、乳頭の蒼白化として認識される。萎縮が確立すると視機能の回復は著しく限定的となる2)。
視神経軸索は直径0.2〜10 μmの有髄・無髄線維の混合体であり、p細胞(輝度・コントラスト担当)とm細胞(動き・輪郭担当)に大別される。視神経症では特にATP消費の激しいp細胞が障害されやすく、中毒性・栄養性視神経症での中心暗点の発生機序と関連する2)。
Aperçu épidémiologique
Section intitulée « Aperçu épidémiologique »Aperçu de l’incidence annuelle des principales neuropathies optiques (pour 100 000 adultes). La NAION est la plus fréquente avec 2,3 à 10,2 (États-Unis)3). La névrite optique idiopathique est estimée à 1,6 (adultes japonais)13), et la LHON (neuropathie optique héréditaire de Leber) compte environ 117 nouveaux cas par an au Japon (enquête 2014), ce qui en fait une maladie rare14). L’incidence annuelle estimée de l’AAION/GCA chez les plus de 50 ans est de 0,36 pour 100 000, plus fréquente chez les Blancs nordiques (environ 30 pour 100 000 en Norvège). Les complications visuelles de la GCA surviennent dans 10 à 30 % des cas (jusqu’à 70 % selon certains rapports), et l’AAION en représente 60 à 90 %1). L’incidence annuelle de la MOGAD est estimée entre 1,6 et 4,8 par million d’habitants6).
Classification des neuropathies optiques
Section intitulée « Classification des neuropathies optiques »Les neuropathies optiques sont classées selon plusieurs perspectives. La classification la plus utile cliniquement est présentée ci-dessous.
Classification selon le mode d’apparition
- Aiguë (quelques heures à quelques jours) : NAION, AAION, traumatique
- Subaigu (quelques jours à quelques semaines) : névrite optique idiopathique, LHON, compressif (partiel)
- Chronique (mois à années) : ADOA, compressif chronique, radique (tardif)
Classification par cause
- Ischémique : NAION, AAION, PION
- Inflammatoire (névrite optique) : idiopathique, lié à la SEP, lié au NMOSD, lié au MOGAD, infectieux
- Compressif : tumeur, kyste, anévrisme, orbitopathie thyroïdienne
- Toxique : éthambutol, amiodarone, alcool, etc.
- Nutritionnel : carence en vitamine B12/B1, acide folique, cuivre
- Héréditaire : LHON, ADOA, syndrome de Wolfram
- Traumatique : fracture du canal optique, lésion directe
- Radique : dégénérescence ischémique tardive
Classification par localisation
- Neuropathie optique antérieure (avec modifications de la papille) : NAION, AAION, névrite optique antérieure
- Neuropathie optique rétrobulbaire (papille normale) : toxique, héréditaire, névrite optique liée à la SEP (la plupart)
- Lésion chiasmatique : adénome hypophysaire, craniopharyngiome (hémianopsie bitemporale)
Cadre diagnostique de la neuropathie optique
Section intitulée « Cadre diagnostique de la neuropathie optique »Le diagnostic de la neuropathie optique se fait en 5 étapes.
Étape 1 : Confirmation du dysfonctionnement du nerf optique Utiliser le RAPD, l’acuité visuelle, la vision des couleurs et le champ visuel pour confirmer objectivement le dysfonctionnement du nerf optique.
Étape 2 : Localisation de la lésion Antérieure (avec modification papillaire) ou rétrobulbaire (papille normale), intra-orbitaire, intracanalaire ou intracrânienne. Estimer la localisation à l’aide du schéma de déficit du champ visuel.
Étape 3 : Unilatéral ou bilatéral ? Aigu ou chronique ? Cela permet de réduire considérablement le diagnostic différentiel.
Étape 4 : Exclusion des formes dangereuses Exclure en priorité l’ACG (VS, CRP), les causes compressives (IRM) et infectieuses (syphilis, champignons).
Étape 5 : Examens spécifiques Ajouter les anticorps anti-AQP4, anti-MOG, l’analyse de l’ADNmt et les examens nutritionnels selon le type.
2. Différence avec la névrite optique (clarification conceptuelle)
Section intitulée « 2. Différence avec la névrite optique (clarification conceptuelle) »La « névrite optique » et la « neuropathie optique » sont souvent confondues en pratique clinique, mais elles entretiennent une relation de sous-concept et de sur-concept.
Confondre une neuropathie optique non inflammatoire (ischémique, compressive, toxique, héréditaire) avec une névrite optique peut entraîner une administration inappropriée de stéroïdes. En particulier, l’aspergillose infiltrante est une contre-indication aux stéroïdes 2), et l’administration de stéroïdes dans la phase aiguë de la LHON est non seulement inefficace mais retarde également le diagnostic définitif.
Principales caractéristiques cliniques de la névrite optique
Section intitulée « Principales caractéristiques cliniques de la névrite optique »La névrite optique (inflammatoire) présente les caractéristiques suivantes qui aident à la distinguer de la névrite non inflammatoire.
- Début aigu : progression sur quelques jours à 2 semaines, puis tendance à la récupération dans les 5 semaines.
- Douleur oculaire lors des mouvements : présente dans environ 50 % des cas. Habituellement absente dans les formes ischémiques, compressives ou toxiques.
- Âge de prédilection : 15 à 45 ans (la forme ischémique survient généralement après 50 ans).
- Imagerie IRM : prise de contraste typique du nerf optique (T1 avec gadolinium).
- Récupération spontanée : dans les formes idiopathiques ou associées à la SEP, plus de 90 % des patients retrouvent une acuité visuelle d’au moins 0,5 après un an (étude ONTT)4).
- Risque de transition vers la SEP : 15 ans après le premier épisode, 25 % sans lésion IRM cérébrale et 78 % avec lésion évoluent vers la SEP4).
Situations de diagnostic difficile
Section intitulée « Situations de diagnostic difficile »Ci-dessous, le diagnostic différentiel entre névrite optique et neuropathie optique non inflammatoire devient difficile.
- Femme de plus de 50 ans avec baisse d’acuité visuelle aiguë unilatérale : NAION vs névrite optique avec anticorps anti-AQP4 (NMOSD)
- Baisse d’acuité visuelle aiguë bilatérale chez un jeune : LHON vs névrite optique bilatérale simultanée vs neuropathie optique toxique
- Baisse d’acuité visuelle unilatérale avec œdème papillaire : NAION vs névrite optique antérieure vs papillite vasculaire
La névrite optique avec anticorps anti-AQP4 est une maladie réfractaire aux stéroïdes représentant environ 10 % des névrites optiques idiopathiques, survenant à un âge plus avancé que la névrite optique typique et touchant principalement les femmes (ratio femme/homme 1:9) 5). Les anticorps anti-AQP4 ciblent les canaux aquaporine-4 exprimés sur les astrocytes du nerf optique, provoquant une lésion cellulaire dépendante du complément 5). Les stratégies thérapeutiques diffèrent fondamentalement entre les cas positifs et négatifs pour les anticorps anti-AQP4, donc un test d’anticorps doit être demandé avant la corticothérapie pulsée. La méthode de dosage cellulaire (CBA) a une sensibilité et une spécificité plus élevées que l’ELISA, et la CBA est recommandée 5).
Avant d’administrer une corticothérapie pulsée pour une névrite optique, il est impératif d’exclure les infections (hépatite B, syphilis, VIH, infections fongiques) 2). L’administration de fortes doses de stéroïdes à un porteur du virus de l’hépatite B peut provoquer une hépatite fulminante. Dans la névrite optique syphilitique, les antibiotiques sont prioritaires sur les stéroïdes.
3. Formes cliniques à haute urgence
Section intitulée « 3. Formes cliniques à haute urgence »Le tableau ci-dessous présente les formes de neuropathie optique nécessitant une prise en charge urgente.
| Forme clinique | Urgence | Conséquences en cas d’omission |
|---|---|---|
| Neuropathie optique ischémique antérieure artéritique (NOIAA/AOC) | Très urgent | Cécité de l’œil controlatéral (65% non traités dans les 10 jours) 1) |
| Neuropathie optique compressive aiguë (tumeur, kyste, hématome) | Urgent | Atrophie optique progressive et perte visuelle irréversible |
| Neuropathie optique nasale (aspergillose infiltrante) | Urgence | Mortalité rapportée de 94% 2) |
| Neuropathie optique traumatique (fracture du canal optique) | Urgence | Traitement précoce peut préserver la fonction visuelle |
| Neuropathie optique ischémique postérieure (NOIP) | Urgence | Survient après une chirurgie ou une perte sanguine massive, souvent irréversible |
Protocole d’urgence pour la GCA
Section intitulée « Protocole d’urgence pour la GCA »L’amaurose fugace (amaurosis fugax) apparaît comme symptôme précurseur dans environ 30 % des cas de perte visuelle permanente, en moyenne 8,5 jours avant 1). À ce stade, suspecter une artérite à cellules géantes (ACG) et débuter activement les stéroïdes est crucial pour la prévention secondaire.
4. Porte d’entrée du diagnostic différentiel
Section intitulée « 4. Porte d’entrée du diagnostic différentiel »Le diagnostic différentiel des neuropathies optiques se systématise selon quatre axes : aigu ou chronique, unilatéral ou bilatéral, présence ou absence de douleur, et aspect de la papille.
Aigu ou chronique
Section intitulée « Aigu ou chronique »Aigu (atteignant le maximum en quelques heures à quelques jours)
- NAION : baisse soudaine de la vision remarquée au réveil, typique
- AAION : baisse rapide de la vision d’un œil, sévère (acuité visuelle inférieure à 20/200 dans plus de 60 % des cas) 1)
- Traumatique : immédiatement à quelques heures après le traumatisme
Subaigu (quelques jours à quelques semaines)
- Névrite optique idiopathique : progression sur 2 semaines, puis début de récupération
- LHON : baisse d’acuité visuelle unilatérale aiguë indolore, devenant bilatérale en quelques semaines à quelques mois
- Compressif : peut évoluer de manière subaiguë en cas de croissance tumorale rapide ou d’hémorragie
Chronique (progression lente sur des mois à des années)
- ADOA (atrophie optique autosomique dominante) : apparition à l’âge scolaire, bilatérale, lentement progressive
- Compressif chronique : dû à un adénome hypophysaire, une tumeur orbitaire, etc.
- Toxique ou nutritionnel : progression subaiguë à chronique en cas d’exposition prolongée ou de carence nutritionnelle
Un œil ou les deux yeux
Section intitulée « Un œil ou les deux yeux »Maladies à prédominance unilatérale
- NAION : généralement unilatérale (bilatérale simultanée extrêmement rare)
- AAION : débute unilatéralement, sans traitement, 65 % s’étendent à l’autre œil dans les 10 jours1)
- Névrite optique idiopathique / liée à la SEP : typiquement unilatérale
- Compressive, traumatique, radique : souvent unilatérale
Maladies à prédominance bilatérale
- LHON : d’abord unilatéral, puis bilatéral en quelques semaines à quelques mois (finalement presque 100 % bilatéral)
- ADOA : début bilatéral symétrique
- Toxique/nutritionnel : généralement bilatéral (si un œil est complètement normal, envisager d’exclure une cause toxique) 2)
- NMOSD/AQP4-IgG positif : sévère, bilatéral, récurrent. 60 à 69 % présentent une déficience permanente ≤ 20/200 dans au moins un œil 5)
- MOGAD : début bilatéral fréquent (très rare dans la SEP idiopathique) 6)
Présence ou absence de douleur
Section intitulée « Présence ou absence de douleur »| Avec douleur | Sans douleur (indolore) |
|---|---|
| Névrite optique idiopathique (douleur oculomotrice dans environ 50 % des cas)13) | NAION (pas de douleur oculaire, céphalées et claudication de la mâchoire sont des symptômes systémiques de l’ACG) |
| Névrite optique associée à la SEP | AAION (pas de douleur oculaire, claudication de la mâchoire et céphalées présentes) |
| NMOSD associé (douleur périorbitaire) | LHON·ADOA (indolore) 14) |
| MOGAD (souvent accompagné de céphalées) 6) | Toxique·nutritionnel (pas de douleur oculomotrice) |
| Traumatique (douleur due à la blessure) | Compressif (généralement indolore mais peut s’accompagner de douleur orbitaire) |
Classification basée sur les signes papillaires
Section intitulée « Classification basée sur les signes papillaires »5. Examen et tests
Section intitulée « 5. Examen et tests »Évaluation ophtalmologique obligatoire
Section intitulée « Évaluation ophtalmologique obligatoire »En cas de suspicion de neuropathie optique, effectuer systématiquement les évaluations suivantes.
Acuité visuelle et vision des couleurs L’acuité visuelle corrigée est fondamentale pour évaluer le degré de handicap et l’évolution. La vision des couleurs (Ishihara, Farnsworth-Munsell 100 hue) est souvent altérée précocement dans les neuropathies optiques, et des anomalies de la vision des couleurs peuvent précéder une baisse d’acuité visuelle. Dans les neuropathies optiques toxiques et nutritionnelles, un affaiblissement de la sensibilité au rouge est un signe précoce2). Dans l’ADOA (atrophie optique dominante autosomique), une anomalie acquise de la vision des couleurs du troisième type (anomalie bleu-jaune) est caractéristique, montrant un axe d’anomalie du troisième type au test de Farnsworth-Munsell 100 hue2).
RAPD (déficit pupillaire afférent relatif)
Le RAPD est évalué par la méthode de la lumière oscillante (test de l’éclairage alterné) et constitue un indicateur objectif de dysfonctionnement du nerf optique. Il est également utile pour différencier la simulation et les troubles visuels fonctionnels2).
OCT (tomographie par cohérence optique)
Section intitulée « OCT (tomographie par cohérence optique) »L’OCT est un examen essentiel pour l’évaluation du stade et le suivi de la neuropathie optique.
| Indicateur d’évaluation | Signes en phase aiguë | Signes en phase chronique |
|---|---|---|
| pRNFL (épaisseur de la RNFL péripapillaire) | Épaississement en cas d’œdème papillaire (attention aux faux positifs) | Amincissement en cas d’atrophie optique |
| GCL-IPL (épaisseur des cellules ganglionnaires + couche plexiforme interne) | Peu de changements | Amincissement reflétant une atteinte des cellules ganglionnaires rétiniennes |
| Forme de la tête du nerf optique | Disparition ou réduction de l’excavation | Fixation après atrophie |
Motif d’amincissement du pRNFL et diagnostic différentiel
Le motif d’amincissement du pRNFL à l’OCT est utile pour le diagnostic différentiel à partir de quelques semaines à quelques mois après l’apparition.
- Amincissement sévère circonférentiel : La NMOSD (type à anticorps anti-AQP4) est la plus sévère. Amincissement sévère sur toute la circonférence.
- Amincissement temporal prédominant (faisceau papillomaculaire) : toxique, nutritionnel, LHON, ADOA. Correspond à un scotome central.
- Amincissement sectoriel supérieur ou inférieur : NAION. Correspond à un déficit fasciculaire supérieur ou inférieur.
- MOGAD vs. lié à la SEP : L’amincissement du pRNFL après MOG-ON est plus sévère que dans la SEP6).
- Diagnostic différentiel avec le glaucome : Dans le glaucome, les modifications de la tête du nerf optique (élargissement de l’excavation) précèdent et le motif d’amincissement du GCL est différent.
Examen du champ visuel (périmètre de Humphrey)
Section intitulée « Examen du champ visuel (périmètre de Humphrey) »Le motif du déficit du champ visuel est directement lié à l’estimation anatomique du site de la lésion.
| Motif de déficit du champ visuel | Maladie principalement suspectée | Correspondance anatomique |
|---|---|---|
| Scotome central, scotome centro-cæcal | Toxique, nutritionnel, LHON, ADOA, névrite optique idiopathique2) | Lésion du faisceau papillo-maculaire (PMB) |
| Déficit horizontal (inféro-temporal à inférieur) | NAION (déficit fasciculaire) 3) | Ischémie de la moitié supérieure ou inférieure de la papille |
| Hémianopsie bitemporale | Compression chiasmatique (adénome hypophysaire, craniopharyngiome) | Fibres croisées centrales du chiasma |
| Hémianopsie homonyme (même côté) | Lésion post-chiasmatique (voie optique, radiations optiques, lobe occipital) | Voie visuelle centrale |
| Scotome jonctionnel | Lésion de la partie antérieure du chiasma, un type de neuropathie optique nasale | Faisceau papillo-maculaire + quadrant temporal supérieur controlatéral |
| Diminution générale de la sensibilité | Lié à la NMOSD / après une névrite optique sévère5) | Lésion étendue des fibres du nerf optique |
| Élargissement de la tache aveugle de Mariotte (acuité visuelle normale) | Drusen de la papille, papillite, périnévrite optique | Uniquement autour de la papille |

Analyses sanguines et du liquide céphalorachidien
Section intitulée « Analyses sanguines et du liquide céphalorachidien »Tests recommandés pour l’évaluation initiale de la neuropathie optique aiguë.
| Paramètre du test | Objectif | Signification clinique |
|---|---|---|
| VS, CRP, plaquettes | Exclusion de GCA (AAION) | Priorité maximale. La CRP a une spécificité plus élevée que la VS 1) |
| Anticorps anti-AQP4 (test cell-based) | Diagnostic de NMOSD | La méthode ELISA a une sensibilité et une spécificité inférieures à la méthode CBA 5) |
| Anticorps anti-MOG (test cell-based assay) | Diagnostic de MOGAD | Un CBA reconnaissant la molécule MOG native est essentiel6) |
| Sérologie syphilitique (TPHA, RPR) et VIH | Exclusion d’une névrite optique infectieuse | À vérifier impérativement avant les stéroïdes |
| Vitamine B12, B1, acide folique, cuivre | Évaluation de la neuropathie optique nutritionnelle | Particulièrement important après chirurgie bariatrique ou régime végétalien |
| Gènes mitochondriaux (mt11778, mt14484, mt3460) | Diagnostic de LHON | Ces 3 mutations couvrent plus de 95% des cas14) |
| β-D-glucane et culture fongique | Suspicion d’aspergillose invasive | Souvent élevé dans les formes invasives2) |
| ACE, lysozyme, TDM thoracique | Exclusion de la sarcoïdose | — |
| ANA, dsDNA, ANCA | Maladies auto-immunes systémiques (LED, vascularite) | — |
Indications de la ponction lombaire Suspicion de méningite infectieuse ou d’encéphalite, aide au diagnostic de NMOSD/MOGAD (pléiocytose du LCR, index IgG élevé), aide au diagnostic de SEP (bandes oligoclonales du LCR). Dans la NMOSD, une pléiocytose marquée pouvant atteindre plus de 50 cellules/μL peut survenir6).
Examens d’imagerie
Section intitulée « Examens d’imagerie »| Examen | Principales évaluations | Remarques |
|---|---|---|
| IRM orbitaire (T2 avec suppression de graisse / T1 avec contraste) | Inflammation, œdème, masse, rehaussement du nerf optique | Présence de rehaussement dans la névrite optique. Pas de rehaussement en phase aiguë de LHON14) |
| IRM cérébrale (FLAIR) | Lésions démyélinisantes (SEP, NMOSD), lésions intracrâniennes | Utilisé dans les critères de McDonald pour le diagnostic de SEP |
| CT (os) | Fracture du canal optique (traumatisme), pathologie sinusienne, calcification (drusen) | Indispensable en cas de traumatisme ou de maladie nasale |
| Échographie crânienne (Doppler couleur) | Signe du halo pour le diagnostic de GCA | Sensibilité 68%, spécificité 91% (100% si bilatéral) 1) |
| TEP-TDM (FDG) | Évaluation des lésions des gros vaisseaux dans l’ACG | Sensibilité 92%, spécificité 85% (essai GAPS)1) |
| Échographie orbitaire | Confirmation de la calcification de la drusen du disque optique | — |
Dans la neuropathie optique aiguë, une IRM orbitaire est en principe nécessaire. L’exclusion d’une lésion compressive est prioritaire, et la stratégie thérapeutique diffère considérablement selon qu’il s’agit d’un rehaussement (inflammatoire) concordant avec le nerf optique ou d’une compression/déformation (compressive) 2). En l’absence de signes inflammatoires du nerf optique à l’IRM avec contraste, on envisage une origine toxique, héréditaire ou nutritionnelle. Au stade aigu de la LHON, il n’y a pas de signes inflammatoires, et l’angiographie à la fluorescéine ne montre pas de fuite de colorant au niveau de la papille, ce qui constitue un point de différenciation important avec la névrite optique inflammatoire 14). En cas de contre-indication à l’IRM, un scanner des sinus, de l’orbite et du canal optique est réalisé.
Utilisation des potentiels évoqués visuels (PEV)
Section intitulée « Utilisation des potentiels évoqués visuels (PEV) »Les potentiels évoqués visuels (PEV) sont utiles comme marqueur de la névrite optique démyélinisante. Un allongement de la latence de P100 (normal ≤130 ms) suggère une démyélinisation, et dans la névrite optique associée à la SEP ou idiopathique, cet allongement persiste souvent après la récupération 13). Une diminution de l’amplitude est nettement observée dans les lésions axonales (toxiques, ischémiques). Dans la neuropathie optique toxique, il n’y a pas de retard de la latence de P100, seule l’amplitude est réduite, ce qui aide à la différenciation avec la névrite démyélinisante 13). Une diminution de la fréquence critique de fusion (CFF) reflète également le dysfonctionnement de la neuropathie optique, et est particulièrement marquée dans la névrite optique associée à la NMOSD 13).
6. Caractéristiques selon la cause
Section intitulée « 6. Caractéristiques selon la cause »Classification des principales neuropathies optiques par cause et résumé des caractéristiques de chaque type.
6-1. Neuropathie optique ischémique
Section intitulée « 6-1. Neuropathie optique ischémique »Neuropathie optique ischémique antérieure non artéritique (NAION)
Section intitulée « Neuropathie optique ischémique antérieure non artéritique (NAION) »La NAION est le type le plus fréquent de neuropathie optique aiguë chez l’adulte, survenant principalement après 50 ans3). Un infarctus ischémique de la tête du nerf optique est causé par une insuffisance circulatoire aiguë des artères ciliaires courtes postérieures (artères SPC).
- Épidémiologie : Incidence annuelle aux États-Unis de 2,3 à 10,2 pour 100 000 personnes3). La majorité des cas survient après 50 ans, mais l’incidence avant 50 ans est en augmentation.
- Facteurs de risque : Hypertension, diabète, hyperlipidémie, syndrome d’apnée du sommeil, disque à risque (petite papille avec rapport C/D < 0,2). Le disque à risque est présent dans environ 80 % des yeux controlatéraux3).
- Symptômes : baisse de vision unilatérale aiguë et indolore, souvent remarquée au réveil. RAPD positif du côté atteint.
- Aspect de la papille : rougeur et gonflement (en éventail prédominant en bas). Peut être accompagné d’hémorragies.
- Champ visuel : déficit fasciculaire horizontal (déficit inférotemporal typique).
- Traitement : Aucun traitement efficace n’est établi pour la phase aiguë. La gestion des facteurs de risque vasculaires et le traitement du syndrome d’apnée du sommeil sont au cœur de la prévention des récidives.
- Point d’attention récent : Une étude observationnelle de 2024 a rapporté un risque accru de NAION chez les utilisateurs de sémaglutide (agoniste du récepteur GLP-1). Cependant, la relation de cause à effet n’est pas établie, et la décision de prescription doit peser les bénéfices dans le traitement du diabète et de l’obésité7).
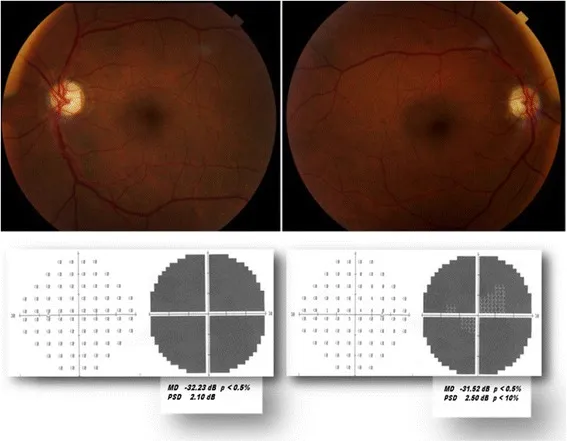
動脈炎性前部虚血性視神経症(AAION/GCA)
Section intitulée « 動脈炎性前部虚血性視神経症(AAION/GCA) »AAIONは前部虚血性視神経症全体の5〜10%を占めるが、最緊急の視神経症である1)。視神経乳頭を栄養する短後毛様動脈の血管炎が本態であり、原疾患の90%以上が巨細胞性動脈炎(GCA)である。
- 疫学:50歳以上(特に75歳以上)の高齢女性に多い(男女比1:3)1)。日本での発症率は10万人あたり1.47人と欧米に比べて極めて低い。
- 症状:急激な片眼重度視力低下(60%以上で視力20/200未満、20%以上で光覚なし)1)。一過性黒内障を約30%が先行して経験する。
- 全身症状:頭痛(65〜90%)・顎跛行(11〜45%)・頭皮圧痛・発熱・PMR様症状。
- Signes papillaires : gonflement pâle crayeux (pallid swelling) caractéristique.
- Examens : VS et CRP élevés (augmentés dans plus de 80% des cas)1). Biopsie de l’artère temporale (sensibilité et spécificité >95%)1).
- Traitement : Corticostéroïdes à haute dose (mPSL 500-1000 mg IV pendant 3 jours, puis prednisolone orale en diminution progressive)1). Le tocilizumab (antagoniste du récepteur de l’IL-6) est efficace pour réduire les stéroïdes (essai GiACTA, preuves RCT)1).
- Pronostic : La récupération visuelle de l’œil atteint est presque impossible, mais le traitement stéroïdien est efficace pour prévenir l’atteinte de l’autre œil.
6-2. Névrite optique inflammatoire
Section intitulée « 6-2. Névrite optique inflammatoire »Névrite optique idiopathique
Section intitulée « Névrite optique idiopathique »Maladie inflammatoire du nerf optique due à un mécanisme auto-immun, représentant la majorité des névrites optiques 13). L’âge de prédilection est de 15 à 45 ans, avec environ 70 % de femmes, et l’incidence annuelle au Japon est de 1,6 pour 100 000 adultes 13).
- Symptômes : Baisse d’acuité visuelle aiguë unilatérale et douleur oculaire aux mouvements (environ 50 %). Progression sur quelques jours à 2 semaines, avec tendance à la récupération spontanée dans les 5 semaines.
- Champ visuel : Scotome central ou scotome centro-cæcal fréquent.
- IRM : Prise de contraste (gadolinium) concordant avec le nerf optique.
- Pronostic : Plus de 90 % récupèrent une acuité visuelle ≥ 0,5 après 1 an (étude ONTT) 4).
- Traitement : La corticothérapie par bolus de mPSL 1 000 mg/jour × 3 jours accélère la récupération. La corticothérapie orale seule n’est pas pratiquée en raison d’un risque accru de récidive (étude ONTT) 4).
- Risque de conversion en SEP : incidence cumulative de 50 % sur 15 ans après le premier épisode. Absence de lésions à l’IRM cérébrale → 25 %, présence → 78 %4).
Névrite optique associée à la SEP
Section intitulée « Névrite optique associée à la SEP »Environ 30% des patients présentent une névrite optique comme premier symptôme de la SEP, et jusqu’à 75% des patients atteints de SEP connaîtront au moins un épisode de névrite optique au cours de leur vie 8). Elle est souvent unilatérale, avec douleur aux mouvements oculaires, et l’atteinte rétrobulbaire est fréquente (fond d’œil normal dans 65% des cas). Les lésions de démyélinisation à l’IRM cérébrale (hypersignal T2/FLAIR) sont la clé du diagnostic. Après confirmation du diagnostic selon les critères de McDonald (version 2017, révisée en 2024), un traitement de fond (DMT : interféron bêta, natalizumab, fingolimod, anti-CD20, etc.) est utilisé pour prévenir les rechutes.
Névrite optique associée au NMOSD (trouble du spectre de la neuromyélite optique)
Section intitulée « Névrite optique associée au NMOSD (trouble du spectre de la neuromyélite optique) »AQP4-IgG positif. Survient principalement chez les femmes (ratio hommes:femmes 1:9), d’âge moyen, d’origine asiatique, et est plus sévère, bilatérale et récurrente que la névrite optique associée à la SEP 5). Au moins 60 à 69 % des patients développent une déficience visuelle permanente de 20/200 ou moins dans au moins un œil 5). L’IRM orbitaire montre une lésion longue du nerf optique (avec une implication fréquente du chiasma). Le traitement comprend une corticothérapie pulsée en phase aiguë, suivie d’une plasmaphérèse, puis d’une immunothérapie préventive des récidives (éculizumab, rituximab, satralizumab) 5).
Névrite optique associée au MOGAD (maladie liée aux anticorps anti-MOG)
Section intitulée « Névrite optique associée au MOGAD (maladie liée aux anticorps anti-MOG) »MOG-IgG positif. Incidence annuelle de 1,6 à 4,8 par million d’habitants6). Atteinte bilatérale fréquente avec œdème papillaire marqué, prédominance antérieure. À l’IRM, œdème papillaire, lésion optique étendue et périnévrite optique sont caractéristiques6). Comparaison des sexes : MS-ON 3:1, AQP4-ON 7-9:1, MOG-ON 1:16). Répond aux stéroïdes mais récidive facilement en cas de réduction précoce, nécessitant une diminution prudente6).
6-3. Neuropathie optique compressive
Section intitulée « 6-3. Neuropathie optique compressive »Causée par une compression du nerf optique par une tumeur, un anévrisme, un hématome, un abcès, un kyste ou des muscles extra-oculaires hypertrophiés. Les symptômes et les schémas de perte du champ visuel varient considérablement selon le site de compression.
- Apex orbitaire : Orbitopathie thyroïdienne (la neuropathie optique thyroïdienne complique 3 à 8,6 % des orbitopathies thyroïdiennes, bilatérale dans 70 %), tumeurs orbitaires (bénignes : inflammation orbitaire idiopathique 20 %, adénome pléomorphe 13 %, hémangiome 13 % ; malignes : lymphome malin le plus fréquent)9).
- Chiasma optique : Adénome hypophysaire (le plus fréquent chez l’adulte, hémianopsie bitemporale), craniopharyngiome (le plus fréquent chez l’enfant).
- Neuropathie optique nasale (mention spéciale) : La forme invasive de la sinusite fongique (Aspergillus, Mucor) a un taux de mortalité rapporté de 94 %2). Les stéroïdes sont temporairement efficaces, ce qui conduit à un diagnostic erroné de névrite optique rétrobulbaire ; la poursuite des stéroïdes sans le savoir peut être fatale. Les signes de destruction osseuse au scanner/IRM sont essentiels au diagnostic, nécessitant une collaboration urgente avec un ORL.
Le principe du traitement est l’ablation chirurgicale de la lésion causale. Plus la décompression est précoce, meilleure est la récupération de la fonction visuelle ; une fois l’atrophie optique établie, la récupération est limitée.
6-4. Neuropathie optique toxique
Section intitulée « 6-4. Neuropathie optique toxique »Il s’agit d’un groupe de maladies où la voie visuelle antérieure est endommagée par l’exposition à des substances chimiques2). En principe, elle est bilatérale et indolore ; si un œil est complètement normal, une neuropathie optique toxique doit être exclue2).
- Substances causales : tabac, alcool, solvants (médicaments : éthambutol [le plus connu], amiodarone, linézolide, cisplatine, immunosuppresseurs, etc.).
- Champ visuel : caractéristiquement un scotome centro-cæcal ou un scotome central (atteinte prédominante des cellules P)2).
- Vision des couleurs : un affaiblissement de la perception du rouge est un signe précoce.
- Fond d’œil : normal ou légère rougeur au début → pâleur temporale de la papille et déficit du faisceau papillo-maculaire en phase chronique.
- RAPD : généralement négatif en raison de la symétrie bilatérale.
- VEP : diminution de l’amplitude, sans retard de la latence de P100 (le retard de latence est caractéristique de la névrite optique démyélinisante)13).
- Éthambutol : dose-dépendant (risque accru au-delà de 15 mg/kg). Un examen visuel de base avant le traitement et une surveillance régulière sont essentiels.
- Traitement : l’arrêt de l’agent causal est fondamental. Il n’existe pas de médicament spécifique.
6-5. Neuropathie optique nutritionnelle
Section intitulée « 6-5. Neuropathie optique nutritionnelle »Il s’agit d’une neuropathie optique bilatérale symétrique et progressive due à une carence en vitamines B (B12, B1, B2, B9) et en cuivre. Elle se situe dans le même spectre que la neuropathie optique toxique, mais s’en distingue par sa cause nutritionnelle. Les risques modernes incluent la chirurgie bariatrique (surveillance à vie obligatoire), le régime végétalien et l’alcoolisme. Les symptômes, le champ visuel et les résultats du fond d’œil sont similaires à ceux de la neuropathie toxique (scotome central, indolore, pâleur temporale de la papille). Une supplémentation nutritionnelle précoce peut permettre une récupération, mais les cas chroniques laissent des séquelles irréversibles.
6-6. Neuropathie optique héréditaire
Section intitulée « 6-6. Neuropathie optique héréditaire »LHON (Neuropathie optique héréditaire de Leber)
Section intitulée « LHON (Neuropathie optique héréditaire de Leber) »Il s’agit d’une neuropathie optique aiguë ou subaiguë à transmission maternelle, causée par des mutations ponctuelles de l’ADN mitochondrial (ADNmt)14). Les trois mutations principales (mt3460, mt11778, mt14484) représentent plus de 95 % de tous les cas, et mt11778 représente environ 90 % de tous les cas en Asie14).
- Épidémiologie : Prévalence de 1/31 000 à 1/68 000. Pénétrance de 2,5 à 17,5 %, la majorité des porteurs ne développant pas la maladie14). Au Japon, environ 117 nouveaux cas par an (enquête 2014). Maladie rare désignée.
- Symptômes : Survient principalement chez les jeunes hommes (rapport hommes/femmes d’environ 93:7). Scotome central bilatéral subaigu et indolore (un œil est atteint en premier, puis les deux yeux en quelques semaines à quelques mois).
- 急性期眼底:視神経乳頭の発赤・腫脹と乳頭近傍毛細血管の拡張・蛇行。蛍光眼底造影で乳頭からの蛍光漏出を認めない(炎症性視神経炎との重要鑑別)14)。
- 対光反射:他の視神経疾患に比べて保たれるか、障害されても軽微14)。
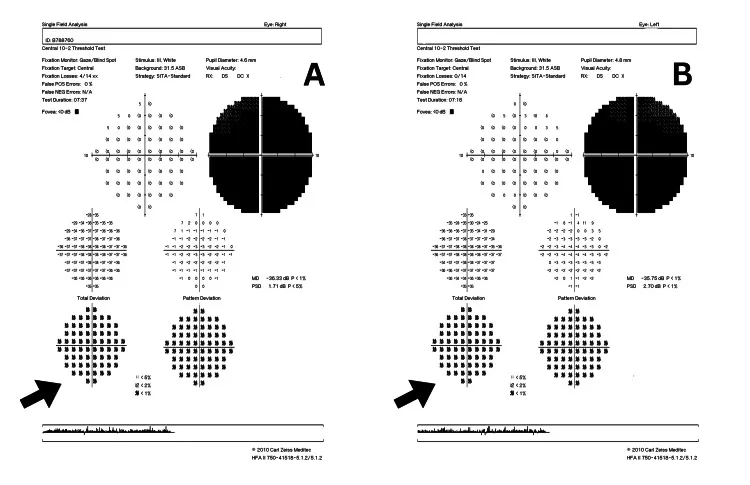
- 最終視力:mt11778では0.01前後が多い。mt14484は自然回復率が最も高い14)。
- 治療:イデベノン900 mg/日(欧州EMA承認)。LEROS試験ではCRR(有意義な視力回復)が46.0%(プラセボ対照)10)。ウェールズコホート試験では27カ月時点でCRR 86%を達成10)。遺伝子治療も第III相試験で有効性を示している11)。禁煙指導が発症・重症化予防に重要。
ADOA (atrophie optique dominante autosomique)
Section intitulée « ADOA (atrophie optique dominante autosomique) »Neuropathie optique héréditaire la plus fréquente, principalement due à une mutation du gène OPA1. Elle est découverte pendant l’âge scolaire comme un trouble du développement visuel bilatéral d’origine inconnue. Une anomalie de la vision des couleurs acquise de type tritanopie (bleu-jaune) est caractéristique. L’OCT montre un amincissement de la couche des fibres nerveuses rétiniennes (RNFL) prédominant dans les quadrants temporal et inférieur 2). Il n’existe actuellement aucun traitement efficace ; la prise en charge repose sur les soins de basse vision et le conseil génétique.
6-7. Neuropathie optique traumatique
Section intitulée « 6-7. Neuropathie optique traumatique »Lésion du nerf optique survenant après un traumatisme contondant de la tête ou de l’orbite, souvent due à une force indirecte dans le canal optique. Une baisse aiguë de l’acuité visuelle apparaît immédiatement après la blessure. La fracture du canal optique est confirmée par tomodensitométrie osseuse. On envisage un traitement par corticostéroïdes à haute dose ou une décompression du canal optique, mais les preuves sont limitées pour les deux.
6-8. Neuropathie optique radique
Section intitulée « 6-8. Neuropathie optique radique »Il s’agit d’une lésion ischémique tardive après radiothérapie pour des tumeurs de la tête et du cou ou de l’orbite. La fonction visuelle est perdue par un mécanisme principalement dû à des lésions endothéliales vasculaires. L’apparition survient de 3 mois à 9 ans après l’irradiation, le plus souvent entre 10 et 20 mois, avec une moyenne d’environ 18 mois 12). Le risque augmente avec une dose totale supérieure à 50 Gy ou une dose unique supérieure à 10 Gy. Généralement indolore et de mauvais pronostic. Il n’existe pas de traitement établi ; l’efficacité des corticostéroïdes systémiques, de l’anticoagulation et de l’oxygénothérapie hyperbare est limitée 12). L’IRM montre un rehaussement de contraste correspondant au nerf optique.
6-9. その他の特殊な視神経症
Section intitulée « 6-9. その他の特殊な視神経症 »後部虚血性視神経症(PION) 眼窩内後部または管内部の視神経虚血。大量出血・低血圧・脊椎手術・心臓手術後に発症する術後PIGNが代表的である。眼底所見は正常(乳頭変化なし)で急激な視力低下をきたす。対光反射はRAPD陽性となる。有効な治療法は確立されていない。
視神経网膜炎(neuroretinitis) 視神経乳頭浮腫と網膜の星芒状白斑(star figure)が特徴的な症候群。Bartonella henselae(ネコひっかき病)・梅毒・Leber特発性星芒状視神経網膜症などが原因。星芒状白斑は浮腫液が黄斑部でHenle線維層に沿って沈着したものであり、乳頭浮腫が消退する数週間後に出現する。自然寛解傾向があるが、感染症は原因に対する特異的治療を行う。
乳頭血管炎(papillophlebitis) 若年〜壮年者に生じる、視機能障害を伴わない片眼性乳頭浮腫と網膜静脈拡張蛇行を示す症候群。Mariotte盲点の拡大を認めるが矯正視力は正常。眼窩MRIは正常。予後良好で治療不要であるが、うっ血乳頭・視神経炎・虚血性視神経症との鑑別が重要である2)。
免疫チェックポイント阻害薬関連視神経症 がん免疫療法(ニボルマブ・ペムブロリズマブ等)の免疫関連有害事象(irAE)として視神経症が稀に生じる。ステロイドパルス療法で治療し、がん治療との継続可否をオンコロジストと協議する。
視神経症ワンライナーまとめ表
Section intitulée « 視神経症ワンライナーまとめ表 »| Maladie | Latéralité | Douleur | Aspect de la papille | Champ visuel | Point clé |
|---|---|---|---|---|---|
| NAION | Unilatéral | Aucun | Rougeur et gonflement (inférieur) | Déficit en faisceau horizontal | Survenue au réveil, disque à risque3) |
| AAION/GCA | Un œil → les deux yeux | Aucun (céphalée, claudication de la mâchoire) | Œdème pâle | Variable (sévère) | Urgence maximale, VS/CRP élevés1) |
| Névrite optique idiopathique | Unilatéral | Présent (50%) | Œdème ou normal | Scotome central | Femme jeune, risque de transition vers la SEP 13) |
| NMOSD associé | Tendance à la bilatéralisation | Oui | Œdème ou normal | Variable (sévère) | Anticorps AQP4 positif, réfractaire5) |
| MOGAD associé | Souvent bilatéral | Oui (céphalée) | Œdème sévère | Variable | Anticorps MOG, périnévrite6) |
| Compressif | Unilatéral/Bilatéral | Aucun | Normal ou atrophié | Divers | IRM obligatoire9) |
| Toxique | Les deux yeux | Aucun | Normal → pâleur temporale | Scotome centro-cæcal | Interroger sur la substance causale2) |
| Nutritionnelle | Les deux yeux | Aucune | Normale → pâleur temporale | Scotome central | Carence en B12/cuivre |
| LHON | Bilatéral (un œil en premier) | Aucune | Rougeur/télangiectasies | Scotome central | Homme jeune, pas de fuite fluorescente14) |
| ADOA | Les deux yeux | Aucun | Pâle | Scotome central | Âge scolaire, dyschromatopsie bleu-jaune2) |
| Traumatique | Unilatéral | Oui (traumatisme) | Normal | Variable | Scanner du canal optique pour confirmer la fracture |
| Radique | Unilatéral/Bilatéral | Aucun | Normal → Atrophie | Divers | Moyenne 18 mois12) |
7. Principes du traitement
Section intitulée « 7. Principes du traitement »Le traitement de la neuropathie optique dépend de la cause et diffère fondamentalement selon le type de maladie. Les principes communs sont indiqués ci-dessous.
Situations nécessitant un traitement d’urgence
Section intitulée « Situations nécessitant un traitement d’urgence »- GCA/AAION : Administration systémique de corticostéroïdes à haute dose (dès le jour même). Ne pas attendre les résultats des examens 1).
- Compression aiguë : décompression chirurgicale (collaboration urgente avec ORL et neurochirurgie). Dans l’aspergillose invasive, arrêter les stéroïdes et passer aux antifongiques2).
- Traumatique : évaluation de l’indication de la décompression du canal optique.
Traitement de l’inflammation (névrite optique)
Section intitulée « Traitement de l’inflammation (névrite optique) »La corticothérapie par bolus (mPSL 1 000 mg/jour × 3 jours) accélère la vitesse de récupération en phase aiguë4). La corticothérapie orale seule n’est pas pratiquée dans la névrite optique idiopathique car elle augmente le risque de récidive (étude ONTT)4). En phase aiguë de NMOSD, un traitement par étapes est effectué : bolus de corticoïdes → échange plasmatique en cas de réponse insuffisante → immunothérapie préventive des récidives5). La névrite optique associée aux MOGAD est sensible aux corticoïdes, mais une réduction précoce entraîne des récidives, nécessitant une diminution prudente6).
Traitement de l’ischémie (NAION)
Section intitulée « Traitement de l’ischémie (NAION) »Aucun traitement efficace n’est établi en phase aiguë. La prise en charge des facteurs de risque vasculaires (hypertension, diabète, hyperlipidémie, syndrome d’apnée du sommeil) est essentielle, et la prévention de l’atteinte de l’œil controlatéral constitue l’objectif thérapeutique. Concernant le sémaglutide (agoniste du récepteur GLP-1), des études observationnelles suggèrent une association avec la NAION ; chez les patients ayant des antécédents ou un risque, une information attentive et une surveillance sont souhaitables7).
Traitement de l’héréditaire (LHON)
Section intitulée « Traitement de l’héréditaire (LHON) »L’idébénone 900 mg/jour est approuvé par l’EMA européenne et a atteint un CRR de 46 % dans l’essai LEROS (comparaison contre placebo) 10). La cohorte galloise a rapporté un CRR de 86 % à 27 mois, montrant de bons résultats en pratique clinique 10). La thérapie génique (lénadogène nolparvovec) a montré son efficacité dans un essai de phase III, et une extension des indications est attendue 11). Le conseil d’arrêt du tabac (le tabagisme est un facteur de risque de déclenchement) et des soins appropriés en basse vision sont essentiels 14).
Traitement des neuropathies toxiques et nutritionnelles
Section intitulée « Traitement des neuropathies toxiques et nutritionnelles »Le traitement de base consiste à arrêter la substance responsable ou à supplémenter les nutriments déficients. Une intervention précoce peut permettre une récupération de la fonction visuelle, mais les cas chroniques peuvent laisser des séquelles irréversibles. La neuropathie optique à l’éthambutol étant dose-dépendante, un examen visuel de base avant le traitement et une surveillance régulière (acuité visuelle, vision des couleurs, champ visuel) sont indispensables.
Traitement des neuropathies compressives
Section intitulée « Traitement des neuropathies compressives »Le principe est l’ablation chirurgicale de la lésion causale. Dans la neuropathie optique thyroïdienne, une décompression orbitaire en urgence ou programmée est réalisée. Une fois l’atrophie optique avancée, la récupération visuelle après ablation chirurgicale est limitée, d’où l’importance d’un diagnostic et d’un traitement précoces.
Aperçu du pronostic
Section intitulée « Aperçu du pronostic »| Type de maladie | Pronostic visuel | Possibilité de récupération |
|---|---|---|
| Névrite optique idiopathique | Plus de 90 % ont une acuité visuelle ≥ 0,5 après 1 an4) | Bonne récupération |
| NAION | 1/3 amélioration, 1/3 inchangé, 1/3 aggravation | Récupération partielle |
| AAION/GCA | La récupération de l’œil atteint est presque impossible | La prévention de l’œil controlatéral est l’objectif1) |
| NMOSD associé | Grave. Au moins un œil ≤ 20/200 dans 60-69%5) | Prévention des rechutes importante |
| LHON (mt11778) | Acuité visuelle finale souvent autour de 0.01 | Récupération spontanée seulement partielle14) |
| LHON (mt14484) | Type de mutation avec le taux de récupération spontanée le plus élevé | Cas de récupération rapportés14) |
| ADOA | Progression lente, rarement une cécité sévère | Aucune inhibition de la progression |
| Compressif | Récupérable par ablation précoce | Avant progression de l’atrophie |
| Toxique ou nutritionnel | Récupération par arrêt précoce ou supplémentation | Irréversible dans les cas chroniques |
| Radique | Fréquente baisse de vision aiguë, sévère et irréversible 12) | Aucun traitement établi |
L’identification rapide de la maladie causale. En cas de suspicion d’ACG, commencer les stéroïdes le jour même sans attendre les résultats des tests pour prévenir la cécité de l’autre œil 1). En cas de compression, l’ablation chirurgicale de la lésion causale est le seul moyen de préserver la fonction visuelle, et un retard de diagnostic conduit à une atrophie optique irréversible. Dans les cas inflammatoires (névrite optique), la corticothérapie par bolus accélère la récupération, mais la stratégie de traitement supplémentaire varie considérablement selon le type. En particulier, en cas de positivité des anticorps anti-AQP4, les stéroïdes seuls entraînent des récidives répétées, donc l’introduction précoce d’un traitement immunomodulateur préventif des récidives est essentielle pour préserver la fonction visuelle 5).
Les deux présentent des symptômes initiaux similaires de « baisse de vision indolore aiguë à subaiguë », et sont souvent confondus, en particulier dans la phase aiguë de la LHON où un gonflement papillaire est présent. Le point de différenciation le plus important est la présence ou l’absence de fuite de fluorescence papillaire à l’angiographie à la fluorescéine. La névrite optique inflammatoire montre un rehaussement et une fuite de fluorescence, tandis que la LHON aiguë n’en présente pas 14). De plus, la douleur oculaire lors des mouvements est observée dans environ 50 % des cas de névrite optique, mais la LHON est indolore. Le diagnostic définitif peut être posé par test génétique mitochondrial (mt11778, mt14484, mt3460), réalisable en laboratoire externe 14). L’administration de stéroïdes aux patients atteints de LHON est non seulement inefficace, mais retarde également le diagnostic définitif. Par conséquent, chez les jeunes hommes présentant une baisse de vision bilatérale aiguë, il est essentiel d’inclure la LHON dans le diagnostic différentiel.
8. Articles connexes (neuropathies optiques)
Section intitulée « 8. Articles connexes (neuropathies optiques) »Neuropathie optique ischémique antérieure artéritique (AAION)
Neuropathie optique compressive
Neuropathie optique toxique
Neuropathie optique par carence nutritionnelle
Neuropathie optique héréditaire de Leber (LHON)
Atrophie optique autosomique dominante (ADOA)
Neuropathie optique radique
Maladies et tumeurs du nerf optique à différencier
Section intitulée « Maladies et tumeurs du nerf optique à différencier »Névrite optique idiopathique
Névrite optique associée à la SEP
Neuromyélite optique (NMOSD)
Maladie associée aux anticorps MOG (MOGAD)
Références
Section intitulée « Références »- Piccus R, Hansen MS, Hamann S, et al. An update on the clinical approach to giant cell arteritis. Eye 2023.
- Biousse V, Newman NJ. Diagnosis and clinical features of common optic neuropathies. Lancet Neurol 2016;15:1355–67.
- Salvetat ML, Pellegrini F, Spadea L, et al. Non-Arteritic Anterior Ischemic Optic Neuropathy (NA-AION): A Comprehensive Overview. Vision 2023;7:72.
- Beck RW, Gal RL. The Optic Neuritis Treatment Trial: a report on the visual function at 15 years. Ophthalmology 2008;115:1079–82.
- Wingerchuk DM, Banwell B, Bennett JL, et al. International consensus diagnostic criteria for neuromyelitis optica spectrum disorders. Neurology 2015;85:177–89.
- Jeyakumar N, Lerch M, Dale RC, Ramanathan S. MOG antibody-associated optic neuritis. Eye 2024.
- Hathaway JT, Shah MP, Hathaway DB, et al. Risk of nonarteritic anterior ischemic optic neuropathy in patients prescribed semaglutide. JAMA Ophthalmol. 2024;142:740-741. PMID: 38958939. doi:10.1001/jamaophthalmol.2024.2514.
- Thompson AJ, Banwell BL, Barkhof F, et al. Diagnosis of multiple sclerosis: 2017 revisions of the McDonald criteria. Lancet Neurol 2018;17:162–73.
- Biousse V, Newman NJ. Compressive Optic Neuropathies. J Neuroophthalmol 2015;35 Suppl 1:S67–S74.
- Sanders FWB, Votruba M. Outcomes of idebenone therapy for Leber hereditary optic neuropathy in a cohort of patients from Wales. Eye 2025.
- Newman NJ, et al. Hereditary optic neuropathy: advances in treatment. Eye 2024.
- Danesh-Meyer HV. Radiation-induced optic neuropathy. J Clin Neurosci 2008;15:95–100.
- Toosy AT, Mason DF, Miller DH. Optic neuritis. Lancet Neurol 2014;13:83–99.
- Carelli V, Ross-Cisneros FN, Sadun AA. Mitochondrial dysfunction as a cause of optic neuropathies. Prog Retin Eye Res 2004;23:53–89.
