Non artéritique
Examen de la papille : normale en phase aiguë. Pâleur après 6 à 8 semaines.
Acuité visuelle : 20/200 ou moins dans 69 % des cas.
Évolution : apparition rare. Des améliorations du champ visuel sous corticoïdes ont été rapportées.

La neuropathie optique ischémique postérieure (NOIP) est une neuropathie optique ischémique causée par une insuffisance circulatoire du nerf optique en arrière de la lame criblée. Elle se distingue clairement de la neuropathie optique ischémique antérieure (NOIA) par l’absence d’œdème de la papille optique en phase aiguë. La NOIA s’accompagne d’un œdème papillaire en phase aiguë et est classée en types artéritique (AION artéritique) et non artéritique (NAION). La NAION est essentiellement toujours de type antérieur, tandis que la forme artéritique de la NOIP est classée comme type postérieur (PAION).
La NOIP est une maladie rare, représentant seulement environ 10 % de tous les cas d’ischémie du nerf optique, et survient principalement après l’âge de 50 ans. Elle est classée en trois types :
La principale différence réside dans l’aspect de la papille optique en phase aiguë. Dans la NOIA, un œdème papillaire apparaît en phase aiguë, tandis que dans la NOIP, la papille semble normale en phase aiguë, et une pâleur (atrophie) apparaît 6 à 8 semaines plus tard. Le site de l’ischémie est antérieur à la lame criblée dans la NOIA et postérieur dans la NOIP.
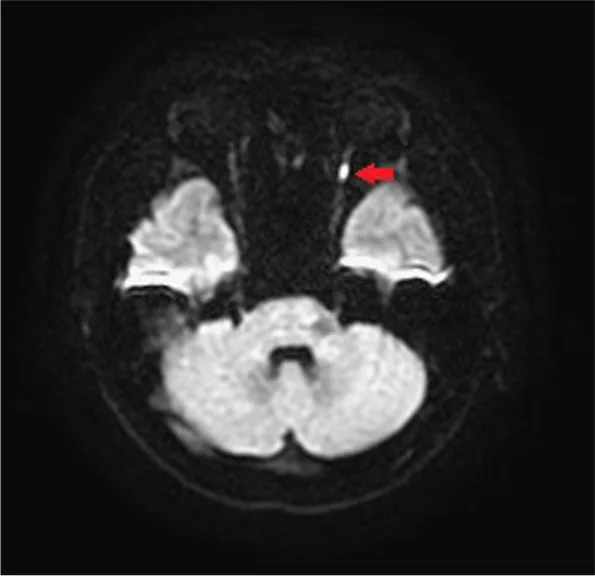
Cela varie considérablement selon le type. Dans la PION non artéritique, 69 % des cas ont une acuité visuelle ≤ 20/200, et seulement 20 % maintiennent ≥ 20/40. Dans la PION périopératoire, l’acuité finale la plus fréquente est l’absence de perception lumineuse (NLP), et 75,8 % des yeux ont une acuité ≤ compter les doigts. 1)
Non artéritique
Examen de la papille : normale en phase aiguë. Pâleur après 6 à 8 semaines.
Acuité visuelle : 20/200 ou moins dans 69 % des cas.
Évolution : apparition rare. Des améliorations du champ visuel sous corticoïdes ont été rapportées.
Artéritique (artérite à cellules géantes)
Examen de la papille : normale en phase aiguë. Pâleur ensuite.
Symptômes généraux : céphalées, claudication de la mâchoire, élévation de la VS et de la CRP.
Évolution : moins de chances de récupération visuelle que la forme non artéritique.
Périopératoire
Mode d’apparition : constaté au réveil ou dans les jours suivant la chirurgie.
Côté atteint : bilatéral dans 70 % des cas.
Évolution : la plus sévère. La NLP est l’issue la plus fréquente.
Secondaire à une maladie des petits vaisseaux, impliquant les facteurs de risque vasculaires suivants.
Survient chez des patients plus jeunes que ceux atteints de PION artéritique. Les facteurs de risque suivants sont connus.
Facteurs de risque préexistants :
Facteurs de risque peropératoires :
Procédures chirurgicales associées (par ordre de fréquence) :
L’incidence après chirurgie rachidienne est rapportée à 0,087 %, et après évidement cervical à 0,08 %.1)
L’incidence après chirurgie rachidienne est rapportée à 0,087 %, et après évidement cervical à 0,08 %.1) Bien que la fréquence soit faible, le pronostic visuel en cas de survenue est extrêmement défavorable, d’où l’importance d’une explication préopératoire aux patients à haut risque et d’une gestion périopératoire appropriée.
La PION est un diagnostic clinique, et également un diagnostic d’exclusion. La démarche diagnostique est la suivante.
Baisse aiguë de l’acuité visuelle + déficit du champ visuel + RAPD positif + aspect normal de la papille en phase aiguë → pâleur papillaire 6 à 8 semaines plus tard → exclusion des autres causes (névrite optique rétrobulbaire, maladie rétinienne, compression, intoxication, etc.). La PION périopératoire survient après une chirurgie non ophtalmique, ce qui rend le diagnostic relativement clair.
Chez les patients de 50 ans et plus, mesurer la VS et la CRP pour exclure une artérite à cellules géantes.
Voici la sensibilité et la spécificité de chaque test pour le diagnostic de l’artérite à cellules géantes.
| Test | Sensibilité | Spécificité |
|---|---|---|
| VS + CRP combinées | Jusqu’à 100 % | 97 % |
| Thrombocytose | 57,0 % | 96,5 % |
| Faible taux d’hémoglobine | 46,3 % | 92,9 % |
| Hématocrite bas | 39,8 % | 91,3 % |
| Leucocytose | 28,1 % | 85,7 % |
La CRP a une spécificité plus élevée que la VS. La valeur normale de la VS à 1 heure est la moitié de l’âge chez l’homme et la moitié de (âge + 10) chez la femme. La biopsie de l’artère temporale (TAB) est le gold standard pour le diagnostic de l’artérite à cellules géantes, avec une sensibilité et une spécificité supérieures à 95 % si elle est réalisée correctement. La biopsie doit être effectuée dans les jours suivant le début de la corticothérapie. Dans la PION non artéritique, ces valeurs sont normales.
Les principaux diagnostics différentiels sont la névrite optique rétrobulbaire, les maladies maculaires et rétiniennes, la neuropathie optique toxique, et la compression ou inflammation du nerf optique postérieur. Pour différencier la neuropathie optique ischémique de la névrite optique rétrobulbaire, on combine VEP, électrorétinogramme, OCT et DWI IRM.
Le protocole suivant est recommandé :
Selon des rapports étrangers, la dose initiale médiane est de 80 mg/jour de prednisolone, avec une diminution progressive après stabilisation de la VS et de la CRP. La durée totale du traitement, y compris la diminution, est d’environ 2,5 mois.
Il n’existe pas de traitement efficace établi. L’anticoagulation, les vasodilatateurs, les corticoïdes oraux et la décompression de la gaine du nerf optique ont été essayés, mais aucune amélioration significative du pronostic visuel n’a été prouvée. Une méthode de prednisolone 80 mg/jour pendant 2 semaines suivie d’une diminution progressive peut être envisagée, mais il n’existe pas de données d’essais randomisés contrôlés.
Il n’existe pas de traitement établi. Les corticoïdes ne sont généralement pas recommandés. Les mesures générales comprennent :
Practice Advisory (directives de gestion périopératoire) pour la chirurgie rachidienne
Une gestion systématique préopératoire, peropératoire et postopératoire est importante pour prévenir la perte de vision.
Préopératoire :
Peropératoire :
Postopératoire :
Le pronostic varie considérablement selon le type. Dans la PION artéritique, l’administration immédiate de stéroïdes peut réduire la progression et l’atteinte de l’autre œil, mais une amélioration significative de l’acuité visuelle déjà diminuée de l’œil atteint est peu probable. La PION périopératoire ne répond pas aux stéroïdes et suit souvent une évolution bilatérale, irréversible et sévère. Pour la PION non artéritique, des rapports ont montré une amélioration du champ visuel avec les stéroïdes, mais il n’existe pas de preuves établies.
Le nerf optique postérieur est divisé en trois parties : intra-orbitaire, intracanalaire et intracrânienne. La partie postérieure à la lame criblée reçoit son apport sanguin du plexus vasculaire pie-mérien et des branches de l’artère centrale de la rétine.
L’hémorragie postopératoire et l’augmentation de la pression intracrânienne due à la compression bilatérale des veines jugulaires internes (VJI) réduisent la perfusion du nerf optique, contribuant au développement de la maladie. 1) La ligature des VJI a été suggérée comme facteur de risque de neuropathie optique ischémique, et on suppose que la congestion veineuse altère la perfusion artérielle. 1) Les mécanismes de diminution de l’apport en oxygène comprennent : ① un faible niveau d’oxygène dans le sang circulant, ② une diminution de la pression de perfusion artérielle, et ③ une augmentation de la résistance au flux sanguin. 1)
Kohyama et al. (2022) ont rapporté un cas de PION survenu après une laryngopharyngectomie avec curage cervical bilatéral et reconstruction par lambeau libre de jéjunum. 1) Il s’agit du premier cas rapporté de PION causée par une hémorragie postopératoire et une compression bilatérale des VJI.
Durée de l’opération : 13,5 heures, saignement total : 740 g. La pression artérielle systolique, d’environ 150 mmHg avant l’opération, a chuté à un minimum de 80 mmHg (pendant quelques minutes). L’hémoglobine est passée de 13,5 g/dL avant l’opération à 9,5 g/dL après l’opération, puis a chuté à 6,1 g/dL en raison de l’hémorragie. L’hématocrite est passé de 38,1 % avant l’opération à 29,3 % après l’opération, puis à 19,3 %. Un œdème du visage et du cou est survenu après l’opération, et les deux VJI ont été comprimées par un hématome. 1)
L’administration de prednisolone orale à 1 mg/kg/jour pendant plus de 2 mois n’a pas amélioré l’acuité visuelle, qui est restée au niveau de perception lumineuse, et aucune récupération visuelle n’a été observée après un an. 1) Les auteurs notent qu’il y a eu un délai de 7 heures entre l’apparition de l’œdème et la décompression de l’hématome, et qu’une incision exploratoire précoce aurait pu prévenir la PION. 1) Il a également été rapporté que 75,8 % des yeux atteints de PION périopératoire conservent une acuité visuelle inférieure au comptage des doigts. 1)
Concernant le traitement par stéroïdes pour la PION non artéritique, une amélioration significative du champ visuel (P = 0,030) a été rapportée dans le groupe traité par stéroïdes par rapport au groupe témoin, ainsi qu’une amélioration significative du champ visuel (P < 0,001) et de l’acuité visuelle (P = 0,031) par rapport aux valeurs de base. Cependant, il n’existe pas de données d’essais contrôlés randomisés.
Il a été rapporté que l’association d’une oxygénothérapie hyperbare dans les 72 heures suivant l’apparition et de stéroïdes a réussi dans un petit nombre de cas de PION périopératoire. L’accumulation de cas et les recherches futures sont attendues.