No arterítica
Hallazgos papilares: Normal en la fase aguda. Palidez después de 6–8 semanas.
Agudeza visual: 20/200 o peor en el 69%.
Evolución: Aparición rara. Se ha informado mejoría del campo visual con esteroides.

La neuropatía óptica isquémica posterior (PION) es una neuropatía óptica isquémica causada por insuficiencia circulatoria en el nervio óptico posterior a la lámina cribosa. Se distingue claramente de la neuropatía óptica isquémica anterior (AION) por la ausencia de edema del disco óptico en la fase aguda. La neuropatía óptica isquémica anterior (AION) presenta edema del disco en la fase aguda y se clasifica en arterítica (AAION) y no arterítica (NAION) según la etiología. La NAION es esencialmente siempre anterior, mientras que la PION arterítica se clasifica como posterior (PAION).
La PION es una enfermedad rara que representa solo aproximadamente el 10% de todos los casos de isquemia del nervio óptico, y ocurre con mayor frecuencia después de los 50 años. Se clasifica en los siguientes tres tipos:
La principal diferencia es la apariencia del disco óptico en la fase aguda. En la AION, se produce edema del disco de forma aguda, mientras que en la PION, el disco parece normal en la fase aguda y la palidez (atrofia) aparece 6 a 8 semanas después. El sitio de isquemia es anterior a la lámina cribosa en la AION y posterior a la lámina cribosa en la PION.
Varía mucho según el tipo. En la PION no arterítica, el 69% de los casos tienen una agudeza visual de 20/200 o peor, y solo el 20% mantiene 20/40 o mejor. En la PION perioperatoria, la agudeza visual final más común es sin percepción de luz (NLP), y el 75.8% de los ojos tienen cuenta dedos o peor. 1)
No arterítica
Hallazgos papilares: Normal en la fase aguda. Palidez después de 6–8 semanas.
Agudeza visual: 20/200 o peor en el 69%.
Evolución: Aparición rara. Se ha informado mejoría del campo visual con esteroides.
Arterítica (arteritis de células gigantes)
Hallazgos papilares: Normal en la fase aguda. Palidez posterior.
Síntomas sistémicos: Acompañados de cefalea, claudicación mandibular y elevación de VSG/PCR.
Evolución: Menor probabilidad de recuperación visual que en la forma no arterítica.
Perioperatorio
Forma de inicio: Se nota al despertar o dentro de los pocos días posteriores a la cirugía.
Lado afectado: Bilateral en el 70%.
Evolución: Más grave. NLP es el resultado más común.
Secundario a enfermedad microvascular, que involucra los siguientes factores de riesgo vascular.
Ocurre en pacientes más jóvenes que la PION arterítica. Se conocen los siguientes factores de riesgo.
Factores de riesgo preexistentes:
Factores de riesgo intraoperatorios:
Procedimientos quirúrgicos asociados (en orden de frecuencia):
La incidencia después de cirugía espinal se reporta como 0.087%, y después de disección de cuello como 0.08%.1)
La incidencia después de cirugía espinal se reporta como 0.087%, y después de disección de cuello como 0.08%.1) Aunque la frecuencia es baja, el pronóstico visual es extremadamente malo una vez que ocurre, por lo que la explicación preoperatoria y el manejo perioperatorio para pacientes de alto riesgo son importantes.
La PION es un diagnóstico clínico y también un diagnóstico de exclusión. El proceso diagnóstico es el siguiente.
El proceso es: disminución aguda de la visión + defecto del campo visual + RAPD positivo + hallazgos normales de la papila en la fase aguda → palidez de la papila después de 6 a 8 semanas → exclusión de otras causas (neuritis óptica retrobulbar, enfermedad retiniana, compresión, toxicidad, etc.). La PION perioperatoria es relativamente clara de diagnosticar porque la pérdida de visión ocurre después de una cirugía no oftálmica.
En pacientes de 50 años o más, se miden la ESR y la PCR para descartar arteritis de células gigantes.
A continuación se muestran la sensibilidad y especificidad de cada prueba para el diagnóstico de arteritis de células gigantes.
| Prueba | Sensibilidad | Especificidad |
|---|---|---|
| ESR + PCR combinados | Hasta 100% | 97% |
| Trombocitosis | 57.0% | 96.5% |
| Hemoglobina baja | 46.3% | 92.9% |
| Disminución del hematocrito | 39.8% | 91.3% |
| Leucocitosis | 28.1% | 85.7% |
La PCR tiene mayor especificidad que la VSG. El valor de referencia de la VSG es la mitad de la edad en hombres y la mitad de (edad + 10) en mujeres. La biopsia de la arteria temporal (BAT) es el estándar de oro para el diagnóstico de arteritis de células gigantes, con sensibilidad y especificidad superiores al 95% si se realiza adecuadamente. La biopsia debe realizarse dentro de los pocos días incluso después de iniciar el tratamiento con esteroides. En la PION no arterítica, estos valores de laboratorio son normales.
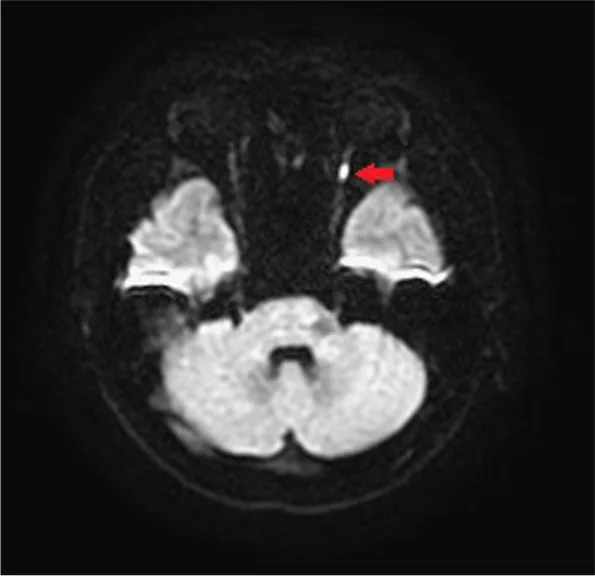
Los principales diagnósticos diferenciales incluyen neuritis óptica retrobulbar, enfermedades maculares/retinianas, neuropatía óptica tóxica y compresión o inflamación del nervio óptico posterior. Para diferenciar la neuropatía óptica isquémica de la neuritis óptica retrobulbar, se evalúan en combinación VEP, electrorretinografía, OCT y DWI MRI.
Se recomienda el siguiente protocolo:
Según informes internacionales, la dosis inicial mediana es de prednisolona 80 mg/día, que se reduce después de que la VSG y la PCR se estabilicen. La duración total del tratamiento, incluida la reducción, es de aproximadamente 2.5 meses.
No existe un tratamiento eficaz establecido. Se han intentado anticoagulación, vasodilatadores, esteroides orales y descompresión de la vaina del nervio óptico, pero no se ha demostrado una mejora significativa en el pronóstico visual. Se puede considerar un régimen de prednisolona 80 mg/día durante 2 semanas seguido de reducción gradual, pero no hay datos de ECA.
No existe un tratamiento establecido. Generalmente no se recomiendan los esteroides. Las medidas generales incluyen:
Recomendación práctica para cirugía de columna (Guía de manejo perioperatorio)
El manejo sistemático preoperatorio, intraoperatorio y postoperatorio es importante para prevenir la pérdida de visión.
Preoperatorio:
Intraoperatorio:
Postoperatorio:
El pronóstico varía mucho según el subtipo. En la PION arterítica, la administración inmediata de esteroides puede reducir la progresión y la afectación del ojo contralateral, pero es difícil esperar una mejora significativa en la visión ya disminuida del ojo afectado. La PION perioperatoria no responde a los esteroides y a menudo sigue un curso bilateral, irreversible y grave. Para la PION no arterítica, hay informes de mejora del campo visual con esteroides, pero no hay evidencia establecida.
El nervio óptico posterior se divide en tres segmentos: intraorbitario, intracanalicular e intracraneal. La porción retrolaminar del nervio óptico recibe irrigación del plexo vascular pial y de ramas de la arteria central de la retina.
La hemorragia postoperatoria y el aumento de la presión intracraneal por compresión bilateral de la vena yugular interna (IJV) reducen la perfusión del nervio óptico, contribuyendo al desarrollo. 1) La ligadura de la IJV se ha sugerido como factor de riesgo para la neuropatía óptica isquémica, y se asume un deterioro de la perfusión arterial debido a la congestión venosa. 1) Los mecanismos de reducción del suministro de oxígeno incluyen: ① niveles bajos de oxígeno en la sangre circulante, ② disminución de la presión de perfusión arterial y ③ aumento de la resistencia al flujo sanguíneo. 1)
Kohyama et al. (2022) reportaron un caso de PION que se desarrolló después de una laringofaringectomía con disección cervical bilateral y reconstrucción con colgajo yeyunal libre. 1) Se considera el primer caso reportado de PION causado por hemorragia postoperatoria y compresión bilateral de la IJV.
Tiempo quirúrgico 13.5 horas, pérdida sanguínea total 740 g. La presión arterial sistólica disminuyó de aproximadamente 150 mmHg preoperatorio a un mínimo de 80 mmHg (durante varios minutos). La hemoglobina disminuyó de 13.5 g/dL preoperatorio a 9.5 g/dL postoperatorio, luego cayó bruscamente a 6.1 g/dL debido a la hemorragia. El hematocrito disminuyó de 38.1% preoperatorio a 29.3% postoperatorio, luego cayó a 19.3%. Postoperatoriamente, se produjo edema facial y cervical, y ambas IJVs fueron comprimidas por un hematoma. 1)
Se administró prednisolona oral a 1 mg/kg/día durante más de 2 meses, pero la agudeza visual se mantuvo en el nivel de percepción de luz sin mejoría, y no se observó recuperación visual incluso después de 1 año. 1) Hubo un retraso de 7 horas desde el inicio del edema hasta la liberación del hematoma, y los autores señalan que una incisión exploratoria temprana podría haber prevenido la PION. 1) También se ha informado que el 75.8% de los ojos con PION perioperatoria tienen una agudeza visual de contar dedos o peor. 1)
En cuanto al tratamiento con esteroides para la PION no arterítica, se observó una mejora significativa del campo visual (P=0.030) en el grupo tratado con esteroides en comparación con el grupo control, y también se informaron mejoras significativas en el campo visual (P<0.001) y la agudeza visual (P=0.031) en comparación con el valor basal. Sin embargo, no existen datos de ECA.
Existen informes de que la combinación de oxigenoterapia hiperbárica dentro de las 72 horas del inicio y esteroides tuvo éxito en un pequeño número de casos de PION perioperatoria. Se espera una mayor acumulación de casos e investigación.