Nicht-arteriitisch
Papillenbefund : in der Akutphase normal. Nach 6–8 Wochen Abblassung.
Sehschärfe : 20/200 oder schlechter bei 69 %.
Verlauf : seltenes Auftreten. Es gibt Berichte über Gesichtsfeldverbesserung unter Steroiden.

Die posteriore ischämische Optikusneuropathie (PION) ist eine ischämische Optikusneuropathie, die durch eine Kreislaufinsuffizienz des Sehnervs hinter der Lamina cribrosa verursacht wird. Sie unterscheidet sich klar von der anterioren ischämischen Optikusneuropathie (AION) durch das Fehlen einer Papillenschwellung in der akuten Phase. Die AION geht in der akuten Phase mit einer Papillenschwellung einher und wird je nach Ätiologie in arteriitisch (AAION) und nicht-arteriitisch (NAION) unterteilt. Die NAION ist grundsätzlich immer vom anterioren Typ, während die arteriitische Form der PION als posteriorer Typ (PAION) klassifiziert wird.
Die PION ist eine seltene Erkrankung, die nur etwa 10 % aller Fälle von Sehnervenischämie ausmacht und bevorzugt nach dem 50. Lebensjahr auftritt. Sie wird in drei Typen unterteilt:
Der Hauptunterschied liegt im Befund der Papille in der akuten Phase. Bei der AION kommt es in der akuten Phase zu einer Papillenschwellung, während bei der PION die Papille in der akuten Phase normal erscheint und nach 6–8 Wochen eine Blässe (Atrophie) auftritt. Die Ischämielokalisation ist bei der AION vor der Lamina cribrosa und bei der PION dahinter.
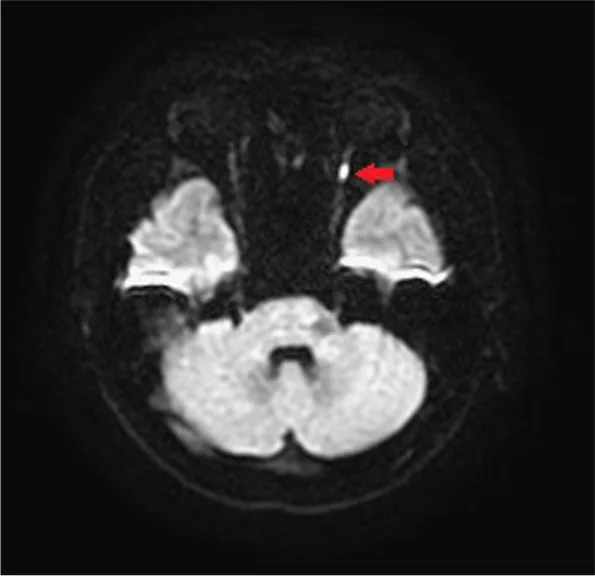
Variiert stark je nach Typ. Bei der nicht-arteriitischen PION haben 69 % der Fälle eine Sehschärfe von ≤ 20/200, und nur 20 % behalten ≥ 20/40. Bei der perioperativen PION ist die häufigste endgültige Sehschärfe keine Lichtwahrnehmung (NLP), und 75,8 % der Augen haben eine Sehschärfe von ≤ Fingerzählen. 1)
Nicht-arteriitisch
Papillenbefund : in der Akutphase normal. Nach 6–8 Wochen Abblassung.
Sehschärfe : 20/200 oder schlechter bei 69 %.
Verlauf : seltenes Auftreten. Es gibt Berichte über Gesichtsfeldverbesserung unter Steroiden.
Arteriitisch (Riesenzellarteriitis)
Papillenbefund : in der Akutphase normal. Danach Abblassung.
Allgemeinsymptome : Kopfschmerzen, Kieferclaudicatio, erhöhte BSG/CRP.
Verlauf : geringere Wahrscheinlichkeit einer Seherholung als bei der nicht-arteriitischen Form.
Perioperativ
Auftretensweise : bemerkt beim Erwachen oder innerhalb weniger Tage nach der Operation.
Betroffene Seite : in 70 % beidseitig.
Verlauf : am schwerwiegendsten. NLP ist das häufigste Ergebnis.
Sekundär zu einer Mikroangiopathie, mit Beteiligung der folgenden vaskulären Risikofaktoren.
Tritt bei jüngeren Patienten auf als die arteriitische PION. Folgende Risikofaktoren sind bekannt.
Bestehende Risikofaktoren:
Intraoperative Risikofaktoren:
Assoziierte chirurgische Verfahren (nach Häufigkeit):
Die Inzidenz nach Wirbelsäulenchirurgie wird mit 0,087 % und nach Neck Dissection mit 0,08 % angegeben.1)
Die Inzidenz nach Wirbelsäulenchirurgie wird mit 0,087 % und nach Neck Dissection mit 0,08 % angegeben.1) Die Häufigkeit ist gering, aber die Sehprognose im Falle des Auftretens ist äußerst schlecht, daher sind präoperative Aufklärung von Hochrisikopatienten und perioperatives Management wichtig.
PION ist eine klinische Diagnose und auch eine Ausschlussdiagnose. Der diagnostische Ablauf ist wie folgt.
Akuter Sehverlust + Gesichtsfeldausfall + positiver RAPD + normale Papille in der Akutphase → Papillenblässe nach 6–8 Wochen → Ausschluss anderer Ursachen (retrobulbäre Neuritis, Netzhauterkrankung, Kompression, Vergiftung usw.). Die perioperative PION tritt nach nicht-ophthalmologischen Operationen auf, daher ist die Diagnose relativ klar.
Bei Patienten ab 50 Jahren sollten BSG und CRP gemessen werden, um eine Riesenzellarteriitis auszuschließen.
Nachfolgend sind Sensitivität und Spezifität der einzelnen Tests für die Diagnose der Riesenzellarteriitis aufgeführt.
| Test | Sensitivität | Spezifität |
|---|---|---|
| BSG + CRP kombiniert | Bis zu 100 % | 97 % |
| Thrombozytose | 57,0 % | 96,5 % |
| Niedriges Hämoglobin | 46,3 % | 92,9 % |
| Niedriger Hämatokrit | 39,8 % | 91,3 % |
| Leukozytose | 28,1 % | 85,7 % |
CRP hat eine höhere Spezifität als BSG. Der Normalwert der BSG nach 1 Stunde beträgt bei Männern die Hälfte des Alters, bei Frauen die Hälfte von (Alter + 10). Die Temporalarterienbiopsie (TAB) ist der Goldstandard für die Diagnose der Riesenzellarteriitis und hat bei korrekter Durchführung eine Sensitivität und Spezifität von über 95 %. Die Biopsie sollte auch nach Beginn der Steroidtherapie innerhalb weniger Tage durchgeführt werden. Bei nicht-arteriitischer PION sind diese Laborwerte normal.
Die wichtigsten Differentialdiagnosen sind retrobulbäre Neuritis, Makula- und Netzhauterkrankungen, toxische Optikusneuropathie sowie Kompression oder Entzündung des hinteren Sehnervs. Zur Unterscheidung zwischen ischämischer Optikusneuropathie und retrobulbärer Neuritis werden VEP, Elektroretinogramm, OCT und DWI-MRT kombiniert.
Das folgende Protokoll wird empfohlen:
Laut ausländischen Berichten beträgt die mediane Anfangsdosis 80 mg/Tag Prednisolon, die nach Stabilisierung von BSG und CRP reduziert wird. Die Behandlungsdauer einschließlich Ausschleichen beträgt etwa 2,5 Monate.
Es gibt keine etablierte wirksame Behandlung. Antikoagulation, Vasodilatatoren, orale Steroide und eine Dekompression der Sehnervenscheide wurden versucht, aber eine signifikante Verbesserung der Sehprognose wurde nicht nachgewiesen. Eine Methode mit Prednisolon 80 mg/Tag für 2 Wochen gefolgt von einer schrittweisen Reduktion kann in Betracht gezogen werden, aber es liegen keine RCT-Daten vor.
Es gibt keine etablierte Behandlung. Steroide werden in der Regel nicht empfohlen. Allgemeine Maßnahmen umfassen:
Practice Advisory (perioperative Managementrichtlinien) für Wirbelsäulenchirurgie
Ein systematisches prä-, intra- und postoperatives Management ist wichtig zur Prävention von Sehverlust.
Präoperativ:
Intraoperativ:
Postoperativ:
Die Prognose variiert stark je nach Typ. Bei arteriitischer PION kann eine sofortige Steroidgabe das Fortschreiten und die Beteiligung des anderen Auges reduzieren, aber eine signifikante Verbesserung des bereits verminderten Sehvermögens des betroffenen Auges ist unwahrscheinlich. Perioperative PION spricht nicht auf Steroide an und verläuft oft beidseitig, irreversibel und schwerwiegend. Bei nicht-arteriitischer PION gibt es Berichte über eine Verbesserung des Gesichtsfelds mit Steroiden, aber keine etablierte Evidenz.
Der hintere Sehnerv wird in drei Abschnitte unterteilt: intraorbital, intrakranial und intrakraniell. Der Sehnerv hinter der Lamina cribrosa wird vom Plexus der Pia mater und den Ästen der Zentralarterie der Netzhaut versorgt.
Postoperative Blutung und erhöhter intrakranieller Druck durch bilaterale Kompression der Vena jugularis interna (VJI) vermindern die Perfusion des Sehnervs und tragen zur Entstehung bei. 1) Die Ligatur der VJI wurde als Risikofaktor für ischämische Optikusneuropathie vorgeschlagen, und es wird angenommen, dass venöse Stauung die arterielle Perfusion beeinträchtigt. 1) Zu den Mechanismen der verminderten Sauerstoffversorgung gehören: ① niedriger Sauerstoffgehalt im zirkulierenden Blut, ② verminderter arterieller Perfusionsdruck und ③ erhöhter Blutflusswiderstand. 1)
Kohyama et al. (2022) berichteten über einen Fall von PION nach Laryngopharyngektomie mit bilateraler Neck Dissection und freiem Jejunumlappen-Transplantat. 1) Dies gilt als der erste berichtete Fall von PION, verursacht durch postoperative Blutung und bilaterale VJI-Kompression.
Operationszeit 13,5 Stunden, Gesamtblutverlust 740 g. Der systolische Blutdruck fiel von präoperativ etwa 150 mmHg auf minimal 80 mmHg (für einige Minuten). Hämoglobin fiel von präoperativ 13,5 g/dL auf postoperativ 9,5 g/dL und dann aufgrund der Blutung auf 6,1 g/dL. Hämatokrit fiel von präoperativ 38,1 % auf postoperativ 29,3 % und dann auf 19,3 %. Postoperativ traten Gesichts- und Halsödeme auf, und beide VJI wurden durch ein Hämatom komprimiert. 1)
Die orale Gabe von Prednisolon 1 mg/kg/Tag über mehr als 2 Monate verbesserte die Sehschärfe nicht, die auf Lichtwahrnehmungsniveau blieb, und auch nach einem Jahr wurde keine Seherholung festgestellt. 1) Die Autoren weisen darauf hin, dass es eine Verzögerung von 7 Stunden zwischen dem Auftreten des Ödems und der Entlastung des Hämatoms gab und dass eine frühe explorative Inzision die PION möglicherweise verhindert hätte. 1) Es wurde auch berichtet, dass 75,8 % der Augen mit perioperativer PION eine Sehschärfe unterhalb des Fingerzählens behalten. 1)
Bezüglich der Steroidtherapie bei nicht-arteriitischer PION wurde im Vergleich zur Kontrollgruppe eine signifikante Verbesserung des Gesichtsfelds (P=0,030) in der Steroidgruppe berichtet, sowie eine signifikante Verbesserung des Gesichtsfelds (P<0,001) und der Sehschärfe (P=0,031) im Vergleich zum Ausgangswert. Es liegen jedoch keine RCT-Daten vor.
Es gibt Berichte, dass die Kombination von hyperbarer Sauerstofftherapie innerhalb von 72 Stunden nach Beginn und Steroiden bei einer kleinen Anzahl von Fällen perioperativer PION erfolgreich war. Zukünftige Fallansammlungen und Forschung werden erwartet.