Non arteritica
Reperti papillari : normali in fase acuta. Pallore dopo 6-8 settimane.
Acuità visiva : 20/200 o inferiore nel 69% dei casi.
Decorso : insorgenza rara. Segnalati miglioramenti del campo visivo con steroidi.

La neuropatia ottica ischemica posteriore (NOIP) è una neuropatia ottica ischemica causata da insufficienza circolatoria del nervo ottico posteriormente alla lamina cribrosa. Si distingue chiaramente dalla neuropatia ottica ischemica anteriore (NOIA) per l’assenza di edema della papilla ottica in fase acuta. La NOIA si accompagna a edema papillare in fase acuta e viene classificata in base all’eziologia in arteritica (AAION) e non arteritica (NAION). La NAION è in linea di principio sempre di tipo anteriore, mentre la forma arteritica della NOIP è classificata come tipo posteriore (PAION).
La NOIP è una malattia rara, rappresentando solo circa il 10% di tutti i casi di ischemia del nervo ottico, e si verifica prevalentemente dopo i 50 anni. Si classifica in tre tipi:
La differenza principale è il reperto della papilla ottica in fase acuta. Nella NOIA si verifica edema papillare in fase acuta, mentre nella NOIP la papilla appare normale in fase acuta e dopo 6-8 settimane compare pallore (atrofia). La sede dell’ischemia è anteriore alla lamina cribrosa nella NOIA e posteriore nella NOIP.
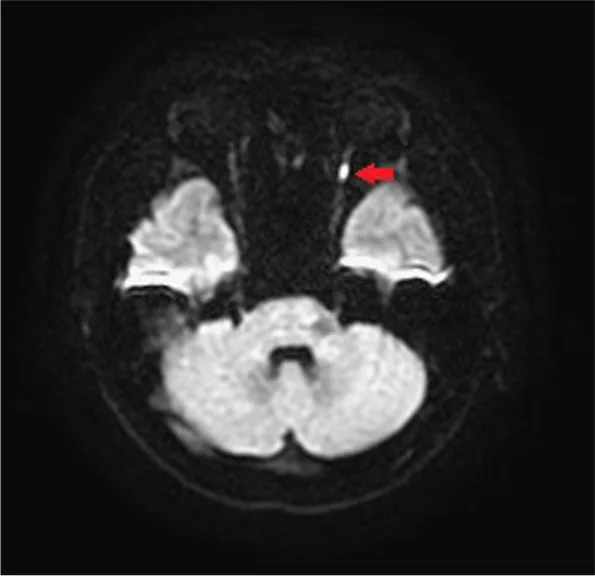
Varia notevolmente a seconda del tipo. Nella PION non arteritica, il 69% dei casi ha un’acuità visiva ≤ 20/200, e solo il 20% mantiene ≥ 20/40. Nella PION perioperatoria, l’acuità visiva finale più frequente è l’assenza di percezione luminosa (NLP), e il 75,8% degli occhi ha un’acuità ≤ contare le dita. 1)
Non arteritica
Reperti papillari : normali in fase acuta. Pallore dopo 6-8 settimane.
Acuità visiva : 20/200 o inferiore nel 69% dei casi.
Decorso : insorgenza rara. Segnalati miglioramenti del campo visivo con steroidi.
Arteritica (arterite a cellule giganti)
Reperti papillari : normali in fase acuta. Successivo pallore.
Sintomi sistemici : cefalea, claudicatio mandibolare, aumento di VES/PCR.
Decorso : minori possibilità di recupero visivo rispetto alla forma non arteritica.
Perioperatoria
Modalità di insorgenza : notata al risveglio o entro pochi giorni dall’intervento.
Lato colpito : bilaterale nel 70% dei casi.
Decorso : la più grave. La NLP è l’esito più comune.
Secondaria a malattia dei piccoli vasi, con coinvolgimento dei seguenti fattori di rischio vascolari.
Si verifica in pazienti più giovani rispetto alla PION arteritica. Sono noti i seguenti fattori di rischio.
Fattori di rischio preesistenti:
Fattori di rischio intraoperatori:
Procedure chirurgiche associate (in ordine di frequenza):
L’incidenza dopo chirurgia spinale è riportata allo 0,087% e dopo dissezione del collo allo 0,08%.1)
L’incidenza dopo chirurgia spinale è riportata allo 0,087% e dopo dissezione del collo allo 0,08%.1) La frequenza è bassa, ma in caso di insorgenza la prognosi visiva è estremamente sfavorevole, quindi sono importanti la spiegazione preoperatoria ai pazienti ad alto rischio e la gestione perioperatoria.
La PION è una diagnosi clinica, ed è anche una diagnosi di esclusione. Il processo diagnostico è il seguente.
Riduzione acuta della vista + difetto del campo visivo + RAPD positivo + papilla normale in fase acuta → pallore papillare dopo 6-8 settimane → esclusione di altre cause (neurite ottica retrobulbare, malattia retinica, compressione, intossicazione, ecc.). La PION perioperatoria si verifica dopo interventi chirurgici non oftalmici, quindi la diagnosi è relativamente chiara.
Nei pazienti di età pari o superiore a 50 anni, misurare VES e PCR per escludere l’arterite a cellule giganti.
Di seguito sono riportati sensibilità e specificità di ciascun test per la diagnosi di arterite a cellule giganti.
| Test | Sensibilità | Specificità |
|---|---|---|
| VES + PCR combinati | Fino al 100% | 97% |
| Piastrinosi | 57,0% | 96,5% |
| Bassa emoglobina | 46,3% | 92,9% |
| Ematocrito basso | 39,8% | 91,3% |
| Leucocitosi | 28,1% | 85,7% |
La PCR ha una specificità maggiore della VES. Il valore normale della VES a 1 ora è la metà dell’età negli uomini e la metà di (età + 10) nelle donne. La biopsia dell’arteria temporale (TAB) è il gold standard per la diagnosi di arterite a cellule giganti, con sensibilità e specificità superiori al 95% se eseguita correttamente. La biopsia deve essere eseguita entro pochi giorni dall’inizio della terapia steroidea. Nella PION non arteritica questi valori sono normali.
Le principali diagnosi differenziali sono la neurite ottica retrobulbare, le malattie maculari e retiniche, la neuropatia ottica tossica e la compressione o infiammazione del nervo ottico posteriore. Per distinguere la neuropatia ottica ischemica dalla neurite ottica retrobulbare, si combinano VEP, elettroretinogramma, OCT e DWI RM.
Si raccomanda il seguente protocollo:
Secondo report internazionali, la dose iniziale mediana è di 80 mg/die di prednisolone, con riduzione graduale dopo stabilizzazione di VES e PCR. La durata del trattamento, inclusa la riduzione, è di circa 2,5 mesi.
Non esiste un trattamento efficace stabilito. Sono stati tentati anticoagulanti, vasodilatatori, steroidi orali e decompressione della guaina del nervo ottico, ma non è stato dimostrato un miglioramento significativo della prognosi visiva. Un metodo con prednisolone 80 mg/die per 2 settimane seguito da riduzione graduale può essere considerato, ma non esistono dati di RCT.
Non esiste un trattamento stabilito. Gli steroidi generalmente non sono raccomandati. Le misure generali includono:
Practice Advisory (linee guida per la gestione perioperatoria) per la chirurgia spinale
Una gestione sistematica pre-, intra- e post-operatoria è importante per prevenire la perdita della vista.
Pre-operatorio:
Intra-operatorio:
Post-operatorio:
La prognosi varia notevolmente a seconda del tipo. Nella PION arteritica, la somministrazione immediata di steroidi può ridurre la progressione e il coinvolgimento dell’altro occhio, ma è improbabile un miglioramento significativo della vista già ridotta dell’occhio colpito. La PION perioperatoria non risponde agli steroidi e spesso ha un decorso bilaterale, irreversibile e grave. Per la PION non arteritica, ci sono segnalazioni di miglioramento del campo visivo con steroidi, ma non ci sono prove consolidate.
Il nervo ottico posteriore è diviso in tre parti: intraorbitaria, intracanalicolare e intracranica. La parte posteriore alla lamina cribrosa riceve apporto ematico dal plesso vascolare piale e dai rami dell’arteria centrale della retina.
L’emorragia postoperatoria e l’aumento della pressione intracranica dovuto alla compressione bilaterale delle vene giugulari interne (VGI) riducono la perfusione del nervo ottico, contribuendo allo sviluppo. 1) La legatura delle VGI è stata suggerita come fattore di rischio per la neuropatia ottica ischemica e si ipotizza che la congestione venosa comprometta la perfusione arteriosa. 1) I meccanismi di riduzione dell’apporto di ossigeno includono: ① basso livello di ossigeno nel sangue circolante, ② diminuzione della pressione di perfusione arteriosa e ③ aumento della resistenza al flusso sanguigno. 1)
Kohyama et al. (2022) hanno riportato un caso di PION insorta dopo laringofaringectomia con dissezione cervicale bilaterale e ricostruzione con lembo libero digiunale. 1) È considerato il primo caso riportato di PION causata da emorragia postoperatoria e compressione bilaterale delle VGI.
Durata dell’intervento 13,5 ore, perdita ematica totale 740 g. La pressione arteriosa sistolica è scesa da circa 150 mmHg preoperatori a un minimo di 80 mmHg (per alcuni minuti). L’emoglobina è scesa da 13,5 g/dL preoperatori a 9,5 g/dL postoperatori, per poi crollare a 6,1 g/dL a causa dell’emorragia. L’ematocrito è sceso dal 38,1% preoperatorio al 29,3% postoperatorio, per poi scendere al 19,3%. Dopo l’intervento si sono verificati edema facciale e cervicale, ed entrambe le VGI sono state compresse da un ematoma. 1)
La somministrazione orale di prednisolone 1 mg/kg/die per oltre 2 mesi non ha migliorato l’acuità visiva, che è rimasta a livello di percezione luminosa, e non è stato osservato alcun recupero visivo dopo un anno. 1) Gli autori notano che c’è stato un ritardo di 7 ore tra l’insorgenza dell’edema e la decompressione dell’ematoma, e che un’incisione esplorativa precoce avrebbe potuto prevenire la PION. 1) È stato anche riportato che il 75,8% degli occhi con PION perioperatoria rimane con un’acuità visiva inferiore al conteggio delle dita. 1)
Per quanto riguarda la terapia steroidea per la PION non arteritica, è stato riportato un miglioramento significativo del campo visivo (P=0,030) nel gruppo trattato con steroidi rispetto al gruppo di controllo, e un miglioramento significativo del campo visivo (P<0,001) e dell’acuità visiva (P=0,031) rispetto al basale. Tuttavia, non esistono dati provenienti da studi randomizzati controllati.
È stato riportato che la combinazione di ossigenoterapia iperbarica entro 72 ore dall’esordio e steroidi ha avuto successo in un piccolo numero di casi di PION perioperatoria. Sono attesi l’accumulo di casi e ulteriori ricerche.