Neuropatia Óptica Isquêmica Anterior Não Arterítica (NAION)

Neuropatia óptica
1. O que é neuropatia óptica?
Seção intitulada “1. O que é neuropatia óptica?”Neuropatia óptica (optic neuropathy) é um termo geral para um grupo de doenças nas quais ocorre dano ao nervo óptico, resultando em declínio da função visual. Manifesta-se por diminuição da acuidade visual, defeitos de campo visual, anormalidades na visão de cores, redução da sensibilidade ao contraste, ou uma combinação destes 2).
O nervo óptico é composto por aproximadamente 1,2 milhão de axônios de células ganglionares da retina (RGC). Dentro do globo ocular, eles se agrupam para formar o disco óptico e, em seguida, passam pelo canal óptico até o quiasma óptico. A lesão do disco óptico até a porção anterior ao quiasma é chamada de “lesão de via óptica anterior”, e a maioria das neuropatias ópticas clinicamente significativas ocorre nessa região 2). As lesões após o quiasma (trato óptico, radiações ópticas, lobo occipital) são chamadas de “lesões de via óptica posterior” e são tratadas como “distúrbios de via óptica”, não como neuropatia óptica.
O nervo óptico é dividido em quatro partes. A parte intraocular (disco óptico, cerca de 1 mm) é um local comum para neuropatia óptica isquêmica e inflamatória. A parte intraorbitária (cerca de 25 mm) é frequentemente afetada por neuropatia compressiva e inflamatória. A parte intracanalicular (canal óptico, cerca de 5–8 mm) é suscetível a trauma e compressão óssea. A parte intracraniana (cerca de 10 mm) é frequentemente comprimida por adenomas hipofisários ou craniofaringiomas. Também é importante distinguir entre “neuropatia óptica anterior”, onde o disco óptico pode ser observado diretamente, e “neuropatia óptica retrobulbar”, onde o fundo de olho parece normal. Na neuropatia óptica retrobulbar, não há alterações no disco óptico, tornando-a facilmente negligenciada como causa de baixa acuidade visual.
O fluxo sanguíneo para o disco óptico é fornecido principalmente pelas artérias ciliares posteriores curtas (artérias SPC). Essas artérias são ramos terminais da artéria oftálmica e irrigam a camada pré-laminar do disco óptico, a lâmina cribrosa e a região retrolaminar. O distúrbio circulatório nessa área é a base fisiopatológica principal da NAION e da AAION 3). O interior do nervo óptico é protegido pela barreira hematoencefálica, mas esse mecanismo de proteção é rompido na neurite óptica inflamatória e em doenças autoimunes 2).
Via Comum da Fisiopatologia e Atrofia Óptica
Seção intitulada “Via Comum da Fisiopatologia e Atrofia Óptica”Independentemente da causa, todos os casos seguem, em última análise, uma via comum: dano às células ganglionares da retina e aos axônios do nervo óptico → apoptose → atrofia óptica. A atrofia óptica é o estágio final da neuropatia óptica, reconhecida pela palidez do disco óptico. Uma vez estabelecida a atrofia, a recuperação da função visual é extremamente limitada 2).
Os axônios do nervo óptico consistem em uma mistura de fibras mielinizadas e não mielinizadas com diâmetro de 0,2 a 10 μm, e são divididos em células p (responsáveis pelo brilho e contraste) e células m (responsáveis pelo movimento e bordas). Na neuropatia óptica, as células p, que consomem muito ATP, são mais suscetíveis a danos, e isso está relacionado ao mecanismo de ocorrência do escotoma central na neuropatia óptica tóxica e nutricional 2).
Visão Geral da Epidemiologia
Seção intitulada “Visão Geral da Epidemiologia”Visão geral das taxas de incidência anuais das principais neuropatias ópticas (por 100.000 adultos). NAION é a mais comum com 2,3–10,2 (EUA)3). Neurite óptica idiopática é relatada como 1,6 (adultos japoneses)13), LHON (Neuropatia Óptica Hereditária de Leber) tem cerca de 117 novos casos por ano no Japão (pesquisa de 2014), sendo uma doença rara14). A taxa de incidência anual estimada de AAION/GCA é de 0,36 por 100.000 em maiores de 50 anos, mais comum em caucasianos nórdicos (cerca de 30 por 100.000 na Noruega). Complicações visuais da GCA ocorrem em 10–30% (até 70% em alguns relatos), e AAION representa 60–90% delas1). A taxa de incidência anual de MOGAD é estimada em 1,6–4,8 por milhão de pessoas6).
Sistema de Classificação das Neuropatias Ópticas
Seção intitulada “Sistema de Classificação das Neuropatias Ópticas”As neuropatias ópticas são classificadas sob várias perspectivas. Abaixo está a classificação mais útil clinicamente.
Classificação pelo padrão de início
- Agudo (horas a dias): NAION, AAION, traumática
- Subagudo (dias a semanas): Neurite óptica idiopática, LHON, compressivo (parcial)
- Crônico (meses a anos): ADOA, compressivo crônico, radiação (tardio)
Classificação por causa
- Isquêmico: NAION, AAION, PION
- Inflamatório (neurite óptica): Idiopática, relacionada à EM, relacionada à NMOSD, relacionada à MOGAD, infecciosa
- Compressivo: Tumor, cisto, aneurisma, oftalmopatia tireoidiana
- Tóxico: etambutol, amiodarona, álcool, etc.
- Nutricional: deficiência de vitamina B12/B1/folato/cobre
- Hereditário: LHON, ADOA, síndrome de Wolfram
- Traumático: fratura do canal óptico, lesão direta
- Radiação: degeneração isquêmica tardia
Classificação por localização
- Neuropatia óptica anterior (com alterações na papila): NAION, AAION, neurite óptica anterior
- Neuropatia óptica retrobulbar (papila normal): tóxica, hereditária, neurite óptica relacionada à EM (a maioria)
- Lesões do quiasma óptico: adenoma hipofisário, craniofaringioma (hemianopsia bitemporal)
Estrutura de Diagnóstico da Neuropatia Óptica
Seção intitulada “Estrutura de Diagnóstico da Neuropatia Óptica”O diagnóstico da neuropatia óptica é feito em 5 etapas.
Etapa 1: Confirmação da disfunção do nervo óptico Use RAPD, acuidade visual, visão de cores e campo visual para confirmar objetivamente a disfunção do nervo óptico.
Passo 2: Localização da lesão Anterior (com alterações papilares) ou retrobulbar (papila normal), intraorbital, intracanalicular ou intracraniana. A localização é estimada pelo padrão de defeito de campo visual.
Passo 3: Um olho ou ambos? Agudo ou crônico? Permite estreitar significativamente o diagnóstico diferencial.
Passo 4: Exclusão de tipos perigosos Exclusão prioritária de arterite de células gigantes (VHS, PCR), compressão (RM) e infecção (sífilis, fungos).
Passo 5: Exames específicos Adicionar testes de anti-AQP4, anti-MOG, DNA mitocondrial e exames nutricionais conforme o tipo.
2. Diferença da neurite óptica (esclarecimento conceitual)
Seção intitulada “2. Diferença da neurite óptica (esclarecimento conceitual)”“Neurite óptica” e “neuropatia óptica” são frequentemente confundidas na prática clínica, mas estão em uma relação de conceito subordinado e superordenado.
Confundir neuropatia óptica não inflamatória (isquêmica, compressiva, tóxica, genética) com neurite óptica pode levar à administração incorreta de esteroides. Especialmente na aspergilose infiltrativa, os esteroides são contraindicados 2), e na fase aguda da LHON, a administração de esteroides não é apenas ineficaz, mas também atrasa o diagnóstico definitivo.
Principais Características Clínicas da Neurite Óptica
Seção intitulada “Principais Características Clínicas da Neurite Óptica”A neurite óptica (inflamatória) apresenta as seguintes características que ajudam a diferenciá-la da não inflamatória.
- Início agudo: Progride em dias a 2 semanas, com tendência à recuperação em até 5 semanas.
- Dor à movimentação ocular: Presente em cerca de 50% dos casos. Geralmente ausente em casos isquêmicos, compressivos ou tóxicos.
- Idade de predileção: 15–45 anos (isquêmica geralmente acima de 50 anos).
- Achados de RM: Realce pelo contraste (T1 com gadolínio) coincidente com o nervo óptico.
- Recuperação espontânea: Em casos idiopáticos ou relacionados à EM, mais de 90% recuperam acuidade visual de 0,5 ou mais após 1 ano (estudo ONTT)4).
- Risco de transição para EM: 15 anos após o primeiro episódio, sem lesões na RM cerebral → 25%, com lesões → 78% evoluem para EM4).
Situação difícil de diferenciar
Seção intitulada “Situação difícil de diferenciar”Abaixo, a diferenciação entre neurite óptica e neuropatia óptica não inflamatória torna-se difícil.
- Perda visual aguda unilateral em mulheres com mais de 50 anos: NAION vs. Neurite óptica com anticorpo AQP4 positivo (NMOSD)
- Queda aguda bilateral da acuidade visual em jovens: LHON vs. Neurite óptica bilateral simultânea vs. Neuropatia óptica tóxica
- Baixa visual unilateral com edema de papila: NAION vs. neurite óptica anterior vs. papilite vascular
A neurite óptica com anticorpo AQP4 positivo é uma doença refratária resistente a esteroides que representa cerca de 10% das neurites ópticas idiopáticas, com idade de início mais avançada que a neurite óptica comum e maior prevalência em mulheres (proporção sexual 1:9) 5). O anticorpo AQP4 tem como alvo os canais de aquaporina 4 expressos em astrócitos dentro do nervo óptico, causando lesão celular dependente de complemento 5). Como as estratégias de tratamento diferem fundamentalmente entre casos positivos e negativos para anticorpo AQP4, o teste de anticorpos deve ser solicitado antes do pulso de esteroide. O método de medição usando ensaio baseado em células (CBA) tem maior sensibilidade e especificidade que o ELISA, sendo o CBA recomendado 5).
Antes de realizar o pulso de esteroide para neurite óptica, infecções (hepatite B, sífilis, HIV, fúngicas) devem ser excluídas 2). A administração de altas doses de esteroides em portadores do vírus da hepatite B pode causar hepatite fulminante. Na neurite óptica sifilítica, antibióticos têm prioridade sobre esteroides.
3. Subtipos de alta urgência
Seção intitulada “3. Subtipos de alta urgência”A tabela abaixo mostra os subtipos de neuropatia óptica que requerem atendimento de emergência especialmente.
| Subtipo | Nível de urgência | Impacto se perdido |
|---|---|---|
| Neuropatia óptica isquêmica anterior arterítica (AAION/GCA) | Máxima urgência | Cegueira no olho contralateral (65% dos não tratados desenvolvem em 10 dias) 1) |
| Neuropatia óptica compressiva aguda (tumor, cisto, hematoma) | Urgência | Atrofia óptica progressiva e perda visual irreversível |
| Neuropatia óptica nasal (aspergilose infiltrativa) | Emergência | Mortalidade de 94% relatada 2) |
| Neuropatia óptica traumática (fratura do canal óptico) | Emergência | Tratamento precoce pode preservar a função visual |
| Neuropatia óptica isquêmica posterior (PION) | Emergência | Ocorre após cirurgia ou perda maciça de sangue, frequentemente irreversível |
Fluxo de atendimento de emergência para GCA
Seção intitulada “Fluxo de atendimento de emergência para GCA”A amaurose fugaz (amaurosis fugax) aparece como sintoma prodrômico em cerca de 30% dos casos de perda visual permanente, sendo observada em média 8,5 dias antes1). Nesse ponto, é crucial suspeitar de arterite de células gigantes (ACG) e iniciar corticoides imediatamente como prevenção secundária.
4. Porta de Entrada para Diagnóstico Diferencial
Seção intitulada “4. Porta de Entrada para Diagnóstico Diferencial”O diagnóstico diferencial da neuropatia óptica é organizado sistematicamente em quatro eixos: “agudo ou crônico”, “unilateral ou bilateral”, “presença ou ausência de dor” e “achados papilares”.
Agudo ou Crônico
Seção intitulada “Agudo ou Crônico”Agudo (atinge dano máximo em horas a dias)
- NAION: queda súbita da visão percebida ao acordar é típica
- AAION: queda súbita da visão em um olho, grave (visão inferior a 20/200 em mais de 60%) 1)
- Traumático: imediatamente após o trauma até algumas horas
Subagudo (dias a semanas)
- Neurite óptica idiopática: progride ao longo de 2 semanas, depois a recuperação começa
- LHON: diminuição visual subaguda indolor em um olho, tornando-se bilateral em semanas a meses
- Compressivo: pode progredir subagudamente com crescimento tumoral rápido ou hemorragia
Crônico (progressão lenta ao longo de meses a anos)
- ADOA (Atrofia Óptica Dominante Autossômica): início na idade escolar, progressão lenta bilateral
- Compressivo crônico: devido a adenoma hipofisário, tumor orbitário, etc.
- Tóxico e nutricional: exposição prolongada ou deficiência nutricional levam a progressão subaguda a crônica
Um olho ou ambos os olhos
Seção intitulada “Um olho ou ambos os olhos”Doenças que tendem a ser unilaterais
- NAION: geralmente unilateral (início bilateral é extremamente raro)
- AAION: começa unilateralmente; sem tratamento, 65% se espalha para o olho contralateral em 10 dias1)
- Neurite óptica idiopática/associada a EM: tipicamente unilateral
- Compressiva, traumática, por radiação: frequentemente unilateral
Doenças com tendência bilateral
- LHON: inicialmente unilateral, torna-se bilateral em semanas a meses (eventualmente quase 100% bilateral)
- ADOA: início bilateral simétrico
- Tóxico/nutricional: geralmente bilateral (se um olho for completamente normal, considere excluir causa tóxica) 2)
- NMOSD/AQP4-IgG positivo: grave, bilateral, recorrente. 60-69% apresentam deficiência permanente em pelo menos um olho com acuidade ≤20/200 5)
- MOGAD: início bilateral frequente (muito raro na EM relacionada ou idiopática) 6)
Presença de dor
Seção intitulada “Presença de dor”| Com dor | Sem dor (indolor) |
|---|---|
| Neurite óptica idiopática (dor ao movimento ocular em cerca de 50%)13) | NAION (sem dor ocular, cefaleia e claudicação mandibular são sintomas sistêmicos de GCA) |
| Neurite óptica relacionada à EM | AAION (sem dor ocular, com claudicação mandibular e cefaleia) |
| Relacionado a NMOSD (dor periorbital) | LHON e ADOA (indolor) 14) |
| MOGAD (frequentemente associado a cefaleia) 6) | Tóxico/nutricional (sem dor à movimentação ocular) |
| Traumático (dor devido à lesão) | Compressivo (geralmente indolor, mas pode haver dor orbitária) |
Classificação com base nos achados da papila
Seção intitulada “Classificação com base nos achados da papila”5. Exame e Testes
Seção intitulada “5. Exame e Testes”Avaliação Oftalmológica Obrigatória
Seção intitulada “Avaliação Oftalmológica Obrigatória”Se houver suspeita de neuropatia óptica, realize a seguinte avaliação de forma sistemática.
Visão e visão de cores A acuidade visual corrigida é a base para avaliar a gravidade e a progressão do distúrbio. A visão de cores (Ishihara, Farnsworth-Munsell 100 hue) é frequentemente prejudicada precocemente na neuropatia óptica, e anormalidades de cor podem preceder a perda de acuidade visual. Na neuropatia óptica tóxica ou nutricional, a diminuição da sensação ao vermelho é um sinal precoce 2). Na ADOA (Atrofia Óptica Dominante Autossômica), a anomalia de cor terciária adquirida (anomalia azul-amarelo) é característica, mostrando um eixo de anomalia de cor terciária no teste Farnsworth-Munsell 100 hue 2).
RAPD (Defeito Pupilar Aferente Relativo)
O RAPD é avaliado pelo teste da lanterna oscilante e é um indicador objetivo de disfunção do nervo óptico. Também ajuda a diferenciar de distúrbios funcionais 2).
OCT (Tomografia de Coerência Óptica)
Seção intitulada “OCT (Tomografia de Coerência Óptica)”A OCT é um exame essencial para estadiamento e acompanhamento da neuropatia óptica.
| Indicador de avaliação | Achados na fase aguda | Achados na fase crônica |
|---|---|---|
| pRNFL (espessura da RNFL peripapilar) | Espessamento no edema de papila (cuidado com falso positivo) | Afinamento na atrofia do nervo óptico |
| GCL-IPL (camada de células ganglionares + camada plexiforme interna) | Pouca alteração | Afinamento refletindo dano às células ganglionares da retina |
| Forma da papila óptica | Escavação desaparece ou reduz | Fixa após atrofia |
Padrão de afinamento da pRNFL e diferenciação do tipo de doença
O padrão de afinamento da pRNFL na OCT é útil para diferenciar o tipo de doença a partir de algumas semanas a alguns meses após o início.
- Afinamento circunferencial grave: NMOSD (tipo positivo para anticorpo AQP4) é o mais grave. Ocorre afinamento grave em toda a circunferência.
- Afinamento temporal predominante (papillomacular bundle): Tóxico, nutricional, LHON, ADOA. Corresponde a escotoma central.
- Afinamento em leque superior ou inferior: NAION. Corresponde a defeitos fasciculares superiores ou inferiores.
- MOGAD vs. relacionado à EM: O afinamento da pRNFL após MOG-ON é mais grave que na EM6).
- Diferenciação do glaucoma: No glaucoma, as alterações na forma do disco (escavação aumentada) precedem, e o padrão de afinamento da GCL é diferente.
Exame de Campo Visual (Campímetro de Humphrey)
Seção intitulada “Exame de Campo Visual (Campímetro de Humphrey)”O padrão de defeito de campo visual está diretamente ligado à estimativa anatômica do local da lesão.
| Padrão de defeito de campo visual | Doença principalmente suspeita | Correspondência anatômica |
|---|---|---|
| Escotoma central e escotoma cego central | Tóxico, nutricional, LHON, ADOA, neurite óptica idiopática2) | Lesão do feixe papilomacular (PMB) |
| Defeito horizontal (temporal inferior para inferior) | NAION (defeito fascicular) 3) | Isquemia da metade superior ou inferior do disco óptico |
| Hemianopsia bitemporal | Compressão do quiasma óptico (adenoma hipofisário, craniofaringioma) | Fibras de decussação central do quiasma óptico |
| Hemianopsia homônima (mesmo lado) | Lesões pós-quiasmáticas (trato óptico, radiações ópticas, lobo occipital) | Via óptica central |
| Escotoma juncional | Lesões da extremidade anterior do quiasma, um tipo de neuropatia óptica nasal | Feixe papilomacular + temporal superior contralateral |
| Redução da sensibilidade geral | Relacionado à NMOSD / após neurite óptica grave 5) | Dano extenso das fibras do nervo óptico |
| Alargamento do ponto cego de Mariotte (visão normal) | Drusas de papila / papilite vasculite / perineurite óptica | Apenas ao redor da papila |

Exames de Sangue e Líquido Cefalorraquidiano
Seção intitulada “Exames de Sangue e Líquido Cefalorraquidiano”Mostra os exames recomendados como avaliação inicial da neuropatia óptica aguda.
| Item do Exame | Objetivo | Significância Clínica |
|---|---|---|
| VHS, PCR, plaquetas | Exclusão de GCA (AAION) | Prioridade máxima. PCR tem maior especificidade que VHS1) |
| Anticorpo anti-AQP4 (ensaio baseado em células) | Diagnóstico de NMOSD | O método ELISA tem sensibilidade e especificidade menores que o método CBA5) |
| Anticorpo anti-MOG (ensaio baseado em células) | Diagnóstico de MOGAD | CBA que reconhece a molécula MOG nativa é essencial 6) |
| Teste de sífilis (TPHA e RPR) e HIV | Exclusão de neurite óptica infecciosa | Deve ser confirmado antes do uso de esteroides |
| Vitamina B12, B1, ácido fólico, cobre | Avaliação de neuropatia óptica nutricional | Particularmente importante após cirurgia bariátrica ou dieta vegana |
| Genes mitocondriais (mt11778, mt14484, mt3460) | Diagnóstico de LHON | Essas três mutações cobrem mais de 95% dos casos14) |
| β-D-glucano e cultura fúngica | Suspeita de aspergilose invasiva | Tende a aumentar no tipo invasivo2) |
| ACE, lisozima, TC de tórax | Exclusão de sarcoidose | — |
| ANA, dsDNA, ANCA | Relacionado a doenças autoimunes sistêmicas (LES/vasculite) | — |
Indicações da Punção Lombar As indicações incluem: suspeita de meningite/encefalite infecciosa, auxílio diagnóstico de NMOSD/MOGAD (pleocitose no LCR e aumento do índice de IgG), auxílio diagnóstico de EM (bandas oligoclonais no LCR). Na NMOSD, pode ocorrer pleocitose acentuada com ≥50 células/μL6).
Exames de Imagem
Seção intitulada “Exames de Imagem”| Exame | Principais Avaliações | Observações Especiais |
|---|---|---|
| RM de órbita (T2 com supressão de gordura / T1 com contraste) | Inflamação do nervo óptico, edema, massa, realce pelo contraste | Na neurite óptica há realce pelo contraste. Na fase aguda da LHON não há realce 14) |
| RM de crânio (FLAIR) | Lesões desmielinizantes (EM, NMOSD) e lesões intracranianas | Usado nos critérios de McDonald para diagnóstico de EM |
| TC (condição óssea) | Fratura do canal óptico (trauma) - Patologia dos seios paranasais - Calcificação (drusas) | Essencial em trauma e doenças nasais |
| Ultrassonografia craniana (Doppler colorido) | Sinal de halo para diagnóstico de GCA | Sensibilidade 68%, especificidade 91% (100% se bilateral positivo)1) |
| PET-CT (FDG) | Avaliação de lesões de grandes vasos na GCA | Sensibilidade 92%, especificidade 85% (estudo GAPS) 1) |
| Ultrassonografia orbitária | Confirmação de calcificação de drusas do disco óptico | — |
Na neuropatia óptica aguda, a ressonância magnética (RM) orbitária é geralmente necessária. A prioridade máxima é excluir lesões compressivas, e a abordagem terapêutica difere significativamente dependendo se há realce pelo contraste (inflamatório) concordante com o nervo óptico ou compressão/deformidade (compressivo) 2). Se a RM com contraste não mostrar achados inflamatórios do nervo óptico, considere causas tóxicas, hereditárias ou nutricionais. Na fase aguda da LHON, não há achados inflamatórios, e não há extravasamento de fluoresceína do disco óptico na angiografia fluoresceínica de fundo, um ponto importante de diferenciação da neurite óptica inflamatória 14). Se a RM for contraindicada, realize tomografia computadorizada (TC) para avaliar seios paranasais, órbita e canal óptico.
Utilização do Potencial Evocado Visual (VEP)
Seção intitulada “Utilização do Potencial Evocado Visual (VEP)”O potencial evocado visual (VEP) é útil como marcador de neurite óptica desmielinizante. O prolongamento da latência de P100 (normal até 130 ms) sugere desmielinização, e o prolongamento frequentemente persiste após a recuperação na neurite óptica relacionada à esclerose múltipla (EM) e idiopática 13). A redução da amplitude é proeminente na lesão axonal (tóxica, isquêmica). Na neuropatia óptica tóxica, não há atraso na latência de P100, apenas redução da amplitude, o que ajuda na diferenciação da desmielinização 13). A redução da frequência crítica de flicker (CFF) também reflete a disfunção da neuropatia óptica, e mostra uma redução acentuada na neurite óptica relacionada ao transtorno do espectro da neuromielite óptica (NMOSD) 13).
6. Características por causa
Seção intitulada “6. Características por causa”As principais neuropatias ópticas são classificadas por causa e as características de cada tipo são resumidas.
6-1. Neuropatia Óptica Isquêmica
Seção intitulada “6-1. Neuropatia Óptica Isquêmica”Neuropatia Óptica Isquêmica Anterior Não Arterítica (NAION)
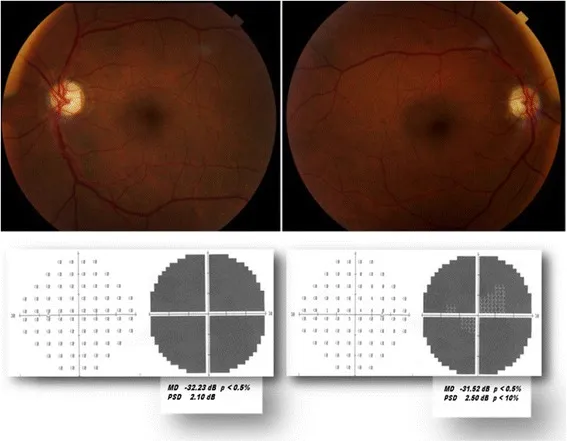
Seção intitulada “Neuropatia Óptica Isquêmica Anterior Não Arterítica (NAION)”NAION é o tipo mais comum de neuropatia óptica aguda em adultos, ocorrendo frequentemente acima dos 50 anos3). Ocorre infarto isquêmico na cabeça do nervo óptico devido à insuficiência circulatória aguda das artérias ciliares posteriores curtas.
- Epidemiologia: Incidência anual nos EUA é de 2,3 a 10,2 por 100.000 pessoas3). A maioria tem mais de 50 anos, mas a incidência abaixo dos 50 anos também está aumentando.
- Fatores de risco: Hipertensão, diabetes, hiperlipidemia, apneia do sono, disco em risco (relação escavação/disco <0,2). Disco em risco é encontrado em cerca de 80% do olho contralateral3).
- Sintomas: Perda visual aguda unilateral indolor, frequentemente notada ao acordar. RAPD positivo no olho afetado.
- Achados papilares: Hiperemia e edema (em leque com predomínio inferior). Pode haver hemorragia.
- Campo visual: Defeito fascicular horizontal (defeito temporal inferior típico).
- Tratamento: Não há terapia eficaz comprovada na fase aguda. O manejo dos fatores de risco vasculares e o tratamento da apneia do sono são a base da prevenção de recorrência.
- Atenção recente: Um estudo observacional de 2024 relatou aumento do risco de NAION em usuários de semaglutida (agonista do receptor GLP-1). No entanto, a relação causal não foi estabelecida, e a decisão de prescrição deve considerar os benefícios no tratamento de diabetes e obesidade7).
Neuropatia Óptica Isquêmica Anterior Arterítica (AAION/GCA)
Seção intitulada “Neuropatia Óptica Isquêmica Anterior Arterítica (AAION/GCA)”AAION representa 5-10% de todas as neuropatias ópticas isquêmicas anteriores, mas é a neuropatia óptica mais urgente 1). A causa subjacente é a vasculite das artérias ciliares posteriores curtas que irrigam o disco óptico, e mais de 90% dos casos são devidos à arterite de células gigantes (GCA).
- Epidemiologia: Mais comum em mulheres idosas acima de 50 anos (especialmente acima de 75 anos) com proporção homem:mulher de 1:3 1). A incidência no Japão é de 1,47 por 100.000 pessoas, muito menor em comparação com a Europa e os EUA.
- Sintomas: Perda visual grave unilateral aguda (menos de 20/200 em mais de 60% dos casos, e sem percepção de luz em mais de 20%) 1). Cerca de 30% dos pacientes experimentam amaurose fugaz precedente.
- Sintomas sistêmicos: Cefaleia (65-90%), claudicação mandibular (11-45%), dor à palpação do couro cabeludo, febre e sintomas semelhantes à PMR.
- Achados papilares: Edema pálido como giz (pallid swelling) é característico.
- Exames: VHS e PCR elevados (elevados em >80% dos casos)1). Biópsia de artéria temporal (sensibilidade e especificidade >95%)1).
- Tratamento: Corticosteroides em altas doses (mPSL 500-1000 mg IV por 3 dias → prednisolona oral em redução gradual)1). Tocilizumabe (antagonista do receptor de IL-6) é eficaz na redução de esteroides (estudo GiACTA, evidência de ECR)1).
- Prognóstico: A recuperação visual no olho afetado é quase improvável, mas o tratamento com esteroides é eficaz na prevenção do envolvimento do olho contralateral.
6-2. Neurite óptica inflamatória
Seção intitulada “6-2. Neurite óptica inflamatória”Neurite óptica idiopática
Seção intitulada “Neurite óptica idiopática”Doença inflamatória do nervo óptico por mecanismo autoimune, que constitui a maioria dos casos de neurite óptica 13). A idade de início comum é entre 15 e 45 anos, com mulheres representando cerca de 70%, e a incidência anual no Japão é de 1,6 por 100.000 adultos 13).
- Sintomas: Diminuição aguda da visão unilateral e dor ao movimento ocular (cerca de 50%). Progride ao longo de alguns dias a 2 semanas e mostra tendência à recuperação espontânea em 5 semanas.
- Campo visual: Escotoma central e escotoma central cego são comuns.
- RM: Realece contrastivo (gadolínio) correspondente ao nervo óptico.
- Prognóstico: Mais de 90% recuperam para acuidade visual de 0,5 ou melhor após 1 ano (estudo ONTT) 4).
- Tratamento: Terapia de pulso com esteroide mPSL 1000 mg/dia por 3 dias acelera a recuperação. A terapia oral isolada com esteroide não é realizada porque aumenta a taxa de recorrência (estudo ONTT) 4).
- Risco de conversão para EM: Incidência cumulativa de 50% em 15 anos após o primeiro episódio. Sem lesões na RM cerebral → 25%, com lesões → 78%4).
Neurite óptica associada à EM
Seção intitulada “Neurite óptica associada à EM”Surge como sintoma inicial da EM em cerca de 30% dos casos, e até 75% dos pacientes com EM apresentam pelo menos um episódio de neurite óptica ao longo da vida8). Geralmente unilateral, com dor à movimentação ocular e lesão retrobulbar (fundo de olho normal em 65%). Lesões desmielinizantes na RM cerebral (hiperintensidade em T2/FLAIR) são a chave diagnóstica. Após confirmação diagnóstica pelos critérios de McDonald (2017, revisão 2024), utiliza-se terapia modificadora da doença (DMT: interferon beta, natalizumabe, fingolimode, anti-CD20, etc.) para prevenir recidivas.
Neurite óptica associada à NMOSD (Doença do espectro da neuromielite óptica)
Seção intitulada “Neurite óptica associada à NMOSD (Doença do espectro da neuromielite óptica)”AQP4-IgG positivo. Predomina em mulheres (proporção 1:9), meia-idade e asiáticos; mais grave, bilateral e recidivante que a neurite óptica associada à EM5). A taxa de perda visual permanente (pelo menos 20/200 em um olho) chega a 60-69%5). A RM orbitária mostra lesões longas do nervo óptico (frequentemente envolvendo o quiasma). Tratamento: pulsoterapia com esteroide na fase aguda → plasmaférese → imunoterapia preventiva de recidivas (eculizumabe, rituximabe, satralizumabe)5).
Neurite óptica associada à MOGAD (Doença associada ao anticorpo MOG)
Seção intitulada “Neurite óptica associada à MOGAD (Doença associada ao anticorpo MOG)”MOG-IgG positivo. A taxa de incidência anual é de 1,6 a 4,8 por milhão de pessoas 6). O início bilateral é frequente com edema papilar intenso, e as lesões anteriores são predominantes. Na RM, as características são edema papilar, lesões longas do nervo óptico e perineurite óptica 6). A comparação da proporção de sexos entre MS-ON, AQP4-ON e MOG-ON é diferente: 3:1 / 7–9:1 / 1:1 6). Responsivo a esteroides, mas propenso a recaídas com redução precoce da dose, necessitando de redução gradual cuidadosa 6).
6-3. Neuropatia óptica compressiva
Seção intitulada “6-3. Neuropatia óptica compressiva”Causada pela compressão do nervo óptico por tumores, aneurismas, hematomas, abscessos, cistos ou músculos extraoculares hipertrofiados. Os sintomas e padrões de defeito de campo visual variam amplamente conforme o local da compressão.
- Ápice orbitário: Oftalmopatia tireoidiana (a neuropatia óptica tireoidiana ocorre em 3–8,6% dos casos de oftalmopatia tireoidiana, 70% bilateral), tumores orbitários (benignos: inflamação orbitária idiopática 20%, adenoma pleomórfico 13%, hemangioma 13% são os mais comuns. Malignos: linfoma maligno é o mais comum) 9).
- Quiasma óptico: Adenoma hipofisário (mais comum em adultos, hemianopsia bitemporal), craniofaringioma (mais comum em crianças).
- Neuropatia óptica nasal (nota especial): O tipo infiltrativo da sinusite fúngica (Aspergillus, Mucor) tem uma taxa de mortalidade de 94% conforme relatos 2). Como os esteroides são temporariamente eficazes, é frequentemente diagnosticado erroneamente como neurite óptica retrobulbar, e a continuação inadvertida de esteroides pode ser fatal. A destruição óssea na TC/RM é a chave para o diagnóstico, exigindo coordenação de emergência com otorrinolaringologia.
O princípio do tratamento é a remoção cirúrgica da lesão causadora. Quanto mais precoce a descompressão, melhor a recuperação esperada da função visual; após o estabelecimento da atrofia do nervo óptico, a recuperação é limitada.
6-4. Neuropatia Óptica Tóxica
Seção intitulada “6-4. Neuropatia Óptica Tóxica”Grupo de doenças que afetam a via visual anterior devido à exposição a substâncias químicas2). O princípio é bilateral e indolor; se um olho estiver completamente normal, a neuropatia óptica tóxica deve ser excluída2).
- Substâncias causadoras: Tabaco, álcool, solventes (medicamentos: etambutol (mais famoso), amiodarona, linezolida, cisplatina, imunossupressores, etc.).
- Campo visual: Caracteristicamente escotoma centrocecal ou escotoma central (dano predominante em células p)2).
- Visão de cores: Diminuição da sensação de vermelho é um sinal precoce.
- Fundo de olho: Normal ou leve vermelhidão no início → palidez temporal do disco e defeito do feixe papilomacular na fase crônica.
- RAPD: Negativo em princípio devido à simetria bilateral.
- VEP: Redução da amplitude, sem atraso na latência do P100 (atraso na latência é característico de neurite óptica desmielinizante) 13).
- Etambutol: Dose-dependente (risco aumenta acima de 15 mg/kg). Exame de função visual basal antes do tratamento e monitoramento regular são essenciais.
- Tratamento: A interrupção da substância causadora é a base. Não há medicamento específico.
6-5. Neuropatia óptica nutricional
Seção intitulada “6-5. Neuropatia óptica nutricional”Neuropatia óptica bilateral simétrica e progressiva devido à deficiência de vitaminas do complexo B (B12, B1, B2, B9) e cobre. Situa-se no mesmo espectro da neuropatia óptica tóxica, mas distingue-se por ser causada por deficiência nutricional. Os riscos modernos incluem cirurgia bariátrica (monitoramento vitalício obrigatório), dieta vegana e alcoolismo. Sintomas, campo visual e achados de fundo de olho são semelhantes aos tóxicos (escotoma central, indolor, palidez temporal da papila). A reposição nutricional precoce pode levar à recuperação, mas casos crônicos podem deixar danos irreversíveis.
6-6. Neuropatia Óptica Hereditária
Seção intitulada “6-6. Neuropatia Óptica Hereditária”LHON (Neuropatia Óptica Hereditária de Leber)
Seção intitulada “LHON (Neuropatia Óptica Hereditária de Leber)”Neuropatia óptica aguda ou subaguda causada por mutações pontuais no DNA mitocondrial (mtDNA) com herança materna 14). As três principais mutações (mt3460, mt11778, mt14484) representam mais de 95% de todos os casos, e mt11778 representa cerca de 90% dos casos na Ásia 14).
- Epidemiologia: Prevalência de 1/31.000 a 1/68.000. Penetrância de 2,5 a 17,5%, a maioria dos portadores não desenvolve a doença 14). No Japão, cerca de 117 novos casos por ano (pesquisa de 2014). Doença rara designada.
- Sintomas: Ocorre predominantemente em homens jovens (proporção sexual de cerca de 93:7). Escotoma central bilateral subagudo e indolor (um olho primeiro, depois bilateral em semanas a meses).
- Fundo de olho agudo: Hiperemia e edema do disco óptico, com dilatação e tortuosidade dos capilares peripapilares. Não há extravasamento de fluoresceína do disco na angiografia fluoresceínica (diferenciação importante da neurite óptica inflamatória) 14).
- Reflexo pupilar: Relativamente preservado em comparação com outras doenças do nervo óptico, ou apenas levemente prejudicado 14).
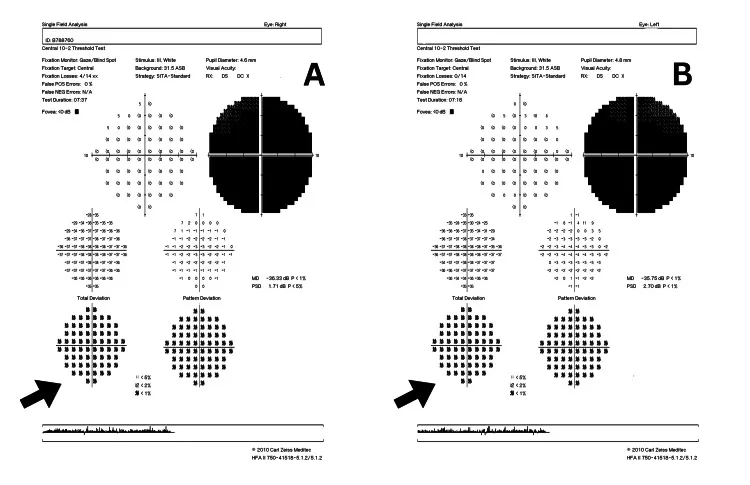
- Acuidade visual final: Na mt11778, frequentemente em torno de 0,01. A mt14484 tem a maior taxa de recuperação espontânea 14).
- Tratamento: Idebenona 900 mg/dia (aprovado pela EMA europeia). No estudo LEROS, a CRR (recuperação visual significativa) foi de 46,0% (vs placebo) 10). No estudo de coorte de Gales, a CRR atingiu 86% em 27 meses 10). A terapia genética também mostrou eficácia em ensaios de fase III 11). A orientação para cessação do tabagismo é importante para prevenir o início e a progressão da doença.
ADOA (Atrofia Óptica Dominante Autossômica)
Seção intitulada “ADOA (Atrofia Óptica Dominante Autossômica)”Neuropatia óptica hereditária mais frequente, causada principalmente por mutações no gene OPA1. Descoberta na idade escolar como um distúrbio de desenvolvimento visual bilateral de causa desconhecida. Caracteriza-se por deficiência de visão de cores terciária adquirida (deficiência azul-amarelo). A OCT mostra afinamento da camada de fibras nervosas da retina predominante nos quadrantes temporal e inferior 2). Atualmente não há tratamento eficaz, sendo o cuidado com baixa visão e o aconselhamento genético as principais abordagens.
6-7. Neuropatia Óptica Traumática
Seção intitulada “6-7. Neuropatia Óptica Traumática”Lesão do nervo óptico após trauma contuso na cabeça ou órbita, frequentemente por força indireta dentro do canal óptico. Ocorre perda visual aguda imediatamente após a lesão. A fratura do canal óptico é confirmada por TC com janela óssea. Considera-se o uso de corticosteroides em altas doses ou descompressão do canal óptico, mas as evidências são limitadas para ambos.
6-8. Neuropatia Óptica por Radiação
Seção intitulada “6-8. Neuropatia Óptica por Radiação”Distúrbio isquêmico tardio após radioterapia para tumores de cabeça e pescoço ou órbita. A função visual é perdida por um mecanismo que envolve principalmente dano endotelial vascular. O início ocorre de 3 meses a 9 anos após a irradiação, mais comumente entre 10 e 20 meses, com média de cerca de 18 meses 12). O risco aumenta com dose total >50 Gy ou dose por fração >10 Gy. Geralmente indolor e de mau prognóstico. Não há tratamento estabelecido; os efeitos de corticosteroides sistêmicos, anticoagulantes e oxigenoterapia hiperbárica são limitados 12). A RM mostra realce pelo contraste correspondente ao nervo óptico.
6-9. Outras neuropatias ópticas especiais
Seção intitulada “6-9. Outras neuropatias ópticas especiais”Neuropatia óptica isquêmica posterior (PION) Isquemia do nervo óptico na porção posterior da órbita ou intracanalicular. O exemplo típico é a PION pós-operatória que ocorre após hemorragia maciça, hipotensão, cirurgia da coluna ou cirurgia cardíaca. O exame de fundo de olho é normal (sem alterações papilares) com diminuição abrupta da acuidade visual. O reflexo pupilar à luz é positivo para RAPD. Não há tratamento eficaz estabelecido.
Neurorretinite (neuroretinitis) Síndrome caracterizada por edema do disco óptico e manchas brancas em estrela (star figure) na retina. Causada por Bartonella henselae (doença da arranhadura do gato), sífilis e neurorretinite estrelada idiopática de Leber. As manchas em estrela resultam do acúmulo de líquido edematoso na camada de fibras de Henle na mácula, surgindo semanas após a regressão do edema do disco. Tendência à remissão espontânea, mas infecções requerem tratamento específico para a causa.
Papiloflebite (papillophlebitis) Síndrome que ocorre em adultos jovens a meia-idade, caracterizada por edema de papila unilateral sem comprometimento visual e dilatação e tortuosidade das veias da retina. Observa-se aumento do ponto cego de Mariotte, mas a acuidade visual corrigida é normal. A ressonância magnética orbitária é normal. O prognóstico é bom e não requer tratamento, mas é importante diferenciar de papiledema, neurite óptica e neuropatia óptica isquêmica2).
Neuropatia óptica associada a inibidores de checkpoint imunológico A neuropatia óptica ocorre raramente como evento adverso relacionado ao sistema imunológico (irAE) da imunoterapia contra o câncer (como nivolumabe e pembrolizumabe). É tratada com pulsoterapia com corticosteroides, e a continuidade do tratamento oncológico é discutida com o oncologista.
Tabela resumo de uma linha para neuropatia óptica
Seção intitulada “Tabela resumo de uma linha para neuropatia óptica”| Doença | Lateralidade | Dor | Achado papilar | Campo visual | Pontos-chave |
|---|---|---|---|---|---|
| NAION | um olho | nenhum | vermelhidão e inchaço (inferior) | defeito fascicular horizontal | início ao acordar, disco em risco3) |
| AAION/GCA | um olho → ambos os olhos | nenhum (cefaleia/claudicação mandibular) | edema pálido | variado (grave) | urgentíssimo, VHS/PCR elevados1) |
| Neurite óptica idiopática | Um olho | Presente (50%) | Edema ou normal | Escotoma central | Mulheres jovens, risco de transição para EM 13) |
| Relacionado a NMOSD | Tende a ser bilateral | Sim | Edema ou normal | Variado (grave) | Anticorpo AQP4 positivo, refratário5) |
| Relacionado a MOGAD | Frequentemente bilateral | Presente (cefaleia) | Edema grave | Variado | Anticorpo MOG, perineurite6) |
| Compressiva | Unilateral/bilateral | Ausente | Normal ou atrófica | Variada | RM obrigatória9) |
| Tóxico | Ambos os olhos | Nenhum | Normal → palidez temporal | Escotoma central cego | Anamnese da substância causadora2) |
| Nutricional | Ambos os olhos | Nenhum | Normal → palidez temporal | Escotoma central | Deficiência de B12/cobre |
| LHON | Ambos os olhos (um primeiro) | Nenhum | Vermelhidão/telangiectasias | Escotoma central | Homens jovens, sem extravasamento de fluoresceína14) |
| ADOA | ambos os olhos | nenhum | pálido | escotoma central | idade escolar, discromatopsia azul-amarela2) |
| Traumática | Monocular | Sim (trauma) | Normal | Variado | Confirmar fratura do canal óptico por TC |
| Radiação | Unilateral/bilateral | Nenhum | Normal → atrofia | Variado | Média de 18 meses12) |
7. Princípios do Tratamento
Seção intitulada “7. Princípios do Tratamento”O tratamento da neuropatia óptica depende da causa e difere fundamentalmente para cada tipo de doença. Os princípios comuns são mostrados abaixo.
Situações que Requerem Tratamento de Emergência
Seção intitulada “Situações que Requerem Tratamento de Emergência”- GCA/AAION: Corticosteroides sistêmicos em altas doses (iniciados no mesmo dia). Não aguarde os resultados dos exames 1).
- Compressão aguda: Descompressão cirúrgica (coordenação de emergência com otorrinolaringologia e neurocirurgia). Na aspergilose infiltrativa, interrompa os corticosteroides e mude para antifúngicos 2).
- Traumática: Avaliação da indicação de descompressão do canal óptico.
Tratamento da inflamatória (neurite óptica)
Seção intitulada “Tratamento da inflamatória (neurite óptica)”A terapia com pulsos de esteroides (mPSL 1.000 mg/dia × 3 dias) acelera a velocidade de recuperação na fase aguda 4). O corticosteroide oral isolado não é realizado na neurite óptica idiopática, pois aumenta o risco de recidiva (estudo ONTT) 4). Na fase aguda da NMOSD, realiza-se tratamento escalonado: pulso de esteroide → plasmaférese se resposta insuficiente → imunoterapia preventiva de recidiva 5). A neurite óptica por MOGAD é responsiva a esteroides, mas a redução precoce causa recidiva, sendo necessária redução gradual cuidadosa 6).
Tratamento da isquêmica (NAION)
Seção intitulada “Tratamento da isquêmica (NAION)”Não há terapia eficaz estabelecida para a fase aguda. O manejo dos fatores de risco vasculares (hipertensão, diabetes, hiperlipidemia, apneia do sono) é o principal, e o objetivo do tratamento é a prevenção do início no olho contralateral. Quanto à semaglutida (agonista do receptor GLP-1), há estudos observacionais mostrando associação com NAION, sendo desejável explicação cuidadosa e acompanhamento em pacientes com histórico ou risco 7).
Tratamento da hereditária (LHON)
Seção intitulada “Tratamento da hereditária (LHON)”Idebenona 900 mg/dia é aprovado pela EMA europeia e alcançou CRR de 46% no estudo LEROS (comparado com placebo) 10). A coorte do País de Gales relatou CRR de 86% em 27 meses, indicando bons resultados clínicos 10). A terapia genética (lenadogene nolparvovec) mostrou eficácia no estudo de fase III, e espera-se expansão de indicações no futuro 11). Aconselhamento para cessação do tabagismo (tabagismo é fator de risco) e cuidados adequados para baixa visão são essenciais 14).
Tratamento tóxico e nutricional
Seção intitulada “Tratamento tóxico e nutricional”O básico é interromper a substância causadora ou repor nutrientes deficientes. A intervenção precoce pode restaurar a função visual, mas casos crônicos podem deixar danos irreversíveis. A neuropatia óptica por etambutol é dose-dependente, portanto, exame de função visual basal antes da administração e monitoramento periódico (acuidade visual, visão de cores, campo visual) são indispensáveis.
Tratamento compressivo
Seção intitulada “Tratamento compressivo”O princípio é a remoção cirúrgica da lesão causadora. Na neuropatia óptica tireoidiana, realiza-se descompressão orbitária de emergência ou eletiva. Após progressão da atrofia do nervo óptico, a recuperação visual após remoção cirúrgica é limitada, portanto, diagnóstico e tratamento precoces são importantes.
Resumo do prognóstico
Seção intitulada “Resumo do prognóstico”| Tipo da doença | Prognóstico visual | Possibilidade de recuperação |
|---|---|---|
| Neurite óptica idiopática | Mais de 90% alcançam acuidade visual de 0,5 ou melhor após 1 ano4) | Boa recuperação |
| NAION | 1/3 melhora, 1/3 inalterado, 1/3 piora | Recuperação parcial |
| AAION/GCA | A recuperação do olho afetado é quase impossível | A prevenção no olho contralateral é o objetivo1) |
| Relacionado a NMOSD | Grave. Pelo menos um olho 20/200 ou pior em 60-69%5) | Prevenção de recorrência é importante |
| LHON (mt11778) | A acuidade visual final é frequentemente em torno de 0.01 | Recuperação espontânea apenas parcial14) |
| LHON (mt14484) | Variante com maior taxa de recuperação espontânea | Casos de recuperação relatados14) |
| ADOA | Progressão lenta, geralmente não leva à cegueira grave | Sem inibição da progressão |
| Compressivo | Recuperável com remoção precoce | A chance é antes da progressão da atrofia |
| Tóxico ou nutricional | Recuperável com interrupção precoce ou suplementação | Irreversível em casos crônicos |
| Radiação | Aguda, grave e frequentemente irreversível 12) | Nenhum tratamento estabelecido |
A identificação rápida da doença causadora. Em caso de suspeita de GCA, iniciar corticoides no mesmo dia sem aguardar resultados de exames para prevenir cegueira no olho contralateral 1). Em casos compressivos, a remoção cirúrgica da lesão causadora é a única maneira de preservar a função visual, e o atraso no diagnóstico leva à atrofia óptica irreversível. Em casos inflamatórios (neurite óptica), a pulsoterapia com corticoides acelera a recuperação, mas a estratégia de tratamento adicional varia muito conforme o subtipo. Especialmente em casos anti-AQP4 positivos, apenas corticoides levam a recidivas repetidas, portanto a introdução precoce de terapia imunossupressora preventiva de recidivas é a chave para preservar a função visual 5).
Ambos são semelhantes nos sintomas iniciais de “diminuição da visão indolor aguda a subaguda”, e especialmente na fase aguda da LHON, há edema de papila, tornando-os facilmente confundíveis. O ponto de diferenciação mais importante é a presença ou ausência de extravasamento de fluoresceína da papila na angiografia fluoresceínica de fundo. Na neurite óptica inflamatória, há efeito de contraste e extravasamento de fluoresceína, mas na fase aguda da LHON não há extravasamento14). Além disso, na neurite óptica, dor à movimentação ocular está presente em cerca de 50% dos casos, enquanto a LHON é indolor. O diagnóstico definitivo é possível por teste genético mitocondrial (mt11778, mt14484, mt3460), podendo ser realizado como exame externo14). A administração de esteroides em pacientes com LHON não é apenas ineficaz, mas também atrasa o diagnóstico definitivo, portanto, em homens jovens com diminuição aguda da visão bilateral, é essencial incluir LHON no diagnóstico diferencial.
8. Artigos Relacionados (Neuropatia Óptica)
Seção intitulada “8. Artigos Relacionados (Neuropatia Óptica)”Neuropatia Óptica Isquêmica Anterior Arterítica (AAION)
Neuropatia Óptica Compressiva
Neuropatia Óptica Tóxica
Neuropatia Óptica por Deficiência Nutricional
Neuropatia Óptica Hereditária de Leber (LHON)
Atrofia Óptica Dominante Autossômica (ADOA)
Neuropatia Óptica por Radiação
Doenças e tumores do nervo óptico a serem diferenciados
Seção intitulada “Doenças e tumores do nervo óptico a serem diferenciados”Neurite óptica idiopática
Neurite óptica associada à EM
Neuromielite Óptica (NMOSD)
Doença associada a anticorpos MOG (MOGAD)
Referências
Seção intitulada “Referências”- Piccus R, Hansen MS, Hamann S, et al. An update on the clinical approach to giant cell arteritis. Eye 2023.
- Biousse V, Newman NJ. Diagnosis and clinical features of common optic neuropathies. Lancet Neurol 2016;15:1355–67.
- Salvetat ML, Pellegrini F, Spadea L, et al. Non-Arteritic Anterior Ischemic Optic Neuropathy (NA-AION): A Comprehensive Overview. Vision 2023;7:72.
- Beck RW, Gal RL. The Optic Neuritis Treatment Trial: a report on the visual function at 15 years. Ophthalmology 2008;115:1079–82.
- Wingerchuk DM, Banwell B, Bennett JL, et al. International consensus diagnostic criteria for neuromyelitis optica spectrum disorders. Neurology 2015;85:177–89.
- Jeyakumar N, Lerch M, Dale RC, Ramanathan S. MOG antibody-associated optic neuritis. Eye 2024.
- Hathaway JT, Shah MP, Hathaway DB, et al. Risk of nonarteritic anterior ischemic optic neuropathy in patients prescribed semaglutide. JAMA Ophthalmol. 2024;142:740-741. PMID: 38958939. doi:10.1001/jamaophthalmol.2024.2514.
- Thompson AJ, Banwell BL, Barkhof F, et al. Diagnosis of multiple sclerosis: 2017 revisions of the McDonald criteria. Lancet Neurol 2018;17:162–73.
- Biousse V, Newman NJ. Compressive Optic Neuropathies. J Neuroophthalmol 2015;35 Suppl 1:S67–S74.
- Sanders FWB, Votruba M. Outcomes of idebenone therapy for Leber hereditary optic neuropathy in a cohort of patients from Wales. Eye 2025.
- Newman NJ, et al. Hereditary optic neuropathy: advances in treatment. Eye 2024.
- Danesh-Meyer HV. Radiation-induced optic neuropathy. J Clin Neurosci 2008;15:95–100.
- Toosy AT, Mason DF, Miller DH. Optic neuritis. Lancet Neurol 2014;13:83–99.
- Carelli V, Ross-Cisneros FN, Sadun AA. Mitochondrial dysfunction as a cause of optic neuropathies. Prog Retin Eye Res 2004;23:53–89.
