营养性视神经病变(NON)是一种因B族维生素或铜缺乏导致双眼视神经 受损的疾病。
特征为无痛性、双眼性、对称性亚急性视力 下降和中心暗点 。
现代主要风险因素包括减肥手术后、纯素食、偏食和酒精依赖。
诊断需进行缺乏营养素的血液检查,以及MRI排除压迫性或脱髓鞘性疾病。
早期营养补充有望恢复视 力。慢性病例恢复有限。
减肥手术后的患者需要终身监测维生素和微量元素。
营养性视神经病变(NON)是由营养缺乏引起的双眼性、对称性、进行性视神经 疾病。它属于代谢性神经病变,与中毒性视神经病变 处于同一谱系,但以营养缺乏为病因加以区分。
主要致病营养素是B族维生素(B12、B1、B2、B9)和铜。它们是线粒体氧化磷酸化所必需的辅因子。
历史上,饥荒和战争期间曾报告过集体发病。
斯特拉坎综合征(19世纪80年代) :牙买加甘蔗工人中多发的营养缺乏性神经病变。热带弱视 :在尼日利亚等撒哈拉以南非洲地区有报告。战俘视神经病变 :第二次世界大战期间日本战俘中发生。古巴流行性视神经病变 (1991-1993年) :约5万人患病,是现代最大规模的集体发病事件。坦桑尼亚流行性视神经病变 :类似集体发病已有报告。
现代,减肥手术(BS)后的患者以及限制性饮食或纯素食者成为新的风险群体。BS后患者发生神经系统并发症的比例约为4.6%,其中周围神经病变占52%,韦尼克脑病占9%,夜盲症 占2.8%2) 。
儿童发病也有报道,文献综述25例中88%为男孩,68%合并自闭症。维生素A和B12缺乏是最常见的原因5) 。
Q
营养性视神经病变有多罕见?
A
该病罕见但容易被忽视。历史上在战争和饥荒期间多发。现代在肥胖外科手术后患者和纯素食者中也有新发病例报道,且呈增加趋势。
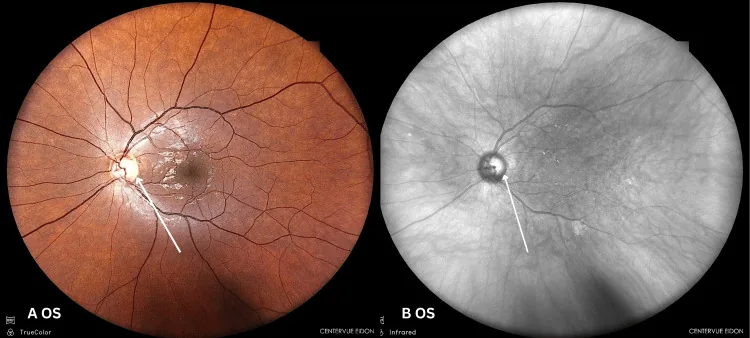
营养性视神经病变的左眼眼底像,显示视盘颞侧苍白。 Nicolaou N, et al. Ethanol and Cyanide: A Case Report on Toxic and Nutritional
Optic Neuropathy Associated With Alcohol and Tobacco. Cureus. 2025. Figure 4. PM
CI D: PMC12712447. License: CC BY.
左眼彩色眼底像和红外眼底像显示视盘轻度颞侧苍白。这显示了营养性视神经病变中视神经 损伤的典型表现。
视力 下降色觉障碍(dyschromatopsia) :早期出现红绿色觉异常 ,表现为红色不如以前鲜艳等主诉。对比敏感度 下降中心暗点 视物模糊 ”,随后进展为进行性视力 下降。
视盘所见 随病程阶段而变化。
早期 :正常或充血 (硫胺素缺乏时可出现视盘水肿 )中期 :视盘颞侧苍白晚期 :弥漫性视盘苍白(视神经萎缩 )
其他表现如下。
RAPD (相对性传入瞳孔 缺陷)对光反射 :通常保留。这是因为参与对光反射的γ细胞得以保存。视野 :中心暗点 或盲点中心暗点 (centrocecal scotoma)。由于乳头黄斑 束选择性受损。VEP OCT 表现RNFL (视网膜神经纤维层 )正常。变薄始于乳头黄斑 束(颞侧),并扩展至所有象限。RNFL 变薄在发病3个月后检测到6) 。而GCL(视网膜神经节细胞 层)可能在RNFL 变化之前出现弥漫性变薄1) 4) 。
Q
OCT正常时是否仍可能患有营养性视神经病变?
A
有可能。由于RNFL 变薄在发病3个月后才被检测到,因此早期即使OCT 正常,也可能出现视功能损害6) 。GCL分析可能在RNFL 变化之前检测到异常1) 4) ,而VEP 有时能更早地发现功能性视路损伤。
B族维生素
维生素B12(钴胺素) :营养性视神经病变的最重要原因。可能伴有恶性贫血、亚急性脊髓联合变性和周围神经病变。
维生素B1(硫胺素) :参与碳水化合物代谢。缺乏会导致脚气病和韦尼克脑病(意识障碍、记忆障碍、眼球运动障碍 )。
维生素B6(吡哆醇) :参与神经递质的生物合成。抗结核药物异烟肼拮抗B6代谢,导致缺乏。
维生素B9(叶酸) :嘌呤和嘧啶合成的辅酶。缺乏会导致巨幼红细胞性贫血和以感觉障碍为主的多发性神经病。
铜
铜 :氧化磷酸化和细胞代谢的辅助因子。导致铜依赖性酶(氧化还原酶、单加氧酶)功能障碍。
胃旁路手术后10-20%的患者会出现神经病变。缺乏症通常在术后3年以上发生,但在合并营养不良的病例中,也有术后18个月发病的报道6) 。
减重手术 :Roux-en-Y胃旁路术、胆胰转流术等。术后1.5-3年发病多见。B1、B6、A缺乏也有术后7个月发病的病例2) 。严格的纯素/素食饮食 :B12、B1、B9缺乏风险高。挑食/回避性限制性食物摄入障碍(ARFID) :儿童的重要风险因素。COVID-19大流行后,正常发育儿童的NON增加5) 。酒精依赖 :非直接原因,但常伴有B12、B9缺乏。炎症性肠病(IBD)/乳糜泻 :导致B12和叶酸吸收不良。恶性贫血 :内因子缺乏导致B12吸收不良。消化道手术史 :Whipple手术、结肠切除术等4) 。不适当的肠外营养 :未补充维生素时,有急性硫胺素缺乏的风险。
均衡饮食是最好的预防措施。
接受过肥胖外科手术的患者,术后需要终身监测和补充维生素及微量元素。请务必定期进行血液检查。
实行纯素食饮食的人必须补充维生素B12。
有偏食习惯的儿童,请咨询家庭医生定期评估营养状况。
Q
肥胖外科手术后多久会发展为视神经病变?
A
一般术后1.5至3年发病较多。铜缺乏通常在3年以上才出现,但合并营养不良的病例中,有术后18个月发病的报道6) 。多种营养素缺乏时,可能更早发病2) 。
斯内伦视力检查
面对面视野检查
石原色觉检查 或Farnsworth D15测试(确认色觉异常 )
阿姆斯勒方格表
视神经 和视网膜 的直接检眼镜检查摆动闪光测试(确认RAPD )
视野检查 (HVF)中心暗点 或盲点中心暗点 。VEP OCT 正常,也能检测到功能损害6) 。OCT (RNFL /GCL分析)RNFL 正常。GCL分析可能在RNFL 变化之前检测到异常,对早期诊断和病程监测有用1) 4) 。视网膜电图 视网膜 疾病。MRI(脑/眼眶 ) :必须用于排除压迫性或脱髓鞘疾病 。
全血细胞计数、外周血涂片、综合代谢面板
血清维生素B12、叶酸
同型半胱氨酸、甲基丙二酸(MMA):当B12低或临界值时加测。MMA仅在B12缺乏时升高,叶酸缺乏时正常,有助于鉴别。
血清铜、铜蓝蛋白
血清硫胺素(B1)、吡哆醇(B6)
与以下疾病的鉴别很重要。
此外,有报道称吸烟与LHON 的发病有关,并且由于两者都具有线粒体功能障碍导致ATP不足的共同机制,因此被认为与NON具有相似性。
Zainuddin等人(2025)引用的Spinazzi诊断标准包括以下三项6) 。
排除其他诊断(炎症性和非炎症性视神经病变 )
生化检测已知可引起视神经病变 的微量营养素缺乏
临床和实验室检查对补充治疗的反应改善
纠正根本的营养素缺乏是治疗的基石。推荐多学科协作(眼科、消化内科、临床心理、营养师、生化)6) 。
口服给药(可逆原因) :每日1000微克,至少持续1个月,之后维持相同剂量。轻度缺乏可减至每日100-500微克。肌内注射(不可逆原因、重症病例) :每日1000微克×1周→每周1000微克×1个月→维持剂量每月1000微克,无限期持续。给药途径可选择口服、鼻内、舌下、皮下和肌内注射。
每日给药1-5毫克。治疗持续3-6个月,直至缺乏原因得到纠正。
韦尼克脑病时给予100-1000毫克。减重手术后缺乏的病例有报道口服100毫克每日三次×3天后改为每日100毫克维持2) 。
口服吡哆醇每日100毫克2) 。服用异烟肼的患者尤其需要补充B6。
使用口服葡萄糖酸铜。Mosenia等人(2024)的报道中,每日两次每次4毫克×1个月后,维持剂量为每日两次每次2毫克4) 。该报道中,6个月时血清铜水平恢复正常,2年后视力 从手动提高到右眼20/25、左眼20/40。
**全肠外营养(TPN)**联合补铜6) 。
如果严重营养缺乏持续存在,胃旁路术后重建正常解剖结构的手术(revision surgery)也是一种选择6) 。
根据手术方式不同,推荐的补充内容也不同。
胃束带术 :继续服用含有叶酸、铁、钙、硫胺素和维生素D的复合维生素。其他减重手术方式 :在上述基础上添加维生素B12和矿物质。
对于中毒性视神经病变 (如乙胺丁醇视神经病变 ),原则是停用致病药物。停用乙胺丁醇后症状仍可能持续进展3个月,因此需口服维生素B12、锌制剂和镁制剂等待恢复。
吸烟对视神经病变 有叠加不良影响,因此应指导戒烟。
同时考虑管理影响血流的基础疾病,如高血压和糖尿病。
如果早期去除病因并开始补充维生素,可预期视力 改善。恢复通常需要半年到两年。然而,在慢性期已进展为视神经萎缩 的病例中,恢复有限或不可逆。
Q
补充维生素能否恢复视力?
A
早期发现和早期治疗可预期良好恢复。在铜缺乏的病例中,有报告在开始补充后两年视力 大幅恢复4) 。另一方面,诊断延迟的慢性病例视力 恢复可能有限3) 。在三个月内开始治疗很可能带来良好结局。
B族维生素和铜对于ATP生成所涉及的线粒体氧化磷酸化至关重要。缺乏这些物质会阻断电子传递链,导致ATP减少,同时自由基(超氧阴离子)积累,氧化应激 增加。
乳头黄斑 束选择性受损的原因被认为是构成该束的小细胞型视网膜神经节细胞 (parvocellular RGC )的线粒体储备有限,凋亡阈值较低4) 6) 。烟草-酒精性视神经病变 的机制类似,p细胞因ATP消耗剧烈而优先受损。
在中毒性和营养性视神经病变中,多个病例报告证实GCL(视网膜神经节细胞 层)先于RNFL (视网膜神经纤维层 )出现弥漫性变薄1) 。RGC 死亡涉及线粒体功能障碍、半胱天冬酶活性(尤其是caspase-7)和神经营养因子缺乏1) 。
在遗传性视神经病变 (ADOA)中,RNFL 和GCL从早期就同时受损,这与NON形成对比1) 。
Sriram等人(2021)报告了5例中毒性和营养性视神经病变,其中RNFL 相对保留,而GCL呈弥漫性变薄1) 。乙胺丁醇对RGC 表现出兴奋性毒性,通过内源性谷氨酸选择性损伤RGC 层。
维生素B9和B12缺乏 :这些维生素作为辅因子参与使用甲酸的嘌呤合成反应。缺乏会导致甲酸积累,抑制电子传递链,抑制线粒体功能,导致ATP耗竭3) 。此外,B12是髓鞘合成的辅因子;缺乏会导致视神经 脱髓鞘和轴突损伤。在酗酒者中,酒精的直接神经毒性与B1和B12缺乏叠加,加剧损伤。
铜缺乏 :导致铜依赖性酶(氧化还原酶、单加氧酶)功能障碍。这会导致神经递质转化障碍、氧化磷酸化障碍和自由基清除障碍复合发生。
多个病例报告证实,即使RNFL 正常,GCL也可能早期变薄1) 4) 。青光眼 领域的数据表明,GCL分析在早期阶段可能比RNFL 更敏感4) 。未来,GCL分析有望常规纳入NON的严重程度评估和病程监测。
Teng等人(2025年)报告了三例发育正常的儿童(13-15岁男孩),因选择性进食(包括ARFID)导致B12缺乏而引发NON5) 。文献综述显示,25例儿童NON中68%合并自闭症,88%为男孩,强调了识别自闭症以外风险因素(创伤性进食经历、多种食物过敏、ARFID)的重要性。
COVID-19大流行后儿童进食障碍增加,发育正常儿童中出现NON的报告作为新课题受到关注。
Mosenia等人(2024年)报告了一例胃肠手术后发生铜缺乏性视神经病变 的病例,补充葡萄糖酸铜后两年,视力 从手动(CF )改善至20/25 OD和20/40 OS4) 。值得注意的是,即使RNFL 正常,也检测到了GCL变薄。
长期未治疗病例恢复有限,因此建议对胃肠手术后患者进行定期铜监测。
Zainuddin等人(2025年)报告了一例胃旁路术后铜缺乏性NON病例,通过全肠外营养、铜补充、多种维生素以及胃旁路重建术恢复正常解剖结构,视力 改善至6/6和N56) 。但中心暗点 在18个月后仍存在。
重建术作为从根本上解决吸收不良的选择受到关注,但患者选择标准和长期结果仍需进一步研究。
Sriram A, Miao Y, Subramanian P, Schultz JS, Zhang C. A differential loss of nerve fiber layer thickness and retinal ganglion cell complex in toxic and nutritional optic neuropathy. Adv Ophthalmol Pract Res. 2021;1:100026.
Khalid MJ, Ayub MA, Kataria S, Hebert M, Parvathaneni A. Concomitant occurrence of peripheral neuropathy and vision loss due to multivitamin deficiency after bariatric surgery. Cureus. 2024;16(5):e59959.
Othman I, Tai E, Kuganasan S, Abu N. Vision loss as a presenting symptom of vitamin B12 deficiency. Cureus. 2024;16(5):e60113.
Mosenia A, Khan S, Aung MH. Visual recovery in a patient with optic neuropathy secondary to copper deficiency. Am J Ophthalmol Case Rep. 2024;36:102197.
Teng RW, Heidary G, Gise RA. Selective diet induced nutritional optic neuropathy in developmentally normal children. Am J Ophthalmol Case Rep. 2025;37:102234.
Zainuddin MZA, Che Hamzah J, Nik Mahmood NRK, Cheng TC, Bastion MLC. Nutritional optic neuropathy: bariatric surgery gone wrong. Cureus. 2025;17(5):e84548.
复制全文后,可以粘贴到你常用的 AI 助手中提问。
打开下面的 AI 助手,并把复制的内容粘贴到聊天框。