營養性視神經病變(NON)是一種因B群維生素或銅缺乏導致雙眼視神經 受損的疾病。
特徵為無痛性、雙眼性、對稱性亞急性視力 下降和中心暗點 。
現代主要風險因素包括減肥手術後、純素食、偏食和酒精依賴。
診斷需進行缺乏營養素的血液檢查,以及MRI排除壓迫性或脫髓鞘性疾病。
早期營養補充有望恢復視力 。慢性病例恢復有限。
減肥手術後的患者需要終身監測維生素和微量元素。
營養性視神經病變(NON)是由營養缺乏引起的雙眼性、對稱性、進行性視神經 疾病。它屬於代謝性神經病變,與中毒性視神經病變 處於同一譜系,但以營養缺乏為病因加以區分。
主要致病營養素是B群維生素(B12、B1、B2、B9)和銅。它們是粒線體氧化磷酸化所必需的輔因子。
歷史上,饑荒和戰爭期間曾報告過集體發病。
斯特拉坎症候群(1880年代) :牙買加甘蔗工人中多發的營養缺乏性神經病變。熱帶弱視 :在奈及利亞等撒哈拉以南非洲地區有報告。戰俘視神經病變 :第二次世界大戰期間日本戰俘中發生。古巴流行性視神經病變 (1991-1993年) :約5萬人患病,是現代最大規模的集體發病事件。坦尚尼亞流行性視神經病變 :類似集體發病已有報告。
現代,減肥手術(BS)後的患者以及限制性飲食或純素食者成為新的風險群體。BS後患者發生神經系統併發症的比例約為4.6%,其中周邊神經病變佔52%,韋尼克腦病佔9%,夜盲症 佔2.8%2) 。
兒童發病也有報告,文獻回顧25例中88%為男童,68%合併自閉症。維生素A和B12缺乏是最常見的原因5) 。
Q
營養性視神經病變有多罕見?
A
罕見但容易被忽略。歷史上在戰爭和饑荒期間多發。現代在減重手術後患者和純素食者中也有新發病例報告,且呈增加趨勢。
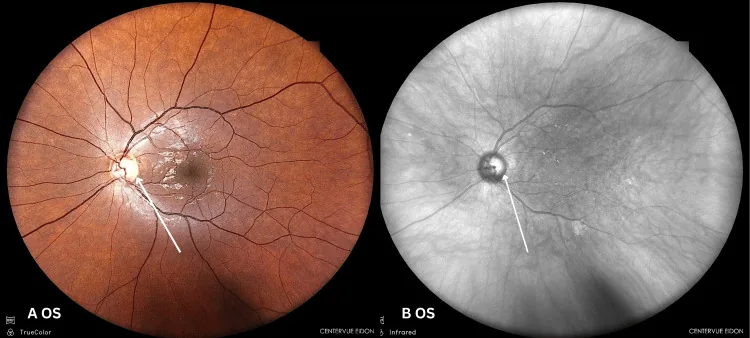
營養性視神經病變的左眼眼底像,顯示視盤顳側蒼白。 Nicolaou N, et al. Ethanol and Cyanide: A Case Report on Toxic and Nutritional
Optic Neuropathy Associated With Alcohol and Tobacco. Cureus. 2025. Figure 4. PM
CI D: PMC12712447. License: CC BY.
左眼彩色眼底像和紅外眼底像顯示視盤輕度顳側蒼白。這顯示了營養性視神經病變中視神經 損傷的典型表現。
視力 下降色覺障礙(dyschromatopsia) :早期出現紅綠色覺異常 ,表現為紅色不如以前鮮豔等主訴。對比敏感度 下降中心暗點 視力 下降。
視盤所見 隨病程階段而變化。
早期 :正常或充血 (硫胺素缺乏時可出現視盤水腫 )中期 :視盤顳側蒼白晚期 :瀰漫性視神經 盤蒼白(視神經萎縮 )
其他發現如下。
RAPD (相對性傳入瞳孔 缺陷)對光反射 :通常保留。這是因為參與對光反射的γ細胞得以保存。視野 :中心暗點 或盲點中心暗點 (centrocecal scotoma)。由於乳頭黃斑 束選擇性受損。VEP OCT 表現RNFL (視網膜神經纖維層 )正常。變薄始於乳頭黃斑 束(顳側),並擴展至所有象限。RNFL 變薄在發病3個月後檢測到6) 。而GCL(視網膜神經節細胞 層)可能在RNFL 變化之前出現瀰漫性變薄1) 4) 。
Q
OCT正常時是否仍可能患有營養性視神經病變?
A
有可能。由於RNFL 變薄在發病3個月後才被檢測到,因此早期即使OCT 正常,也可能出現視功能損害6) 。GCL分析可能在RNFL 變化之前檢測到異常1) 4) ,而VEP 有時能更早地發現功能性視路損傷。
B群維生素
維生素B12(鈷胺素) :營養性視神經病變的最重要原因。可能伴有惡性貧血、亞急性脊髓聯合變性和周邊神經病變。
維生素B1(硫胺素) :參與碳水化合物代謝。缺乏會導致腳氣病和韋尼克腦病(意識障礙、記憶障礙、眼球運動障礙 )。
維生素B6(吡哆醇) :參與神經傳導物質的生合成。抗結核藥物異煙肼拮抗B6代謝,導致缺乏。
維生素B9(葉酸) :嘌呤和嘧啶合成的輔酶。缺乏會導致巨幼紅細胞性貧血和以感覺障礙為主的多發性神經病變。
銅
銅 :氧化磷酸化和細胞代謝的輔助因子。導致銅依賴性酶(氧化還原酶、單加氧酶)功能障礙。
胃繞道手術後10-20%的患者會出現神經病變。缺乏症通常在術後3年以上發生,但在合併營養不良的病例中,也有術後18個月發病的報導6) 。
減重手術 :Roux-en-Y胃繞道術、膽胰分流術等。術後1.5-3年發病多見。B1、B6、A缺乏也有術後7個月發病的病例2) 。嚴格的純素/素食飲食 :B12、B1、B9缺乏風險高。挑食/迴避性限制性食物攝入障礙(ARFID) :兒童的重要風險因素。COVID-19大流行後,正常發育兒童的NON增加5) 。酒精依賴 :非直接原因,但常伴有B12、B9缺乏。炎症性腸病(IBD)/乳糜瀉 :導致B12和葉酸吸收不良。惡性貧血 :內因子缺乏導致B12吸收不良。消化道手術史 :Whipple手術、結腸切除術等4) 。不適當的腸外營養 :未補充維生素時,有急性硫胺素缺乏的風險。
均衡飲食是最好的預防措施。
接受過肥胖外科手術的患者,術後需要終身監測和補充維生素及微量元素。請務必定期進行血液檢查。
實行純素食飲食的人必須補充維生素B12。
有偏食習慣的兒童,請諮詢家庭醫師定期評估營養狀況。
Q
肥胖外科手術後多久會發展為視神經病變?
A
一般術後1.5至3年發病較多。銅缺乏通常在3年以上才出現,但合併營養不良的病例中,有術後18個月發病的報導6) 。多種營養素缺乏時,可能更早發病2) 。
斯內倫視力檢查
面對面視野檢查
石原色覺檢查 或Farnsworth D15測試(確認色覺異常 )
阿姆斯勒方格表
視神經 和視網膜 的直接檢眼鏡檢查擺動閃光測試(確認RAPD )
視野檢查 (HVF)中心暗點 或盲點中心暗點 。VEP OCT 正常,也能檢測到功能障礙6) 。OCT (RNFL /GCL分析)RNFL 正常。GCL分析可能在RNFL 變化之前檢測到異常,對早期診斷和病程監測有用1) 4) 。視網膜電圖 視網膜 疾病。MRI(腦/眼眶 ) :必須用於排除壓迫性或脫髓鞘疾病 。
全血細胞計數、周邊血液抹片、綜合代謝面板
血清維生素B12、葉酸
同型半胱氨酸、甲基丙二酸(MMA):當B12低或邊界值時加測。MMA僅在B12缺乏時升高,葉酸缺乏時正常,有助於鑑別。
血清銅、銅藍蛋白
血清硫胺素(B1)、吡哆醇(B6)
與以下疾病的鑑別很重要。
疾病 主要鑑別點 Leber遺傳性視神經病變 (LHON )母系遺傳、mtDNA突變檢測 體染色體顯性視神經萎縮 (ADOA) 早期即出現RNFL 與GCL同時受損 中毒性視神經病變 乙胺丁醇、甲醇等藥物史 壓迫性視神經病變 透過頭部影像學檢查排除(嚴禁漏診) 視神經炎 眼球運動時有無疼痛是重要的鑑別點 黃斑部 病變透過螢光眼底血管攝影 與局部視網膜電圖 鑑別
此外,有報告指出吸菸與LHON 的發病有關,且因兩者皆具有粒線體功能障礙導致ATP不足的共同機制,因此被認為與NON具有相似性。
Zainuddin等人(2025)引用的Spinazzi診斷標準包含以下三項6) 。
排除其他診斷(發炎性與非發炎性視神經病變 )
生化檢測已知會引起視神經病變 的微量營養素缺乏
臨床與檢驗對補充治療的反應改善
矯正根本的營養素缺乏是治療的基石。建議多專科團隊合作(眼科、腸胃科、臨床心理、營養師、生化)6) 。
口服給藥(可逆原因) :每日1000微克,至少持續1個月,之後維持相同劑量。輕度缺乏可減至每日100-500微克。肌肉注射(不可逆原因、重症病例) :每日1000微克×1週→每週1000微克×1個月→維持劑量每月1000微克,無限期持續。給藥途徑可選擇口服、鼻內、舌下、皮下和肌肉注射。
每日給藥1-5毫克。治療持續3-6個月,直到缺乏原因被矯正。
韋尼克腦病時給予100-1000毫克。減重手術後缺乏的病例有報告口服100毫克每日三次×3天後改為每日100毫克維持2) 。
口服吡哆醇每日100毫克2) 。服用異煙肼的患者尤其需要補充B6。
使用口服葡萄糖酸銅。Mosenia等人(2024)的報告中,每日兩次每次4毫克×1個月後,維持劑量為每日兩次每次2毫克4) 。該報告中,6個月時血清銅水平恢復正常,2年後視力 從手動提高到右眼20/25、左眼20/40。
**全靜脈營養(TPN)**合併銅補充6) 。
如果嚴重營養缺乏持續存在,胃繞道術後重建正常解剖結構的手術(revision surgery)也是一種選擇6) 。
根據手術方式不同,建議的補充內容也不同。
胃束帶術 :持續服用含有葉酸、鐵、鈣、硫胺素和維生素D的綜合維生素。其他減重手術方式 :在上述基礎上添加維生素B12和礦物質。
對於中毒性視神經病變 (如乙胺丁醇視神經病變 ),原則是停用致病藥物。停用乙胺丁醇後症狀仍可能持續進展3個月,因此需口服維生素B12、鋅製劑和鎂製劑等待恢復。
吸菸對視神經病變 有疊加不良影響,因此應指導戒菸。
同時考慮管理影響血流的基礎疾病,如高血壓和糖尿病。
如果早期去除病因並開始補充維生素,可預期視力 改善。恢復通常需要半年到兩年。然而,在慢性期已進展為視神經萎縮 的病例中,恢復有限或不可逆。
Q
補充維生素能否恢復視力?
A
早期發現和早期治療可預期良好恢復。在銅缺乏的病例中,有報告在開始補充後兩年視力 大幅恢復4) 。另一方面,診斷延遲的慢性病例視力 恢復可能有限3) 。在三個月內開始治療很可能帶來良好結局。
B群維生素和銅對於ATP生成所涉及的粒線體氧化磷酸化至關重要。缺乏這些物質會阻斷電子傳遞鏈,導致ATP減少,同時自由基(超氧陰離子)積累,氧化壓力增加。
乳頭黃斑 束選擇性受損的原因被認為是構成該束的小細胞型視網膜神經節細胞 (parvocellular RGC )的粒線體儲備有限,凋亡閾值較低4) 6) 。菸草-酒精性視神經病變 的機轉類似,p細胞因ATP消耗劇烈而優先受損。
在中毒性和營養性視神經病變中,多個病例報告證實GCL(視網膜神經節細胞 層)先於RNFL (視網膜神經纖維層 )出現瀰漫性變薄1) 。RGC 死亡涉及粒線體功能障礙、半胱天冬酶活性(尤其是caspase-7)和神經營養因子缺乏1) 。
在遺傳性視神經病變 (ADOA)中,RNFL 和GCL從早期就同時受損,這與NON形成對比1) 。
Sriram等人(2021)報告了5例中毒性和營養性視神經病變,其中RNFL 相對保留,而GCL呈瀰漫性變薄1) 。乙胺丁醇對RGC 表現出興奮性毒性,通過內源性麩胺酸選擇性損傷RGC 層。
維生素B9和B12缺乏 :這些維生素作為輔因子參與使用甲酸的嘌呤合成反應。缺乏會導致甲酸積累,抑制電子傳遞鏈,抑制粒線體功能,導致ATP耗竭3) 。此外,B12是髓鞘合成的輔因子;缺乏會導致視神經 脫髓鞘和軸突損傷。在酗酒者中,酒精的直接神經毒性與B1和B12缺乏疊加,加劇損傷。
銅缺乏 :導致銅依賴性酶(氧化還原酶、單加氧酶)功能障礙。這會導致神經傳遞物質轉換障礙、氧化磷酸化障礙和自由基清除障礙複合發生。
多個病例報告證實,即使RNFL 正常,GCL也可能早期變薄1) 4) 。青光眼 領域的數據表明,GCL分析在早期階段可能比RNFL 更敏感4) 。未來,GCL分析有望常規納入NON的嚴重程度評估和病程監測。
Teng等人(2025年)報告了三例發育正常的兒童(13-15歲男孩),因選擇性進食(包括ARFID)導致B12缺乏而引發NON5) 。文獻綜述顯示,25例兒童NON中68%合併自閉症,88%為男孩,強調了識別自閉症以外風險因素(創傷性進食經歷、多種食物過敏、ARFID)的重要性。
COVID-19大流行後兒童進食障礙增加,發育正常兒童中出現NON的報告作為新課題受到關注。
Mosenia等人(2024年)報告了一例胃腸手術後發生銅缺乏性視神經病變 的病例,補充葡萄糖酸銅後兩年,視力 從手動(CF )改善至20/25 OD和20/40 OS4) 。值得注意的是,即使RNFL 正常,也檢測到了GCL變薄。
長期未治療病例恢復有限,因此建議對胃腸手術後患者進行定期銅監測。
Zainuddin等人(2025年)報告了一例胃繞道術後銅缺乏性NON病例,通過全腸外營養、銅補充、多種維生素以及胃繞道重建術恢復正常解剖結構,視力 改善至6/6和N56) 。但中心暗點 在18個月後仍存在。
重建術作為從根本上解決吸收不良的選擇受到關注,但患者選擇標準和長期結果仍需進一步研究。
Sriram A, Miao Y, Subramanian P, Schultz JS, Zhang C. A differential loss of nerve fiber layer thickness and retinal ganglion cell complex in toxic and nutritional optic neuropathy. Adv Ophthalmol Pract Res. 2021;1:100026.
Khalid MJ, Ayub MA, Kataria S, Hebert M, Parvathaneni A. Concomitant occurrence of peripheral neuropathy and vision loss due to multivitamin deficiency after bariatric surgery. Cureus. 2024;16(5):e59959.
Othman I, Tai E, Kuganasan S, Abu N. Vision loss as a presenting symptom of vitamin B12 deficiency. Cureus. 2024;16(5):e60113.
Mosenia A, Khan S, Aung MH. Visual recovery in a patient with optic neuropathy secondary to copper deficiency. Am J Ophthalmol Case Rep. 2024;36:102197.
Teng RW, Heidary G, Gise RA. Selective diet induced nutritional optic neuropathy in developmentally normal children. Am J Ophthalmol Case Rep. 2025;37:102234.
Zainuddin MZA, Che Hamzah J, Nik Mahmood NRK, Cheng TC, Bastion MLC. Nutritional optic neuropathy: bariatric surgery gone wrong. Cureus. 2025;17(5):e84548.
開啟下方的 AI 助手,並將複製的內容貼到聊天欄。