โรคเส้นประสาทตาจากโภชนาการ (NON) เป็นโรคที่ทำลายเส้นประสาทตา ทั้งสองข้างเนื่องจากการขาดวิตามินบีหรือทองแดง
มีลักษณะเฉพาะคือการมองเห็น ลดลงแบบกึ่งเฉียบพลัน ไม่เจ็บ ตาทั้งสองข้าง สมมาตร และมีจุดบอดกลาง ภาพ
การผ่าตัดลดน้ำหนัก อาหารมังสวิรัติแบบเคร่งครัด การกินอาหารไม่สมดุล และโรคพิษสุราเรื้อรังเป็นปัจจัยเสี่ยงหลักในยุคปัจจุบัน
การวินิจฉัยต้องตรวจเลือดหาภาวะขาดสารอาหาร และการตรวจ MRI เพื่อแยกโรคกดทับและโรคทำลายปลอกไมอีลิน
สามารถคาดหวังการฟื้นตัวของการมองเห็น ได้หากให้สารอาหารทดแทนตั้งแต่เนิ่นๆ ในกรณีเรื้อรัง การฟื้นตัวมีจำกัด
ผู้ป่วยหลังผ่าตัดลดน้ำหนักจำเป็นต้องได้รับการติดตามระดับวิตามินและธาตุอาหารตลอดชีวิต
โรคเส้นประสาทตาจากโภชนาการ (Nutritional Optic Neuropathy ; NON) เป็นความผิดปกติของเส้นประสาทตา ที่เป็นทั้งสองข้าง สมมาตร และดำเนินไปเรื่อยๆ ซึ่งเกิดจากการขาดสารอาหาร จัดอยู่ในกลุ่มโรคเส้นประสาทจากเมตาบอลิก และอยู่ในสเปกตรัมเดียวกับโรคเส้นประสาทตา จากสารพิษ แต่แตกต่างกันที่สาเหตุมาจากการขาดสารอาหาร
สารอาหารหลักที่ทำให้เกิดโรคคือวิตามินบีรวม (บี12, บี1, บี2, บี9) และทองแดง สารเหล่านี้เป็นโคแฟกเตอร์ที่จำเป็นสำหรับกระบวนการออกซิเดทีฟฟอสโฟรีเลชันในไมโตคอนเดรีย
ในอดีต มีรายงานการระบาดเป็นกลุ่มในช่วงที่เกิดความอดอยากและสงคราม
กลุ่มอาการสตราแชน (คริสต์ทศวรรษ 1880) : โรคเส้นประสาทจากการขาดสารอาหารที่พบบ่อยในคนงานอ้อยในจาเมกาตามัวในเขตร้อน : มีรายงานในไนจีเรียและแอฟริกาใต้สะฮาราโรคเส้นประสาทตา ในเชลยศึกโรคเส้นประสาทตา ระบาดในคิวบา (ค.ศ. 1991-1993)โรคเส้นประสาทตา ระบาดในแทนซาเนีย
ในยุคปัจจุบัน ผู้ป่วยหลังการผ่าตัดลดน้ำหนัก (Bariatric surgery; BS) และผู้ที่รับประทานอาหารแบบจำกัดหรือมังสวิรัติเคร่งครัดกลายเป็นกลุ่มเสี่ยงใหม่ ผู้ป่วยหลัง BS ประมาณ 4.6% เกิดภาวะแทรกซ้อนทางระบบประสาท โดยแบ่งเป็น: โรคเส้นประสาทส่วนปลาย 52%, โรคสมองเวอร์นิคเคอ 9%, ตาบอดกลางคืน 2.8% 2)
มีการรายงานการเกิดในเด็กเช่นกัน โดย 88% ของ 25 รายในการทบทวนวรรณกรรมเป็นเพศชาย และ 68% มีภาวะออทิซึม การขาดวิตามินเอและบี12 เป็นสาเหตุที่พบบ่อยที่สุด 5)
Q
โรคเส้นประสาทตาจากโภชนาการพบได้น้อยเพียงใด?
A
เป็นโรคที่พบได้ยากแต่มักถูกมองข้าม ในอดีตพบได้บ่อยในช่วงสงครามและภาวะอดอยาก ในยุคปัจจุบัน มีรายงานผู้ป่วยรายใหม่ในผู้ป่วยหลังผ่าตัดลดน้ำหนักและผู้ที่รับประทานอาหารมังสวิรัติ และมีแนวโน้มเพิ่มขึ้น
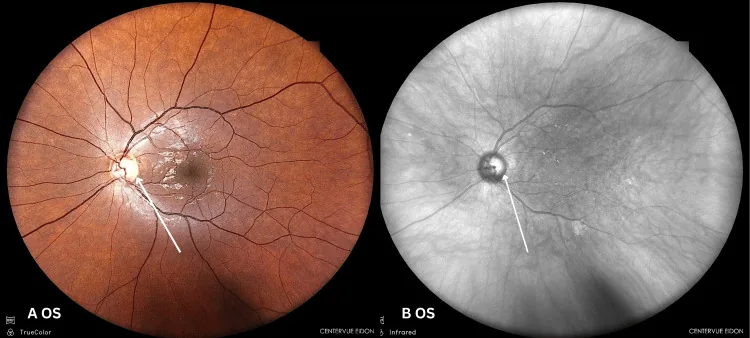
ภาพถ่ายจอประสาทตาข้างซ้ายของโรคเส้นประสาทตาจากโภชนาการ แสดงให้เห็นหัวประสาทตาซีดด้านขมับ Nicolaou N, et al. Ethanol and Cyanide: A Case Report on Toxic and Nutritional
Optic Neuropathy Associated With Alcohol and Tobacco. Cureus. 2025. Figure 4. PM
CI D: PMC12712447. License: CC BY.
ภาพถ่ายจอประสาทตา สีและอินฟราเรดของตาซ้าย แสดงให้เห็นหัวประสาทตาซีดเล็กน้อยด้านขมับ แสดงผลการตรวจที่พบโดยทั่วไปในโรคเส้นประสาทตาจากโภชนาการ
การมองเห็น ลดลงความผิดปกติของการมองเห็นสี (dyschromatopsia)ความผิดปกติของการมองเห็นสี แดง-เขียวปรากฏเร็ว โดยผู้ป่วยบ่นว่าสีแดงดูไม่สดใสเหมือนเดิมความไวต่อความแตกต่าง ลดลงจุดบอดกลาง (central scotoma)การมองเห็น ลดลงแบบค่อยเป็นค่อยไป
ผลการตรวจหัวประสาทตา เปลี่ยนแปลงตามระยะของโรค
ระยะแรก : ปกติ หรือมีเลือดคั่ง (ในภาวะขาดไทอามีนอาจเกิด papilledema)ระยะกลาง : หัวประสาทตาซีดด้านขมับ (temporal pallor)ระยะปลาย : จานประสาทตา ซีดกระจาย (ฝ่อของเส้นประสาทตา )
ผลการตรวจอื่น ๆ มีดังนี้:
RAPD (ความบกพร่องของรูม่านตา ทางนำเข้าสัมพัทธ์)ปฏิกิริยารูม่านตา ต่อแสง : มักคงอยู่ เนื่องจากเซลล์ γ ที่เกี่ยวข้องกับปฏิกิริยาต่อแสงยังคงอยู่ลานสายตา : จุดบอดกลาง หรือ จุดบอดกลาง -จุดบอด (centrocecal scotoma) เนื่องจากการทำลายแบบเลือกสรรของมัดประสาทตาจุดรับภาพVEP ผล OCT : ระยะแรก RNFL (ชั้นใยประสาทจอตา) ปกติ การบางเริ่มจากมัดประสาทตาจุดรับภาพ (ด้านขมับ) และขยายไปทุก quadrant ตรวจพบการบางของ RNFL หลังจากเริ่มมีอาการ 3 เดือน6) ในทางกลับกัน GCL (ชั้นเซลล์ปมประสาทจอตา) อาจแสดงการบางแบบกระจายก่อนการเปลี่ยนแปลงของ RNFL 1) 4)
Q
เป็นไปได้หรือไม่ที่จะมีภาวะเส้นประสาทตาเสื่อมจากโภชนาการแม้ OCT ปกติ?
A
ได้ เนื่องจากการบางของ RNFL ตรวจพบหลังจากเริ่มมีอาการ 3 เดือน ดังนั้นอาจมีความผิดปกติทางการมองเห็น แม้ OCT ปกติในระยะแรก6) การวิเคราะห์ GCL อาจตรวจพบความผิดปกติก่อน RNFL 1) 4) และ VEP อาจจับความผิดปกติทางการทำงานของทางเดินประสาทตาได้เร็วกว่า
วิตามินบี
วิตามินบี12 (โคบาลามิน) : สาเหตุที่สำคัญที่สุดของภาวะเส้นประสาทตา เสื่อมจากโภชนาการ อาจร่วมกับภาวะโลหิตจางชนิดเพอร์นิเชียส ไขสันหลังเสื่อมแบบกึ่งเฉียบพลันร่วม และปลายประสาทอักเสบ
วิตามินบี1 (ไทอามิน) : เกี่ยวข้องกับเมแทบอลิซึมของคาร์โบไฮเดรต การขาดทำให้เกิดโรคเหน็บชา โรคสมองเวอร์นิกเก (ความผิดปกติของสติ ความจำ การเคลื่อนไหวของลูกตา)
วิตามินบี6 (ไพริดอกซิน) : เกี่ยวข้องกับการสังเคราะห์สารสื่อประสาท ยาไอโซไนอะซิดที่ใช้วัณโรคต้านเมแทบอลิซึมของบี6 ทำให้เกิดการขาด
วิตามิน B9 (กรดโฟลิก) : โคเอนไซม์ในการสังเคราะห์พิวรีนและไพริมิดีน การขาดทำให้เกิดเมกะโลบลาสโตซิสและโรคปลายประสาทอักเสบหลายเส้นที่มีความผิดปกติทางประสาทสัมผัสเด่นชัด
ทองแดง
ทองแดง (Copper) : โคแฟกเตอร์ในกระบวนการออกซิเดทีฟฟอสโฟรีเลชันและเมแทบอลิซึมของเซลล์ ทำให้เกิดความผิดปกติของเอนไซม์ที่ขึ้นกับทองแดง (ออกซิโดรีดักเทส, โมโนออกซิเจเนส)
เป็นสาเหตุของอาการทางระบบประสาทในผู้ป่วย 10-20% หลังการผ่าตัดบายพาสกระเพาะอาหาร การขาดมักเกิดขึ้น ≥3 ปีหลังผ่าตัด แต่ในกรณีที่มีภาวะทุพโภชนาการร่วม อาจเกิดขึ้นภายใน 18 เดือนหลังผ่าตัด 6)
การผ่าตัดลดน้ำหนัก (Bariatric surgery) : เช่น Roux-en-Y gastric bypass และ biliopancreatic diversion การขาดมักเกิดขึ้น 1.5-3 ปีหลังผ่าตัด การขาด B1, B6, A ก็มีรายงานภายใน 7 เดือนหลังผ่าตัด 2) การรับประทานอาหารมังสวิรัติ/เจอย่างเคร่งครัด : มีความเสี่ยงสูงต่อการขาด B12, B1, B9การกินเลือกมากและ ARFID (Avoidant/Restrictive Food Intake Disorder) : ปัจจัยเสี่ยงสำคัญในเด็ก หลังการระบาดของ COVID-19, NON ในเด็กที่มีพัฒนาการปกติเพิ่มขึ้น 5) โรคพิษสุราเรื้อรัง : ไม่ใช่สาเหตุโดยตรง แต่มักพบร่วมกับการขาด B12 และ B9โรคลำไส้อักเสบ (IBD) และโรคซีลิแอค : ทำให้การดูดซึม B12 และโฟเลตผิดปกติโรคโลหิตจางเพอร์นิเชียส (Pernicious anemia) : การขาด intrinsic factor ทำให้ดูดซึม B12 ไม่ดีประวัติการผ่าตัดระบบทางเดินอาหาร : เช่น การผ่าตัด Whipple, การตัดลำไส้ใหญ่ 4) การให้สารอาหารทางหลอดเลือดดำที่ไม่เหมาะสม : หากไม่เสริมวิตามิน มีความเสี่ยงต่อการขาดไทอามีนเฉียบพลัน
Q
หลังการผ่าตัดลดน้ำหนัก โรคเส้นประสาทตาอักเสบจะเกิดขึ้นภายในระยะเวลาเท่าใด?
A
โดยทั่วไป อาการจะเกิดขึ้นภายใน 1.5 ถึง 3 ปีหลังการผ่าตัด การขาดทองแดงมักเกิดขึ้นหลังจาก 3 ปีขึ้นไป แต่มีรายงานผู้ป่วยที่มีภาวะทุพโภชนาการร่วมด้วยเกิดอาการหลังผ่าตัด 18 เดือน 6) ในกรณีที่ขาดสารอาหารหลายชนิด อาการอาจเกิดขึ้นเร็วขึ้น 2)
การตรวจวัดสายตา ด้วยแผนภูมิสนีเลนการตรวจลานสายตา แบบเผชิญหน้าการทดสอบการมองเห็นสี แบบอิชิฮาระหรือการทดสอบ Farnsworth D15 (เพื่อยืนยันความผิดปกติของการมองเห็นสี )ตารางอัมสเลอร์
การตรวจจอประสาทตา และเส้นประสาทตา โดยตรงด้วยกล้องตรวจตา
การทดสอบไฟฉายสวิง (เพื่อยืนยันความบกพร่องของรูม่านตา ชนิดรับแสงสัมพัทธ์)
การตรวจลานสายตา (HVF)จุดบอดกลาง หรือจุดบอดกลาง ตาบอดVEP OCT ปกติ6) .OCT (การวิเคราะห์ RNFL และ GCL)RNFL ปกติในระยะแรก การวิเคราะห์ GCL อาจตรวจพบความผิดปกติก่อนการเปลี่ยนแปลงของ RNFL มีประโยชน์สำหรับการวินิจฉัย早期และการติดตาม1) 4) .คลื่นไฟฟ้าจอตา : ใช้เพื่อแยกโรคจอประสาทตา MRI (สมองและเบ้าตา ) : จำเป็นเพื่อแยกโรคกดทับและโรคทำลายปลอกไมอีลิน
การนับเม็ดเลือดสมบูรณ์, การย้อมเลือด peripheral, แผงเมตาบอลิกสมบูรณ์
วิตามินบี 12 และโฟเลตในซีรัม
โฮโมซิสเทอีนและกรดเมทิลมาโลนิก (MMA): เพิ่มเมื่อ B12 ต่ำหรือ borderline MMA เพิ่มขึ้นเฉพาะในการขาด B12 และปกติในการขาดโฟเลต มีประโยชน์ในการแยกโรค
ทองแดงและเซรูโลพลาสมินในซีรัม
ไทอามีน (B1) และไพริดอกซิน (B6) ในซีรัม
สิ่งสำคัญคือต้องแยกโรคต่อไปนี้:
โรค จุดแยกโรคหลัก โรคเส้นประสาทตา ทางพันธุกรรม Leber (LHON )ถ่ายทอดทางมารดา, ค้นหาการกลายพันธุ์ mtDNA ภาวะฝ่อของเส้นประสาทตา ชนิดถ่ายทอดทางพันธุกรรมแบบเด่น (ADOA) ความเสียหายพร้อมกันของ RNFL และ GCL ตั้งแต่ระยะแรก โรคเส้นประสาทตา จากสารพิษประวัติการใช้ยา เช่น ethambutol หรือ methanol โรคเส้นประสาทตา จากการกดทับแยกออกโดยการถ่ายภาพศีรษะ (ห้ามพลาดเด็ดขาด) เส้นประสาทตา อักเสบการมีอาการปวดเมื่อขยับลูกตาเป็นจุดแยกที่สำคัญ โรคจุดรับภาพ แยกโดยการตรวจหลอดเลือดด้วยฟลูออเรสซีน และการตรวจคลื่นไฟฟ้าจอประสาทตา เฉพาะที่
ทั้งนี้ มีรายงานว่าการสูบบุหรี่เกี่ยวข้องกับการเกิด LHON และมีความคล้ายคลึงกับ NON ในกลไกร่วมของความผิดปกติของไมโตคอนเดรียจากการขาด ATP
เกณฑ์การวินิจฉัยของ Spinazzi ที่ Zainuddin และคณะ (2025) อ้างถึงประกอบด้วย 3 ข้อต่อไปนี้ 6)
การแยกการวินิจฉัยอื่น (โรคเส้นประสาทตา อักเสบและไม่อักเสบ)
การตรวจพบทางชีวเคมีของการขาดสารอาหารรองที่ทราบว่าทำให้เกิดโรคเส้นประสาทตา
การตอบสนองทางคลินิกและทางห้องปฏิบัติการที่ดีขึ้นต่อการรักษาด้วยการเสริม
การแก้ไขภาวะขาดสารอาหารที่เป็นสาเหตุเป็นหลักสำคัญของการรักษา แนะนำให้ใช้แนวทางสหสาขาวิชาชีพ (จักษุวิทยา, อายุรศาสตร์ระบบทางเดินอาหาร, จิตวิทยาคลินิก, นักโภชนาการ, ชีวเคมี) 6)
การรับประทาน (สาเหตุที่สามารถแก้ไขได้) : 1,000 ไมโครกรัม/วัน อย่างน้อย 1 เดือน จากนั้นคงขนาดเดิม ในภาวะขาดเล็กน้อย อาจลดลงเหลือ 100-500 ไมโครกรัม/วันการฉีดเข้ากล้าม (สาเหตุที่ไม่สามารถแก้ไขได้/กรณีรุนแรง) : 1,000 ไมโครกรัม/วัน × 1 สัปดาห์ → 1,000 ไมโครกรัม/สัปดาห์ × 1 เดือน → ขนาดคงที่ 1,000 ไมโครกรัม/เดือน อย่างไม่มีกำหนดสามารถเลือกช่องทางการให้ยาได้แก่ ทางปาก, ทางจมูก, ใต้ลิ้น, ใต้ผิวหนัง, หรือฉีดเข้ากล้าม
ให้ 1-5 มก./วัน การรักษาจะดำเนินต่อไป 3-6 เดือนจนกว่าสาเหตุของการขาดจะได้รับการแก้ไข
ในโรคสมองจากเวอร์นิคเคอ ให้ 100-1,000 มก. ในกรณีขาดหลังการผ่าตัดลดน้ำหนัก มีรายงานให้รับประทาน 100 มก. 3 ครั้ง/วัน × 3 วัน แล้วต่อด้วย 100 มก./วัน 2)
ให้ไพริดอกซินชนิดรับประทาน 100 มก./วัน 2) การเสริมบี6 มีความสำคัญเป็นพิเศษในผู้ป่วยที่รับประทานไอโซไนอะซิด
ใช้ทองแดงกลูโคเนตชนิดรับประทาน ในรายงานของ Mosenia และคณะ (2024) ให้ 4 มก. × 2 ครั้ง/วัน × 1 เดือน ตามด้วยขนาดคงที่ 2 มก. × 2 ครั้ง/วัน 4) ในรายงานเดียวกัน ระดับทองแดงในซีรัมกลับสู่ปกติหลังจาก 6 เดือน และการมองเห็น ดีขึ้นหลังจาก 2 ปีจากนับนิ้วมือเป็น 20/25 ตาขวา และ 20/40 ตาซ้าย
การให้สารอาหารทางหลอดเลือดดำทั้งหมด (TPN) ร่วมกับการเสริมทองแดง6) .หากภาวะขาดสารอาหารรุนแรงยังคงอยู่ การผ่าตัดสร้างกระเพาะอาหารกลับสู่สภาพปกติ (revision surgery) ก็เป็นทางเลือกหนึ่ง6) .
อาหารเสริมที่แนะนำแตกต่างกันไปตามประเภทของการผ่าตัด
การรัดกระเพาะอาหาร : รับประทานวิตามินรวมที่มีกรดโฟลิก เหล็ก แคลเซียม ไทอามีน และวิตามินดีต่อไปวิธีการผ่าตัด BS อื่นๆ : เพิ่มวิตามินบี 12 และแร่ธาตุในสูตรข้างต้น
ในโรคเส้นประสาทตา อักเสบจากพิษ (เช่น โรคเส้นประสาทตา จากเอแทมบูทอล) หลักการคือหยุดยาที่เป็นสาเหตุ อาการอาจดำเนินต่อไปได้นานถึง 3 เดือนหลังจากหยุดเอแทมบูทอล ดังนั้นให้รอการฟื้นตัวด้วยวิตามินบี 12 ชนิดรับประทาน สังกะสี และแมกนีเซียม
การสูบบุหรี่มีผลเสียเพิ่มเติมต่อโรคเส้นประสาทตา ดังนั้นควรแนะนำให้เลิกสูบบุหรี่
ควรพิจารณาการจัดการโรคพื้นฐานที่ส่งผลต่อการไหลเวียนเลือด เช่น ความดันโลหิตสูงและเบาหวาน
หากกำจัดสาเหตุได้เร็วและเริ่มเสริมวิตามิน คาดว่าการมองเห็น จะดีขึ้น การฟื้นตัวมักใช้เวลาหกเดือนถึงสองปี อย่างไรก็ตาม ในกรณีเรื้อรังที่ลุกลามและมีฝ่อของเส้นประสาตาอย่างถาวร การฟื้นตัวจะจำกัดหรือไม่สามารถกลับคืนได้
Q
การเสริมวิตามินช่วยให้การมองเห็นดีขึ้นหรือไม่?
A
หากตรวจพบและรักษาตั้งแต่เนิ่นๆ คาดว่าการฟื้นตัวจะดี ในกรณีที่ขาดทองแดง มีรายงานการมองเห็น ดีขึ้นอย่างมีนัยสำคัญสองปีหลังจากเริ่มเสริม4) ในทางกลับกัน ในกรณีเรื้อรังที่วินิจฉัยช้า การมองเห็น อาจดีขึ้นอย่างจำกัด3) การเริ่มรักษาภายใน 3 เดือนมีแนวโน้มที่จะนำไปสู่ผลลัพธ์ที่ดี
วิตามินบีรวมและทองแดงมีความจำเป็นต่อกระบวนการออกซิเดทีฟฟอสโฟรีเลชันในไมโทคอนเดรียซึ่งผลิต ATP การขาดสารเหล่านี้จะขัดขวางห่วงโซ่การขนส่งอิเล็กตรอน ทำให้ ATP ลดลงและสะสมอนุมูลอิสระ (ซูเปอร์ออกไซด์แอนไอออน) เพิ่มภาวะเครียดออกซิเดชัน
การทำลายแบบเลือกสรรของมัดประสาทตาจุดรับภาพเกิดจากเซลล์ปมประสาทจอประสาทตา ชนิดพาร์โว (parvocellular RGC ) ซึ่งประกอบเป็นมัดนี้มีปริมาณสำรองไมโทคอนเดรียจำกัดและมีเกณฑ์การตายแบบอะพอพโทซิส ต่ำ 4) 6) กลไกของโรคเส้นประสาทตา จากบุหรี่และแอลกอฮอล์ก็คล้ายกัน โดยเซลล์ p ใช้ ATP สูงจึงเสียหายได้ง่ายกว่า
ในโรคเส้นประสาทตาจากพิษ และโภชนาการ พบว่าชั้นเซลล์ปมประสาท (GCL) บางลงแบบกระจายก่อนชั้นใยประสาทจอตา (RNFL ) ซึ่งได้รับการยืนยันในรายงานผู้ป่วยหลายราย 1) การตายของเซลล์ปมประสาทจอตา (RGC ) เกี่ยวข้องกับความผิดปกติของไมโทคอนเดรีย การทำงานของแคสเปส (โดยเฉพาะแคสเปส-7) และการขาดนิวโรโทรฟิน 1)
ในโรคเส้นประสาทตา ทางพันธุกรรม (ADOA) RNFL และ GCL จะถูกทำลายพร้อมกันตั้งแต่แรกเริ่ม ซึ่งเป็นข้อแตกต่างจากโรคเส้นประสาทตาจากโภชนาการ 1)
Sriram และคณะ (2021) รายงานผู้ป่วยโรคเส้นประสาทตาจากพิษ และโภชนาการ 5 ราย ซึ่ง RNFL ค่อนข้างคงอยู่ ในขณะที่ GCL บางลงแบบกระจาย 1) นอกจากนี้ยังพบว่า ethambutol แสดงความเป็นพิษต่อเซลล์แบบกระตุ้น (excitotoxicity) ต่อ RGC โดยทำลายชั้น RGC แบบเลือกสรรผ่านกลูตาเมตภายในร่างกาย
การขาดวิตามินบี9 และบี12 : ทำหน้าที่เป็นโคแฟกเตอร์ในปฏิกิริยาที่ใช้กรดฟอร์มิกในการสังเคราะห์พิวรีน การขาดจะทำให้กรดฟอร์มิกสะสม ยับยั้งห่วงโซ่การขนส่งอิเล็กตรอน กดการทำงานของไมโทคอนเดรีย และนำไปสู่การพร่อง ATP 3) นอกจากนี้ บี12 ยังเป็นโคแฟกเตอร์ในการสังเคราะห์ไมอีลิน การขาดทำให้เกิดการสูญเสียไมอีลินและความเสียหายของแอกซอนในเส้นประสาทตา ในผู้ดื่มแอลกอฮอล์หนัก ความเป็นพิษต่อเส้นประสาทโดยตรงของแอลกอฮอล์และการขาดบี1 และบี12 จะซ้อนทับกัน ทำให้ความเสียหายรุนแรงขึ้น
การขาดทองแดง : ทำให้เกิดความผิดปกติของเอนไซม์ที่ขึ้นกับทองแดง (ออกซิโดรีดักเตส, โมโนออกซิเจเนส) เกิดการรวมกันของความผิดปกติในการเปลี่ยนสารสื่อประสาท การบกพร่องของออกซิเดทีฟฟอสโฟรีเลชัน และการบกพร่องในการกำจัดอนุมูลอิสระ
รายงานผู้ป่วยหลายรายแสดงให้เห็นว่า GCL อาจบางลงในระยะแรกแม้ว่า RNFL จะปกติ 1) 4) ข้อมูลจากสาขาต้อหิน ชี้ให้เห็นว่าการวิเคราะห์ GCL อาจมีความไวมากกว่า RNFL ในระยะแรก 4) ในอนาคต คาดว่าการวิเคราะห์ GCL จะถูกนำมาใช้เป็นมาตรฐานในการประเมินความรุนแรงและการติดตามการดำเนินโรคของ NON
Teng และคณะ (2025) รายงานเด็กชาย 3 ราย (อายุ 13-15 ปี) ที่มีพัฒนาการปกติซึ่งเกิด NON จากการขาดวิตามินบี 12 เนื่องจากการกินแบบเลือก (รวมถึง ARFID) 5) การทบทวนวรรณกรรมพบว่า 68% ของ 25 ราย NON ในเด็กมีภาวะออทิซึมร่วมด้วย 88% เป็นเพศชาย และเน้นย้ำถึงความสำคัญของการตระหนักถึงปัจจัยเสี่ยงอื่นนอกเหนือจากออทิซึม (ประสบการณ์การกินที่กระทบกระเทือนจิตใจ การแพ้อาหารหลายชนิด ARFID)
หลังการระบาดของ COVID-19 ความผิดปกติทางการกินในเด็กเพิ่มขึ้น และรายงาน NON ในเด็กที่มีพัฒนาการปกติกลายเป็นประเด็นใหม่ที่ต้องให้ความสนใจ
Mosenia และคณะ (2024) รายงานผู้ป่วย 1 รายที่เป็นโรคเส้นประสาทตา จากการขาดทองแดงหลังการผ่าตัดระบบทางเดินอาหาร ซึ่งได้รับการเสริมทองแดงกลูโคเนต และการมองเห็น ดีขึ้นหลังจาก 2 ปีจาก hand motion (CF ) เป็น 20/25 OD และ 20/40 OS 4) นอกจากนี้ยังน่าสังเกตว่าตรวจพบการบางของ GCL แม้ว่า RNFL จะปกติ
เนื่องจากการฟื้นตัวมีจำกัดในกรณีที่ไม่ได้รับการรักษาเป็นเวลานาน จึงจำเป็นต้องเผยแพร่การติดตามระดับทองแดงอย่างสม่ำเสมอในผู้ป่วยหลังการผ่าตัดระบบทางเดินอาหาร
Zainuddin และคณะ (2025) รายงานผู้ป่วย NON จากการขาดทองแดงหลังบายพาสกระเพาะอาหาร ซึ่งได้รับการผ่าตัดสร้างบายพาสกระเพาะอาหารกลับสู่กายวิภาคปกติร่วมกับการให้สารอาหารทางหลอดเลือดดำ การเสริมทองแดง และวิตามินรวม และการมองเห็น ดีขึ้นเป็น 6/6 และ N5 6) อย่างไรก็ตาม จุดบอดกลาง ยังคงอยู่หลังจาก 18 เดือน
การผ่าตัดสร้างใหม่เป็นทางเลือกในการแก้ปัญหาการดูดซึมผิดปกติอย่างถาวร แต่เกณฑ์การคัดเลือกผู้ป่วยและการศึกษาผลลัพธ์ระยะยาวเป็นความท้าทายในอนาคต
Sriram A, Miao Y, Subramanian P, Schultz JS, Zhang C. A differential loss of nerve fiber layer thickness and retinal ganglion cell complex in toxic and nutritional optic neuropathy. Adv Ophthalmol Pract Res. 2021;1:100026.
Khalid MJ, Ayub MA, Kataria S, Hebert M, Parvathaneni A. Concomitant occurrence of peripheral neuropathy and vision loss due to multivitamin deficiency after bariatric surgery. Cureus. 2024;16(5):e59959.
Othman I, Tai E, Kuganasan S, Abu N. Vision loss as a presenting symptom of vitamin B12 deficiency. Cureus. 2024;16(5):e60113.
Mosenia A, Khan S, Aung MH. Visual recovery in a patient with optic neuropathy secondary to copper deficiency. Am J Ophthalmol Case Rep. 2024;36:102197.
Teng RW, Heidary G, Gise RA. Selective diet induced nutritional optic neuropathy in developmentally normal children. Am J Ophthalmol Case Rep. 2025;37:102234.
Zainuddin MZA, Che Hamzah J, Nik Mahmood NRK, Cheng TC, Bastion MLC. Nutritional optic neuropathy: bariatric surgery gone wrong. Cureus. 2025;17(5):e84548.