กลุ่มอาการจุดขาว (white dot syndromes) เป็นแนวคิดที่ Gass ตั้งขึ้นในปี 1977 หมายถึงกลุ่มโรคอักเสบที่มีลักษณะเป็นจุดสีขาวหรือขาวเหลืองหลายจุดในจอตา คำจำกัดความของโรคที่รวมอยู่แตกต่างกันไปในแต่ละนักวิจัย แต่ปัจจุบันใช้กันอย่างแพร่หลายเพื่อหมายถึงกลุ่มโรคอักเสบไม่ติดเชื้อที่ไม่ทราบสาเหตุซึ่งส่วนใหญ่ส่งผลต่อจอตาชั้นนอก เยื่อบุผิวรับแสง เส้นเลือดฝอยคอรอยด์ และคอรอยด์ 1)
ในแนวทางปฏิบัติทางคลินิกสำหรับม่านตาอักเสบ (วารสารสมาคมจักษุแพทย์ญี่ปุ่น 2019;123(6):635-696) โรค APMPPE , MEWDS , PIC , คอรอยด์ อักเสบหลายจุด, จอตาคอรอยด์ อักเสบแบบ Birdshot, คอรอยด์ อักเสบแบบเซอร์พิจิเนียส และ AZOOR ถูกระบุเป็นโรคอิสระในการจำแนกม่านตาอักเสบ ส่วนหลัง และคำว่า “กลุ่มอาการจุดขาว” ใช้เป็นแนวคิดที่ครอบคลุมโรคเหล่านี้ 2)
ด้วยความก้าวหน้าล่าสุดในการถ่ายภาพหลายรูปแบบ (รวมถึง OCT -A) กลุ่มอาการจุดขาวจึงถูกจำแนกออกเป็นสามกลุ่มตาม ชั้นหลักของรอยโรค 1) .
ชนิดที่จอประสาทตาชั้นนอกเป็นหลัก
MEWDS · AZOOR
ตำแหน่งหลักคือการทำลายชั่วคราวของโซน ellipsoid (รอยต่อระหว่างส่วนในและส่วนนอกของเซลล์รับแสง )
เส้นเลือดฝอยคอรอยด์ โดยหลักการแล้วยังคงอยู่ (ไม่มีหรือมี flow void เล็กน้อยใน OCT -A)
สามารถกลับคืนได้สูงและมีแนวโน้มที่จะดีขึ้นเองอย่างมาก
ชนิดที่เด่นของแผ่นเส้นเลือดฝอยคอรอยด์
APMPPE , จอประสาทตา อักเสบแบบคดเคี้ยว, PIC
หลอดเลือดฝอยคอรอยด์ อักเสบแบบอุดตันเป็นแกนกลางของพยาธิกำเนิด
OCT -A พบช่องว่างการไหลของหลอดเลือดฝอยคอรอยด์ การเปลี่ยนแปลงของจอประสาทตา ชั้นนอกและ RPE เป็นผลรอง
ชนิดที่เด่นของเนื้อเยื่อคั่นคอรอยด์
จอตาและคอรอยด์ อักเสบแบบเบิร์ดช็อต (Birdshot)
การแทรกซึมของลิมโฟไซต์ในสโตรมาของคอรอยด์ เป็นรอยโรคปฐมภูมิ
ใน OCT -A ชั้นฮาลเลอร์ (Haller) พบ flow void และในระยะแรกหลอดเลือดฝอยคอรอยด์ ยังคงปกติ
เป็นโรคเรื้อรังที่ดำเนินไปอย่างช้าๆ และสัมพันธ์อย่างมากกับ HLA-A29
นอกจากนี้ ยังมีแนวคิดเรื่อง กลุ่มอาการ AZOOR ซึ่งมองว่า MEWDS , AZOOR , PIC , MFC, AMN , AIBSE และ AAO R เป็นกลุ่มโรคต่อเนื่องที่มีพื้นฐานทางพันธุกรรมร่วมกันของกลไกภูมิต้านตนเอง/การอักเสบ ทำให้เข้าใจได้อย่างบูรณาการ3) .
ตามสถิติของสมาคมจักษุวิทยาญี่ปุ่น สัดส่วนของโรคแต่ละชนิดในกลุ่มอาการจุดขาวต่อโรคม่านตาอักเสบ ทั้งหมดมีดังนี้ 2) .
โรค สัดส่วนต่อโรคม่านตาอักเสบ ทั้งหมด MEWDS ประมาณ 1-2% (รายงานในประเทศ) APMPPE พบได้น้อย (ไม่มีสถิติชัดเจนเกี่ยวกับอัตราการเกิดต่อปี) PIC พบได้น้อย คอรอยด์ อักเสบแบบคดเคี้ยวประมาณ 0.3% จอตาและคอรอยด์ อักเสบแบบเบิร์ดช็อต พบได้น้อย (พบมากในคนผิวขาว พบน้อยมากในญี่ปุ่น) AZOOR พบได้น้อย (รายงานเพิ่มขึ้นในช่วงไม่กี่ปีที่ผ่านมา)
อาการของแต่ละโรคแตกต่างกัน แต่ลักษณะทางคลินิกต่อไปนี้พบร่วมในกลุ่มโรคจุดขาว1, 2) .
การมองเห็น ลดลงMEWDS , AZOOR ) ถึงรุนแรง (คอรอยด์ อักเสบแบบคดเคี้ยว, PIC ร่วมกับ CNV )เห็นแสงวาบ (โฟทอปเซีย) : อาการที่พบบ่อยที่สุดซึ่งสะท้อนถึงความเสียหายของจอประสาทตา ชั้นนอกและเซลล์รับแสง จุดบอดและข้อบกพร่องของลานสายตา : มักเป็นจุดบอดพาราเซนทรัลหรือเซนทรัลซึ่งสอดคล้องกับตำแหน่งรอยโรคภาพบิดเบี้ยว (เมตามอร์ฟอปเซีย)จอประสาทตา หรือ CNV
กลุ่มโรค การอักเสบของช่องหน้าตาและวุ้นตา MEWDS ・APMPPE ・PIC ปกติไม่มี (APMPPE อาจมีเล็กน้อย) MFC (MFCwP) มีการอักเสบของช่องหน้าลูกตา + กระจกตา อักเสบ (จุดที่แตกต่างจาก PIC ) Birdshot ไม่มีการอักเสบของช่องหน้าลูกตา ถึงน้อยมาก มีกระจกตา อักเสบ คอรอยด์ อักเสบแบบคดเคี้ยวการอักเสบของช่องหน้าม่านตา และวุ้นตา โดยปกติไม่รุนแรง AZOOR โดยปกติไม่มี
หญิงสาว ตาข้างเดียว ดีขึ้นเอง
MEWDS AZOOR PIC )
พบบ่อยในหญิงสายตาสั้น อายุ 20-40 ปี
มักเป็นข้างเดียว (MEWDS มากกว่า 95% เป็นข้างเดียว)
มีแนวโน้มฟื้นตัวเองได้เมื่อติดตามอาการ
อุบัติการณ์รายปีของ MEWDS : ประมาณ 0.22 รายต่อ 100,000 คน
หญิงสาวถึงวัยกลางคน • ตาทั้งสองข้าง • ความเสี่ยง CNV
PIC MFC
หญิงสายตาสั้น อายุ 20–40 ปี (สัดส่วนหญิง >90%)
มักเป็นทั้งสองตา (80% ใน PIC )
ทิ้งรอยแผลเป็นฝ่อที่มีอัตราการเกิดภาวะแทรกซ้อน CNV สูง
ภาวะแทรกซ้อน CNV ใน PIC : 40–76%
วัยหนุ่มสาวถึงวัยกลางคน • ตาทั้งสองข้าง • เริ่มเฉียบพลัน
APMPPE
พบบ่อยในช่วงอายุ 20–30 ปี (เฉลี่ย 25 ปี) ไม่แตกต่างระหว่างเพศ
เป็นทั้งสองตา • เฉียบพลัน • มีแนวโน้มหายได้เอง
ระวังภาวะหลอดเลือดสมองอักเสบร่วม (ต้องตรวจฉุกเฉินหากมีอาการทางระบบประสาท)
วัยกลางคน ตาทั้งสองข้าง เรื้อรังและลุกลาม
Birdshot · คอรอยด์ อักเสบแบบคดเคี้ยว
Birdshot: อายุ 40-60 ปี พบในผู้หญิงมากกว่าเล็กน้อย
คอรอยด์ อักเสบแบบคดเคี้ยว: อายุ 30-50 ปี พบในผู้ชายมากกว่าเล็กน้อยโรคทั้งสองเป็นเรื้อรัง กำเริบซ้ำ ต้องใช้ยากดภูมิคุ้มกันระยะยาว
อัตราการพบ HLA-A29 ใน Birdshot (ชาวผิวขาว): 80-98%
│ ├─ YES → MEWDS・AZOOR・AMN を考慮
│ │ ↳ 眼底ほぼ正常・ERG 異常 → AZOOR
│ └─ YES → APMPPE(FA 蛍光逆転現象を確認)
│ └─ YES → PIC を考慮(CNV 検索:OCTA 必須)
│ └─ YES → 蛇行状脈絡膜炎(結核除外が最優先)
รายการ APMPPE MEWDS PIC MFC (MFCwP) Birdshot คอรอยด์ อักเสบแบบคดเคี้ยวAZOOR อายุที่พบบ่อย 20–30 ปี (เฉลี่ย 25 ปี) 20–50 ปี 18–40 ปี (เฉลี่ย 36 ปี) เฉลี่ย 30 ปี 40–60 ปี 30–50 ปี ส่วนใหญ่ช่วงกลางอายุ 30 ปี เพศ ไม่มีความแตกต่างทางเพศ เพศหญิงมากกว่า (1:4) เพศหญิงมากกว่า (ประมาณ 90%) เพศหญิงมากกว่า (พบมากในหญิงผิวขาว) เพศหญิงมากกว่าเล็กน้อย เพศชายมากกว่าเล็กน้อย เพศหญิงมากกว่า (ประมาณ 75%) ข้างเดียว/สองข้าง สองข้างบ่อย ข้างเดียว (>95%) สองข้างบ่อย (80%) สองข้าง สองข้าง สองข้าง ข้างเดียว→สองข้างแบบค่อยเป็นค่อยไป (สุดท้าย 76% สองข้าง) อาการหลัก สายตาแย่ลง จุดบอดกลาง ภาพ เห็นภาพบิดเบี้ยว สายตาแย่ลง เห็นแสงวาบ เห็นภาพมัว จุดบอด สายตาแย่ลง เห็นภาพบิดเบี้ยว เห็นจุดลอย สายตาแย่ลง เห็นแสงวาบ สายตาแย่ลง ตาบอดกลางคืน การมองเห็น สีผิดปกติ สายตาแย่ลง จุดบอดใกล้ศูนย์กลาง เห็นแสงวาบ การสูญเสียลานสายตา (จอประสาทตา ปกติเกือบปกติ) ลักษณะจุดขาวในจอตา จุดขาวครีมขนาดใหญ่ที่ขั้วหลัง (1/4 ถึง 1/2 เท่าของเส้นผ่านศูนย์กลางจานประสาทตา ) จุดเล็กสีเทาขาวหลายจุดจากขั้วหลังถึงเส้นศูนย์สูตร (100-200 ไมครอน) จุดเล็กสีขาวเหลืองที่ขั้วหลัง (100-300 ไมครอน) จำนวน 12-25 จุด จุดสีเทาเหลืองจากขั้วหลังถึงรอบนอก (45-350 ไมครอน) ร่วมกับวุ้นตา อักเสบ จุดครีมรูปกระสุนปืนจากขั้วหลังถึงเส้นศูนย์สูตร (1/4 ถึง 1/2 เท่าของเส้นผ่านศูนย์กลางจานประสาทตา ) รอยโรคสีเทาเหลืองคล้ายแผนที่แผ่กระจายเป็นแนวคดเคี้ยวรอบจานประสาทตา จอตาปกติเกือบปกติ (ระยะเฉียบพลัน) ต่อมาชั้นนอกฝ่อในระยะปลาย ผล OCT ความผิดปกติของ ellipsoid zone + การสะท้อนสูงของจอประสาทตา ชั้นนอก เหลือฝ่อบางส่วนหลังฟื้นตัว ความผิดปกติชัดเจนและการหายไปของ ellipsoid zone (ระยะเฉียบพลัน) → ฟื้นตัว รอยนูนสะท้อนสูงใต้ RPE + การขาดของ ellipsoid zone (วิวัฒนาการ 5 ระยะ) การสะท้อนสูงใต้ RPE + การขาดของ ellipsoid zone (คล้าย PIC ) รอยโรคคอรอยด์ และจอประสาทตา บวมแบบถุงน้ำ การหายไปของ ellipsoid zone บ่งชี้พยากรณ์โรคไม่ดี ระยะ active: การสะท้อนสูงของจอประสาทตา ชั้นนอกและของเหลวใต้จอประสาทตา ระยะแผลเป็น: RPE ฝ่อ การหายไปของ ellipsoid zone (IS/OS) เป็นผลที่สำคัญที่สุด (สอดคล้องกับจุดบอดในลานสายตา) ผลการตรวจ FA การเรืองแสงต่ำระยะแรก → การเรืองแสงสูงระยะปลาย (ปรากฏการณ์กลับกันของการเรืองแสง) การเรืองแสงสูงแบบพวงหรีด (wreath-like) ต่อเนื่องตั้งแต่แรก ระยะ active: การเรืองแสงสูงระยะแรกในระยะหลอดเลือดแดง → การรั่วระยะปลาย ระยะ active: การเรืองแสงต่ำระยะแรก → การรั่วระยะปลาย การเรืองแสงสูงของรอยโรค (ไม่มีการรั่ว) + การรั่วของหลอดเลือดและการเรืองแสงสูงของหัวประสาทตา ระยะ active: การเรืองแสงต่ำระยะแรก → การเรืองแสงสูงระยะปลาย (มีการรั่ว) ปกติหรือมีความผิดปกติเล็กน้อย ผลการตรวจ ICGA การเรืองแสงลดลงในทุกเฟส (สะท้อนภาวะขาดเลือดของเส้นเลือดฝอยคอรอยด์ โดยตรง) การเรืองแสงลดลงในเฟสปลาย (กว้างกว่าจุดขาว) การเรืองแสงลดลงในเฟสกลาง มีประโยชน์ในการตรวจหารอยโรคที่ไม่แสดงอาการ การเรืองแสงลดลงตั้งแต่เฟสต้นถึงทุกเฟส การเรืองแสงลดลงในเฟสต้นและกลาง → การเรืองแสงเท่ากันในเฟสปลาย (ระยะแรก) → ระยะลุกลาม: การเรืองแสงลดลงในทุกเฟส การเรืองแสงลดลงในทุกเฟส (สะท้อนความผิดปกติของการไหลเวียนคอรอยด์ ) ปกติโดยทั่วไป ผลการตรวจ FAF ระยะเฉียบพลัน: การเรืองแสงอัตโนมัติต่ำหรือมากเกินไป ระยะสงบ: การเรืองแสงอัตโนมัติต่ำ ระยะเฉียบพลัน: การเรืองแสงอัตโนมัติสูง (การเรืองแสงมากเกินไปหลายจุด) หลังฟื้นตัว: กลับสู่ปกติ ระยะ active: การเรืองแสงอัตโนมัติต่ำ (hypoAF) ขอบมีรัศมีการเรืองแสงอัตโนมัติสูง ระยะ active: การเรืองแสงอัตโนมัติต่ำ การเรืองแสงอัตโนมัติต่ำแบบต่อเนื่องรอบขั้วประสาทตา (พบใน 73%) ระยะ active: ขอบการเรืองแสงอัตโนมัติสูง + รัศมีการเรืองแสงอัตโนมัติต่ำ ระยะสงบ: การเรืองแสงอัตโนมัติต่ำ ความผิดปกติของการเรืองแสงอัตโนมัติแบบแถบจากสูงไปต่ำ ผล OCT -A Choriocapillaris flow void (สอดคล้องสูงกับ FA /ICGA ) Choriocapillaris โดยหลักการแล้วคงอยู่ (บางส่วนมี transient flow void) Choriocapillaris flow void (ตำแหน่งรอยโรคอักเสบ) Choriocapillaris flow void Haller layer flow void (ระยะแรก) → ระยะลุกลาม: flow void ทุกชั้น Choriocapillaris flow void (รุนแรง) Choriocapillaris โดยหลักการแล้วคงอยู่ การกลับเป็นซ้ำ พบน้อย (โดยพื้นฐานครั้งเดียว) ประมาณ 10% กลับเป็นซ้ำ สูง (กลับเป็นซ้ำเรื้อรัง) สูง (ตอนอักเสบซ้ำ) สูง (เรื้อรังที่มีการทุเลาและกลับเป็นซ้ำซ้ำ) สูง (กลับเป็นซ้ำทุก 3 เดือนถึง 4 ปี) ส่วนใหญ่คงที่ภายใน 6 เดือน บางส่วนดำเนินต่อ อัตราการเกิด CNV พบได้น้อย พบได้น้อย 40–76% (ความเสี่ยงสูง)สูงสุด 60% CNV ใต้จอประสาทตา : พบได้น้อยสูงสุด 35% แทบไม่มีเลย เกี่ยวข้องกับ HLA ไม่มี HLA-B51 (รายงานเบื้องต้น) HLA-DR2 · HLA-DRB1*15 เกี่ยวข้องกับแฮพลอไทป์ IL-10 HLA-A29 (80-98% ในคนผิวขาว) HLA-B7 · HLA-A2 (รายงานที่เกี่ยวข้อง) ไม่มี (ความโน้มเอียงทางภูมิคุ้มกัน) แผนการรักษา สังเกตอาการ (หายเองได้), รุนแรง: สเตียรอยด์ สังเกตอาการ, รุนแรง: สเตียรอยด์ ระยะสั้น, CNV : ยาต้าน VEGF สังเกตอาการ (ไม่มี CNV ), CNV : ยาต้าน VEGF + สเตียรอยด์ , ยากดภูมิคุ้มกัน สเตียรอยด์ + การปรับภูมิคุ้มกัน, CNV : ยาต้าน VEGF สเตียรอยด์ + ไมโคฟีโนเลต โมเฟทิล / อะดาลิมูแมบ (ระยะยาว)สเตียรอยด์ + ยากดภูมิคุ้มกัน (รวมถึงสารอัลคิเลต), CNV : ยาต้าน VEGF สังเกตอาการ, รุนแรง: สเตียรอยด์ แบบชีพจร พยากรณ์การมองเห็น ดี (มักหายเองได้) ดี (ระวังการกลับเป็นซ้ำ/CNV ) เสี่ยงพยากรณ์ไม่ดีสูงหากมี CNV เสี่ยงพยากรณ์ไม่ดีจาก CNV และจอประสาทตา บวม ไม่รักษา 16-22% มีสายตา ≤0.1 ใน 10 ปี ถ้าลุกลามถึงรอยบุ๋มจอตา ไม่สามารถฟื้นคืน; มากถึง 25% ของตาที่มองเห็นสุดท้าย <20/200 ส่วนใหญ่คงที่ พยากรณ์ไม่ดีในรายที่ความเสียหายชั้นนอกดำเนินไป
Q
โรคใดในกลุ่มอาการจุดขาวที่มีการพยากรณ์โรคทางสายตาแย่ที่สุด?
A
คอรอยด์ อักเสบแบบคดเคี้ยวและคอรอยด์ อักเสบแบบ birdshot มีการพยากรณ์โรคทางสายตาแย่ที่สุด ในคอรอยด์ อักเสบแบบคดเคี้ยว มากถึง 25% ของดวงตามีค่าสายตาสุดท้ายต่ำกว่า 20/200 และใน birdshot ผู้ป่วย 16-22% มีค่าสายตา 0.1 หรือต่ำกว่าภายใน 10 ปีโดยไม่ได้รับการรักษา 2, 4) PIC และ MFC มีความเสี่ยงต่อการพยากรณ์โรคไม่ดีสูงขึ้นในกรณีที่มี CNV APMPPE และ MEWDS มีแนวโน้มสูงที่จะดีขึ้นเองและการพยากรณ์โรคดี
APMPPE พบได้บ่อยในช่วงอายุ 20-30 ปี (เฉลี่ย 25 ปี) โดยไม่มีความแตกต่างทางเพศ ภาวะหลอดเลือดอักเสบอุดตันในหลอดเลือดแดงอาร์เทอริโอลที่นำเลือดเข้าสู่เส้นเลือดฝอยคอรอยด์ ถือเป็นสาเหตุพื้นฐาน และการติดเชื้อไวรัสเป็นปัจจัยกระตุ้นที่สงสัย 1, 2)
อาการนำและดำเนินโรค
ประมาณครึ่งหนึ่งของผู้ป่วยมีอาการคล้ายไข้หวัด (ไข้หวัดใหญ่, ไวรัส EB , อีสุกอีใส, การติดเชื้อสเตรปโตค็อกคัส ฯลฯ)
จุดสีขาวครีมรูปจานขนาด 1/4 ถึง 1/2 ของเส้นผ่านศูนย์กลางจานประสาทตา ปรากฏหลายจุดที่ขั้วหลังของตาทั้งสองข้าง
จุดเริ่มจางลงจากศูนย์กลางภายในไม่กี่วันและหายไปภายใน 7-12 วัน เหลือรอยสีจางเล็กน้อย
โดยทั่วไปจะหายได้เองในครั้งเดียว (การกลับเป็นซ้ำพบได้น้อย)
การพยากรณ์โรคทางสายตามักดี แต่อาจแย่ในกรณีรุนแรงหรือที่发展为เป็นคอรอยด์ อักเสบแบบแผนที่
ภาวะแทรกซ้อนเฉพาะ: หลอดเลือดสมองอักเสบ (MCAT)
APMPPE ร่วมกับหลอดเลือดสมองอักเสบ (MCAT: multiple cerebral arterial thrombosis) เป็นภาวะแทรกซ้อนรุนแรง หากมีอาการปวดศีรษะ ไข้ หรืออาการทางระบบประสาท ต้องทำ MRI และ MRA สมองอย่างเร่งด่วน ในกรณีที่มีหลอดเลือดสมองอักเสบร่วม จำเป็นต้องได้รับการรักษาด้วย methylprednisolone pulse therapy และร่วมมือกับอายุรศาสตร์ระบบประสาท2) .
ความสัมพันธ์กับสเปกตรัมของจอประสาทตา อักเสบชนิด placoid
APMPPE ร่วมกับ PPM (persistent placoid maculopathy) และ RPC (relentless placoid chorioretinitis) ก่อให้เกิด “สเปกตรัมของจอประสาทตา อักเสบชนิด placoid” โดยมีภาวะขาดเลือดของแผ่นเส้นเลือดฝอยคอรอยด์ เป็นพื้นฐานทางพยาธิสรีรวิทยาร่วมกัน5) .
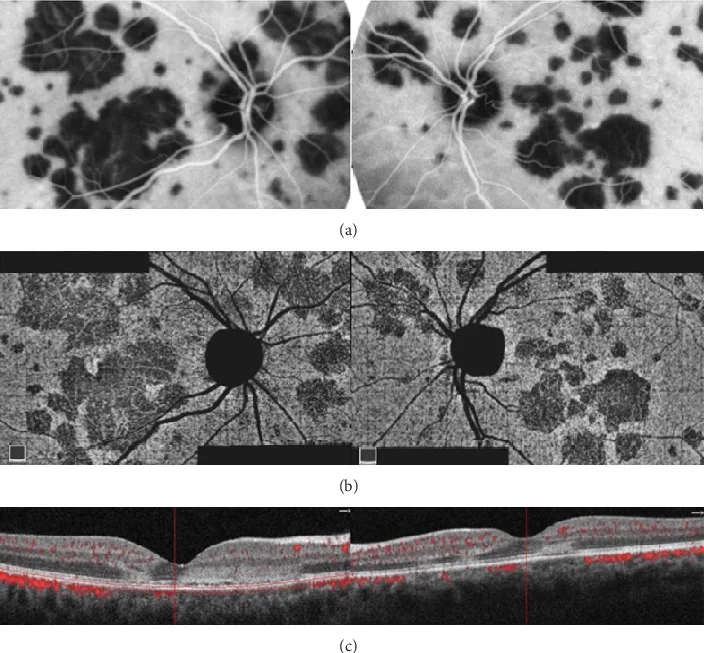
Oliveira MA, et al. Management of Acute Posterior Multifocal Placoid Pigment Epitheliopathy (
APMPPE ): Insights from Multimodal Imaging with
OCTA . Case Rep Ophthalmol Med. 2020. Figure 5. PM
CI D: PMC7094199. License: CC BY.
รอยโรคแบบแผนที่และ placoid หลายจุดที่ขั้วหลังของตาทั้งสองข้างปรากฏเป็น hypofluorescence ใน
ICGA , บริเวณที่เลือดไหลเวียนลดลงในแผ่นเส้นเลือดฝอย
คอรอยด์ ใน
OCTA และการเปลี่ยนแปลง hyperreflective จากชั้น plexiform ชั้นนอกถึง
RPE ใน
OCT ผล multimodal เหล่านี้สอดคล้องกับรอยโรค placoid ที่กล่าวถึงในหัวข้อ “
APMPPE (acute posterior multifocal placoid pigment epitheliopathy)”.
MEWDS พบได้บ่อยในผู้หญิงอายุ 20-50 ปี (อัตราส่วนชาย:หญิง 1:4) มีลักษณะเฉพาะคือ เป็นข้างเดียว เฉียบพลัน และหายได้เอง
ลักษณะทางคลินิกที่จำเพาะ
จุดเล็กสีขาวเทาจางๆ หลายจุด (100-200 ไมครอน) ในชั้นลึกของจอประสาทตา จนถึงระดับ RPE บริเวณขั้วหลังถึงเส้นศูนย์สูตร
การเปลี่ยนแปลงแบบเม็ดที่โฟเวีย (foveal granularity) : พบในผู้ป่วย 74-96% และอาจเป็นสิ่งตรวจพบที่เหลืออยู่เพียงอย่างเดียวหลังจากจุดขาวหายไป แสดงรูปแบบจำเพาะในการตรวจ NIR-FAF 9) ลักษณะจุดสีส้ม (orange-dot appearance) : สิ่งตรวจพบที่จำเพาะในการถ่ายภาพจอประสาทตา หรือการถ่ายภาพอินฟราเรดใกล้รอยโรคสีงาช้าง (ivory lesion) : การเปลี่ยนแปลงสีขาวจางแบบกระจายที่ขั้วหลังของจอตาอาการนำคล้ายไข้หวัดเกิดขึ้นก่อนประมาณ 50% ของผู้ป่วย
อุบัติการณ์รายปีประมาณ 0.22 รายต่อ 100,000 คน และ 10% มีการกลับเป็นซ้ำ
การเรืองแสงมากเกินแบบพวงหรีด (wreath-like hyperfluorescence) ในการตรวจ FA
การเรืองแสงมากเกินแบบพวงหรีดที่ลักษณะเฉพาะในระยะแรกของ FA เป็นจุดสำคัญในการวินิจฉัย MEWDS รอยโรคสีขาวแสดงการเรืองแสงมากเกินในระยะแรกของ FA โดยไม่ขยายตัวในระยะหลัง การเรืองแสงมากเกินในระยะแรกนี้เป็นจุดแยกสำคัญจากการเรืองแสงน้อยในระยะแรกของ APMPPE (ปรากฏการณ์การกลับกันของฟลูออเรสเซนต์)1, 9) .
ความต่อเนื่องกับกลุ่มอาการ AZOOR
MEWDS เกี่ยวข้องกับการทำลายชั่วคราวของ ellipsoid zone (เส้น IS/OS) ของเซลล์รับแสง และเข้าใจว่าเป็นโรคที่อยู่ในกลุ่ม AZOOR complex ในการตรวจ OCT สามารถพบความผิดปกติและการหายไปของ ellipsoid zone ในระยะเฉียบพลัน และจะดีขึ้นเมื่อการมองเห็น ฟื้นตัว3) .
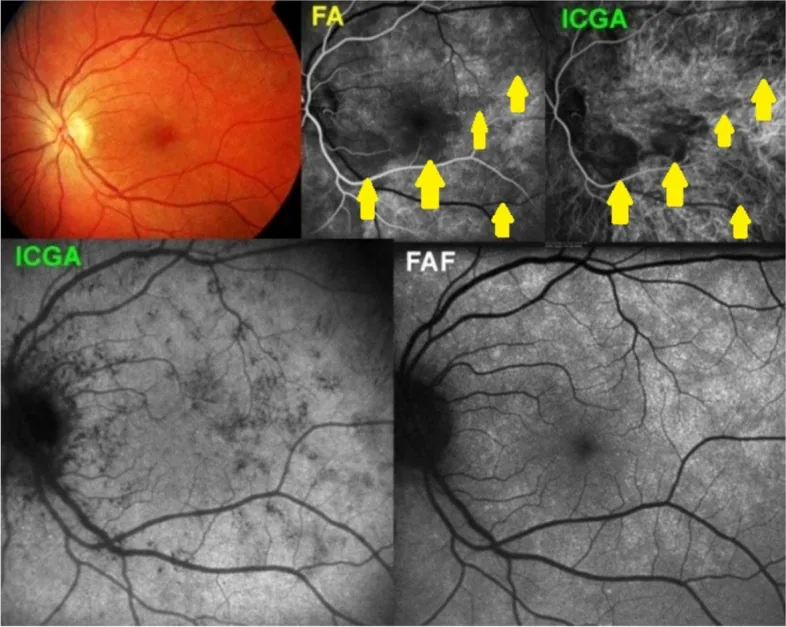
Papasavvas I, et al. Choroidal vasculitis as a biomarker of inflammation of the choroid.
Indocyanine Green Angiography (
ICGA ) spearheading for diagnosis and follow-up, an imaging tutorial. J Ophthalmic Inflamm Infect. 2024. Figure 5. PM
CI D: PMC11618284. License: CC BY.
รอยโรคจุดขาวจางกระจายที่ขั้วหลัง ในการตรวจ
FA และ
ICGA พบความผิดปกติของการไหลเวียนเลือดแบบจุด และในการตรวจ
FAF พบการเรืองแสงอัตโนมัติสูงที่สอดคล้องกัน ผลการตรวจหลายรูปแบบนี้สอดคล้องกับการเรืองแสงสูงแบบพวงหรีดในการตรวจ
FA และจุดเรืองแสงต่ำในการตรวจ
ICGA ที่กล่าวถึงในหัวข้อ “
MEWDS (กลุ่มอาการจุดขาวหลายจุดที่หายไป)“
PIC พบได้บ่อยในหญิงสาว (ประมาณ 90%) อายุ 18-40 ปี ที่มีสายตาสั้น (เฉลี่ยประมาณ -5 D)
ลักษณะทางคลินิกที่จำเพาะ
จุดเล็กสีเหลืองขาวขนาด 100–300 ไมครอน จำกัดเฉพาะบริเวณขั้วหลัง มักมี 12–25 จุด
ไม่มีการอักเสบในช่องหน้าหรือวุ้นตา (นี่คือจุดแยกโรคที่สำคัญที่สุดจาก MFC)
รอยโรคที่ยังทำงานอยู่สามารถเห็นเป็นรอยนูนสะท้อนแสงสูงใต้ RPE ในการตรวจ OCT
เมื่อเกิดแผลเป็น จะทิ้งรอยโรคฝ่อเล็กๆ
ภาวะแทรกซ้อน CNV (40–76%) เป็นปัญหาทางคลินิกที่สำคัญที่สุด
ภาวะแทรกซ้อนที่สำคัญที่สุดของ PIC คือ CNV โดยมีอัตราการเกิด 40-76% 7, 8) CNV มักเกิดจากปัจจัยต่อไปนี้:
ความเปราะบางของเยื่อบรูค เนื่องจากการบางของคอรอยด์ จากสายตาสั้น
การทำลายเยื่อบรูค เนื่องจากการอักเสบใต้ RPE
การเพิ่มขึ้นของการผลิตไซโตไคน์อักเสบเฉพาะที่ (เช่น VEGF)
OCT -A แสดงให้เห็นว่ามีความไวมากกว่า FA ในการคัดกรอง CNV และแนะนำให้ติดตามด้วย OCT -A เป็นประจำ การแย่ลงอย่างกะทันหันของภาพบิดเบี้ยว เป็นสัญญาณของการเกิด CNV และต้องได้รับการตรวจอย่างเร่งด่วน
ความสัมพันธ์กับโรคทางระบบ
มีการรายงานการเกิดร่วมกันของ PIC และซาร์คอยโดซิส และในกรณีที่มีรอยโรคที่ปอดหลายจุด ควรตรวจ CT ทรวงอก ACE ในซีรั่ม และไลโซไซม์ นอกจากนี้ยังมีการรายงานความสัมพันธ์กับ HLA-DR2 และ HLA-DRB1*15 3) .
MFC (multifocal choroiditis with panuveitis; MFCwP) เป็นโรคในสเปกตรัมเดียวกันกับ PIC แต่ การมีวุ้นตา อักเสบและช่องหน้าม่านตาอักเสบ เป็นจุดแยกที่สำคัญที่สุด 7) .
ลักษณะทางคลินิกที่จำเพาะ
จุดสีเหลืองเทาขนาด 45–350 ไมครอน ปรากฏหลายจุดไม่เพียงแต่ที่ขั้วหลัง แต่ยังรวมถึงบริเวณรอบนอกส่วนกลางด้วย.
มีลักษณะเป็นโรคเรื้อรังที่กำเริบเป็นระยะ (มี episodes การอักเสบซ้ำ)
อัตราการเกิดเยื่อเหนือจอประสาทตา (ERM ) สูง (สูงถึง 35%) ส่งผลต่อพยากรณ์การมองเห็น ระยะยาว
ในบางกรณี ไม่สามารถควบคุมการอักเสบได้หากไม่ได้รับการรักษาด้วยยากดภูมิคุ้มกัน
ข้อควรระวังในการรักษา
MFC มักไม่ดีขึ้นเอง และหลายกรณีจำเป็นต้องได้รับการรักษาด้วยการปรับภูมิคุ้มกันระยะยาว เมื่อใช้สเตียรอยด์ เพียงอย่างเดียวไม่เพียงพอ ให้ใช้ methotrexate (MTX), azathioprine (AZA) หรือ mycophenolate mofetil (MMF) เมื่อมี CNV จำเป็นต้องใช้แนวทางสองทางคือ anti-VEGF และการปรับภูมิคุ้มกันร่วมกัน7, 8) .
โรคเบิร์ดช็อต (Birdshot) พบในผู้สูงอายุวัยกลางคน (40-60 ปี เฉลี่ย 50 ปี) พบในผู้หญิงมากกว่าเล็กน้อย (1.5:1) พบมากในคนผิวขาว และเป็นหนึ่งในความสัมพันธ์ทางพันธุกรรมที่แข็งแกร่งที่สุดที่ทราบกับ HLA-A29 (ความเสี่ยงสัมพัทธ์ 50-224 เท่าในคนผิวขาว)4) .
ลักษณะเฉพาะที่พบในจอตา
จุดสีครีมคล้ายรอยกระสุนปืน (ขนาด 1/4 ถึง 1/2 เท่าของเส้นผ่านศูนย์กลางหัวประสาทตา) เกิดขึ้นหลายจุดและสมมาตรกันทั้งสองข้าง จากขั้วหลังไปจนถึงเส้นศูนย์สูตร
จุดเหล่านี้จะเปลี่ยนเป็นรอยแผลเป็นที่ไม่มีเม็ดสี
อาจมีภาวะหลอดเลือดจอตาอักเสบและหัวประสาทตาบวมร่วมด้วย
การเปลี่ยนแปลงการทำงานที่จำเพาะ
ตาบอดกลางคืน และความผิดปกติของการมองเห็นสี การมองเห็น ลดลงชนิดลบในการตรวจคลื่นไฟฟ้าจอประสาทตา แบบเต็มลานสายตา : พบในระยะแรก และเมื่อดำเนินโรค แอมพลิจูดคลื่น a จะลดลงการหน่วงของคลื่นไฟฟ้าจอประสาทตา แบบกะพริบ 30Hz : ตัวบ่งชี้ที่ไวที่สุดในการติดตามกิจกรรม สามารถตรวจพบความผิดปกติได้เร็วกว่าการมองเห็น ลดลง17)
ข้อควรระวังสำหรับคนญี่ปุ่น
เนื่องจากความถี่ของการเป็นพาหะ HLA-A29 ในคนญี่ปุ่นต่ำ ความไวในการวินิจฉัยของ HLA-A29 จึงมีจำกัด การวินิจฉัยต้องเน้นที่ผลการตรวจทางคลินิกตามเกณฑ์การจำแนก SUN 2021 (รอยโรคที่จอประสาทตา คล้ายกระสุนปืน, การอักเสบของช่องหน้าม่านตา เล็กน้อย, การมีวุ้นตา อักเสบ)10) .
ภาวะแทรกซ้อนระยะยาว
จอประสาทตา บวมน้ำชนิดถุงน้ำ (CME ): สาเหตุหลักของการมองเห็น ลดลงหัวประสาทตาบวมและฝ่อของเส้นประสาทตา
ในกรณีที่ใช้การปลูกฝังสเตียรอยด์ (ฟลูโอซิโนโลน) พบว่าความดันลูกตา สูงขึ้นถึง 40% และอาจจำเป็นต้องผ่าตัดโพรงใยแก้วนำแสง
โรคคอรอยด์ อักเสบแบบคดเคี้ยว (Serpiginous choroidopathy) เป็นโรคคอรอยด์ อักเสบเรื้อรังทั้งสองข้าง พบในอายุ 30–50 ปี (พบในผู้ชายมากกว่าเล็กน้อย) มีลักษณะเฉพาะคือ รอยโรคสีเทาเหลืองคล้ายแผนที่ที่ขยายตัวแบบคดเคี้ยวจากรอบขั้วประสาทตา
รูปแบบการดำเนินโรคที่จำเพาะ
เริ่มจากรอบขั้วประสาทตา (peripapillary) เข้าหาศูนย์กลาง และขอบรอยโรคค่อยๆ ขยายตัวแบบคดเคี้ยว
ระยะ active: มีขอบสีเทาขาวปรากฏที่ขอบรอยโรค
ระยะแผลเป็น: กลายเป็นรอยโรคฝ่อของจอประสาทตา และคอรอยด์
เมื่อกลับเป็นซ้ำ การอักเสบใหม่จะเกิดขึ้นจาก ขอบของแผลเป็นเดิม เสมอ (ซึ่งเป็นลักษณะเฉพาะ)
ระยะห่างระหว่างการกลับเป็นซ้ำอยู่ระหว่าง 3 เดือนถึง 4 ปี แตกต่างกันมากในแต่ละบุคคล
สำคัญที่สุด: การแยกจากชนิดที่เกี่ยวข้องกับวัณโรค (SLC)
คอรอยด์ อักเสบแบบเซอร์พิจิโนสที่เกี่ยวข้องกับวัณโรค (serpiginous-like choroiditis; SLC) มีลักษณะภาพถ่ายคล้ายกับคอรอยด์ อักเสบแบบเซอร์พิจิโนสมาก แต่แนวทางการรักษาแตกต่างกันโดยพื้นฐาน:
จุดที่ใช้แยก คอรอยด์ อักเสบแบบเซอร์พิจิโนสชนิดที่เกี่ยวข้องกับวัณโรค (SLC) การกระจายของรอยโรค รอบหัวประสาทตา, เข้าสู่ศูนย์กลาง ขั้วหลังถึงรอบนอก, หลายจุด IGRA/TST ลบ บวก ลักษณะรอยโรค เป็นแผนที่และต่อเนื่อง รอยโรคเล็กหลายแห่งไม่ต่อเนื่อง การรักษา สเตียรอยด์ + ยากดภูมิคุ้มกันยาต้านวัณโรคจำเป็น
เนื่องจากการใช้ยากดภูมิคุ้มกันใน SLC จะทำให้วัณโรคแย่ลงอย่างชัดเจน การตรวจ IGRA (Quantiferon) ก่อนการรักษาจึงเป็นสิ่งที่ขาดไม่ได้โดยเด็ดขาด2) .
การจัดการ CNV ที่เกิดร่วม (สูงสุด 35%)
ในโรคคอรอยด์ อักเสบแบบเซอร์พิจิโนซา พบ CNV ร่วมได้สูงถึง 35% และหากลุกลามถึงโฟเวียจะทำให้สูญเสียการมองเห็น แบบถาวร การฉีดยา anti-VEGF (bevacizumab, ranibizumab) เข้าแก้วตาได้ผลดี18) .
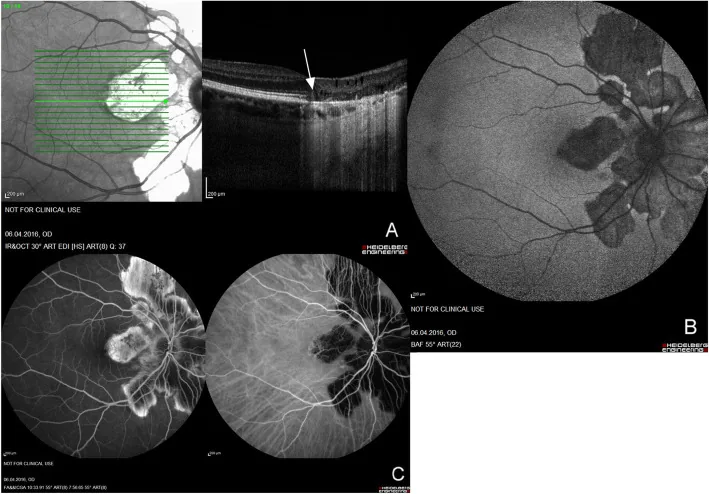
Macedo S, et al. Optical coherence tomography angiography (
OCTA ) findings in Serpiginous Choroiditis. BMC Ophthalmol. 2020. Figure 1. PM
CI D: PMC7325353. License: CC BY.
การถ่ายภาพ autofluorescence จอตา, fluorescein angiography และ OCT แสดงรอยโรคคอริโอเรตินาลแบบเซอร์พิจิโนซาที่แผ่กระจายออกจากรอบขั้วประสาทตา ซึ่งสอดคล้องกับรูปแบบการกระจายแบบเซอร์พิจิโนซารอบขั้วประสาทตาที่กล่าวถึงในหัวข้อ “โรคคอรอยด์ อักเสบแบบเซอร์พิจิโนซา”
AZOOR เป็นแนวคิดโรคที่เสนอโดย Gass ในปี 1992 ซึ่งเป็น จอประสาทตา ชั้นนอกที่ทำให้การมองเห็น ลดลงอย่างเฉียบพลัน มีข้อบกพร่องของลานสายตา และอาการกลัวแสง แม้ว่าจอประสาทตา จะเกือบปกติ3)
แนวคิดของ AZOOR complex
AZOOR complex ที่เสนอโดย Jampol และคณะ เป็นแนวคิดที่เข้าใจ MEWDS , AZOOR , PIC , MFC, AMN (acute macular neuroretinopathy), AIBSE และ AAO R ว่าเป็นความต่อเนื่องที่มีพื้นฐานร่วมกันของภูมิต้านทานตนเอง/การอักเสบทางพันธุกรรม3)
ลักษณะทางคลินิกที่จำเพาะ
พบได้บ่อยในหญิงสาวอายุ 20–50 ปีที่มีสายตาสั้น
อาการเห็นแสงวาบ (photopsia) มักเกิดขึ้นในช่วงเริ่มต้น (โดยเฉพาะแสงที่เห็นเป็นแถบหรือโค้ง)เริ่มเป็นข้างเดียว และสุดท้าย 76% กลายเป็นสองข้าง
จอประสาทตา เกือบปกติ ในระยะเฉียบพลัน (ลักษณะเด่นคือความแตกต่างระหว่างการมองเห็น ที่ลดลงกับผลตรวจจอประสาทตา )ข้อบกพร่องของลานสายตาเป็นแบบแถบไม่สม่ำเสมอ (มักต่อเนื่องกับจุดบอด)
อาจพบร่วมกับโรคภูมิต้านตนเอง (โรคฮาชิโมโตะ, ปลอกประสาทเสื่อมแข็ง)
OCT และ ERG เป็นกุญแจสำคัญในการวินิจฉัย
การหายไปหรือความไม่ชัดเจนของ ellipsoid zone (เส้น IS/OS) ในการตรวจ OCT เป็นสิ่งที่พบได้สำคัญที่สุด
ไม่สามารถคาดหวังการฟื้นฟูการทำงานในบริเวณที่ชั้นนอกหายไปในการตรวจ OCT (มีประโยชน์ในการพยากรณ์โรคด้วย)
สามารถตรวจพบการลดลงของแอมพลิจูดในการตรวจ ERG แบบหลายจุด (mfERG ) ได้แม้จอประสาทตา จะปกติ (mfERG มีความไวมากกว่า ERG แบบเต็มลานสายตา)
การตรวจ FAF ด้วยอินฟราเรดบางครั้งสามารถแสดงขอบเขตระหว่างรอยโรคและบริเวณปกติได้
การรักษาและการพยากรณ์โรค
ยังไม่มีการรักษาที่เป็นมาตรฐานสำหรับ AZOOR ผู้ป่วยที่ไม่รุนแรงเพียงต้องการสังเกตอาการ แต่ผู้ป่วยรุนแรง (สายตาเลือนลางหรือข้อบกพร่องของลานสายตากว้าง) จะได้รับการรักษาด้วย methylprednisolone (1,000 มก. × 3 วัน) ตามด้วย prednisolone รับประทาน2) ผู้ป่วยส่วนใหญ่จะคงที่ภายใน 6 เดือน แต่ลานสายตาในบริเวณที่ชั้นนอกเสียหายจะไม่ฟื้นตัว
Q
จะแยก AZOOR ออกจากโรคประสาทตาอักเสบหลังลูกตาอย่างไร?
A
ทั้ง AZOOR และโรคประสาทตาอักเสบ หลังลูกตา (retrobulbar optic neuritis) ทำให้การมองเห็น และลานสายตาลดลงโดยที่จอประสาทตา ดูเกือบปกติ จึงจำเป็นต้องแยกโรค จุดที่ใช้แยกคือ ① ใน AZOOR จะมี amplitude ของ multifocal ERG ลดลง แต่ใน retrobulbar optic neuritis ค่า ERG ปกติ ② ใน AZOOR ความบกพร่องของลานสายตา เป็นแบบแถบหรือโค้งไม่สม่ำเสมอ ในขณะที่ retrobulbar optic neuritis มักเป็น central scotoma ③ ใน AZOOR มักพบ RAPD เล็กน้อย แต่ใน retrobulbar optic neuritis พบ RAPD ชัดเจน ④ ใน OCT AZOOR แสดงการหายไปของ ellipsoid zone ส่วน retrobulbar optic neuritis แสดง optic disc edema หรือ RNFL บาง ซึ่งช่วยในการวินิจฉัยแยกโรค2, 3) .
การทำความเข้าใจบทบาทของการตรวจภาพแต่ละประเภทอย่างชัดเจนเป็นสิ่งจำเป็นสำหรับการวินิจฉัยที่แม่นยำและการประเมินกิจกรรมของกลุ่มอาการจุดขาว 1, 5) .
รูปแบบ ข้อบ่งชี้และบทบาทที่แข็งแกร่งที่สุด FA (การถ่ายภาพหลอดเลือดด้วยฟลูออเรสซีน )การประเมินการรั่วของหลอดเลือดจอตา, RPE และคอริโอแคปิลลาริส การยืนยันปรากฏการณ์ฟลูออเรสเซนต์กลับด้านใน APMPPE การยืนยันการเรืองแสงมากเกินแบบพวงหรีดใน MEWDS การประเมินหลอดเลือดอักเสบ (Birdshot) ICGA (การตรวจหลอดเลือดด้วยสีอินโดไซยานีนกรีน)การประเมินความผิดปกติของการไหลเวียนเลือดคอรอยด์ โดยตรง สามารถตรวจพบรอยโรคได้เร็วกว่า FA (โดยเฉพาะ Birdshot, APMPPE , Serpiginous) ตรวจพบรอยโรคที่กว้างกว่าที่พบจากการตรวจทางคลินิก (MEWDS , PIC ) มีความไวสูงที่สุดในการตรวจหารอยโรคที่ยัง active FAF (การเรืองแสงอัตโนมัติของจอตา)การประเมินความผิดปกติของ RPE แบบไม่รุกล้ำ การตรวจสอบกิจกรรม (APMPPE , serpentine) การวินิจฉัย MEWDS (จุดขาวระยะแรกมีการเรืองแสงอัตโนมัติสูง) การประเมินภาวะเรื้อรังของ Birdshot (การเรืองแสงอัตโนมัติรอบหัวประสาทตาต่ำ 73%) OCT (การถ่ายภาพตัดขวางด้วยแสง)การประเมินโซน ellipsoid (ลักษณะวินิจฉัยของ MEWDS และ AZOOR ) การประเมินวิวัฒนาการของรอยโรค 5 ระยะ (PIC ) การประเมิน CNV และจอประสาทตา บวมน้ำ การพยากรณ์โรค (การสูญเสีย EZ → การพยากรณ์การมองเห็น ไม่ดี) OCT -Aการตรวจจับช่องว่างการไหลของคอริโอแคปิลลาริสแบบไม่รุกล้ำ (APMPPE , serpentine, PIC ) การตรวจจับ CNV ระยะแรกและไว (ไวกว่า FA ใน PIC และ MFC) การประเมินการไหลเวียนเลือดคอรอยด์ แบบชั้นใน Birdshot การติดตามการตอบสนองต่อการรักษา ERG หลายจุด / ลานสายตาทั้งหมดการวินิจฉัย AZOOR (แอมพลิจูด ERG ลดลงแม้จอตาปกติเกือบปกติ). การติดตามกิจกรรมของ Birdshot (การหน่วงของ flicker 30Hz ไวที่สุด). การประเมินผลการรักษา
เมื่อสงสัย MEWDS
ทำ FAF ก่อน (ความไวสูงที่สุด. ตรวจพบได้แม้ไม่เห็นจุดขาว)FA (ยืนยันการเรืองแสงมากเกินแบบพวงหรีด)OCT (ประเมิน ellipsoid zone)OCT -A (ประเมิน choriocapillaris, ค้นหา CNV )
เมื่อสงสัย APMPPE
FA (ยืนยันปรากฏการณ์การกลับสีของฟลูออเรสเซนต์)ICGA (ประเมินภาวะขาดเลือดของ choriocapillaris โดยตรง)OCT -A (ประเมิน flow void)หากมีอาการทางระบบประสาท: MRI สมองและ MRA (เพื่อแยกภาวะหลอดเลือดอักเสบ)
เมื่อสงสัย PIC/MFC
OCT -A (การตรวจหา CNV ระยะแรก)FA (ประเมินการรั่วของรอยโรคและเครือข่าย CNV )ICGA (การตรวจหารอยโรคที่ไม่แสดงอาการ)FAF (การติดตามกิจกรรม)
เมื่อสงสัยโรคคอรอยด์อักเสบแบบเซอร์พิจิโนซา
IGRA (การแยกวัณโรคออกเป็นลำดับความสำคัญสูงสุด) ICGA (ประเมินการทำงานของรอยโรค)FAF (การเรืองแสงอัตโนมัติสูงที่ขอบที่ทำงาน)OCT -A (ค้นหา flow void ของคอริโอแคปิลลาริสและ CNV )
Q
ควรทำ FA หรือ ICGA ก่อน?
A
กลยุทธ์แตกต่างกันไปตามโรค ใน APMPPE และคอรอยด์ อักเสบแบบเซอร์พิจิเนส (serpiginous choroiditis) ICGA จะแสดงความผิดปกติของการไหลเวียนเลือดคอรอยด์ ได้โดยตรงมากกว่า ดังนั้นการทำ ICGA พร้อมกับหรือหลังจาก FA จะช่วยให้เข้าใจพยาธิสภาพได้ลึกซึ้งยิ่งขึ้น ใน MEWDS การเรืองแสงมากเกินแบบพวงหรีด (wreath-like hyperfluorescence) ใน FA มีความสำคัญในการวินิจฉัย อย่างไรก็ตาม เนื่องจากการตรวจเหล่านี้เป็นการรุกราน ปัจจุบันข้อมูลจำนวนมากสามารถทดแทนได้ด้วย OCT -A และการใช้ FAF ร่วมกับ OCT -A ถูกใช้เป็นการประเมินเบื้องต้น1, 5)
การเรืองแสงน้อยที่รอยโรคกลุ่มอาการจุดขาวแสดงใน ICGA เป็นการสะท้อนโดยตรงของ การหยุดชะงักของการไหลเวียนเลือดคอรอยด์ (การอุดตันของคอริโอแคปิลลาริส) 1) ICGA เป็นวิธีการที่ไวต่อการประเมินการไหลเวียนคอรอยด์ มากกว่า FA โดยมีลักษณะดังนี้:
การเรืองแสงน้อยทุกเฟส : พบใน APMPPE , คอรอยด์ อักเสบแบบเซอร์พิจิเนส, PIC และ MFC สะท้อนถึงการอุดตันอย่างรุนแรงของภาวะขาดเลือดในชั้นเส้นเลือดฝอยคอรอยด์ การเรืองแสงต่ำระยะปลาย (ไม่มีความผิดปกติใน FA ) : การเรืองแสงต่ำระยะปลายใน ICGA ใน MEWDS อธิบายว่าเป็นการเปลี่ยนแปลงการดูดซึม ICG เนื่องจากความผิดปกติของ RPE ไม่ใช่จากตำแหน่งหลักที่ choriocapillaris (choriocapillaris โดยทั่วไปยังคงปกติใน OCT -A) 1) .Flow void ในชั้น Haller → flow void ทุกชั้นในระยะลุกลาม : รูปแบบการดำเนินโรคสองขั้นตอนที่เป็นลักษณะเฉพาะของ Birdshot จากสโตรมาคอรอยด์ ไปยัง choriocapillaris 14) .
ICGA ยังเหนือกว่าในการตรวจหารอยโรคที่ซ่อนอยู่ซึ่งมองไม่เห็นทางคลินิก (subclinical lesions) เมื่อเทียบกับ FA และ OCT -A โดยเฉพาะใน MEWDS และ PIC โดยแสดงรอยโรคคอรอยด์ ที่กว้างกว่าจุดขาว 1, 15) .
รูปแบบ FAF (การเรืองแสงอัตโนมัติของจอตา) สะท้อนสถานะเมแทบอลิซึมของ RPE และมีประโยชน์ในการวินิจฉัยและประเมินกิจกรรมของกลุ่มอาการจุดขาว 16) .
รูปแบบ FAF โรค/ระยะ ความหมาย การเรืองแสงเองสูง (hyper AF) MEWDS ระยะเฉียบพลัน · ขอบที่ active ของ Serpiginousการสะสมของผลิตภัณฑ์เสื่อมของเซลล์รับแสง (เช่น A2E) ใน RPE การเรืองแสงเองต่ำ (hypo AF) APMPPE ระยะแผลเป็น · รอยโรค active ของ PIC · รอบหัวประสาทตาใน Birdshotการสูญเสีย RPE หรือการสูญเสียหน้าที่ AF ต่ำตรงกลาง + รัศมี AF สูงรอบนอก ขอบที่ active ของ Serpiginous และ PIC รูปแบบความเสียหายของ RPE ที่ขอบ active AF ผิดปกติแบบแถบ AZOOR สอดคล้องกับการกระจายของความเสียหายชั้นนอกของเซลล์รับแสง การเรืองแสงอัตโนมัติมากเกินแบบเม็ดเล็กที่โฟเวีย MEWDS (NIR-FAF )การสร้างภาพแบบไม่รุกล้ำของความละเอียดแบบเม็ดเล็กที่โฟเวีย
ในโรค Birdshot พบการเรืองแสงอัตโนมัติน้อยแบบรวมตัวรอบหัวประสาทตาใน 73% ของผู้ป่วย และมีประโยชน์เป็นตัวบ่งชี้การเรื้อรัง17) .
การประเมิน EZ (ellipsoid zone หรือเส้น IS/OS เดิม) มีบทบาทสำคัญในการประเมินกิจกรรมและการพยากรณ์โรคของกลุ่มอาการจุดขาว1) .
ผลการตรวจ EZ โรค/ระยะ การพยากรณ์โรค EZ ผิดปกติอย่างชัดเจน → ฟื้นตัวMEWDS ระยะเฉียบพลัน → ระยะฟื้นตัวดี (การฟื้นตัวของ EZ สัมพันธ์กับการฟื้นตัวของการมองเห็น ) EZ หายไป (ตรงกับรอยโรค)ระยะ active ของ AZOOR ไม่มีการฟื้นฟูการทำงานในบริเวณที่หายไป EZ ผิดปกติ + การสะท้อนสูงของจอประสาทตา ชั้นนอกระยะเฉียบพลันของ APMPPE อาจมีฝ่อบางส่วนหลงเหลือหลังฟื้นตัว รอยนูนสะท้อนแสงสูงใต้ RPE + การขาดของ EZ PIC /MFC (วิวัฒนาการ 5 ระยะ)พยากรณ์โรคไม่ดีเมื่อมี CNV ร่วม การหายไปของ EZ (ร่วมกับจอประสาทตา บวมน้ำแบบถุงน้ำ) Birdshot ระยะลุกลาม ปัจจัยเสี่ยงต่อพยากรณ์การมองเห็น ไม่ดี
ช่องว่างการไหลของคอริโอแคปิลลาริส ในการตรวจ OCT -A แสดงความสอดคล้องสูงกับผลการตรวจ FA และ ICGA (มีประโยชน์โดยเฉพาะใน APMPPE และคอรอยด์ อักเสบแบบเซอร์พิจิโนซา) 5, 13) .
รูปแบบ FA โรค ความสำคัญทางคลินิก การเรืองแสงน้อยในระยะแรก → การเรืองแสงมากในระยะหลัง (ปรากฏการณ์กลับด้านการเรืองแสง) APMPPE ภาวะขาดเลือดของคอริโอแคปิลลาริส การไหลเวียนบกพร่องในระยะแรก → การรั่วของสีที่ล่าช้าจากเนื้อเยื่อรอบข้าง การเรืองแสงมากเกินไปในระยะแรกแบบพวงหรีด (wreath-like) MEWDS สะท้อนความเสียหายของ RPE /เซลล์รับแสง โดยตรง ไม่ขยายตัวในระยะหลัง ช่วยในการวินิจฉัยแยกโรค การเรืองแสงน้อยในระยะแรก → การรั่วในระยะหลัง ระยะ active ของ Serpiginous/MFC หลักฐานของคอรอยด์ อักเสบที่ active การเรืองแสงมากเกินในระยะหลอดเลือดแดงต้น → การรั่วระยะปลาย ระยะ active ของ PIC บ่งชี้ถึง CNV อักเสบ การรั่วของหลอดเลือด + การเรืองแสงมากเกินของจานประสาทตา (ไม่มีการรั่ว) Birdshot หลักฐานโดยตรงของจอประสาทตา อักเสบจากหลอดเลือด ปกติถึงเล็กน้อย AZOOR ลักษณะเฉพาะคือการแยกกัน: พบข้อบกพร่องของลานสายตาและความผิดปกติของ ERG แม้ว่า FA จะเป็นลบ
การรักษากลุ่มอาการจุดขาวแตกต่างกันอย่างมากขึ้นอยู่กับประวัติธรรมชาติของโรค ความรุนแรง และการมี CNV ร่วม
MEWDS และ APMPPE (กรณีไม่รุนแรง)
มีแนวโน้มที่จะดีขึ้นเองสูง มักฟื้นตัวโดยไม่ต้องรักษาพิเศษ2)
MEWDS : จุดขาวหายไปและการมองเห็น ดีขึ้นภายในไม่กี่สัปดาห์ เฉพาะในกรณีรุนแรงหรือมี papilledema จึงใช้สเตียรอยด์ ชนิดรับประทานAPMPPE : จุดขาวยุบลงใน 7-12 วัน การพยากรณ์การมองเห็น มักดี
APMPPE (รุนแรง/มี papillitis ร่วม) · PIC (รอยโรค active ใกล้ fovea) · AZOOR (กรณีรุนแรง)
เริ่ม prednisolone 30–60 มก./วัน แล้วค่อยๆ ลดขนาด
APMPPE ที่มี vasculitis ในสมอง ต้องให้ methylprednisolone pulse และร่วมมือกับอายุรกรรมระบบประสาทเกณฑ์ความรุนแรงของ AZOOR : ค่าสายตาที่แก้ไขแล้วของตาข้างที่ดีกว่า < 0.3 (แนวทางการวินิจฉัยของสมาคมจักษุแพทย์ญี่ปุ่น)
จอประสาทตา อักเสบชนิดเบิร์ดช็อต คอรอยด์ อักเสบแบบคดเคี้ยว และ MFC
เบิร์ดช็อต (การจัดการระยะยาว)
เริ่มด้วยเพรดนิโซโลน 0.5-1 มก./กก./วัน
ไมโคฟีโนเลต โมเฟทิล (MMF) 2-3 กรัม/วัน (ยากดภูมิคุ้มกันอันดับแรก)
เมโธเทรกเซท (MTX) 10-25 มก./สัปดาห์อะซาไธโอพรีน (AZA) 1-3 มก./กก./วันกรณีดื้อต่อการรักษา: Adalimumab (93.2% ใช้เป็นยาชีววัตถุ ทางเลือกแรก)
หากไม่รักษา 16-22% จะมีสายตา ≤0.1 ภายใน 10 ปี
โรคคอรอยด์อักเสบแบบคดเคี้ยว (การจัดการระยะยาว)
Prednisolone 40-80 มก./วัน เป็นขนาดเริ่มต้น (ค่อยๆ ลด)
Azathioprine 1-2.5 มก./กก./วัน (การรักษาคงสภาพทางเลือกแรก)
Mycophenolate mofetil / Methotrexate (ทางเลือกอื่น)
กรณีดื้อต่อการรักษา: คลอแรมบูซิล (มีฤทธิ์แรงที่สุด; ≤0.2 มก./กก./วัน ต้องตรวจเลือดทุกสัปดาห์)
ยาชีววัตถุ : adalimumab (91.0% แนะนำเป็นตัวเลือกแรก)หลังจากคัดกรองวัณโรคแล้ว (ถ้า IGRA เป็นบวก ให้ยาต้านวัณโรคก่อน) จึงเริ่มให้ยากดภูมิคุ้มกัน เนื่องจาก MFC มีแนวทางเรื้อรังที่กลับเป็นซ้ำ ผู้ป่วยหลายรายจึงจำเป็นต้องใช้ยาปรับภูมิคุ้มกันเป็นการรักษาแบบประคับประคองหลังจากค่อยๆ ลดสเตียรอยด์ ลง
ยา ปริมาณที่แนะนำ หมายเหตุพิเศษ เมโธเทรกเซท (MTX)10–25 มก./สัปดาห์ ใช้ร่วมกับกรดโฟลิก 1 มก./วัน ติดตามพิษต่อตับ อะซาไธโอพรีน (AZA)1–3 มก./กก./วัน แนะนำตรวจสอบกิจกรรม TPMT ระวังการกดไขกระดูก ไมโคฟีโนเลต โมเฟทิล (MMF) 1-3 กรัม/วัน อาการทางระบบทางเดินอาหารเป็นผลข้างเคียงที่พบบ่อย ไซโคลสปอริน (CsA)3-5 มก./กก./วัน จำเป็นต้องติดตามการทำงานของไตและความดันโลหิต อะดาลิมูแมบ 40 มก./2 สัปดาห์ (ฉีดใต้ผิวหนัง) กรณีดื้อยาหรือพึ่งสเตียรอยด์ ต้องตรวจคัดกรองวัณโรค
CNV เป็นภาวะแทรกซ้อนที่สำคัญที่สุดที่ส่งผลต่อพยากรณ์การมองเห็น และพบได้บ่อยใน PIC , MFC และคอรอยด์ อักเสบแบบคดเคี้ยว
โรค อัตราการเกิด CNV การรักษา PIC 40–76% การฉีดยา anti-VEGF เข้าแก้วตา (bevacizumab, ranibizumab, aflibercept) ร่วมกับ steroid กลยุทธ์ OCTA PRN MFC สูงสุด 60% การฉีดยา anti-VEGF เข้าแก้วตา + การรักษาด้วยการปรับภูมิคุ้มกัน โรคคอรอยด์ อักเสบแบบคดเคี้ยว สูงสุด 35% การฉีดยา anti-VEGF (bevacizumab, ranibizumab) เข้าแก้วตา MEWDS ・APMPPE พบได้น้อย Anti-VEGF (หากยืนยันว่ามี CNV ) Birdshot พบได้น้อย การรักษาด้วยยากดภูมิคุ้มกันทั่วร่างกาย + Anti-VEGF เมื่อมี CNV
Q
การรักษาด้วย anti-VEGF เพียงอย่างเดียวเพียงพอสำหรับ CNV หรือไม่?
A
CNV อักเสบ (iCNV M) แตกต่างจาก CNV ในจอประสาทตา เสื่อมตามอายุ การควบคุมการอักเสบพื้นฐานก็สำคัญในการป้องกันการกลับเป็นซ้ำของ CNV ใน PIC และ MFC แนวทางสองทิศทางด้วย anti-VEGF และสเตียรอยด์ (หรือยากดภูมิคุ้มกัน) ถือว่ามีประสิทธิภาพ ในขณะที่ anti-VEGF เพียงอย่างเดียวยังมีความเสี่ยงต่อการกลับเป็นซ้ำ 7, 8) .
ข้อควรระวัง โรคที่เกี่ยวข้อง การคัดกรองวัณโรคเป็นลำดับแรก (ก่อนกดภูมิคุ้มกัน) คอรอยด์ อักเสบแบบเซอร์พิจิโนซา / MFCพิจารณา HLA-A29 (การวินิจฉัย) เบิร์ดช็อต (ความไวต่ำในคนญี่ปุ่น) ความเสี่ยงความดันลูกตา สูงจากการปลูกถ่ายสเตียรอยด์ เบิร์ดช็อต (สูงถึง 40% ต้องตัดเนื้อเยื่อ trabecular) ความเสี่ยงการกดไขกระดูกและมะเร็งจากคลอแรมบูซิล คอรอยด์ อักเสบแบบคดเคี้ยว (ต้องตรวจเลือดทุกสัปดาห์)การกลับมาเป็นซ้ำหลังติดเชื้อหรือวัคซีนโควิด-19 PIC และ MEWDS (มีรายงานการกลับมาเป็นซ้ำ)การจัดการฉุกเฉินเมื่อมีภาวะหลอดเลือดสมองอักเสบ APMPPE (ปวดศีรษะ อาการทางระบบประสาท → ทำ MRI สมองฉุกเฉิน)
Q
ควรตรวจอะไรเป็นอันดับแรกเมื่อใช้ยากดภูมิคุ้มกัน?
A
การตรวจที่จำเป็นก่อนเริ่มยากดภูมิคุ้มกันสำหรับกลุ่มอาการจุดขาวมีดังนี้: ① การแยกวัณโรคด้วย IGRA (Quantiferon) (สำคัญที่สุดในคอรอยด์ อักเสบแบบ serpentine), ② การคัดกรองไวรัสตับอักเสบด้วย HBs antigen, HBc antibody และ HCV antibody (เพื่อป้องกันการกลับมาทำงานอีกครั้งจากการกดภูมิคุ้มกัน), ③ เอกซเรย์ปอดและ CT (เพื่อแยกวัณโรคและซาร์คอยโดซิส ), ④ การนับเม็ดเลือดสมบูรณ์และการตรวจการทำงานของตับและไต (เพื่อตรวจค่าพื้นฐาน) สำหรับยาชีววัตถุ เช่น adalimumab การคัดกรองวัณโรคก็จำเป็นตามเอกสารกำกับยาด้วย19, 20) .
Q
จำนวนครั้งและตารางการให้ยา anti-VEGF ถูกกำหนดอย่างไร?
A
แตกต่างจากจอประสาทตา เสื่อมตามอายุ CNV อักเสบ (iCNV M) อาจยุบตัวได้เองเมื่อควบคุมการอักเสบได้ โดยทั่วไปใช้กลยุทธ์ PRN (ให้เมื่อจำเป็น) โดยให้ทุกครั้งที่ตรวจพบ CNV ที่ยังทำงานอยู่ด้วย OCT -A อาจให้ยาโหลดเริ่มต้น (3 ครั้งติดต่อกัน) แต่จำนวนครั้งที่ให้อาจลดลงเมื่อใช้ร่วมกับการรักษาด้วยยากดภูมิคุ้มกัน ความเสี่ยงของการกลับเป็นซ้ำสูงหากใช้ anti-VEGF เพียงอย่างเดียว ดังนั้นแนวทางสองทิศทางร่วมกับการควบคุมการอักเสบพื้นฐานจึงสำคัญ 7, 8) .
โรคแต่ละชนิดในกลุ่มอาการจุดขาวเป็นที่ทราบว่ามีความสัมพันธ์กับโรคทางระบบหรือการติดเชื้อเฉพาะ ดังนั้นการตรวจคัดกรองอย่างเป็นระบบเพื่อแยกสาเหตุทางระบบจึงสำคัญก่อนการรักษา
โรค โรคหรือภาวะทางระบบที่เกี่ยวข้อง ความสำคัญทางคลินิก APMPPE หลอดเลือดสมองอักเสบ (MCAT) · การติดเชื้อสเตรปโตค็อกคัส · ไวรัส EB ปวดศีรษะ · อาการทางระบบประสาท → MRI สมองด่วน Birdshot HLA-A29 (80-98% ในคนผิวขาว) · คล้ายซาร์คอยโดซิส การตรวจ HLA ช่วยในการวินิจฉัย (ความไวต่ำในคนญี่ปุ่น) คอรอยด์ อักเสบแบบคดเคี้ยววัณโรค (SLC) · HLA-B7/A2 IGRA บวก → หลักการให้ยาต้านวัณโรคก่อน PIC ซาร์คอยโดซิส · HLA-DRB1*15พิจารณาเอกซเรย์คอมพิวเตอร์ทรวงอกและการวัด ACE MFC IL-10 แฮพลอไทป์ · EB V · ซาร์คอยโดซิส ประเมินการตรวจร่างกายทั่วร่างกายซ้ำในกรณีเรื้อรังที่กลับเป็นซ้ำ MEWDS การติดเชื้อ COVID-19 · หลังการฉีดวัคซีน · HLA-B51 การติดเชื้อ SARS-CoV-2 ทำหน้าที่เป็นตัวกระตุ้นภูมิคุ้มกัน AZOOR โรคฮาชิโมโตะ โรคปลอกประสาทเสื่อมแข็ง โรคภูมิต้านตนเอง พิจารณาตรวจการทำงานของต่อมไทรอยด์และตรวจแอนติบอดีตนเอง
ปัจจุบัน APMPPE ถูกเข้าใจในภาพรวมร่วมกับโรคจุดรับภาพชนิดพลาคอยด์เรื้อรัง (PPM ) และจอประสาทตา อักเสบชนิดพลาคอยด์รุนแรง (RPC ) ใน “สเปกตรัมของจอประสาทตา อักเสบชนิดพลาคอยด์” ในสามโรคนี้ OCT -A แสดงรูปแบบร่วมกันของช่องว่างการไหลของหลอดเลือดฝอยคอรอยด์ ซึ่งบ่งชี้ว่าภาวะขาดเลือดของแผ่นหลอดเลือดฝอยคอรอยด์ เป็นพื้นฐานทางพยาธิวิทยาร่วมกัน5) .
Klufas และคณะ (2017) รายงานว่า OCT -A ตรวจพบช่องว่างการไหลของหลอดเลือดฝอยคอรอยด์ ใน APMPPE , PPM และ RPC โดยมีความสอดคล้องสูงกับ FA และ ICGA ซึ่งสนับสนุนแนวคิดสเปกตรัมของจอประสาทตา อักเสบชนิดพลาคอยด์5) .
การเปลี่ยนแปลงแบบเม็ดที่โฟเวีย (foveal granularity) เป็นลักษณะวินิจฉัยที่พบใน 74-96% ของผู้ป่วย MEWDS และอาจคงอยู่เป็นลักษณะเดียวหลังจากจุดขาวหายไป การถ่ายภาพเรืองแสงอัตโนมัติอินฟราเรดใกล้ (NIR-FAF ) แสดงรูปแบบเม็ดที่โฟเวียที่มีลักษณะเฉพาะ9) .
PIC และ MFC (MFCwP) มีพื้นฐานทางพันธุกรรมร่วมกัน (IL-10 haplotype · HLA-DRB1*15) และถือเป็นฟีโนไทป์ที่แตกต่างกันของสเปกตรัมโรคเดียวกัน จุดแยกหลักคือการมีหรือไม่มี vitritis และการอักเสบของช่องหน้าม่านตา รวมถึงการกระจายของรอยโรค1, 3) .
จุดแยก PIC MFC (MFCwP) Vitritis ไม่มี มี (จุดแยกสำคัญ) การอักเสบของช่องหน้าลูกตา ไม่มี เล็กน้อย การกระจายของรอยโรค จำกัดเฉพาะขั้วหลัง ขั้วหลัง + บริเวณรอบนอกส่วนกลาง ขนาดรอยโรค 100–300 ไมโครเมตร 45–350 ไมโครเมตร อัตราการเกิด CNV ร่วม 40–76% สูงสุด 60%
PIC กับ MFC
หญิงสาวสายตาสั้น ที่มีรอยโรคเล็กที่ขั้วหลัง ไม่มี vitritis → PIC มีโอกาสมากที่สุด
รอยโรคคล้ายกันร่วมกับ vitritis หรือ anterior chamber inflammation → MFC (MFCwP)
โรคทั้งสองอยู่ในกลุ่ม AZOOR complex ต้องติดตามระยะยาวและตรวจคัดกรอง CNV เป็นระยะ
ความสัมพันธ์ระหว่าง Birdshot กับ HLA-A29 เป็นหนึ่งในความสัมพันธ์ทางพันธุกรรมที่แข็งแกร่งที่สุดในโรคใดๆ โดยเพิ่มความเสี่ยงสัมพัทธ์ 50–224 เท่าในผู้ป่วยผิวขาว4) อย่างไรก็ตาม เนื่องจากผู้ที่มี HLA-A29 พบน้อยในญี่ปุ่น ความไวของการตรวจ HLA-A29 ในการวินิจฉัยจึงมีจำกัด การวินิจฉัยควรเน้นที่ผลการตรวจทางคลินิกตามเกณฑ์ SUN 2021 (ผลตรวจจอตา, การอักเสบของ anterior chamber เล็กน้อย, vitritis)10)
AZOOR เชื่อว่าเกิดจากปัจจัยทางพันธุกรรม (เช่น IL-10 haplotype) ร่วมกับตัวกระตุ้นจากสิ่งแวดล้อม เช่น การติดเชื้อไวรัส วัคซีน หรือยา และเข้าใจว่าเป็นส่วนหนึ่งของ AZOOR complex ร่วมกับ MEWDS , PIC , AMN และ AIBSE3) ผู้ป่วย MEWDS หลังติดเชื้อหรือรับวัคซีน COVID-19 เพิ่มขึ้นทั่วโลก ชี้ว่า SARS-CoV-2 อาจทำหน้าที่เป็นตัวกระตุ้นภูมิคุ้มกัน11)
Q
กลุ่มอาการจุดขาวสามารถเกิดขึ้นหลังการติดเชื้อโควิด-19 หรือการฉีดวัคซีนได้หรือไม่?
A
ได้ มีรายงานหลายกรณีของ MEWDS , PIC และคอรอยด์ อักเสบแบบคดเคี้ยวหลังการติดเชื้อโควิด-19 ซึ่งบ่งชี้ว่าการติดเชื้อ SARS-CoV-2 อาจทำหน้าที่เป็นตัวกระตุ้นภูมิคุ้มกัน11, 12) สำหรับ MEWDS มีการทบทวนอย่างเป็นระบบใน 27 รายหลังการฉีดวัคซีนโควิด-19 โดยวัคซีน mRNA (Pfizer-BioNTech) พบบ่อยที่สุด ผู้ป่วยที่มีประวัติโรคนี้ควรปรึกษาจักษุแพทย์เกี่ยวกับการติดตามก่อนและหลังการฉีดวัคซีน
Q
เมื่อสงสัยกลุ่มอาการจุดขาวเป็นครั้งแรก ลำดับความสำคัญของการตรวจที่ควรทำคืออะไร?
A
เมื่อสงสัยกลุ่มอาการจุดขาวเป็นครั้งแรก ลำดับความสำคัญของการตรวจที่แนะนำคือ ① FAF + OCT MEWDS การประเมินโซน ellipsoid และการยกตัวใต้ RPE ใน PIC ) → ② OCT -ACNV ระยะแรกและการประเมิน flow void ของคอรอยด์ ) → ③ FA + ICGA คอรอยด์ อักเสบแบบคดเคี้ยว ควรให้ความสำคัญกับ IGRA (เพื่อแยกวัณโรค) ก่อน FA หากสงสัย AZOOR จำเป็นต้องทำ ERG ( multifocal)1, 2)
蛇行状脈絡膜炎
乳頭周囲から蛇行状に進展する慢性脈絡膜炎。結核との鑑別が最重要課題。
Testi I, Modugno RL, Pavesio C. Multimodal imaging supporting the pathophysiology of white dot syndromes. J Ophthalmic Inflamm Infect. 2021;11:32.
日本眼炎症学会・日本眼科学会. ぶどう膜炎診療ガイドライン(13〜18節:APMPPE ・MEWDS ・PIC ・多発性脈絡膜炎・バードショット・蛇行状脈絡膜炎・AZOOR ). 日本眼科学会雑誌. 2019;123(6):635-696.
Jampol LM, Becker KG. White spot syndromes of the retina: a hypothesis based on the common genetic hypothesis of autoimmune/inflammatory disease. Am J Ophthalmol. 2003;135(3):376-379.
Agrawal R, et al. The role of HLA-A29 in birdshot chorioretinopathy and immune checkpoint inhibitor-related uveitis. Am J Ophthalmol. 2025. doi:10.1016/j.ajo.2024.01.007
Klufas MA, Phasukkijwatana N, Iafe NA, et al. Optical coherence tomography angiography reveals choriocapillaris flow reduction in placoid chorioretinitis. Ophthalmol Retina. 2017;1(1):77-91.
Stattin M, Forster J, Ahmed D, Krepler K, Ansari-Shahrezaei S. Swept Source-Optical Coherence Tomography Angiography for Management of Secondary Choroidal Neovascularization in Punctate Inner Choroidopathy. Case Rep Ophthalmol. 2021;12:232-238.
Spaide RF, Goldberg N, Freund KB. Redefining multifocal choroiditis and panuveitis and punctate inner choroidopathy through multimodal imaging. Retina. 2013;33(7):1315-1324.
Leclaire MD, Clemens CR, Eter N, Mihailovic N. Choroidale Neovaskularisation infolge einer “punctate inner choroidopathy”, dargestellt mittels optischer Kohärenztomographie-Angiographie. Ophthalmologe. 2021;118:842-846.
Mantovani A, Invernizzi A, Staurenghi G, Herbort CP Jr. Multiple evanescent white dot syndrome: a multimodal imaging study of foveal granularity. Ocul Immunol Inflamm. 2019;27(1):141-147.
Standardization of Uveitis Nomenclature (SUN) Working Group. Classification criteria for birdshot chorioretinitis. Am J Ophthalmol. 2021;228:65-71.
Chen N, Mandell M, Arjmand P. Multimodal imaging findings of multiple evanescent white dot syndrome in COVID-19 patients. IDCases. 2024;38:e02110.
Seddigh S, Pinto A, Zaki AM, Gupta RR. Serpiginous choroiditis after COVID-19 infection. J Vitreoretinal Dis. 2025;9(2):246-252.
Pakzad-Vaezi K, Khaksari K, Chu Z, Van Gelder RN, Wang RK, Pepple KL. Swept-source OCT angiography of serpiginous choroiditis. Ophthalmol Retina. 2018;2(7):712-719.
Pepple KL, Chu Z, Weinstein J, Munk MR, Van Gelder RN, Wang RK. Use of en face swept-source optical coherence tomography angiography in identifying choroidal flow voids in 3 patients with birdshot chorioretinopathy. JAMA Ophthalmol. 2018;136(11):1288-1292. doi:10.1001/jamaophthalmol.2018.3474. PMID:30128478. PMCI D:PMC6248174
Khochtali S, Dridi T, Abroug N, et al. Swept-source optical coherence tomography angiography shows choriocapillaris flow reduction in multiple evanescent white dot syndrome. J Curr Ophthalmol. 2020;32(2):211-215.
Yeh S, Forooghian F, Wong WT, et al. Fundus autofluorescence imaging of the white dot syndromes. Arch Ophthalmol. 2010;128(1):46-56.
Minos E, Barry RJ, Southworth S, et al. Birdshot chorioretinopathy: current knowledge and new concepts in pathophysiology, diagnosis, monitoring and treatment. Orphanet J Rare Dis. 2016;11(1):61.
Maleki A, Maldonado Cerda A, Garcia CM, et al. Chlorambucil combination therapy in refractory serpiginous choroiditis: a cure? Am J Ophthalmol Case Rep. 2021;21:101014.
Niederer RL, Al-Janabi A, Engelbrecht C, et al. Immunomodulatory therapy prescribing practices for non-infectious uveitis: a survey of international experts. Br J Ophthalmol. 2024;108:482-489.
Tomkins-Netzer O, et al. Treatment of non-infectious uveitis with biologics: a survey of the International Ocular Inflammation Society. Br J Ophthalmol. 2022;106:482-488.