
Uveítis Infecciosa
Puntos clave de un vistazo
Sección titulada «Puntos clave de un vistazo»1. ¿Qué es la uveítis infecciosa?
Sección titulada «1. ¿Qué es la uveítis infecciosa?»La uveítis es un término general para la inflamación intraocular. Según la etiología, se clasifica ampliamente en uveítis exógena (infecciosa) y uveítis endógena (no infecciosa). La uveítis infecciosa se refiere a la inflamación intraocular causada directa o indirectamente por mecanismos inmunomediados por patógenos como bacterias, virus, hongos y parásitos. La incidencia anual de uveítis se estima en 17–52 por 100,000 habitantes, y la prevalencia en 38–714 por 100,000 habitantes 1,16).
En una encuesta epidemiológica realizada por la Sociedad Japonesa de Inflamación Ocular en 2002 (3,060 casos), la uveítis infecciosa representó aproximadamente el 16% del total 1,7). Las principales enfermedades incluyeron iritis herpética 3.6%, endoftalmitis bacteriana 3.8%, necrosis retiniana aguda (ARN) 1.3%, toxoplasmosis ocular 1.1%, toxocariasis ocular 1.1%, retinitis por CMV 0.8% y uveítis asociada a HTLV-1 1.0%. A nivel internacional, se informa que la toxoplasmosis y la uveítis tuberculosa representan más del 50% de la uveítis infecciosa en países en desarrollo 2,13), mostrando diferencias regionales marcadas 8).
Identificar la causa de la uveítis infecciosa es importante porque la estrategia de tratamiento difiere fundamentalmente de la uveítis no infecciosa. La uveítis no infecciosa se trata principalmente con inmunosupresión (esteroides y fármacos inmunomoduladores), mientras que la uveítis infecciosa requiere primero un tratamiento específico contra el patógeno, y la administración imprudente de esteroides puede empeorar rápidamente la enfermedad.
2. Clasificación
Sección titulada «2. Clasificación»2-1. Clasificación por Localización
Sección titulada «2-1. Clasificación por Localización»La uveítis se clasifica en los siguientes cuatro tipos según el sitio principal de inflamación (clasificación del Grupo de Trabajo SUN):
| Clasificación | Sitio | Enfermedades representativas (infecciosas) |
|---|---|---|
| Uveítis anterior | Iris y cuerpo ciliar (iritis, iridociclitis) | Iritis por HSV/VZV, uveítis anterior por CMV, enfermedad de Lyme |
| Uveítis intermedia | Vítreo, pars plana | Uveítis asociada a HTLV-1, enfermedad de Lyme |
| Uveítis posterior | Retinocoroides, vítreo posterior | Retinitis por CMV, toxoplasmosis ocular, toxocariasis ocular |
| Panuveítis | De espesor total | ARN, tuberculosa, sifilítica, endoftalmitis fúngica |
2-2. Clasificación por patógeno
Sección titulada «2-2. Clasificación por patógeno»La uveítis infecciosa se clasifica en cuatro grupos según el tipo de patógeno.
La familia de los herpesvirus (HHV-1 a 8) es la más frecuente, siendo HSV-1/2, VZV, CMV y HTLV-1 clínicamente importantes. Según el estado inmunitario del huésped, se presentan diversos cuadros clínicos: en inmunocompetentes, HSV/VZV causan uveítis anterior y ARN; en inmunodeprimidos, son típicos la retinitis por CMV y la PORN.
Bacteriana
Sección titulada «Bacteriana»Los principales patógenos incluyen Mycobacterium tuberculosis, Treponema pallidum (sífilis), Bartonella (enfermedad por arañazo de gato) y Borrelia (enfermedad de Lyme). En la endoftalmitis bacteriana endógena, son frecuentes los bacilos gramnegativos (p. ej., Escherichia coli, Klebsiella), con progresión rápida y mal pronóstico.
Fúngica
Sección titulada «Fúngica»Candida, Aspergillus y Cryptococcus causan infecciones endógenas en huéspedes inmunocomprometidos (p. ej., catéter venoso central, inmunosupresión, infección por VIH). La endoftalmitis tras candidemia es particularmente problemática.
Parasitaria
Sección titulada «Parasitaria»La toxoplasmosis ocular (Toxoplasma gondii) y la toxocariasis ocular (Toxocara canis/cati) son enfermedades representativas. La toxoplasmosis puede reactivarse incluso después de una infección adquirida en adultos, causando linfadenopatía y retinitis coroidea adquirida.
2-3. Clasificación por vía de infección
Sección titulada «2-3. Clasificación por vía de infección»| Clasificación | Vía de infección | Enfermedades representativas |
|---|---|---|
| Endógena | Diseminación hematógena (otros órganos → ojo) | Endoftalmitis bacteriana, endoftalmitis fúngica, tuberculosis, sífilis, retinitis por CMV |
| Exógeno | Invasión directa (trauma/cirugía) | Endoftalmitis infecciosa postoperatoria, endoftalmitis postraumática |
3. Descripción general de la uveítis viral
Sección titulada «3. Descripción general de la uveítis viral»La inflamación de la úvea, la retina y el vítreo en la que intervienen virus se denomina uveítis viral. Los herpesvirus humanos (HHV) tienen una fuerte afinidad por el tejido retiniano y causan diversas enfermedades oculares. La uveítis viral se caracteriza por presentar cuadros clínicos diversos según la inmunidad del huésped, debido a la toxicidad viral directa y la inflamación desencadenada por la respuesta inmune. La detección exhaustiva mediante PCR de líquidos intraoculares ha mejorado enormemente la tasa de diagnóstico.
3-1. Patógenos de la familia de los herpesvirus y lesiones oculares
Sección titulada «3-1. Patógenos de la familia de los herpesvirus y lesiones oculares»| Virus | Lesiones oculares en pacientes inmunocompetentes | Lesiones oculares en pacientes inmunocomprometidos |
|---|---|---|
| HSV-1/2 (HHV-1/2) | Iridociclitis herpética, ARN | PORN (raro) |
| VZV (HHV-3) | Herpes zoster oftálmico, iridociclitis herpética, ARN | PORN |
| CMV (HHV-5) | Endoteliitis corneal, uveítis anterior por CMV | Retinitis por CMV, uveítis por recuperación inmune (IRU) |
| VEB (HHV-4) | Uveítis leve (rara) | Lesiones similares a ARN (raras) |
| HTLV-1 | Uveítis intermedia a panuveítis (opacidades vítreas en velo) | Ídem izquierda (grave) |
| Virus de la rubéola | Asociación con iridociclitis heterocrómica de Fuchs | ─ |
3-2. Necrosis retiniana aguda (ARN)
Sección titulada «3-2. Necrosis retiniana aguda (ARN)»La ARN se presenta como iridociclitis aguda con precipitados queráticos pigmentados y es una retinitis necrosante en la que las lesiones granulares de color blanco amarillento en el fondo periférico se fusionan y expanden rápidamente. El VZV es el más común (a menudo casos graves), seguido del HSV-1/2. El desprendimiento de retina regmatógeno con desgarros retinianos ocurre en una alta tasa (aproximadamente 75%), y el pronóstico visual es malo18).
Criterios diagnósticos de ARN de la Sociedad Japonesa de Inflamación Ocular (Grupo de diagnóstico definitivo):
- Hallazgos oculares iniciales: ① células en cámara anterior o KP en grasa de carnero, ② una o más lesiones amarillo-blancas (periféricas), ③ arteritis retiniana, ④ hiperemia del disco óptico, ⑤ opacidades vítreas inflamatorias, ⑥ elevación de la presión intraocular; ① y ② son esenciales.
- Ítems de progresión: uno o más de expansión circunferencial rápida, desgarro/desprendimiento de retina, oclusión vascular, atrofia óptica, respuesta a fármacos antiherpéticos.
- Prueba de líquido intraocular: PCR de humor acuoso o vítreo positiva para HSV-1, HSV-2 o VZV.
El grupo de diagnóstico clínico (que no requiere prueba de líquido intraocular) se puede diagnosticar cuando están presentes los hallazgos iniciales ① y ②, más dos ítems de ③ a ⑥ y un ítem de progresión.
3-3. Retinitis por CMV
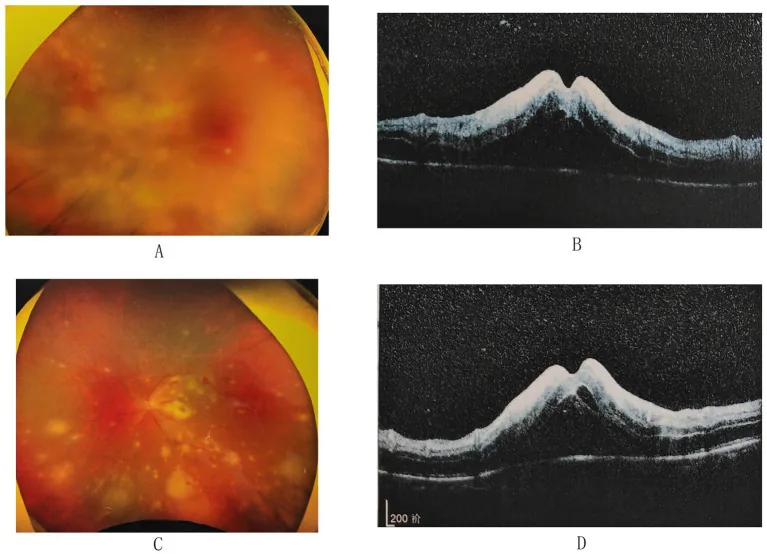
Sección titulada «3-3. Retinitis por CMV»El CMV es una infección oportunista que ocurre en pacientes inmunocomprometidos, principalmente con SIDA, y es más frecuente en pacientes con SIDA cuyo recuento de linfocitos T CD4 positivos ha descendido a 50–100/µL 20). Existen tres tipos clínicos: (1) tipo granular periférico (lesiones en abanico con gránulos blancos), (2) tipo vasculitis del polo posterior (hemorragia y edema), y (3) tipo vasculitis en rama de árbol helado (blanqueamiento perivascular de grandes vasos), que a menudo coexisten. La uveítis por recuperación inmune (IRU) tras la recuperación inmunitaria es una complicación importante 15), y es necesario el manejo oftalmológico después del inicio de la terapia antirretroviral.
3-4. Uveítis asociada a HTLV-1 (HAU)
Sección titulada «3-4. Uveítis asociada a HTLV-1 (HAU)»La HAU ocurre en aproximadamente el 0.1% de los portadores de HTLV-1 y es más común en regiones como Kyushu y Okinawa 12). Los hallazgos característicos incluyen precipitados queráticos granulares blancos, nódulos iridianos, opacidades vítreas en forma de velo, filamentosas o granulares, y depósitos granulares blancos alrededor de los vasos retinianos. El hipertiroidismo se asocia con frecuencia. El pronóstico visual es relativamente bueno, pero puede haber recurrencia tras la reducción o suspensión de los esteroides.
3-5. Virus de la rubéola e iridociclitis heterocrómica de Fuchs
Sección titulada «3-5. Virus de la rubéola e iridociclitis heterocrómica de Fuchs»Se ha sugerido que la iridociclitis heterocrómica de Fuchs (caracterizada por la tríada de heterocromía, iridociclitis y catarata) está asociada con el virus de la rubéola. En el síndrome de rubéola congénita, la infección transplacentaria dentro de los primeros tres meses de embarazo conduce a una retinitis coroidea con aspecto de fondo de ojo en sal y pimienta.
4. Descripción general de la uveítis bacteriana
Sección titulada «4. Descripción general de la uveítis bacteriana»4-1. Uveítis tuberculosa
Sección titulada «4-1. Uveítis tuberculosa»La inflamación intraocular causada por Mycobacterium tuberculosis implica dos mecanismos: infección directa e inmunomediada (reacción de hipersensibilidad). Las formas clínicas son diversas, incluyendo granulomas coroideos (tubérculos), desprendimiento seroso de retina, coroiditis perdigonada, vasculitis y panuveítis.
La IGRA (QuantiFERON®-TB Gold Plus o T-SPOT®.TB) es útil para el diagnóstico. Tenga en cuenta que la prueba de tuberculina puede ser negativa en ancianos y en pacientes con inmunidad celular disminuida, como en el SIDA. En cuanto al pronóstico visual de la uveítis tuberculosa, se ha informado que la mejor agudeza visual corregida es inferior a 3/60 en aproximadamente un tercio de los casos 3). Los criterios de clasificación de la uveítis tuberculosa propuestos por el SUN Working Group (2021) incluyen: (1) uveítis anterior con nódulos iridianos, (2) coroiditis serpiginosa-like, (3) nódulos coroideos (tuberculomas), (4) coroiditis multifocal en casos de tuberculosis sistémica activa y (5) vasculitis retiniana oclusiva 5). En India e Indonesia, aproximadamente el 22,9–48,0% de las uveítis infecciosas se atribuyen a tuberculosis 3,14), lo que destaca su importancia particular en regiones de alta prevalencia de tuberculosis.
4-2. Uveítis sifilítica
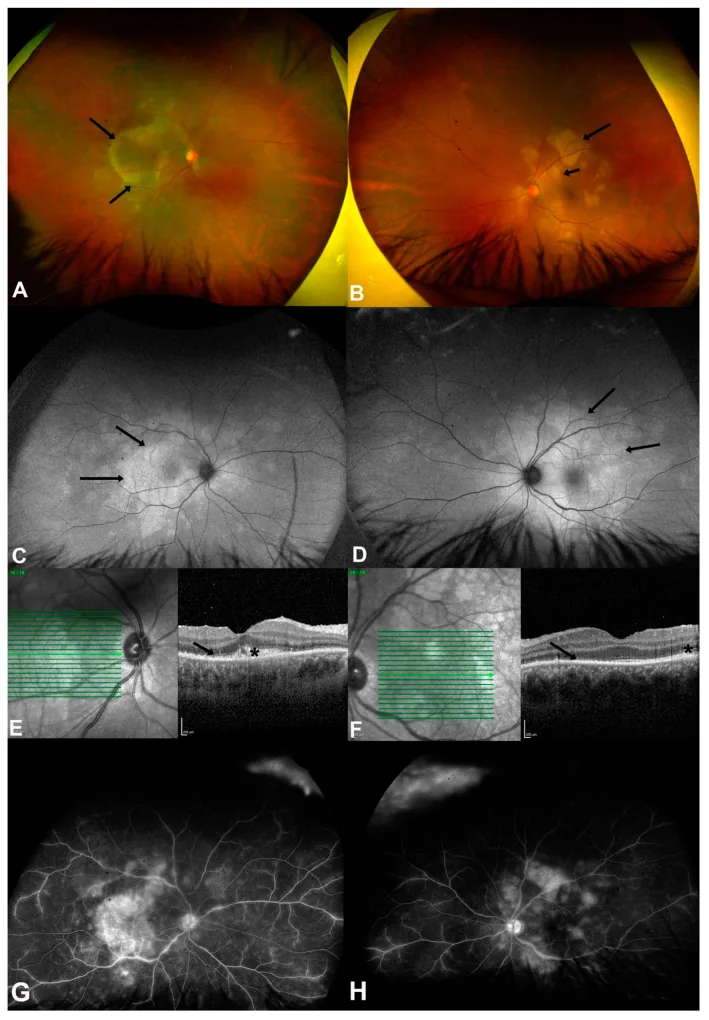
Sección titulada «4-2. Uveítis sifilítica»La inflamación intraocular causada por Treponema pallidum se conoce como la “gran imitadora” y puede presentarse como uveítis anterior, posterior o panuveítis. En los últimos años, se ha observado un resurgimiento global, particularmente entre hombres que tienen sexo con hombres (HSH), y los pacientes coinfectados con VIH tienen aproximadamente el doble de riesgo de sífilis ocular4). A nivel mundial, se reportan anualmente entre 5.7 y 6 millones de nuevas infecciones por sífilis (edades 15–49)4), y la afectación ocular ocurre en aproximadamente el 1–1.5% de los pacientes con sífilis4,10).
El diagnóstico se realiza mediante pruebas serológicas (TPHA, RPR/VDRL), interpretadas con una combinación de métodos treponémicos y no treponémicos. El tratamiento sigue las pautas de neurosífilis: penicilina G benzatínica intravenosa (Aqacillin®) 24 millones de unidades/día durante 10–14 días es de primera línea, con ceftriaxona intravenosa como alternativa. Se debe estar alerta a la reacción de Jarisch-Herxheimer (fiebre y exacerbación de la inflamación dentro de las 24 horas posteriores al tratamiento).
4-3. Enfermedad por arañazo de gato (infección por Bartonella)
Sección titulada «4-3. Enfermedad por arañazo de gato (infección por Bartonella)»Infección causada por Bartonella henselae, siendo el antecedente de contacto con gatos un dato importante en la anamnesis. Los hallazgos de fondo de ojo incluyen neuritis óptica (signo de estrella macular), manchas blancas estrelladas maculares y desprendimiento seroso de retina, presentándose a menudo como uveítis posterior. El diagnóstico se realiza mediante la medición de anticuerpos anti-Bartonella henselae, y se administra tratamiento antibiótico con azitromicina, doxiciclina o rifampicina.
4-4. Enfermedad de Lyme
Sección titulada «4-4. Enfermedad de Lyme»Enfermedad infecciosa causada por espiroquetas del género Borrelia transmitidas por garrapatas, con diversas manifestaciones oculares (uveítis, vasculitis retiniana, neuritis óptica, queratitis, etc.) que aparecen en las etapas 2 a 3. El eritema migratorio crónico es la erupción característica de la etapa 1, y el antecedente de picadura de garrapata es una pista diagnóstica. El diagnóstico se realiza mediante la elevación de anticuerpos IgM séricos por ELISA, y el tratamiento es con antibióticos penicilínicos o tetraciclinas. Se requiere diferenciación de sífilis y sarcoidosis.
4-5. Enfermedad de Hansen (lepra)
Sección titulada «4-5. Enfermedad de Hansen (lepra)»Infección granulomatosa crónica causada por Mycobacterium leprae, con afectación ocular reportada en el 70-80% de los casos (30-40% en pacientes nuevos recientes). Predomina la uveítis anterior granulomatosa crónica, con hallazgos característicos como perlas de iris, atrofia de iris, pupila pequeña y sinequias anteriores periféricas en tienda de campaña. Se utiliza terapia multidroga (rifampicina, dapsona, clofazimina), y se añaden gotas oftálmicas de esteroides cuando hay uveítis.
4-6. Endoftalmitis bacteriana endógena
Sección titulada «4-6. Endoftalmitis bacteriana endógena»La endoftalmitis bacteriana endógena, en la que la infección se disemina por vía hematógena al ojo desde otros órganos (absceso hepático, endocarditis, neumonía, etc.), está causada principalmente por bacilos gramnegativos (Klebsiella, Escherichia coli) y tiene un pronóstico extremadamente malo. Progresa más rápidamente que la infección exógena (postoperatoria) por cocos grampositivos, y es esencial buscar y tratar el foco infeccioso sistémico.
5. Descripción general de la uveítis fúngica
Sección titulada «5. Descripción general de la uveítis fúngica»La endoftalmitis fúngica es mayoritariamente endógena, siendo Candida spp. la más frecuente, y Aspergillus y Cryptococcus también son patógenos importantes.
Principales factores de riesgo:
- Nutrición venosa central (NVC) y catéteres permanentes
- Uso prolongado de antibióticos de amplio espectro
- Inmunosupresión (infección por VIH, trasplante de órganos, neoplasia maligna, quimioterapia)
- Diabetes mellitus
- Uso de drogas intravenosas
La endoftalmitis fúngica se caracteriza por opacidades vítreas blancas esféricas o algodonosas (“opacidades en grumos”) y progresa más lentamente que la endoftalmitis bacteriana. En etapas tempranas puede ser asintomática o presentar solo moscas volantes leves, por lo que es fácil pasarla por alto. Al progresar, aparecen enrojecimiento, dolor ocular y panuveítis. El 30% de las endoftalmitis fúngicas endógenas ocurren en ambos ojos8).
El diagnóstico se realiza mediante cultivo de sangre/punta de catéter, β-D-glucano, medición de antígeno de Candida y cultivo de vítreo. El tratamiento se basa en la combinación de fármacos antifúngicos (voriconazol, anfotericina B, fluconazol) y vitrectomía.
6. Descripción general de la uveítis parasitaria
Sección titulada «6. Descripción general de la uveítis parasitaria»6-1. Toxoplasmosis ocular
Sección titulada «6-1. Toxoplasmosis ocular»Toxoplasma gondii (un protozoo parásito intracelular) infecta aproximadamente a un tercio de la población mundial, y la tasa de positividad de anticuerpos en adultos japoneses se reporta en 20–30% 11). Los felinos son los hospedadores definitivos, y la infección ocurre por ingestión oral de ooquistes de heces de gato o consumo de carne poco cocida.
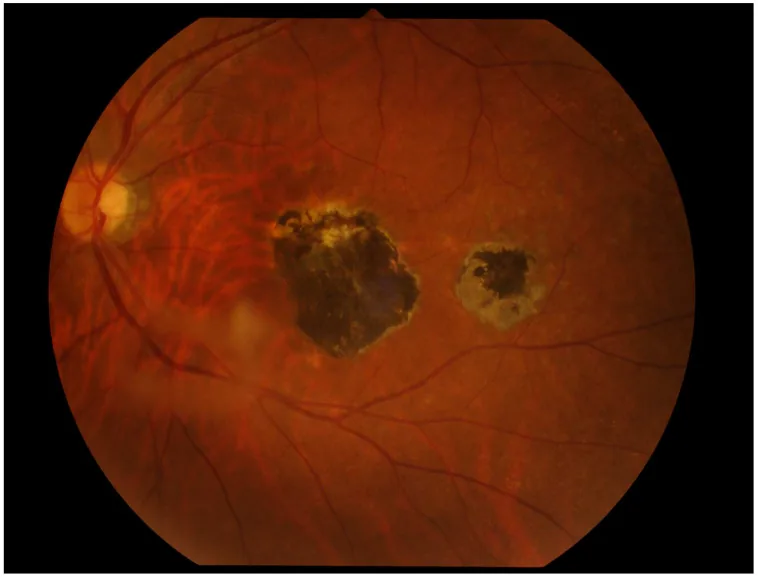
La toxoplasmosis ocular representa aproximadamente el 1% de las causas de uveítis 11). Los hallazgos de fondo de ojo en la infección adquirida son coriorretinitis exudativa blanca a blanco lechosa, mal delimitada en la periferia, y las “lesiones satélite” adyacentes a cicatrices antiguas son hallazgos característicos en la recurrencia. Se acompaña de inflamación de la cámara anterior y opacidades vítreas (“faros en la niebla”). En la infección congénita, se observan cicatrices con proliferación fibrosa gris-blanca central y pigmentación en ambas máculas.
El diagnóstico se basa principalmente en los hallazgos oculares característicos y la medición de anticuerpos séricos (IgG, IgM). El examen del líquido intraocular mediante el coeficiente Q (Goldmann-Witmer) o PCR también es útil. El tratamiento consiste en la administración oral de acetato de espiramicina (acetilespiramicina) o clindamicina 1.2 g/día durante 4 a 6 semanas, combinado con esteroides 0.5 mg/kg/día para controlar las lesiones exudativas.
6-2. Toxocariasis ocular
Sección titulada «6-2. Toxocariasis ocular»Es una enfermedad por migración larval del gusano redondo del perro (Toxocara canis) o del gato (Toxocara cati), y suele ser unilateral. Existen tres tipos: tipo endoftalmitis, tipo masa del polo posterior y tipo masa periférica (el más común), que pueden causar opacidades vítreas severas y desprendimiento de retina. El diagnóstico se realiza mediante la detección de anticuerpos séricos (ELISA Toxocara CHECK®) y hallazgos oculares característicos. El tratamiento incluye antihelmínticos orales (dietilcarbamazina), esteroides orales, y puede requerir criocoagulación, fotocoagulación con láser o vitrectomía.
7. Estrategia diagnóstica
Sección titulada «7. Estrategia diagnóstica»7-1. Puntos clave en la anamnesis
Sección titulada «7-1. Puntos clave en la anamnesis»La anamnesis sistemática es esencial para el diagnóstico de uveítis infecciosa:
- Edad y sexo: La retinitis por CMV es común en pacientes con SIDA (mayoría hombres de 20-40 años), HAU en residentes de Kyushu y Okinawa
- Región y antecedentes de viaje: Viaje a áreas de alta prevalencia de tuberculosis (p. ej., Sudeste Asiático, África)
- Antecedentes de contacto con animales: Gatos (Toxoplasma, Bartonella), Perros (Toxocara)
- Antecedentes dietéticos: Consumo de carne o pescado crudos (Toxoplasma)
- Antecedentes sexuales y pruebas de VIH: Sífilis, CMV
- Estado de inmunosupresión: VIH, neoplasia maligna, trasplante de órgano, uso de inmunosupresores
- Antecedentes de NPT o catéter: Endoftalmitis fúngica
- Antecedentes de herpes zóster o herpes labial: Iritis por VZV o HSV
7-2. Diferenciación por hallazgos oculares
Sección titulada «7-2. Diferenciación por hallazgos oculares»| Hallazgo | Enfermedad infecciosa sugerida |
|---|---|
| KP en grasa de carnero | Iritis por HSV/VZV, ARN, uveítis tuberculosa |
| Uveítis anterior con presión intraocular alta (≥25 mmHg) | Iritis por HSV/VZV, uveítis anterior por CMV |
| Lesiones necróticas blancas confluentes periféricas | ARN (VZV/HSV) |
| Infiltrados blancos con hemorragia del polo posterior | Retinitis por CMV (tipo vasculítico) |
| Opacidades vítreas masivas (progresivas) | Endoftalmitis fúngica |
| Opacidades vítreas en velo o en hebras | Uveítis asociada a HTLV-1 |
| Cicatriz antigua + lesiones satélite | Toxoplasmosis ocular |
| Masa blanca periférica + hebras vítreas | Toxocariasis ocular |
| Iritis granulomatosa + granuloma coroideo | Uveítis tuberculosa, sifilítica |
| Neuritis óptica + estrella macular | Enfermedad por arañazo de gato (Bartonella) |
7-3. Examen sistémico
Sección titulada «7-3. Examen sistémico»| Examen | Enfermedad diana |
|---|---|
| TPHA sérica・RPR/VDRL | Uveítis sifilítica |
| IGRA (QuantiFERON・T-SPOT) | Uveítis tuberculosa |
| Antigenemia por CMV (método C7-HRP)・CMV-PCR | Retinitis por CMV |
| Anticuerpo anti-HTLV-1 | Uveítis asociada a HTLV-1 |
| Anticuerpo anti-VIH / recuento de CD4 | CMV / PORN / sífilis ocular |
| β-D-glucano / antígeno de Candida | Endoftalmitis fúngica |
| IgG/IgM anti-Toxoplasma | Toxoplasmosis ocular |
| Anticuerpo anti-Toxocara (ELISA) | Toxocariasis ocular |
| Anticuerpo anti-Bartonella henselae | Enfermedad por arañazo de gato |
| Hemocultivo y ecocardiografía | Endoftalmitis bacteriana endógena |
7-4. Examen de líquido intraocular (humor acuoso y vítreo)
Sección titulada «7-4. Examen de líquido intraocular (humor acuoso y vítreo)»El examen con líquido intraocular es el método de confirmación más importante para el diagnóstico de uveítis infecciosa, y se obtienen muestras mediante paracentesis de la cámara anterior (recolección de humor acuoso) o vitrectomía (recolección de humor vítreo)9).
Método de PCR
Sección titulada «Método de PCR»Se extrae ADN del humor acuoso o vítreo y se detecta el ADN de cada patógeno mediante PCR. La PCR múltiple en tiempo real permite la detección integral de múltiples virus con una pequeña cantidad de muestra y es particularmente útil para el diagnóstico diferencial de ARN19).
Kit de uveítis infecciosa (atención médica avanzada): Puede detectar simultáneamente HSV-1/2, VZV, CMV, EBV, HHV-6/7, HTLV-1, ADN de Toxoplasma gondii, etc., y se utiliza para diagnosticar coinfecciones con múltiples patógenos y casos refractarios. Sin embargo, tenga en cuenta que la PCR puede no detectar la retinitis por CMV en la etapa inicial (antes de que aparezcan células inflamatorias en la cámara anterior).
Relación de Goldmann-Witmer (valor Q, tasa de anticuerpos)
Sección titulada «Relación de Goldmann-Witmer (valor Q, tasa de anticuerpos)»Este método detecta la presencia de producción de anticuerpos específicos contra patógenos dentro del ojo y se calcula mediante la siguiente fórmula:
Valor Q = (Título de anticuerpos virales en líquido intraocular ÷ Nivel de IgG en líquido intraocular) ÷ (Título de anticuerpos virales en suero ÷ Nivel de IgG en suero)
- Valor Q >1: Posible producción local de anticuerpos dentro del ojo
- Valor Q ≥6: Se confirma una producción local significativa de anticuerpos, lo que permite identificar el virus como agente causal
Tenga en cuenta que el valor Q puede subestimarse en los primeros 10 días del inicio debido a que la producción de anticuerpos intraoculares es insuficiente. El diagnóstico etiológico no puede basarse únicamente en los títulos de anticuerpos séricos (la mayoría de los adultos son seropositivos debido a infecciones pasadas)6).
Flujo de uso de PCR en líquido intraocular
Sección titulada «Flujo de uso de PCR en líquido intraocular»眼内炎症患者 ├─ ウイルス性疑い(高眼圧・前房炎症・壊死性網膜炎) │ → 前房水PCR(HSV/VZV/CMV)+ Q値 ← 第一選択 │ ─ 前房水で陰性かつ壊死性病変 → 硝子体液PCR │ ─ 免疫不全者 → マルチプレックスPCR(先進医療) ├─ 寄生虫疑い(衛星病巣・周辺部腫瘤) │ → 眼内液Q値(Toxoplasma)または眼内液PCR ├─ 真菌疑い(塊状混濁・リスク因子あり) │ → 硝子体液培養 + β-D-グルカン(血液) └─ 細菌疑い(急速進行・IVH歴) → 硝子体液グラム染色・培養(至急)8. Principios del tratamiento
Sección titulada «8. Principios del tratamiento»8-1. Tratamiento específico según el patógeno
Sección titulada «8-1. Tratamiento específico según el patógeno»| Patógeno | Tratamiento de primera línea | Notas |
|---|---|---|
| VHS (ARN, iritis) | ACV 10 mg/kg ×3 veces IV durante 2 semanas → VACV 1,000 mg ×3 veces/día oral | Combinar con gotas oftálmicas de esteroides y IV para antiinflamación |
| VZV (ARN, iritis) | ACV 10-15 mg/kg x3 IV + VACV oral | PORN sigue el tratamiento de CMV |
| CMV (retinitis) | GCV 5 mg/kg x2 IV durante 2-3 semanas (inducción) → VGCV 900 mg x2/día oral (mantenimiento) | La recuperación inmune es el tratamiento curativo |
| CMV (uveítis anterior) | Gel de GCV al 0.15% en gotas oftálmicas (73% de especialistas lo eligen como primera línea) ± VGCV oral | Para curso crónico, considerar tratamiento de mantenimiento de 12 meses (73% de especialistas eligen gel de GCV al 0.15%) 2) |
| Tuberculosis | INH, RFP, PZA, EMB (régimen estándar de 6 meses) | Corticosteroides según sea necesario |
| Sífilis | Bencilpenicilina G 24 millones de unidades/día IV durante 10-14 días | Vigilar la reacción de Jarisch-Herxheimer |
| Hongos (Candida) | Voriconazol o anfotericina B ± vitrectomía | Monitorizar con índice de β-D-glucano |
| Toxoplasma | Acetilspiramicina + esteroide o clindamicina | Precaución en embarazo (usar espiramicina) |
| Toxocara | Dietilcarbamazina + esteroide | Considerar láser/vitrectomía |
| Enfermedad de Lyme | Amoxicilina o doxiciclina durante 3 semanas | Agregar gotas oftálmicas de esteroides para afectación ocular |
| Lepra | MDT (rifampicina, DDS, clofazimina) | Se necesitan esteroides durante la reacción leprosa |
8-2. Uso adecuado de los esteroides
Sección titulada «8-2. Uso adecuado de los esteroides»Cuando se usan esteroides en la uveítis infecciosa, el tratamiento antipatógeno debe preceder o realizarse concomitantemente. El papel de los esteroides es reducir el daño tisular secundario causado por la inflamación, y se utilizan en combinación con el tratamiento patógeno adecuado en muchas uveítis infecciosas como ARN, toxoplasmosis, uveítis tuberculosa y uveítis por enfermedad de Hansen.
Por otro lado, en la retinitis por CMV (una infección oportunista pura), el tratamiento de la enfermedad subyacente (SIDA) para mejorar la función inmunológica es la terapia curativa, y los esteroides generalmente no se usan.
8-3. Midriáticos y manejo de la presión intraocular
Sección titulada «8-3. Midriáticos y manejo de la presión intraocular»Para prevenir sinequias posteriores, se utilizan gotas oftálmicas de tropicamida-fenilefrina (1–6 veces/día) para la inflamación del segmento anterior. Para la presión intraocular elevada (característica de la iritis por HSV/VZV y la uveítis anterior por CMV), se seleccionan fármacos hipotensores oculares como inhibidores de la anhidrasa carbónica y betabloqueantes, pero los fármacos relacionados con prostaglandinas conllevan riesgo de exacerbar la inflamación y deben usarse con precaución.
9. Matriz de riesgo según el estado de inmunosupresión
Sección titulada «9. Matriz de riesgo según el estado de inmunosupresión»| Antecedentes | Patógenos que requieren atención especial | Pruebas prioritarias |
|---|---|---|
| Infección por VIH (CD4 <50/µL) | CMV (retinitis, ARN, PORN), hongos (Cryptococcus), sífilis | PCR de líquido intraocular (multiplex), antígeno de CMV, β-D-glucano |
| Después de trasplante de órgano sólido / uso de inmunosupresores | CMV, hongos (Aspergillus, Candida), VEB | PCR-CMV, β-D-glucano, hemocultivo |
| Neoplasia maligna / después de quimioterapia | Hongos (Candida, Aspergillus), CMV | β-D-glucano, hemocultivo |
| IVH prolongado / colocación de catéter | Endoftalmitis por Candida | β-D-glucano / hemocultivo (consulta oftalmológica obligatoria) |
| Alto riesgo de tuberculosis (antecedentes de viaje/contacto) | Tuberculosis (granuloma coroideo / tipo vasculítico) | IGRA / TC de tórax |
| HSH (hombres que tienen sexo con hombres) / VIH+ | Sífilis (sífilis ocular aprox. 1–1.5%), CMV | Pruebas de TPHA, RPR, VIH |
| Inmunocompetente (mediana edad o mayor) | Iridociclitis por HSV/VZV, ARN | PCR de humor acuoso, valor Q |
| Antecedentes de contacto con niños/mascotas | Toxocara/Toxoplasma | Anticuerpos séricos (ELISA) |
10. Preguntas frecuentes
Sección titulada «10. Preguntas frecuentes»Cuando es difícil diferenciar entre uveítis infecciosa y no infecciosa solo con los hallazgos clínicos, o cuando las pruebas serológicas son negativas a pesar de la sospecha de infección, se considera activamente la punción de la cámara anterior. En particular, cuando se sospecha retinitis necrosante (ARN, PORN, retinitis por CMV), se realiza PCR del líquido intraocular lo antes posible porque el diagnóstico precoz afecta directamente la elección del tratamiento y el pronóstico. La PCR múltiple es útil en casos con PCR negativa en la etapa inicial o casos refractarios.
Primero, se debe realizar rápidamente una PCR del líquido intraocular para identificar el patógeno, e iniciar la terapia antimicrobiana específica tan pronto como se identifique el patógeno. Dado que la interrupción brusca de los esteroides puede causar inflamación de rebote, la dosis debe reducirse cuidadosamente después de iniciar el tratamiento antipatógeno. En particular, cuando se han administrado esteroides solos para la uveítis tuberculosa, el riesgo de reactivación y diseminación de la tuberculosis latente aumenta, por lo que se debe realizar una evaluación sistémica urgente (TC de tórax, IGRA) en colaboración con un neumólogo.
Después del tratamiento, Toxoplasma permanece como quistes resistentes a los fármacos dentro de las lesiones cicatriciales atróficas. La recurrencia ocurre en aproximadamente el 5–30% de los casos, desencadenada por inmunosupresión o embarazo. Para pacientes con recurrencias frecuentes, se puede considerar la profilaxis a largo plazo con trimetoprim-sulfametoxazol. Durante el embarazo, si una mujer embarazada con anticuerpos negativos para Toxoplasma tiene una infección primaria, existe riesgo de transmisión vertical al feto (aproximadamente 40%), por lo que se le debe aconsejar evitar el contacto con heces de gato, tierra y consumo de carne cruda.
11. Artículos relacionados
Sección titulada «11. Artículos relacionados»Uveítis viral
Sección titulada «Uveítis viral»Uveítis bacteriana y otras infecciosas
Sección titulada «Uveítis bacteriana y otras infecciosas»Referencias
Sección titulada «Referencias»- 日本眼炎症学会ぶどう膜炎診療ガイドライン作成委員会. ぶどう膜炎診療ガイドライン. 日眼会誌. 2019;123(6):635–702.
- Thng ZX, Putera I, Testi I, et al. The Infectious Uveitis Treatment Algorithm Network (TITAN) Report 2—global current practice patterns for the management of Cytomegalovirus anterior uveitis. Eye. 2023. https://doi.org/10.1038/s41433-023-02503-3
- Putera I, Schrijver B, ten Berge JCEM, et al. The immune response in tubercular uveitis and its implications for treatment: From anti-tubercular treatment to host-directed therapies. Prog Retin Eye Res. 2023;95:101173.
- Chauhan K, Fonollosa A, Giralt L, et al. Demystifying Ocular Syphilis – A Major Review. Ocul Immunol Inflamm. 2023. https://doi.org/10.1080/09273948.2023.2217246
- Jabs DA, et al. Standardization of Uveitis Nomenclature (SUN) Working Group. Classification Criteria for Tubercular Uveitis. Am J Ophthalmol. 2021;228:142–149.
- 八代成子. ウイルス性ぶどう膜炎の診断と治療. 眼科. 2007;49:1193–1198.
- 大野重昭. ぶどう膜炎の疫学と分類. 日眼会誌. 2019;123(6).
- Tsirouki T, Dastiridou A, Symeon CI, et al. A focus on the epidemiology of uveitis. Ocul Immunol Inflamm. 2018;26(1):2–16.
- 慶野博. 感染性ぶどう膜炎の眼内液診断. 臨床眼科. 2019.
- Oliver SE, Aubin M, Atwell L, et al. Ocular Syphilis — Eight Jurisdictions, United States, 2014–2015. MMWR Morb Mortal Wkly Rep. 2016;65:1185–1188.
- 岡田アナベルあやめ. 眼トキソプラズマ症の診断と治療. 眼科. 2018.
- 中尾久美子. HTLV-1関連ぶどう膜炎の疫学と治療. 日本臨床. 2020.
- La Distia Nora R, et al. Infectious uveitis etiology in developing vs. developed countries. Curr Opin Ophthalmol. 2021.
- Agrawal R, et al. Collaborative Ocular Tuberculosis Study (COTS)—Report 1. Ophthalmology. 2019;126(11):1566–1577.
- 八代成子. CMV網膜炎・免疫回復ぶどう膜炎の管理. 眼科. 2007.
- Kempen JH, et al. The prevalence of uveitis in the United States. Arch Ophthalmol. 2004;122(4):543–557.
- Groen-Hakan F, et al. Diagnostic value of aqueous humor analysis for uveitis. Ocul Immunol Inflamm. 2020.
- 堤雅幸. 急性網膜壊死診断基準(日本眼炎症学会). 日眼会誌. 2020.
- 蕪城俊克. 眼内液PCRによるウイルス性ぶどう膜炎診断. 眼科. 2021.
- Bodaghi B, et al. Blindness prevention in HIV patients: CMV retinitis management update. Prog Retin Eye Res. 2023.
