
Uvéite infectieuse
Points clés en un coup d’œil
Section intitulée « Points clés en un coup d’œil »1. Qu’est-ce que l’uvéite infectieuse ?
Section intitulée « 1. Qu’est-ce que l’uvéite infectieuse ? »L’uvéite (uveitis) est un terme générique désignant une inflammation intraoculaire. Selon la classification étiologique, elle se divise en « uvéite exogène (infectieuse) » et « uvéite endogène (non infectieuse) ». L’uvéite infectieuse (infectious uveitis) fait référence à une inflammation intraoculaire causée directement ou par des mécanismes immunitaires par des agents pathogènes tels que des bactéries, virus, champignons ou parasites. L’incidence annuelle des nouveaux cas d’uvéite est de 17 à 52 pour 100 000 personnes, et la prévalence est de 38 à 714 pour 100 000 personnes1,16).
Selon une enquête épidémiologique menée en 2002 par la Société japonaise d’inflammation oculaire (3 060 cas), les uvéites infectieuses représentaient environ 16 % du total 1,7). Parmi celles-ci, l’iritis herpétique 3,6 %, l’endophtalmie bactérienne 3,8 %, la nécrose rétinienne aiguë (ARN) 1,3 %, la toxoplasmose oculaire 1,1 %, la toxocarose oculaire 1,1 %, la rétinite à CMV 0,8 % et l’uvéite liée au HTLV-1 1,0 % sont les principales maladies. À l’échelle internationale, la toxoplasmose et l’uvéite tuberculeuse représenteraient plus de 50 % des uvéites infectieuses dans les pays en développement 2,13), avec des variations régionales marquées 8).
L’identification de la cause des uvéites infectieuses est cruciale car la stratégie thérapeutique diffère fondamentalement de celle des uvéites non infectieuses. Pour les uvéites non infectieuses, l’immunosuppression (corticostéroïdes, immunomodulateurs) est le traitement principal, tandis que pour les uvéites infectieuses, un traitement spécifique contre l’agent pathogène est indispensable, et l’administration imprudente de corticostéroïdes risque d’aggraver rapidement la maladie.
2. Classification
Section intitulée « 2. Classification »2-1. Classification par localisation
Section intitulée « 2-1. Classification par localisation »L’uvéite est classée en quatre types selon le site principal de l’inflammation (classification du SUN Working Group) :
| Classification | Site | Maladies représentatives (infectieuses) |
|---|---|---|
| Uvéite antérieure | Iris et corps ciliaire (iritis, iridocyclite) | Iritis HSV/VZV, uvéite antérieure à CMV, maladie de Lyme |
| Uvéite intermédiaire | Corps vitré / pars plana du corps ciliaire | Uvéite associée au HTLV-1, maladie de Lyme |
| Uvéite postérieure | Choriorétine et vitré postérieur | Rétinite à CMV, toxoplasmose oculaire, toxocarose oculaire |
| Panuvéite | Toute l’épaisseur | ARN, tuberculeuse, syphilitique, endophtalmie fongique |
2-2. Classification par agent pathogène
Section intitulée « 2-2. Classification par agent pathogène »L’uvéite infectieuse est classée en quatre groupes selon le type d’agent pathogène.
La famille des virus de l’herpès (HHV-1 à 8) est la plus fréquente, et HSV-1/2, VZV, CMV et HTLV-1 sont particulièrement importants en clinique. Selon l’état immunitaire de l’hôte, ils présentent des tableaux cliniques variés : chez les immunocompétents, l’uvéite antérieure et le ARN dus à HSV/VZV sont typiques ; chez les immunodéprimés, la rétinite à CMV et le PORN sont caractéristiques.
Bactérienne
Section intitulée « Bactérienne »Les principaux agents pathogènes sont Mycobacterium tuberculosis, Treponema pallidum (syphilis), Bartonella (maladie des griffes du chat) et Borrelia (maladie de Lyme). Dans l’endophtalmie bactérienne endogène, les bacilles à Gram négatif (E. coli, Klebsiella, etc.) sont fréquents, avec une progression rapide et un mauvais pronostic.
Fongique
Section intitulée « Fongique »Candida, Aspergillus et Cryptococcus provoquent des infections endogènes chez les hôtes immunodéprimés (cathéter veineux central, immunosuppression, infection par le VIH). L’endophtalmie post-candidémie est particulièrement problématique.
Parasitaire
Section intitulée « Parasitaire »La toxoplasmose oculaire (Toxoplasma gondii) et la toxocarose oculaire (Toxocara canis/cati) sont les maladies représentatives. La toxoplasmose peut se réactiver même après une infection acquise à l’âge adulte, provoquant une lymphadénopathie et une rétinochoroïdite acquise.
2-3. Classification par voie d’infection
Section intitulée « 2-3. Classification par voie d’infection »| Classification | Voie d’infection | Maladies représentatives |
|---|---|---|
| Endogène | Dissémination hématogène (autre organe → œil) | Endophtalmie bactérienne, endophtalmie fongique, tuberculose, syphilis, rétinite à CMV |
| Exogène (exogenous) | Pénétration directe (traumatisme, chirurgie) | Endophtalmie infectieuse postopératoire, endophtalmie post-traumatique |
3. Aperçu de l’uvéite virale
Section intitulée « 3. Aperçu de l’uvéite virale »L’inflammation de l’uvée, de la rétine et du vitré impliquant un virus est appelée uvéite virale. Les herpèsvirus humains (HHV) ont une forte affinité pour le tissu rétinien et provoquent diverses maladies oculaires. L’uvéite virale se caractérise par une toxicité virale directe et une inflammation induite par la réponse immunitaire, présentant des tableaux cliniques variés selon l’immunocompétence de l’hôte. Le dépistage exhaustif par PCR sur liquide intraoculaire a considérablement amélioré le taux de diagnostic.
3-1. Agents pathogènes de la famille des virus de l’herpès et lésions oculaires
Section intitulée « 3-1. Agents pathogènes de la famille des virus de l’herpès et lésions oculaires »| Virus | Lésions oculaires chez les immunocompétents | Lésions oculaires chez les immunodéprimés |
|---|---|---|
| HSV-1/2 (HHV-1/2) | Iridocyclite herpétique, ARN | PORN (rare) |
| VZV (HHV-3) | Zona ophtalmique, iridocyclite herpétique, NRA | PORN |
| CMV (HHV-5) | Endothélite cornéenne, uvéite antérieure à CMV | Rétinite à CMV, uvéite de reconstitution immunitaire (IRU) |
| EBV (HHV-4) | Uvéite légère (rare) | Lésion similaire à l’ARN (rare) |
| HTLV-1 | Uvéite intermédiaire à panuvéite (opacité vitréenne en voile) | Idem (aggravation) |
| Virus de la rubéole | Association avec l’iritis hétérochromique de Fuchs | ─ |
3-2. Nécrose rétinienne aiguë (ARN)
Section intitulée « 3-2. Nécrose rétinienne aiguë (ARN) »L’ARN se manifeste par une iridocyclite aiguë avec des précipités rétro-cornéens pigmentés, et évolue rapidement vers une rétinite nécrosante avec des lésions granuleuses blanc-jaunâtre dans la périphérie rétinienne qui confluent et s’étendent. Le VZV est le plus fréquent (souvent des cas graves), suivi du HSV-1/2 comme agents étiologiques. Un décollement de rétine rhegmatogène avec déchirure rétinienne survient dans environ 75 % des cas, et le pronostic visuel est sombre18).
Critères diagnostiques de l’ARN de la Société japonaise d’inflammation oculaire (groupe de diagnostic certain) :
- Signes oculaires initiaux : ① cellules de la chambre antérieure ou précipités rétro-cornéens en graisse de mouton, ② une ou plusieurs lésions blanc-jaunâtre (périphériques), ③ artérite rétinienne, ④ hyperhémie papillaire, ⑤ opacité vitréenne inflammatoire, ⑥ augmentation de la pression intraoculaire. Parmi ceux-ci, ① et ② sont obligatoires.
- Éléments d’évolution : au moins un des éléments suivants : expansion circonférentielle rapide, déchirure/décollement de la rétine, occlusion vasculaire, atrophie optique, réponse aux anti-herpétiques
- Examen du liquide intraoculaire : PCR de l’humeur aqueuse ou du vitré positive pour HSV-1, HSV-2 ou VZV
Le groupe de diagnostic clinique (ne nécessitant pas d’examen du liquide intraoculaire) peut être diagnostiqué si, en plus des signes initiaux ①②, deux éléments parmi ③ à ⑥ et un élément d’évolution sont satisfaits.
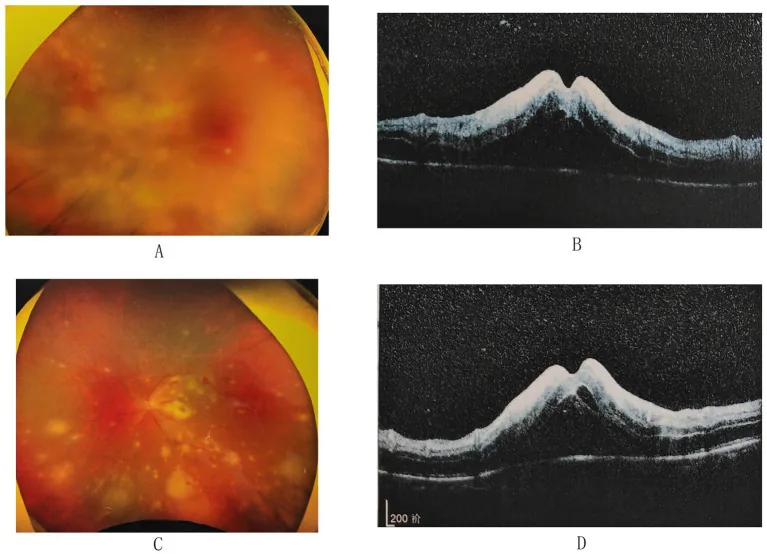
3-3. CMV網膜炎
Section intitulée « 3-3. CMV網膜炎 »CMVはAIDSを中心とした免疫不全患者に発症する日和見感染であり、CD4陽性T細胞数が50〜100/µLまで低下したAIDS患者に多く発症する20)。病型は①周辺部顆粒型(白色顆粒を伴う扇型病巣)、②後極部血管炎型(出血と浮腫)、③樹氷状血管炎型(大血管中心の白輯化)の3型があり、臨床上は混在することが多い。免疫回復に伴う免疫回復ぶどう膜炎(IRU)も重要な合併症であり15)、抗レトロウイルス療法開始後の眼科管理が必要である。
3-4. HTLV-1関連ぶどう膜炎(HAU)
Section intitulée « 3-4. HTLV-1関連ぶどう膜炎(HAU) »HTLV-1のキャリアの**約0.1%**に発症し、九州・沖縄を中心とした地域に多い12)。白色顆粒状KP、虹彩結節、ベール状・索状・顆粒状の硝子体混濁、網膜血管周囲の白色顆粒付着が特徴的所見である。甲状腺機能亢進症を高頻度に合併する。視力予後は比較的良好であるが、ステロイドへの反応後に減量・中止で再燃することがある。
3-5. 風疹ウイルスとFuchs虹彩異色性虹彩毛様体炎
Section intitulée « 3-5. 風疹ウイルスとFuchs虹彩異色性虹彩毛様体炎 »Fuchs虹彩異色性虹彩毛様体炎(虹彩異色・虹彩毛様体炎・白内障の3主徴)は風疹ウイルスとの関連が示唆されている。先天風疹症候群では妊娠3か月以内の経胎盤感染により、salt-and-pepper様眼底所見を呈する網脈絡膜炎が発症する。
4. Aperçu de l’uvéite bactérienne
Section intitulée « 4. Aperçu de l’uvéite bactérienne »4-1. Uvéite tuberculeuse
Section intitulée « 4-1. Uvéite tuberculeuse »L’inflammation intraoculaire due à Mycobacterium tuberculosis implique deux mécanismes : l’infection directe et l’immunomédiation (réaction d’hypersensibilité). Les formes cliniques sont variées, incluant le granulome choroïdien (nodule), le décollement séreux de la rétine, la choriorétinite en grains de plomb, la vascularite et la panuvéite.
L’IGRA (QuantiFERON®-TB Gold Plus ou T-SPOT®-TB) est utile pour le diagnostic, et il faut noter que la réaction tuberculinique peut être négative chez les personnes âgées ou celles présentant une immunité cellulaire diminuée, comme dans le SIDA. Concernant le pronostic visuel de l’uvéite tuberculeuse, il a été rapporté qu’environ un tiers des cas atteignent une meilleure acuité visuelle corrigée inférieure à 3/60 3). Les critères de classification de l’uvéite tuberculeuse proposés par le SUN Working Group (2021) incluent : ① uvéite antérieure avec nodules iriens, ② choriorétinite serpigineuse, ③ nodules choroïdiens (tuberculomes), ④ choriorétinite multifocale en cas de tuberculose systémique active, et ⑤ vascularite rétinienne occlusive 5). En Inde et en Indonésie, environ 22,9 à 48,0 % des uvéites infectieuses sont considérées comme tuberculeuses 3,14), ce qui souligne l’importance particulière de cette pathologie dans les régions à forte prévalence de tuberculose.
4-2. Uvéite syphilitique
Section intitulée « 4-2. Uvéite syphilitique »L’inflammation intraoculaire causée par Treponema pallidum est appelée « le grand imitateur » et peut prendre la forme d’une uvéite antérieure, postérieure ou panuvéite. Ces dernières années, on observe une recrudescence mondiale, principalement chez les hommes ayant des rapports sexuels avec des hommes (HSH), et le risque d’uvéite syphilitique est environ 2 fois plus élevé en cas de co-infection par le VIH4). Environ 5,7 à 6 millions de nouveaux cas de syphilis (15-49 ans) sont signalés chaque année dans le monde4), et environ 1 à 1,5 % des patients atteints de syphilis développent une atteinte oculaire4,10).
Le diagnostic repose sur des tests sérologiques (TPHA, RPR/VDRL) et est interprété par la combinaison de méthodes TP et non TP. Le traitement de première intention est la benzylpénicilline G (Aqvasiline®) 24 millions d’unités/jour en perfusion intraveineuse pendant 10 à 14 jours, selon le schéma de la neurosyphilis, et la ceftriaxone intraveineuse est une alternative. Il faut surveiller la réaction de Jarisch-Herxheimer (fièvre et exacerbation de l’inflammation dans les 24 heures suivant le traitement).
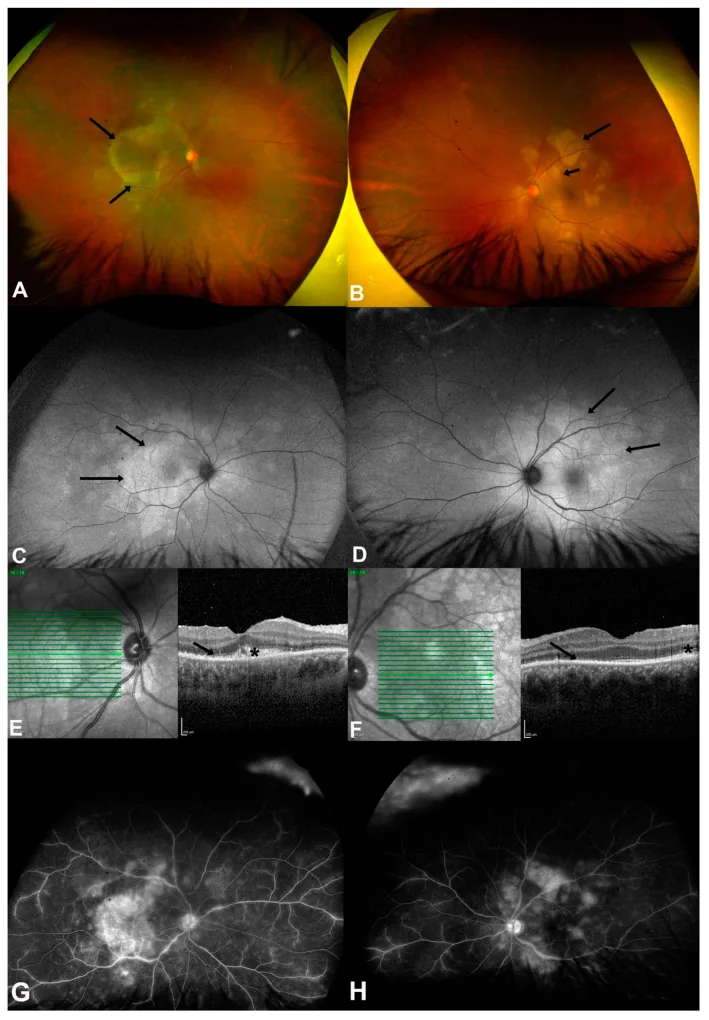
4-3. Maladie des griffes du chat (infection à Bartonella)
Section intitulée « 4-3. Maladie des griffes du chat (infection à Bartonella) »Infection par Bartonella henselae, l’exposition aux chats est un élément important de l’interrogatoire. Les signes du fond d’œil comprennent une névrite optique (aspect d’étoile maculaire), des taches blanches stellaires maculaires et un décollement séreux de la rétine, prenant souvent la forme d’une uvéite postérieure. Le diagnostic repose sur le dosage des anticorps anti-Bartonella henselae, et le traitement antibiotique fait appel à l’azithromycine, la doxycycline ou la rifampicine.
4-4. Maladie de Lyme
Section intitulée « 4-4. Maladie de Lyme »Infection à spirochètes du genre Borrelia transmise par les tiques, avec apparition de diverses lésions oculaires (uvéite, vascularite rétinienne, névrite optique, kératite, etc.) aux stades 2 et 3. L’érythème chronique migrant est une éruption cutanée caractéristique du premier stade, et une morsure de tique est un indice diagnostique. Le diagnostic repose sur l’augmentation des IgM sériques par ELISA, et le traitement utilise des antibiotiques de la famille des pénicillines ou des tétracyclines. Un diagnostic différentiel avec la syphilis et la sarcoïdose est nécessaire.
4-5. Lèpre (bacille de Hansen)
Section intitulée « 4-5. Lèpre (bacille de Hansen) »Infection granulomateuse chronique due à Mycobacterium leprae, avec une atteinte oculaire survenant dans 70 à 80 % des cas (30 à 40 % chez les nouveaux patients récents). L’uvéite antérieure granulomateuse chronique est prédominante, avec des signes caractéristiques tels que les perles iriennes, l’atrophie irienne, la myosis et les synéchies antérieures périphériques en tente. Le traitement repose sur une polychimiothérapie (rifampicine, dapsone, clofazimine) et, en cas d’uvéite, des corticostéroïdes topiques sont ajoutés.
4-6. Endophtalmie bactérienne endogène
Section intitulée « 4-6. Endophtalmie bactérienne endogène »L’endophtalmie bactérienne endogène, où l’infection se propage par voie hématogène à partir d’autres organes (abcès hépatique, endocardite, pneumonie, etc.), est principalement causée par des bacilles à Gram négatif (Klebsiella, Escherichia coli, etc.) et son pronostic est extrêmement mauvais. Par rapport à l’infection exogène (postopératoire) à cocci à Gram positif, sa progression est plus rapide, et la recherche et le traitement de la source infectieuse systémique sont essentiels.
5. Aperçu des uvéites fongiques
Section intitulée « 5. Aperçu des uvéites fongiques »La plupart des endophtalmies fongiques sont d’origine endogène, Candida (Candida spp.) étant le plus fréquent, tandis qu’Aspergillus et Cryptococcus sont également des agents pathogènes importants.
Principaux facteurs de risque :
- Nutrition parentérale centrale (IVH) · cathéter à demeure
- Utilisation prolongée d’antibiotiques à large spectre
- Immunosuppression (infection par le VIH, transplantation d’organe, tumeur maligne, chimiothérapie)
- Diabète sucré
- Usage de drogues intraveineuses
Dans l’endophtalmie fongique, une opacité vitréenne blanche sphérique ou cotonneuse (“opacité en masse”) est caractéristique, et la progression est plus lente que dans l’endophtalmie bactérienne. Au début, elle est asymptomatique ou ne présente que de légers corps flottants, ce qui la rend facile à négliger. En progressant, une hyperhémie, une douleur oculaire et une panuvéite apparaissent. 30% des endophtalmies fongiques endogènes surviennent dans les deux yeux8).
Le diagnostic repose sur l’hémoculture, la culture de l’extrémité du cathéter, le dosage du β-D-glucane, la mesure de l’antigène candidosique et la culture du vitré. Le traitement associe généralement des antifongiques (voriconazole, amphotéricine B, fluconazole) et une vitrectomie.
6. Aperçu des uvéites parasitaires
Section intitulée « 6. Aperçu des uvéites parasitaires »6-1. Toxoplasmose oculaire
Section intitulée « 6-1. Toxoplasmose oculaire »Toxoplasma gondii (protozoaire intracellulaire obligatoire) infecterait environ un tiers de la population mondiale, et la séroprévalence chez les adultes japonais est estimée à 20-30%11). Les félidés sont l’hôte définitif ; l’infection se produit par ingestion orale d’oocystes provenant des excréments de chats ou par consommation de viande insuffisamment cuite.
眼トキソプラズマ症はぶどう膜炎の原因疾患の**約1%**を占める11)。後天感染の眼底所見は周辺部の境界不鮮明な白色〜乳白色の滲出性網脲絡膜炎であり、陳旧性瘢痕病巣に接する「衛星病巣(satellite lesion)」が再発時の特徴的所見となる。前房炎症・硝子体混濁(「霧中のヘッドライト headlights in the fog」)を伴う。先天感染では両黄斑部に中心部厌白色線維性増殖と色素沈着を伴う瘢痕病巣がみられる。
診断は特徴的な眼所見と血清抗体価(IgG・IgM)の測定が主体となる。Q値(Goldmann-Witmer比)やPCRによる眼内液検査も有用である。治療はスピラマイシン酢酸エステル(アセチルスピラマイシン)あるいはクリンダマイシン1.2 g/日を4〜6週間内服し、滲出病変のコントロール目的でステロイド0.5 mg/kg/日を併用する。
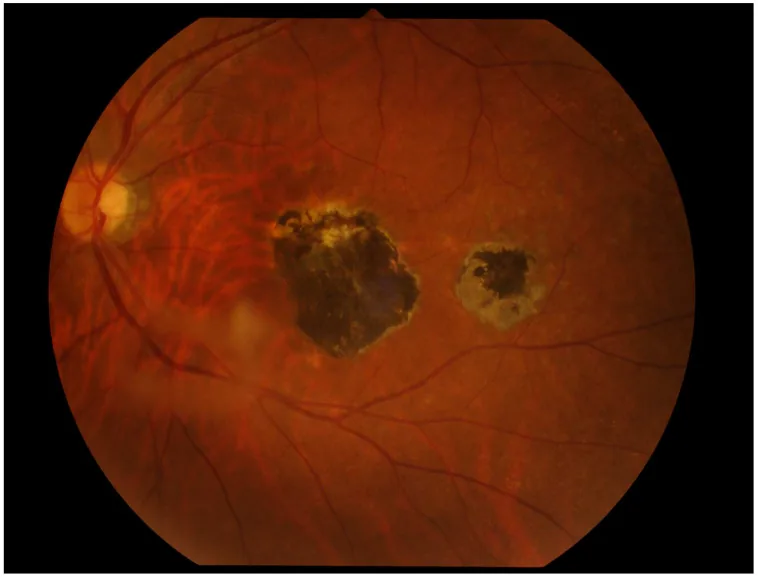
6-2. 眼トキソカラ症
Section intitulée « 6-2. 眼トキソカラ症 »イヌ回虫(Toxocara canis)またはネコ回虫(Toxocara cati)の幼虫移行症であり、片眼性が多い。眼内炎型・後極部腫瘤型・周辺部腫瘤型(最多)の3病型があり、強い硝子体混濁・網膜剥離をきたすことがある。ELISA(Toxocara CHECK®等)による血清抗体検索と特徴的眼所見で診断する。治療は駆虫薬(ジエチルカルバマジン)内服・ステロイド内服に加え、冷凍凝固・レーザー凝固・硝子体手術が適応となりうる。
7. Stratégie diagnostique
Section intitulée « 7. Stratégie diagnostique »7-1. Points clés de l’anamnèse
Section intitulée « 7-1. Points clés de l’anamnèse »Pour le diagnostic des uvéites infectieuses, une anamnèse systématique est indispensable :
- Âge et sexe : la rétinite à CMV est fréquente chez les patients atteints du SIDA (hommes de 20 à 40 ans), l’HAU chez les résidents de Kyushu et Okinawa
- Région et antécédents de voyage : antécédents de voyage dans des zones de forte endémie tuberculeuse (Asie du Sud-Est, Afrique, etc.)
- Antécédents de contact animal : chat (Toxoplasma, Bartonella), chien (Toxocara)
- Antécédents alimentaires : viande crue, poisson cru (Toxoplasma)
- Antécédents sexuels et test VIH : syphilis, CMV
- État d’immunosuppression : VIH, tumeur maligne, transplantation d’organe, utilisation d’immunosuppresseurs
- Antécédents de nutrition parentérale et de cathéter : endophtalmie fongique
- Antécédents de zona et d’herpès labial : iritis à VZV et HSV
7-2. Diagnostic différentiel basé sur les signes oculaires
Section intitulée « 7-2. Diagnostic différentiel basé sur les signes oculaires »| Signe | Maladie infectieuse suggérée |
|---|---|
| Précipités kératiques en graisse de mouton (KP mutton-fat) | Iritis HSV/VZV, ARN, uvéite tuberculeuse |
| Uvéite antérieure avec hypertension oculaire (PIO ≥ 25 mmHg) | Iritis HSV/VZV, uvéite antérieure à CMV |
| Lésions nécrotiques blanches confluentes périphériques | ARN (VZV/HSV) |
| Infiltrat blanc avec hémorragie polaire postérieure | Rétinite à CMV (type vasculitique) |
| Opacité vitréenne en masse (tendance à l’augmentation) | Endophtalmie fongique |
| Opacité vitréenne en voile ou en cordon | Uvéite associée au HTLV-1 |
| Cicatrice ancienne + lésions satellites | Toxoplasmose oculaire |
| Masse blanche périphérique + cordon vitréen | Toxocarose oculaire |
| Iritis granulomateuse + granulome choroïdien | Uvéite tuberculeuse, syphilitique |
| Papillite + tache étoilée maculaire | Maladie des griffes du chat (Bartonella) |
7-3. Examens systémiques
Section intitulée « 7-3. Examens systémiques »| Examen | Maladies cibles |
|---|---|
| TPHA sérique et RPR/VDRL | Uvéite syphilitique |
| IGRA (QuantiFERON, T-SPOT) | Uvéite tuberculeuse |
| Antigénémie CMV (méthode C7-HRP) et PCR CMV | Rétinite à CMV |
| Anticorps anti-HTLV-1 | Uvéite associée au HTLV-1 |
| Anticorps anti-VIH et numération des CD4 | CMV/PORN/syphilis oculaire |
| β-D-glucane et antigène candidosique | Endophtalmie fongique |
| IgG/IgM anti-Toxoplasma | Toxoplasmose oculaire |
| Anticorps anti-Toxocara (ELISA) | Toxocarose oculaire |
| Anticorps anti-Bartonella henselae | Maladie des griffes du chat |
| Hémoculture et échocardiographie | Endophtalmie bactérienne endogène |
7-4. Examen des liquides intraoculaires (humeur aqueuse et vitré)
Section intitulée « 7-4. Examen des liquides intraoculaires (humeur aqueuse et vitré) »L’examen des liquides intraoculaires est la méthode de confirmation la plus importante pour le diagnostic des uvéites infectieuses. Les échantillons sont obtenus par ponction de la chambre antérieure (prélèvement d’humeur aqueuse) ou par vitrectomie (prélèvement de vitré) 9).
L’ADN est extrait de l’humeur aqueuse ou du vitré, et l’ADN de chaque agent pathogène est détecté par PCR. La PCR multiplex en temps réel permet de rechercher plusieurs virus de manière exhaustive avec un petit échantillon, et est particulièrement utile pour le diagnostic différentiel de la rétinite nécrosante aiguë 19).
Kit de l’uvéite infectieuse (médecine avancée) : permet de rechercher simultanément l’ADN de HSV-1/2, VZV, CMV, EBV, HHV-6/7, HTLV-1, Toxoplasma gondii, etc., et est utilisé pour le diagnostic des co-infections multiples et des cas réfractaires. Cependant, il faut noter qu’au début de la rétinite à CMV (avant l’apparition des cellules inflammatoires dans la chambre antérieure), la PCR peut ne pas détecter le virus.
Rapport de Goldmann-Witmer (valeur Q, taux d’anticorps)
Section intitulée « Rapport de Goldmann-Witmer (valeur Q, taux d’anticorps) »Il s’agit d’une méthode pour détecter la présence ou l’absence de production d’anticorps spécifiques à l’agent pathogène dans l’œil, calculée à l’aide de la formule suivante :
Valeur Q = (taux d’anticorps viraux dans le liquide intraoculaire ÷ quantité d’IgG dans le liquide intraoculaire) ÷ (taux d’anticorps viraux sériques ÷ quantité d’IgG sérique)
- Valeur Q > 1 : possibilité de production locale d’anticorps dans l’œil
- Valeur Q ≥6 : production locale significative d’anticorps confirmée, permettant d’identifier le virus comme agent causal
Il faut noter que la valeur Q est sous-estimée dans les 10 premiers jours suivant l’apparition des symptômes, car la production d’anticorps intraoculaires est insuffisante. Le diagnostic étiologique ne peut être posé uniquement par le titre d’anticorps sériques (la plupart des adultes sont positifs en raison d’une infection antérieure) 6).
Arbre décisionnel pour l’utilisation de la PCR sur les liquides intraoculaires
Section intitulée « Arbre décisionnel pour l’utilisation de la PCR sur les liquides intraoculaires »眼内炎症患者 ├─ ウイルス性疑い(高眼圧・前房炎症・壊死性網膜炎) │ → 前房水PCR(HSV/VZV/CMV)+ Q値 ← 第一選択 │ ─ 前房水で陰性かつ壊死性病変 → 硝子体液PCR │ ─ 免疫不全者 → マルチプレックスPCR(先進医療) ├─ 寄生虫疑い(衛星病巣・周辺部腫瘤) │ → 眼内液Q値(Toxoplasma)または眼内液PCR ├─ 真菌疑い(塊状混濁・リスク因子あり) │ → 硝子体液培養 + β-D-グルカン(血液) └─ 細菌疑い(急速進行・IVH歴) → 硝子体液グラム染色・培養(至急)8. Principes du traitement
Section intitulée « 8. Principes du traitement »8-1. Traitement spécifique selon l’agent pathogène
Section intitulée « 8-1. Traitement spécifique selon l’agent pathogène »| Agent pathogène | Traitement de première intention | Remarques |
|---|---|---|
| HSV (ARN, iritis) | ACV 10 mg/kg × 3 fois/j IV 2 sem → VACV 1 000 mg × 3 fois/j PO | Associer des corticostéroïdes en collyre et IV pour l’anti-inflammation |
| VZV (ARN・iritis) | ACV 10-15 mg/kg x3 fois IV + VACV oral | PORN suit le traitement du CMV |
| CMV (rétinite) | GCV 5 mg/kg x2 fois IV 2-3 sem (induction) → VGCV 900 mg x2 fois/jour oral (maintien) | La restauration immunitaire est le traitement curatif |
| CMV (uvéite antérieure) | Gel de GCV 0,15% en collyre (73% des spécialistes le choisissent en première intention) ± VGCV oral | Pour les cas chroniques, envisager un traitement d’entretien de 12 mois (73% des spécialistes choisissent le gel de GCV 0,15%) 2) |
| Tuberculose | Quadrithérapie INH, RFP, PZA, EMB (régime standard de 6 mois) | Corticostéroïdes associés si nécessaire |
| Syphilis | Benzylpénicilline G 24 millions d’unités/jour IV 10-14 jours | Attention à la réaction de Herxheimer |
| Champignons (Candida) | Voriconazole ou amphotéricine B ± vitrectomie | Surveillance par l’indice β-D-glucane |
| Toxoplasme | Acétylspiramycine + stéroïde ou clindamycine | Attention chez la femme enceinte (utiliser la spiramycine) |
| Toxocara | Diéthylcarbamazine + stéroïde | Envisager laser ou vitrectomie |
| Maladie de Lyme | Amoxicilline ou doxycycline 3 semaines | Ajouter des gouttes ophtalmiques de stéroïdes pour les lésions oculaires |
| Lèpre | MDT (rifampicine, DDS, clofazimine) | Stéroïdes nécessaires en cas de réaction lépreuse |
8-2. Utilisation appropriée des corticostéroïdes
Section intitulée « 8-2. Utilisation appropriée des corticostéroïdes »En cas d’uvéite infectieuse, si des corticostéroïdes sont utilisés, un traitement anti-pathogène doit toujours être administré avant ou en parallèle. Le rôle des corticostéroïdes est de réduire les lésions tissulaires secondaires causées par l’inflammation. Ils sont utilisés en association avec un traitement anti-pathogène approprié dans de nombreuses uvéites infectieuses, telles que la nécrose rétinienne aiguë (ARN), la toxoplasmose, l’uvéite tuberculeuse et l’uvéite lépreuse.
En revanche, dans la rétinite à CMV (infection opportuniste pure), l’amélioration de l’immunité par le traitement de la maladie sous-jacente (SIDA) est le traitement curatif, et les corticostéroïdes ne sont généralement pas utilisés.
8-3. Mydriatiques et gestion de la pression intraoculaire
Section intitulée « 8-3. Mydriatiques et gestion de la pression intraoculaire »Pour prévenir les synéchies postérieures de l’iris, en cas d’inflammation du segment antérieur, on utilise des collyres de tropicamide et de phényléphrine (1 à 6 fois par jour). En cas d’hypertension oculaire (caractéristique de l’iritis à HSV/VZV et de l’uvéite antérieure à CMV), on choisit des hypotenseurs oculaires tels que les inhibiteurs de l’anhydrase carbonique et les bêta-bloquants. Cependant, les prostaglandines présentent un risque d’exacerbation de l’inflammation et doivent être utilisées avec prudence.
9. Matrice de risque selon l’état d’immunosuppression
Section intitulée « 9. Matrice de risque selon l’état d’immunosuppression »| Contexte | Agents pathogènes particulièrement à surveiller | Examens prioritaires |
|---|---|---|
| Infection par le VIH (CD4 < 50/µL) | CMV (rétinite, ARN, PORN), champignons (Cryptococcus), syphilis | PCR du liquide intraoculaire (multiplex), antigène CMV, β-D-glucane |
| Après transplantation d’organe solide et utilisation d’immunosuppresseurs | CMV, champignons (Aspergillus, Candida), EBV | PCR CMV, β-D-glucane, hémoculture |
| Après tumeur maligne et chimiothérapie | Champignons (Candida, Aspergillus), CMV | β-D-glucane, hémoculture |
| IVL à long terme / cathéter à demeure | Endophtalmie à Candida | β-D-glucane / hémoculture (consultation ophtalmologique obligatoire) |
| Haut risque de tuberculose (voyage / antécédents de contact) | Tuberculose (granulome choroïdien / type vascularite) | IGRA / TDM thoracique |
| HSH (hommes ayant des rapports sexuels avec des hommes) · VIH+ | Syphilis (syphilis oculaire environ 1 à 1,5 %), CMV | TPHA · RPR · test VIH |
| Immunocompétent (âge moyen ou plus) | Iridocyclite à HSV/VZV · ARN | PCR de l’humeur aqueuse · valeur Q |
| Enfants / antécédents de contact avec des animaux domestiques | Toxocara / Toxoplasma | Anticorps sériques (ELISA) |
10. Questions fréquentes
Section intitulée « 10. Questions fréquentes »Lorsqu’il est difficile de distinguer une cause infectieuse d’une cause non infectieuse sur la seule base des signes cliniques, ou lorsque l’infection est suspectée mais que les tests sérologiques sont négatifs, une ponction de la chambre antérieure est activement envisagée. En particulier en cas de suspicion de rétinite nécrosante (ARN, PORN, rétinite à CMV), un diagnostic précoce est directement lié au choix du traitement et au pronostic, donc une PCR des fluides intraoculaires est réalisée dans la mesure du possible. La PCR multiplex est utile en cas de PCR négative au stade initial ou de cas réfractaires.
Tout d’abord, effectuez rapidement une PCR des fluides intraoculaires pour identifier l’agent pathogène, puis commencez un traitement spécifique dès que l’agent est identifié. L’arrêt brutal des stéroïdes peut provoquer un rebond inflammatoire, donc réduisez-les prudemment après le début du traitement anti-pathogène. En particulier, si des stéroïdes ont été administrés seuls pour une uvéite tuberculeuse, le risque de réactivation et de dissémination de la tuberculose latente est accru ; une évaluation systémique urgente (CT thoracique, IGRA) doit être réalisée en collaboration avec un pneumologue.
Après la fin du traitement, Toxoplasma reste sous forme de kystes résistants aux médicaments dans les lésions cicatricielles atrophiques. Une récidive survient dans environ 5 à 30 % des cas, déclenchée par une baisse de l’immunité ou une grossesse. Chez les patients présentant des récidives fréquentes, un traitement prophylactique à long terme par triméthoprime-sulfaméthoxazole peut être envisagé. Pendant la grossesse, si une femme séronégative pour la toxoplasmose contracte une primo-infection, il existe un risque de transmission verticale au fœtus (environ 40 %) ; il faut donc conseiller d’éviter tout contact avec les excréments de chat, la terre et la consommation de viande crue.
11. Articles connexes
Section intitulée « 11. Articles connexes »Uvéite virale
Section intitulée « Uvéite virale »Uvéite bactérienne et autres uvéites infectieuses
Section intitulée « Uvéite bactérienne et autres uvéites infectieuses »Références
Section intitulée « Références »- 日本眼炎症学会ぶどう膜炎診療ガイドライン作成委員会. ぶどう膜炎診療ガイドライン. 日眼会誌. 2019;123(6):635–702.
- Thng ZX, Putera I, Testi I, et al. The Infectious Uveitis Treatment Algorithm Network (TITAN) Report 2—global current practice patterns for the management of Cytomegalovirus anterior uveitis. Eye. 2023. https://doi.org/10.1038/s41433-023-02503-3
- Putera I, Schrijver B, ten Berge JCEM, et al. The immune response in tubercular uveitis and its implications for treatment: From anti-tubercular treatment to host-directed therapies. Prog Retin Eye Res. 2023;95:101173.
- Chauhan K, Fonollosa A, Giralt L, et al. Demystifying Ocular Syphilis – A Major Review. Ocul Immunol Inflamm. 2023. https://doi.org/10.1080/09273948.2023.2217246
- Jabs DA, et al. Standardization of Uveitis Nomenclature (SUN) Working Group. Classification Criteria for Tubercular Uveitis. Am J Ophthalmol. 2021;228:142–149.
- 八代成子. ウイルス性ぶどう膜炎の診断と治療. 眼科. 2007;49:1193–1198.
- 大野重昭. ぶどう膜炎の疫学と分類. 日眼会誌. 2019;123(6).
- Tsirouki T, Dastiridou A, Symeon CI, et al. A focus on the epidemiology of uveitis. Ocul Immunol Inflamm. 2018;26(1):2–16.
- 慶野博. 感染性ぶどう膜炎の眼内液診断. 臨床眼科. 2019.
- Oliver SE, Aubin M, Atwell L, et al. Ocular Syphilis — Eight Jurisdictions, United States, 2014–2015. MMWR Morb Mortal Wkly Rep. 2016;65:1185–1188.
- 岡田アナベルあやめ. 眼トキソプラズマ症の診断と治療. 眼科. 2018.
- 中尾久美子. HTLV-1関連ぶどう膜炎の疫学と治療. 日本臨床. 2020.
- La Distia Nora R, et al. Infectious uveitis etiology in developing vs. developed countries. Curr Opin Ophthalmol. 2021.
- Agrawal R, et al. Collaborative Ocular Tuberculosis Study (COTS)—Report 1. Ophthalmology. 2019;126(11):1566–1577.
- 八代成子. CMV網膜炎・免疫回復ぶどう膜炎の管理. 眼科. 2007.
- Kempen JH, et al. The prevalence of uveitis in the United States. Arch Ophthalmol. 2004;122(4):543–557.
- Groen-Hakan F, et al. Diagnostic value of aqueous humor analysis for uveitis. Ocul Immunol Inflamm. 2020.
- 堤雅幸. 急性網膜壊死診断基準(日本眼炎症学会). 日眼会誌. 2020.
- 蕪城俊克. 眼内液PCRによるウイルス性ぶどう膜炎診断. 眼科. 2021.
- Bodaghi B, et al. Blindness prevention in HIV patients: CMV retinitis management update. Prog Retin Eye Res. 2023.
