
Infektiöse Uveitis
Auf einen Blick: Wichtige Punkte
Abschnitt betitelt „Auf einen Blick: Wichtige Punkte“1. Was ist eine infektiöse Uveitis?
Abschnitt betitelt „1. Was ist eine infektiöse Uveitis?“Uveitis ist ein Sammelbegriff für intraokulare Entzündungen. Nach der ätiologischen Klassifikation wird sie in „exogene (infektiöse) Uveitis“ und „endogene (nicht-infektiöse) Uveitis“ unterteilt. Die infektiöse Uveitis (infectious uveitis) bezeichnet eine intraokulare Entzündung, die direkt oder über immunvermittelte Mechanismen durch Krankheitserreger wie Bakterien, Viren, Pilze oder Parasiten verursacht wird. Die jährliche Inzidenz neuer Uveitis-Fälle beträgt 17 bis 52 pro 100.000 Personen, die Prävalenz 38 bis 714 pro 100.000 Personen1,16).
Laut einer epidemiologischen Studie der Japanischen Gesellschaft für Augenentzündung aus dem Jahr 2002 (3.060 Fälle) machten infektiöse Uveitiden etwa 16 % aller Fälle aus 1,7). Zu den wichtigsten Erkrankungen zählten die herpetische Iritis (3,6 %), die bakterielle Endophthalmitis (3,8 %), die akute Netzhautnekrose (ARN) (1,3 %), die okuläre Toxoplasmose (1,1 %), die okuläre Toxokariasis (1,1 %), die CMV-Retinitis (0,8 %) und die HTLV-1-assoziierte Uveitis (1,0 %). International wird angenommen, dass Toxoplasmose und tuberkulöse Uveitis in Entwicklungsländern mehr als 50 % der infektiösen Uveitiden ausmachen 2,13), was auf deutliche regionale Unterschiede hinweist 8).
Die Identifizierung der Ursache einer infektiösen Uveitis ist wichtig, da sich die Behandlungsstrategie grundlegend von der nicht-infektiösen unterscheidet. Bei nicht-infektiösen Formen steht die Immunsuppression (Steroide/Immunmodulatoren) im Vordergrund, während bei infektiösen Formen zunächst eine spezifische Behandlung gegen den Erreger erforderlich ist; eine unbedachte Steroidgabe kann den Krankheitsverlauf drastisch verschlechtern.
2. Klassifikation
Abschnitt betitelt „2. Klassifikation“2-1. Klassifikation nach Lokalisation
Abschnitt betitelt „2-1. Klassifikation nach Lokalisation“Die Uveitis wird nach dem Hauptort der Entzündung in vier Typen eingeteilt (SUN Working Group-Klassifikation):
| Klassifikation | Lokalisation | Repräsentative Erkrankungen (infektiös) |
|---|---|---|
| Vordere Uveitis | Iris und Ziliarkörper (Iritis, Iridozyklitis) | HSV/VZV-Iritis, CMV-vordere Uveitis, Lyme-Borreliose |
| Intermediate Uveitis | Glaskörper / Pars plana des Ziliarkörpers | HTLV-1-assoziierte Uveitis, Lyme-Borreliose |
| Posteriore Uveitis | Netzhaut-Aderhaut und hinterer Glaskörper | CMV-Retinitis, okuläre Toxoplasmose, okuläre Toxokariasis |
| Panuveitis | Vollschichtig | ARN, tuberkulös, syphilitisch, Pilz-Endophthalmitis |
2-2. Klassifikation nach Erreger
Abschnitt betitelt „2-2. Klassifikation nach Erreger“Die infektiöse Uveitis wird je nach Erregerart in vier Gruppen eingeteilt.
Die Familie der Herpesviren (HHV-1 bis 8) ist am häufigsten, wobei HSV-1/2, VZV, CMV und HTLV-1 klinisch besonders wichtig sind. Je nach Immunstatus des Wirts zeigen sie unterschiedliche klinische Bilder: Bei Immunkompetenten sind HSV/VZV-bedingte anteriore Uveitis und ARN typisch, bei Immunsupprimierten CMV-Retinitis und PORN.
Bakteriell
Abschnitt betitelt „Bakteriell“Haupterreger sind Mycobacterium tuberculosis, Treponema pallidum (Syphilis), Bartonella (Katzenkratzkrankheit) und Borrelia (Lyme-Borreliose). Bei endogener bakterieller Endophthalmitis überwiegen gramnegative Stäbchen (E. coli, Klebsiella etc.), die schnell fortschreiten und eine schlechte Prognose haben.
Pilzbedingt
Abschnitt betitelt „Pilzbedingt“Candida, Aspergillus und Cryptococcus verursachen endogene Infektionen bei immungeschwächten Wirten (zentraler Venenkatheter, Immunsuppression, HIV-Infektion). Besonders problematisch ist die Endophthalmitis nach Candidämie.
Parasitär
Abschnitt betitelt „Parasitär“Die okuläre Toxoplasmose (Toxoplasma gondii) und die okuläre Toxokariose (Toxocara canis/cati) sind die repräsentativen Erkrankungen. Toxoplasmose kann auch nach einer erworbenen Infektion im Erwachsenenalter reaktivieren und zu Lymphknotenschwellung und erworbener Retinochoroiditis führen.
2-3. Klassifikation nach Infektionsweg
Abschnitt betitelt „2-3. Klassifikation nach Infektionsweg“| Klassifikation | Infektionsweg | Repräsentative Erkrankungen |
|---|---|---|
| Endogen | Hämatogene Streuung (anderes Organ → Auge) | Bakterielle Endophthalmitis, Pilzendophthalmitis, Tuberkulose, Syphilis, CMV-Retinitis |
| Exogen (exogenous) | Direkte Penetration (Trauma/Operation) | Postoperative infektiöse Endophthalmitis, posttraumatische Endophthalmitis |
3. Überblick über virale Uveitis
Abschnitt betitelt „3. Überblick über virale Uveitis“Eine Entzündung der Uvea, Netzhaut und des Glaskörpers, an der Viren beteiligt sind, wird als virale Uveitis bezeichnet. Humane Herpesviren (HHV) haben eine starke Affinität zum Netzhautgewebe und verursachen verschiedene Augenerkrankungen. Die virale Uveitis ist dadurch gekennzeichnet, dass die direkte virale Toxizität und die durch Immunreaktionen ausgelöste Entzündung je nach Immunstatus des Wirts ein vielfältiges klinisches Bild zeigen. Die umfassende Untersuchung mittels PCR aus Intraokularflüssigkeit hat die Diagnoserate erheblich verbessert.
3-1. Erreger der Herpesvirus-Familie und Augenläsionen
Abschnitt betitelt „3-1. Erreger der Herpesvirus-Familie und Augenläsionen“| Virus | Augenläsionen bei Immunkompetenten | Augenläsionen bei Immunsupprimierten |
|---|---|---|
| HSV-1/2 (HHV-1/2) | Herpes-Iridozyklitis, ARN | PORN (selten) |
| VZV (HHV-3) | Augengürtelrose, Herpes-Iridozyklitis, ARN | PORN |
| CMV (HHV-5) | Hornhautendothelitis, CMV-Anterior-Uveitis | CMV-Retinitis, Immunrekonstitutions-Uveitis (IRU) |
| EBV (HHV-4) | Leichte Uveitis (selten) | ARN-ähnliche Läsion (selten) |
| HTLV-1 | Intermediate bis Panuveitis (schleierartige Glaskörpertrübung) | Ebenso (schwerer Verlauf) |
| Rötelnvirus | Assoziation mit Fuchs-Heterochromie-Iridozyklitis | ─ |
3-2. Akute Netzhautnekrose (ARN)
Abschnitt betitelt „3-2. Akute Netzhautnekrose (ARN)“Die ARN manifestiert sich als akute Iridozyklitis mit pigmentierten Hornhautendothelbeschlägen und entwickelt sich schnell zu einer nekrotisierenden Retinitis mit gelb-weißen granulären Läsionen in der Netzhautperipherie, die konfluieren und sich ausbreiten. VZV ist am häufigsten (oft schwere Fälle), gefolgt von HSV-1/2 als ätiologische Erreger. Eine rhegmatogene Netzhautablösung mit Netzhautriss tritt in etwa 75 % der Fälle auf, und die Sehprognose ist schlecht18).
ARN-Diagnosekriterien der Japanischen Gesellschaft für Augenentzündung (Gruppe der gesicherten Diagnose) :
- Frühe Augenveränderungen: ① Vorderkammerzellen oder speckige Hornhautpräzipitate, ② eine oder mehrere gelb-weiße Läsionen (peripher), ③ Netzhautarteriitis, ④ Papillenrötung, ⑤ entzündliche Glaskörpertrübung, ⑥ erhöhter Augeninnendruck. Davon sind ① und ② obligatorisch.
- Verlaufspunkte: mindestens eines der folgenden: schnelle zirkuläre Ausdehnung, Netzhautriss/-ablösung, Gefäßverschluss, Optikusatrophie, Ansprechen auf Anti-Herpes-Medikamente
- Untersuchung der intraokularen Flüssigkeit: PCR von Kammerwasser oder Glaskörperflüssigkeit positiv für HSV-1, HSV-2 oder VZV
Die klinische Diagnosegruppe (keine intraokulare Flüssigkeitsuntersuchung erforderlich) kann diagnostiziert werden, wenn zusätzlich zu den initialen Befunden ①② zwei der Punkte ③ bis ⑥ und ein Verlaufspunkt erfüllt sind.
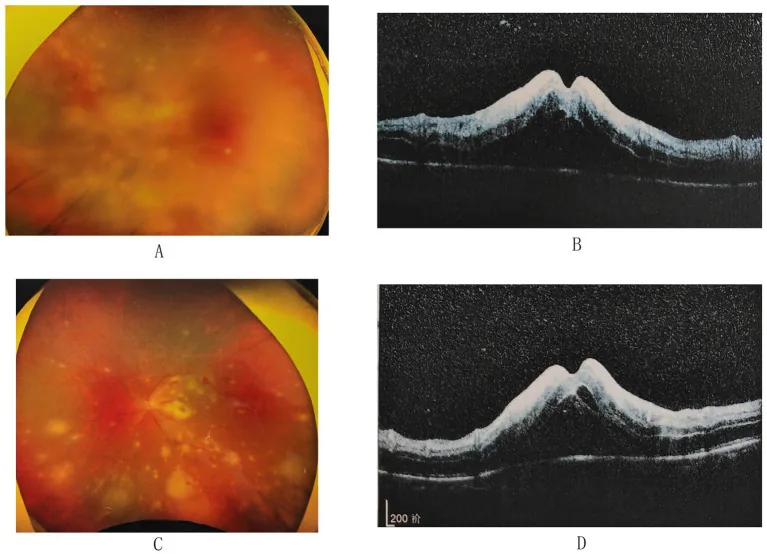
3-3. CMV網膜炎
Abschnitt betitelt „3-3. CMV網膜炎“CMVはAIDSを中心とした免疫不全患者に発症する日和見感染であり、CD4陽性T細胞数が50〜100/µLまで低下したAIDS患者に多く発症する20)。病型は①周辺部顆粒型(白色顆粒を伴う扇型病巣)、②後極部血管炎型(出血と浮腫)、③樹氷状血管炎型(大血管中心の白輯化)の3型があり、臨床上は混在することが多い。免疫回復に伴う免疫回復ぶどう膜炎(IRU)も重要な合併症であり15)、抗レトロウイルス療法開始後の眼科管理が必要である。
3-4. HTLV-1関連ぶどう膜炎(HAU)
Abschnitt betitelt „3-4. HTLV-1関連ぶどう膜炎(HAU)“HTLV-1のキャリアの**約0.1%**に発症し、九州・沖縄を中心とした地域に多い12)。白色顆粒状KP、虹彩結節、ベール状・索状・顆粒状の硝子体混濁、網膜血管周囲の白色顆粒付着が特徴的所見である。甲状腺機能亢進症を高頻度に合併する。視力予後は比較的良好であるが、ステロイドへの反応後に減量・中止で再燃することがある。
3-5. 風疹ウイルスとFuchs虹彩異色性虹彩毛様体炎
Abschnitt betitelt „3-5. 風疹ウイルスとFuchs虹彩異色性虹彩毛様体炎“Fuchs虹彩異色性虹彩毛様体炎(虹彩異色・虹彩毛様体炎・白内障の3主徴)は風疹ウイルスとの関連が示唆されている。先天風疹症候群では妊娠3か月以内の経胎盤感染により、salt-and-pepper様眼底所見を呈する網脈絡膜炎が発症する。
4. Überblick über die bakterielle Uveitis
Abschnitt betitelt „4. Überblick über die bakterielle Uveitis“4-1. Tuberkulöse Uveitis
Abschnitt betitelt „4-1. Tuberkulöse Uveitis“Die intraokulare Entzündung durch Mycobacterium tuberculosis umfasst zwei Mechanismen: direkte Infektion und immunvermittelte (Überempfindlichkeitsreaktion). Die klinischen Formen sind vielfältig und umfassen Aderhautgranulome (Knoten), seröse Netzhautablösung, Schrotschuss-Choroiditis, Vaskulitis und Panuveitis.
Für die Diagnose ist der IGRA (QuantiFERON®-TB Gold Plus oder T-SPOT®-TB) nützlich, und es ist zu beachten, dass die Tuberkulinreaktion bei älteren Menschen oder bei Patienten mit verminderter zellulärer Immunität wie AIDS negativ ausfallen kann. Hinsichtlich der Sehprognose der tuberkulösen Uveitis wurde berichtet, dass bei etwa einem Drittel der Fälle der bestkorrigierte Visus unter 3/60 fällt 3). Die vom SUN Working Group (2021) vorgeschlagenen Krankheitstypkriterien für tuberkulöse Uveitis umfassen: ① anteriore Uveitis mit Irisknötchen, ② serpiginöse Chorioiditis, ③ Aderhautknötchen (Tuberkulome), ④ multifokale Chorioiditis bei aktiver systemischer Tuberkulose und ⑤ obstruktive Netzhautvaskulitis 5). In Indien und Indonesien werden etwa 22,9 bis 48,0 % der infektiösen Uveitiden als tuberkulös angesehen 3,14), was die besondere Bedeutung in Regionen mit hoher Tuberkuloseprävalenz unterstreicht.
4-2. Syphilitische Uveitis
Abschnitt betitelt „4-2. Syphilitische Uveitis“Die durch Treponema pallidum verursachte intraokulare Entzündung wird als „großer Nachahmer“ bezeichnet und kann als anteriore, posteriore oder Panuveitis auftreten. In den letzten Jahren ist weltweit ein erneuter Anstieg zu verzeichnen, insbesondere bei Männern, die Sex mit Männern haben (MSM). Bei HIV-Koinfektion ist das Risiko einer okulären Syphilis etwa doppelt so hoch4). Weltweit werden jährlich etwa 5,7 bis 6 Millionen neue Syphilis-Infektionen (15–49 Jahre) gemeldet4), und etwa 1–1,5 % der Syphilis-Patienten entwickeln Augenveränderungen4,10).
Die Diagnose erfolgt mittels serologischer Tests (TPHA, RPR/VDRL) und wird durch die Kombination von TP-Antigen- und Nicht-TP-Methoden interpretiert. Die Behandlung richtet sich nach der Neurosyphilis: Benzylpenicillin G (Aquacillin®) 24 Millionen Einheiten/Tag i.v. für 10–14 Tage ist die erste Wahl, Ceftriaxon i.v. ist eine Alternative. Auf die Jarisch-Herxheimer-Reaktion (Fieber und Entzündungsverschlechterung innerhalb von 24 Stunden nach Behandlung) ist zu achten.
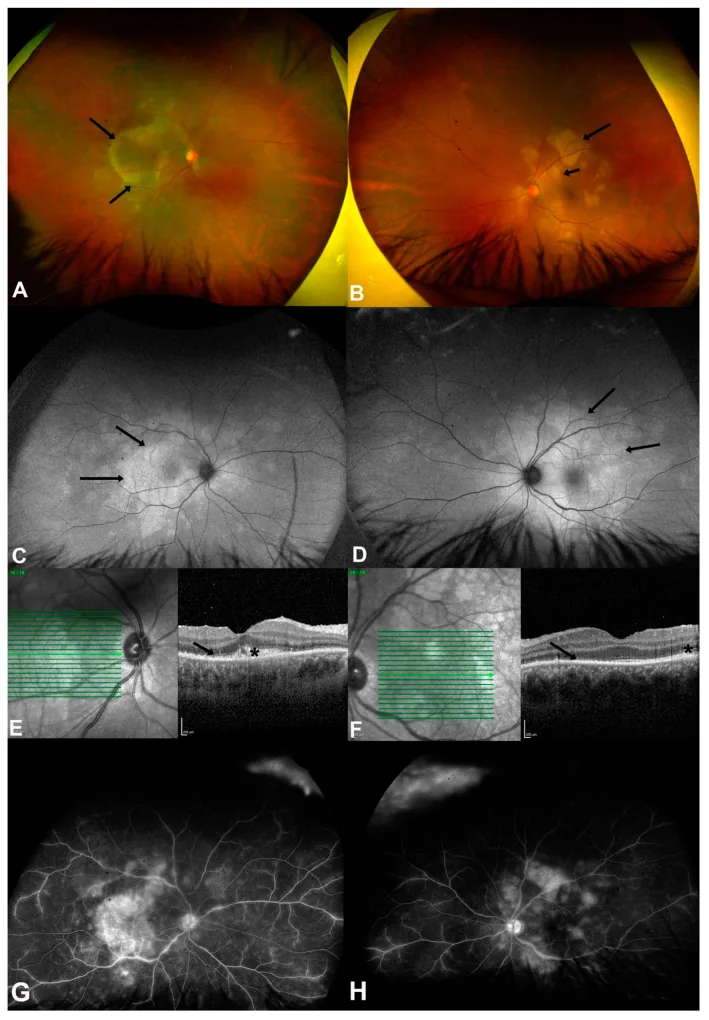
4-3. Katzenkratzkrankheit (Bartonellen-Infektion)
Abschnitt betitelt „4-3. Katzenkratzkrankheit (Bartonellen-Infektion)“Infektion durch Bartonella henselae, wobei der Kontakt zu Katzen ein wichtiger anamnestischer Punkt ist. Fundusbefunde umfassen Optikusneuritis (makuläre Sternfigur), makuläre sternförmige weiße Flecken und seröse Netzhautablösung, die häufig als hintere Uveitis auftreten. Die Diagnose erfolgt durch Messung des Anti-Bartonella-henselae-Antikörpertiters, und die antibiotische Behandlung wird mit Azithromycin, Doxycyclin oder Rifampicin durchgeführt.
4-4. Lyme-Borreliose
Abschnitt betitelt „4-4. Lyme-Borreliose“Durch Zecken übertragene Borrelien-Spirochäten-Infektion, bei der im zweiten und dritten Stadium verschiedene Augenveränderungen (Uveitis, retinale Vaskulitis, Optikusneuritis, Keratitis usw.) auftreten. Das Erythema chronicum migrans ist der charakteristische Hautausschlag des ersten Stadiums, und ein Zeckenstich ist ein diagnostischer Hinweis. Die Diagnose erfolgt durch einen Anstieg der Serum-IgM-Antikörper mittels ELISA, und die Behandlung erfolgt mit Penicillin- oder Tetracyclin-Antibiotika. Eine Abgrenzung zu Syphilis und Sarkoidose ist erforderlich.
4-5. Lepra (Hansen-Bazillus)
Abschnitt betitelt „4-5. Lepra (Hansen-Bazillus)“Chronische granulomatöse Infektion durch Mycobacterium leprae, bei der in 70–80 % (bei neueren Patienten 30–40 %) Augenveränderungen auftreten. Chronische granulomatöse anteriore Uveitis steht im Vordergrund, mit charakteristischen Befunden wie Irisperlen, Irisatrophie, Miosis und zeltförmigen peripheren anterioren Synechien. Die Behandlung erfolgt mit einer Multidrug-Therapie (Rifampicin, Dapson, Clofazimin), und bei Uveitis werden zusätzlich steroidale Augentropfen gegeben.
4-6. Endogene bakterielle Endophthalmitis
Abschnitt betitelt „4-6. Endogene bakterielle Endophthalmitis“Die endogene bakterielle Endophthalmitis, bei der sich die Infektion von anderen Organen (Leberabszess, Endokarditis, Pneumonie usw.) hämatogen im Auge ausbreitet, wird hauptsächlich durch gramnegative Stäbchen (Klebsiella, Escherichia coli usw.) verursacht und hat eine äußerst schlechte Prognose. Im Vergleich zur exogenen (postoperativen) Infektion mit grampositiven Kokken schreitet sie schneller voran, und die Suche nach der systemischen Infektionsquelle sowie deren Behandlung sind zwingend erforderlich.
5. Überblick über Pilz-Uveitis
Abschnitt betitelt „5. Überblick über Pilz-Uveitis“Die Pilz-Endophthalmitis ist überwiegend endogen, wobei Candida (Candida spp.) am häufigsten vorkommt; Aspergillus und Cryptococcus sind ebenfalls wichtige Erreger.
Hauptrisikofaktoren:
- Zentrale Venenkatheterernährung (IVH) · Verweilkatheter
- Langzeitige Anwendung von Breitbandantibiotika
- Immunsuppression (HIV-Infektion, Organtransplantation, bösartiger Tumor, Chemotherapie)
- Diabetes mellitus
- Intravenöser Drogenkonsum
Bei der Pilz-Endophthalmitis sind weiße kugelförmige oder watteartige Glaskörpertrübungen („klumpige Trübungen“) charakteristisch, und der Verlauf ist langsamer als bei der bakteriellen Endophthalmitis. Anfangs ist sie asymptomatisch oder zeigt nur leichte Mouches volantes, sodass sie leicht übersehen wird. Im Fortschreiten treten Rötung, Augenschmerzen und Panuveitis auf. 30% der endogenen Pilz-Endophthalmitiden treten an beiden Augen auf8).
Die Diagnose erfolgt mittels Blut-/Katheterspitzenkultur, β-D-Glucan, Candida-Antigenbestimmung und Glaskörperkultur. Die Behandlung basiert auf der Kombination von Antimykotika (Voriconazol, Amphotericin B, Fluconazol) und Vitrektomie.
6. Überblick über die parasitäre Uveitis
Abschnitt betitelt „6. Überblick über die parasitäre Uveitis“6-1. Augen-Toxoplasmose
Abschnitt betitelt „6-1. Augen-Toxoplasmose“Toxoplasma gondii (ein intrazellulärer Parasit) infiziert schätzungsweise ein Drittel der Weltbevölkerung, und die Seroprävalenz bei japanischen Erwachsenen beträgt 20-30%11). Katzenartige sind der Endwirt; die Infektion erfolgt durch orale Aufnahme von Oozysten aus Katzenkot oder durch den Verzehr von unzureichend gegartem Fleisch.
眼トキソプラズマ症はぶどう膜炎の原因疾患の**約1%**を占める11)。後天感染の眼底所見は周辺部の境界不鮮明な白色〜乳白色の滲出性網脲絡膜炎であり、陳旧性瘢痕病巣に接する「衛星病巣(satellite lesion)」が再発時の特徴的所見となる。前房炎症・硝子体混濁(「霧中のヘッドライト headlights in the fog」)を伴う。先天感染では両黄斑部に中心部厌白色線維性増殖と色素沈着を伴う瘢痕病巣がみられる。
診断は特徴的な眼所見と血清抗体価(IgG・IgM)の測定が主体となる。Q値(Goldmann-Witmer比)やPCRによる眼内液検査も有用である。治療はスピラマイシン酢酸エステル(アセチルスピラマイシン)あるいはクリンダマイシン1.2 g/日を4〜6週間内服し、滲出病変のコントロール目的でステロイド0.5 mg/kg/日を併用する。
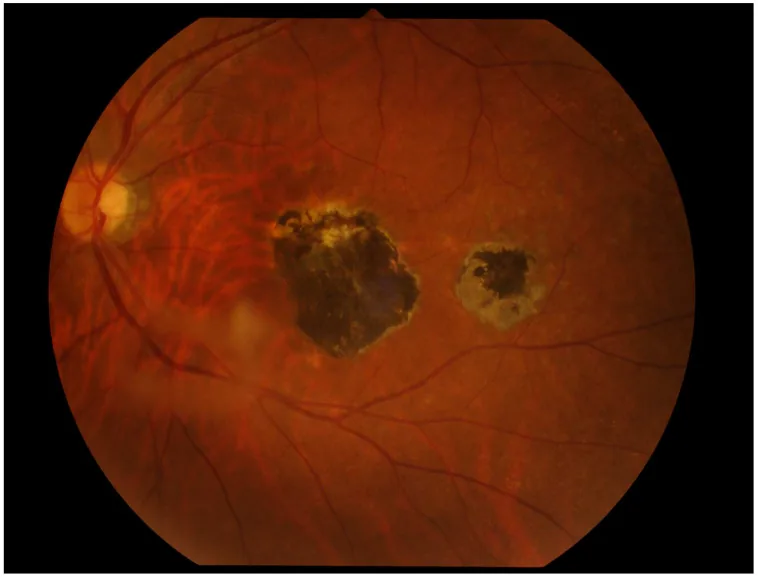
6-2. 眼トキソカラ症
Abschnitt betitelt „6-2. 眼トキソカラ症“イヌ回虫(Toxocara canis)またはネコ回虫(Toxocara cati)の幼虫移行症であり、片眼性が多い。眼内炎型・後極部腫瘤型・周辺部腫瘤型(最多)の3病型があり、強い硝子体混濁・網膜剥離をきたすことがある。ELISA(Toxocara CHECK®等)による血清抗体検索と特徴的眼所見で診断する。治療は駆虫薬(ジエチルカルバマジン)内服・ステロイド内服に加え、冷凍凝固・レーザー凝固・硝子体手術が適応となりうる。
7. Diagnosestrategie
Abschnitt betitelt „7. Diagnosestrategie“7-1. Wichtige Punkte der Anamnese
Abschnitt betitelt „7-1. Wichtige Punkte der Anamnese“Für die Diagnose einer infektiösen Uveitis ist eine systematische Anamnese unerlässlich:
- Alter und Geschlecht : CMV-Retinitis tritt häufig bei AIDS-Patienten (Männer zwischen 20 und 40 Jahren) auf, HAU bei Bewohnern von Kyushu und Okinawa
- Region und Reiseanamnese : Reisen in Gebiete mit hoher Tuberkuloseprävalenz (Südostasien, Afrika usw.)
- Tierkontakt : Katze (Toxoplasma, Bartonella), Hund (Toxocara)
- Ernährungsgeschichte : rohes Fleisch, roher Fisch (Toxoplasma)
- Sexualanamnese und HIV-Test : Syphilis, CMV
- Immunsuppression : HIV, bösartiger Tumor, Organtransplantation, Einnahme von Immunsuppressiva
- IVH- und Katheteranamnese : Pilz-Endophthalmitis
- Frühere Gürtelrose und Lippenherpes : VZV- und HSV-Iritis
7-2. Differenzialdiagnose anhand von Augenbefunden
Abschnitt betitelt „7-2. Differenzialdiagnose anhand von Augenbefunden“| Befund | Hinweis auf infektiöse Erkrankung |
|---|---|
| Mutton-Fett-KP (mutton-fat KP) | HSV/VZV-Iritis, ARN, tuberkulöse Uveitis |
| Vordere Uveitis mit erhöhtem Augeninnendruck (IOD ≥ 25 mmHg) | HSV/VZV-Iritis, CMV-vordere Uveitis |
| Periphere konfluierende weiße Nekroseherde | ARN (VZV/HSV) |
| Weißes Infiltrat mit hinterer Polblutung | CMV-Retinitis (vaskulitischer Typ) |
| Klumpige Glaskörpertrübung (wachsend) | Pilzendophthalmitis |
| Schleier- oder strangförmige Glaskörpertrübung | HTLV-1-assoziierte Uveitis |
| Alte Narbe + Satellitenherde | Okuläre Toxoplasmose |
| Peripherer weißer Tumor + Glaskörperstrang | Okuläre Toxokariasis |
| Granulomatöse Iritis + Aderhautgranulom | Tuberkulöse Uveitis, syphilitisch |
| Papillitis + makulärer Sternfleck | Katzenkratzkrankheit (Bartonella) |
7-3. Systemische Untersuchungen
Abschnitt betitelt „7-3. Systemische Untersuchungen“| Untersuchung | Zielerkrankungen |
|---|---|
| Serum-TPHA und RPR/VDRL | Syphilitische Uveitis |
| IGRA (QuantiFERON, T-SPOT) | Tuberkulöse Uveitis |
| CMV-Antigenämie (C7-HRP-Methode) und CMV-PCR | CMV-Retinitis |
| Anti-HTLV-1-Antikörper | HTLV-1-assoziierte Uveitis |
| Anti-HIV-Antikörper und CD4-Zahl | CMV/PORN/okuläre Syphilis |
| β-D-Glucan und Candida-Antigen | Pilz-Endophthalmitis |
| Anti-Toxoplasma IgG/IgM | Okuläre Toxoplasmose |
| Anti-Toxocara-Antikörper (ELISA) | Okuläre Toxokariasis |
| Anti-Bartonella-henselae-Antikörper | Katzenkratzkrankheit |
| Blutkultur und Echokardiographie | Endogene bakterielle Endophthalmitis |
7-4. Untersuchung der Intraokularflüssigkeit (Kammerwasser und Glaskörper)
Abschnitt betitelt „7-4. Untersuchung der Intraokularflüssigkeit (Kammerwasser und Glaskörper)“Die Untersuchung der Intraokularflüssigkeit ist die wichtigste Bestätigungsmethode für die Diagnose einer infektiösen Uveitis. Die Proben werden durch Vorderkammerpunktion (Kammerwasserentnahme) oder Vitrektomie (Glaskörperentnahme) gewonnen 9).
PCR-Methode
Abschnitt betitelt „PCR-Methode“Aus Kammerwasser oder Glaskörper wird DNA extrahiert und die DNA jedes Erregers mittels PCR nachgewiesen. Die Multiplex-Echtzeit-PCR ermöglicht den umfassenden Nachweis mehrerer Viren in einer kleinen Probe und ist besonders nützlich für die Differentialdiagnose der akuten retinalen Nekrose 19).
Kit für infektiöse Uveitis (fortschrittliche Medizin): Ermöglicht die gleichzeitige Suche nach HSV-1/2, VZV, CMV, EBV, HHV-6/7, HTLV-1, Toxoplasma gondii-DNA usw. und wird für die Diagnose von Mehrfachinfektionen und therapierefraktären Fällen verwendet. Beachten Sie jedoch, dass die CMV-Retinitis im Frühstadium (bevor Entzündungszellen in der Vorderkammer auftreten) möglicherweise nicht durch PCR nachweisbar ist.
Goldmann-Witmer-Quotient (Q-Wert, Antikörperrate)
Abschnitt betitelt „Goldmann-Witmer-Quotient (Q-Wert, Antikörperrate)“Dies ist eine Methode zum Nachweis des Vorhandenseins oder Fehlens einer pathogenspezifischen Antikörperproduktion im Auge und wird mit der folgenden Formel berechnet:
Q-Wert = (Virusantikörpertiter im Intraokularflüssigkeit ÷ IgG-Menge im Intraokularflüssigkeit) ÷ (Virusantikörpertiter im Serum ÷ IgG-Menge im Serum)
- Q-Wert > 1: Möglichkeit einer lokalen Antikörperproduktion im Auge
- Q-Wert ≥6: Signifikante lokale Antikörperproduktion bestätigt, das betreffende Virus kann als ätiologisches Agens identifiziert werden
Beachten Sie, dass der Q-Wert innerhalb der ersten 10 Tage nach Krankheitsbeginn unterschätzt wird, da die intraokuläre Antikörperproduktion unzureichend ist. Die ätiologische Diagnose kann nicht allein anhand des Serumantikörpertiters gestellt werden (die meisten Erwachsenen sind aufgrund einer früheren Infektion positiv) 6).
PCR-Auswahlfluss für Intraokularflüssigkeiten
Abschnitt betitelt „PCR-Auswahlfluss für Intraokularflüssigkeiten“眼内炎症患者 ├─ ウイルス性疑い(高眼圧・前房炎症・壊死性網膜炎) │ → 前房水PCR(HSV/VZV/CMV)+ Q値 ← 第一選択 │ ─ 前房水で陰性かつ壊死性病変 → 硝子体液PCR │ ─ 免疫不全者 → マルチプレックスPCR(先進医療) ├─ 寄生虫疑い(衛星病巣・周辺部腫瘤) │ → 眼内液Q値(Toxoplasma)または眼内液PCR ├─ 真菌疑い(塊状混濁・リスク因子あり) │ → 硝子体液培養 + β-D-グルカン(血液) └─ 細菌疑い(急速進行・IVH歴) → 硝子体液グラム染色・培養(至急)8. Behandlungsprinzipien
Abschnitt betitelt „8. Behandlungsprinzipien“8-1. Erregerspezifische Behandlung
Abschnitt betitelt „8-1. Erregerspezifische Behandlung“| Erreger | Erstlinientherapie | Anmerkungen |
|---|---|---|
| HSV (ARN, Iritis) | ACV 10 mg/kg × 3×/Tag i.v. 2 Wochen → VACV 1.000 mg × 3×/Tag oral | Kombination mit Steroid-Augentropfen und i.v. zur Entzündungshemmung |
| VZV (ARN・Iritis) | ACV 10-15 mg/kg x3 i.v. + VACV oral | PORN wird wie CMV behandelt |
| CMV (Retinitis) | GCV 5 mg/kg x2 i.v. 2-3 Wochen (Induktion) → VGCV 900 mg x2/Tag oral (Erhaltung) | Immunwiederherstellung ist die kurative Therapie |
| CMV (vordere Uveitis) | GCV-Gel 0,15% Augentropfen (73% der Spezialisten als erste Wahl) ± VGCV oral | Bei chronischem Verlauf auch 12-monatige Erhaltungstherapie erwägen (73% der Spezialisten wählen GCV-Gel 0,15%) 2) |
| Tuberkulose | INH, RFP, PZA, EMB Vierfachtherapie (Standard-6-Monats-Regime) | Bei Bedarf Kortikosteroide ergänzend |
| Syphilis | Benzylpenicillin G 24 Millionen Einheiten/Tag i.v. 10-14 Tage | Achtung auf Herxheimer-Reaktion |
| Pilze (Candida) | Voriconazol oder Amphotericin B ± Vitrektomie | Überwachung mittels β-D-Glucan-Index |
| Toxoplasma | Acetylspiramycin + Steroid oder Clindamycin | Vorsicht bei Schwangeren (Spiramycin verwenden) |
| Toxocara | Diethylcarbamazin + Steroid | Erwägung von Laser oder Vitrektomie |
| Lyme-Borreliose | Amoxicillin oder Doxycyclin 3 Wochen | Bei Augenläsionen zusätzlich Steroid-Augentropfen |
| Lepra | MDT (Rifampicin, DDS, Clofazimin) | Bei Leprareaktion sind Steroide erforderlich |
8-2. Angemessene Anwendung von Steroiden
Abschnitt betitelt „8-2. Angemessene Anwendung von Steroiden“Bei infektiöser Uveitis muss bei der Anwendung von Steroiden immer eine antipathogene Behandlung vorausgehen oder parallel erfolgen. Die Rolle der Steroide besteht darin, sekundäre Gewebeschäden durch Entzündungen zu reduzieren. Sie werden bei vielen infektiösen Uveitiden wie ARN, Toxoplasmose, tuberkulöser Uveitis und Lepra-Uveitis in Kombination mit einer geeigneten antipathogenen Behandlung eingesetzt.
Andererseits wird bei CMV-Retinitis (reine opportunistische Infektion) die Verbesserung der Immunfunktion durch Behandlung der Grunderkrankung (AIDS) als kurative Therapie angesehen, und Steroide werden grundsätzlich nicht eingesetzt.
8-3. Mydriatika und Augeninnendruckmanagement
Abschnitt betitelt „8-3. Mydriatika und Augeninnendruckmanagement“Zur Vorbeugung von hinteren Synechien der Iris werden bei Entzündungen des vorderen Augenabschnitts Tropicamid-Phenylephrin-Augentropfen (1-6 mal täglich) verwendet. Bei erhöhtem Augeninnendruck (charakteristisch für HSV/VZV-Iritis und CMV-Anterior-Uveitis) werden drucksenkende Mittel wie Carboanhydrasehemmer und Betablocker ausgewählt. Prostaglandin-bezogene Medikamente bergen jedoch ein Risiko der Entzündungsverschlimmerung und sollten mit Vorsicht angewendet werden.
9. Risikomatrix nach Immunsuppressionsstatus
Abschnitt betitelt „9. Risikomatrix nach Immunsuppressionsstatus“| Hintergrund | Besonders zu beachtende Erreger | Priorisierte Tests |
|---|---|---|
| HIV-Infektion (CD4 < 50/µL) | CMV (Retinitis, ARN, PORN), Pilze (Cryptococcus), Syphilis | Intraokulare Flüssigkeits-PCR (Multiplex), CMV-Antigen, β-D-Glucan |
| Nach solider Organtransplantation und Immunsuppressiva-Einnahme | CMV, Pilze (Aspergillus, Candida), EBV | CMV-PCR, β-D-Glucan, Blutkultur |
| Nach bösartigem Tumor und Chemotherapie | Pilze (Candida, Aspergillus), CMV | β-D-Glucan, Blutkultur |
| Langzeit-IVH / Katheterverweil | Candida-Endophthalmitis | β-D-Glucan / Blutkultur (Augenarztkonsultation obligatorisch) |
| Hohes Tuberkuloserisiko (Reise-/Kontaktgeschichte) | Tuberkulose (Aderhautgranulom / Vaskulitis-Typ) | IGRA / Thorax-CT |
| MSM (Männer, die Sex mit Männern haben) · HIV+ | Syphilis (okuläre Syphilis ca. 1–1,5 %), CMV | TPHA · RPR · HIV-Test |
| Immunkompetent (mittleres Alter oder älter) | HSV/VZV-Iridozyklitis · ARN | Kammerwasser-PCR · Q-Wert |
| Kinder / Haustierkontakt in der Vorgeschichte | Toxocara / Toxoplasma | Serumantikörper (ELISA) |
10. Häufig gestellte Fragen
Abschnitt betitelt „10. Häufig gestellte Fragen“Wenn allein anhand der klinischen Befunde eine Unterscheidung zwischen infektiöser und nicht-infektiöser Ursache schwierig ist oder bei Verdacht auf eine Infektion die serologischen Tests negativ ausfallen, wird eine Vorderkammerpunktion aktiv in Betracht gezogen. Insbesondere bei Verdacht auf nekrotisierende Retinitis (ARN, PORN, CMV-Retinitis) ist eine frühzeitige definitive Diagnose direkt mit der Therapiewahl und Prognose verbunden, daher wird nach Möglichkeit eine PCR der Intraokularflüssigkeit durchgeführt. Bei initial PCR-negativen oder therapierefraktären Fällen ist die Multiplex-PCR hilfreich.
Führen Sie zunächst umgehend eine PCR der Intraokularflüssigkeit zur Erregeridentifikation durch und beginnen Sie mit der spezifischen Therapie, sobald der Erreger identifiziert ist. Ein abruptes Absetzen der Steroide kann zu einem Entzündungsrebound führen, daher reduzieren Sie die Dosis vorsichtig nach Beginn der antiinfektiösen Therapie. Insbesondere bei tuberkulöser Uveitis, wenn Steroide allein verabreicht wurden, ist das Risiko einer Reaktivierung und Dissemination einer latenten Tuberkulose erhöht; eine dringende systemische Abklärung (CT-Thorax, IGRA) sollte in Zusammenarbeit mit der Pneumologie erfolgen.
Auch nach Therapieende verbleibt Toxoplasma als medikamentenresistente Zyste in atrophischen Narbenherden. Bei etwa 5–30 % der Fälle kommt es zu einem Rezidiv, ausgelöst durch Immunschwäche oder Schwangerschaft. Bei Patienten mit häufigen Rezidiven kann eine langfristige Prophylaxe mit Trimethoprim-Sulfamethoxazol in Betracht gezogen werden. Während der Schwangerschaft besteht bei einer Toxoplasma-Antikörper-negativen Schwangeren, die eine Erstinfektion erleidet, ein Risiko der vertikalen Übertragung auf den Fötus (ca. 40 %); daher sollte der Kontakt mit Katzenkot, Erde und der Verzehr von rohem Fleisch vermieden werden.
11. Verwandte Artikel
Abschnitt betitelt „11. Verwandte Artikel“Virale Uveitis
Abschnitt betitelt „Virale Uveitis“Bakterielle und andere infektiöse Uveitis
Abschnitt betitelt „Bakterielle und andere infektiöse Uveitis“Literaturverzeichnis
Abschnitt betitelt „Literaturverzeichnis“- 日本眼炎症学会ぶどう膜炎診療ガイドライン作成委員会. ぶどう膜炎診療ガイドライン. 日眼会誌. 2019;123(6):635–702.
- Thng ZX, Putera I, Testi I, et al. The Infectious Uveitis Treatment Algorithm Network (TITAN) Report 2—global current practice patterns for the management of Cytomegalovirus anterior uveitis. Eye. 2023. https://doi.org/10.1038/s41433-023-02503-3
- Putera I, Schrijver B, ten Berge JCEM, et al. The immune response in tubercular uveitis and its implications for treatment: From anti-tubercular treatment to host-directed therapies. Prog Retin Eye Res. 2023;95:101173.
- Chauhan K, Fonollosa A, Giralt L, et al. Demystifying Ocular Syphilis – A Major Review. Ocul Immunol Inflamm. 2023. https://doi.org/10.1080/09273948.2023.2217246
- Jabs DA, et al. Standardization of Uveitis Nomenclature (SUN) Working Group. Classification Criteria for Tubercular Uveitis. Am J Ophthalmol. 2021;228:142–149.
- 八代成子. ウイルス性ぶどう膜炎の診断と治療. 眼科. 2007;49:1193–1198.
- 大野重昭. ぶどう膜炎の疫学と分類. 日眼会誌. 2019;123(6).
- Tsirouki T, Dastiridou A, Symeon CI, et al. A focus on the epidemiology of uveitis. Ocul Immunol Inflamm. 2018;26(1):2–16.
- 慶野博. 感染性ぶどう膜炎の眼内液診断. 臨床眼科. 2019.
- Oliver SE, Aubin M, Atwell L, et al. Ocular Syphilis — Eight Jurisdictions, United States, 2014–2015. MMWR Morb Mortal Wkly Rep. 2016;65:1185–1188.
- 岡田アナベルあやめ. 眼トキソプラズマ症の診断と治療. 眼科. 2018.
- 中尾久美子. HTLV-1関連ぶどう膜炎の疫学と治療. 日本臨床. 2020.
- La Distia Nora R, et al. Infectious uveitis etiology in developing vs. developed countries. Curr Opin Ophthalmol. 2021.
- Agrawal R, et al. Collaborative Ocular Tuberculosis Study (COTS)—Report 1. Ophthalmology. 2019;126(11):1566–1577.
- 八代成子. CMV網膜炎・免疫回復ぶどう膜炎の管理. 眼科. 2007.
- Kempen JH, et al. The prevalence of uveitis in the United States. Arch Ophthalmol. 2004;122(4):543–557.
- Groen-Hakan F, et al. Diagnostic value of aqueous humor analysis for uveitis. Ocul Immunol Inflamm. 2020.
- 堤雅幸. 急性網膜壊死診断基準(日本眼炎症学会). 日眼会誌. 2020.
- 蕪城俊克. 眼内液PCRによるウイルス性ぶどう膜炎診断. 眼科. 2021.
- Bodaghi B, et al. Blindness prevention in HIV patients: CMV retinitis management update. Prog Retin Eye Res. 2023.
