NF1與TSC(mTOR路徑)

母斑症的眼部症狀
一目瞭然的要點
Section titled “一目瞭然的要點”1. 什麼是斑痣性錯構瘤病的眼部症狀?
Section titled “1. 什麼是斑痣性錯構瘤病的眼部症狀?”斑痣性錯構瘤病是一組以皮膚、中樞神經系統和眼睛的錯構瘤性病變為特徵的先天性疾病總稱。也稱為神經皮膚症候群。
該命名由荷蘭眼科醫生Van der Hoeve提出,源自希臘語“phakos”(透鏡或斑點)。最初包括神經纖維瘤病、結節性硬化症和馮·希佩爾-林道病,隨後加入了斯特奇-韋伯症候群和毛細血管擴張性運動失調症。目前已有超過60種症候群被描述。
共同的病理基礎是神經嵴細胞的形成、遷移和分化異常。由於神經嵴細胞來源於外胚層,產生許旺細胞、黑色素細胞等多種細胞,因此神經、皮膚和眼睛等多個器官會出現病變。已知涉及的訊號通路包括RAS、MAPK/MEK、mTOR、PI3K/AKT、GNAQ和VHL-HIF通路。
六大主要疾病的發生頻率如下。
| 疾病 | 發生率(每X人中1例) |
|---|---|
| NF1(神經纖維瘤病1型) | 3,000~5,000 |
| 結節性硬化症(TSC) | 6,000~10,000 |
| SWS(史德奇-韋伯症候群) | 20,000~50,000 |
| VHL(馮·希佩爾-林道病) | 36,000 |
| NF2(神經纖維瘤病第2型) | 25,000~100,000 |
| 毛細血管擴張性運動失調症(AT) | 88,000至100,000以下 |
2. 主要症狀與臨床所見
Section titled “2. 主要症狀與臨床所見”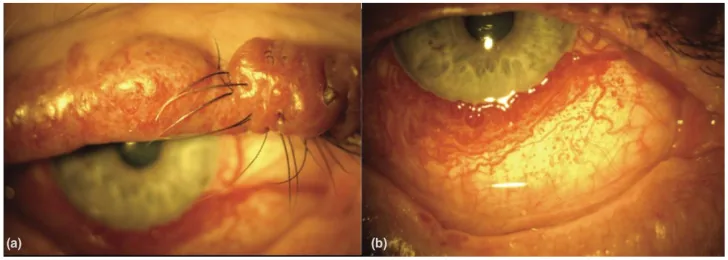
各疾病的眼部併發症類型不同,自覺症狀也多樣。
- NF1:視路腫瘤(視神經膠質瘤)進展時,會出現視力下降、色覺喪失和視野缺損。叢狀神經纖維瘤可能導致眼球突出。
- 結節性硬化症:視網膜星形細胞錯構瘤通常無症狀。當累及黃斑或視盤時,會導致視力障礙。
- SWS:伴有先天性青光眼時,會出現角膜混濁、流淚和畏光。遲發性青光眼導致無痛性進行性視野缺損。
- VHL:早期無症狀。視網膜微血管瘤進展時出現滲出性變化、黃斑部水腫、環狀白斑,導致視力下降。
- AT:視力通常維持正常。主要表現為眼球運動障礙(眼震、眼球運動失用)。
NF1(神經纖維瘤病第一型)的眼部表現
Section titled “NF1(神經纖維瘤病第一型)的眼部表現”- Lisch結節:NF1最常見的眼部表現。虹膜上多發淡褐色、邊界清晰、圓頂狀小結節(<1–2 mm)。年齡別盛行率:<3歲5%,3–4歲42%,5–6歲55%,≥21歲100%,隨年齡增加,並納入NF1診斷標準(≥2個)。日本人虹膜顏色偏棕,因此裂隙燈下仔細檢查很重要。
- 視路腫瘤(視神經膠質瘤):約15–25%的NF1患者合併。多為低惡性度毛細胞星狀細胞瘤,常無症狀。進展時可導致視神經萎縮、視力障礙和視野缺損。可能侵犯視交叉。
- 叢狀神經纖維瘤:發生於不到10%的NF1患者。特徵為眼瞼的「S形變形」,觸診時有「蟲袋」樣感覺。可導致眼球突出、斜視、弱視和先天性青光眼。
- 蝶骨翼發育不全:眼眶骨壁的先天性缺損,可能引起搏動性眼球突出。
- 青光眼:發生於1-2%的NF1患者。有先天性(單眼)和遲發性兩種型態。
- 其他:角膜有髓神經纖維明顯、脈絡膜增厚、視網膜有髓神經纖維。
NF2(神經纖維瘤病第2型)的眼部表現
Section titled “NF2(神經纖維瘤病第2型)的眼部表現”- 視神經鞘腦膜瘤:NF2的特徵性表現。與NF1的視路膠質瘤形成對比的腫瘤類型。
- 白內障:可見青年性白內障。
- 視網膜/RPE過誤瘤、視網膜上膜:可能合併出現。
- 暴露性角膜炎:雙側聽神經瘤導致第V、第VII腦神經功能障礙,引起面部麻木、複視、兔眼,繼發暴露性角膜炎。
- Lisch結節罕見。
結節性硬化症(TSC)的眼部表現
Section titled “結節性硬化症(TSC)的眼部表現”- 視網膜星形細胞過誤瘤:約50%合併出現。分為三型:(i) 扁平、半透明、非鈣化型;(ii) 隆起、多結節、鈣化型(桑葚樣外觀);(iii) 過渡型。通常在後極部可見多個。
- 視網膜脫色素病變:呈現「打孔狀」外觀。
- 視網膜血管異常:可能出現動脈瘤樣擴張和動靜脈畸形,導致玻璃體出血、增殖性玻璃體視網膜病變和視網膜剝離。
- 其他:眼瞼血管纖維瘤、虹膜脫色素斑、非典型脈絡膜缺損。
SWS(史德奇-韋伯症候群)的眼部表現
Section titled “SWS(史德奇-韋伯症候群)的眼部表現”三大主要特徵為:(1)三叉神經分布區的臉部血管瘤,(2)同側顱內血管瘤,(3)同側青光眼或脈絡膜血管瘤。
- 青光眼:SWS最重要的眼部表現。發生率30%~70%。先天性青光眼(出生至4歲)約佔60%,導致牛眼、角膜混濁和大角膜。病因被認為涉及隅角發育異常、鞏膜上靜脈壓升高和脈絡膜血管瘤。在眼瞼血管瘤存在時發生頻率高。
- 脈絡膜血管瘤:約20-70%的患者發生。瀰漫性、邊界不清,常規眼底檢查難以識別。眼底呈「番茄醬樣」外觀。通常無增大趨勢,但可引起滲出性變化和滲出性視網膜剝離。
- 其他:結膜、上鞏膜和虹膜的血管擴張迂曲。
VHL(馮·希佩爾-林道病)的眼部表現
Section titled “VHL(馮·希佩爾-林道病)的眼部表現”- 視網膜毛細血管瘤(血管母細胞瘤):43-85%的VHL患者發生(國內報告約60%)。約1/3為雙眼性、多發性。好發於視網膜顳側周邊部,表現為伴有擴張迂曲的輸入和輸出血管的橙紅色結節。平均發病年齡為25歲,通常在30歲前出現。
- 進展可引起滲出性改變、視網膜出血、黃斑水腫、環狀白斑和視力下降。
- 進一步進展可導致玻璃體出血、牽拉性視網膜剝離、新生血管性青光眼和失明。
- 螢光眼底攝影顯示染劑流入輸入動脈→輸出靜脈灌流,腫瘤區域早期出現明顯染劑滲漏。
AT(毛細血管擴張性運動失調症)的眼部表現
Section titled “AT(毛細血管擴張性運動失調症)的眼部表現”- 球結膜毛細血管擴張:最常見的眼部表現。通常在5~8歲前出現,見於80%~90%的患者1)。
- 眼球運動障礙:可見眼震、眼球運動失用、掃視異常、輻輳與調節異常、斜視。
- 視力通常維持正常。
3. 原因與風險因素
Section titled “3. 原因與風險因素”各疾病的遺傳形式、致病基因和染色體座位如下所示。
| 疾病 | 遺傳形式 | 致病基因 | 染色體座位 |
|---|---|---|---|
| NF1 | 體染色體顯性 | NF1 | 17q11.2 |
| NF2 | 體染色體顯性 | NF2 | 22q11.1-q13.1 |
| TSC | 體染色體顯性 | TSC1/TSC2 | 9q34/16p13 |
| VHL | 體染色體顯性 | VHL | 3p25-26 |
| SWS | 散發性(體細胞鑲嵌) | GNAQ | 9q21 |
| AT | 體染色體隱性 | ATM | 11q22 |
各疾病的遺傳特徵如下。
- NF1:約50%為新發突變。幾乎完全外顯,但表現型多樣。神經纖維蛋白作為RAS-GAP,將GTP-RAS轉化為GDP-RAS2)。
- NF2:梅林蛋白功能喪失。主要表現於許旺細胞和腦膜細胞的腫瘤抑制因子,其缺失導致許旺瘤、腦膜瘤和室管膜瘤。
- TSC:散發病例約佔2/3。TSC2突變佔散發病例的75-80%,且比TSC1突變表現更嚴重的表型1)。錯構蛋白/結節蛋白直接抑制mTOR路徑2)。
- SWS:散發性,由GNAQ基因體細胞嵌合突變引起1)。累及三叉神經第一支(V1)整個區域的葡萄酒色斑(PWB)具有較高的眼部和神經系統併發症風險。
- VHL:外顯率幾乎100%,約20%為新發突變。pVHL參與HIF-α的泛素化和蛋白酶體降解2)。第1型(無嗜鉻細胞瘤)約佔80%,第2型(有嗜鉻細胞瘤)約佔20%2)。
- AT:體染色體隱性遺傳,ATM激酶參與DNA雙股斷裂修復及基因組穩定性維持1)。惡性腫瘤(淋巴系統)風險及放射線敏感性顯著增高。
4. 診斷與檢查方法
Section titled “4. 診斷與檢查方法”NF1的診斷與眼科檢查
Section titled “NF1的診斷與眼科檢查”NF1的診斷標準(NIH標準、日本皮膚科學會2008年)需滿足以下7項中的2項或以上方可確診。
- 6個或更多咖啡牛奶斑(青春期前:最大直徑≥5mm;青春期後:≥15mm)
- 2個或更多神經纖維瘤或1個瀰漫性神經纖維瘤
- 腋窩或腹股溝區雀斑樣色素沉著
- 視神經膠質瘤
- 2個或更多Lisch虹膜結節
- 特徵性骨病變(如蝶骨發育不良)
- 一等親患有相同疾病
眼科檢查的作用如下。
- 裂隙燈顯微鏡:檢測Lisch結節(在年輕患者中可能困難)。
- 眼前段OCT和超音波生物顯微鏡:有助於輔助檢測Lisch結節。
- MRI:視路腫瘤的最佳診斷方法。對視交叉和視束的評估至關重要。
- 視野檢查:視路腫瘤篩查(在幼兒中難以實施)。
- 光學同調斷層掃描(OCT):評估視路腫瘤相關的視網膜神經纖維層變薄。
- VEP(視覺誘發電位):早期檢測視神經損傷。
- 定期檢查間隔:僅有Lisch結節→每年1次。伴有視神經膠質瘤→每3個月1次。
NF2的診斷
Section titled “NF2的診斷”臨床標準中,雙側前庭神經鞘瘤是特徵性表現。由於皮膚症狀不明顯,診斷可能比NF1更困難。基因檢測可檢出90%以上的突變。CT/MRI可確認雙側聽神經瘤。
結節性硬化症(TSC)的診斷
Section titled “結節性硬化症(TSC)的診斷”確診需符合2項主要特徵,或1項主要特徵加上2項以上次要特徵。TSC1/TSC2致病性變異的鑑定被認可為獨立的診斷標準1)。
視網膜星狀細胞缺陷瘤的評估使用眼底檢查、螢光眼底攝影和OCT。最重要的鑑別診斷是視網膜母細胞瘤。根據兒童期無鈣化、營養血管稀少、伴隨全身症狀的特點可進行鑑別,但與桑椹狀腫瘤的鑑別有時較困難。
SWS的診斷
Section titled “SWS的診斷”Roach診斷量表要求至少符合面部葡萄酒色斑、眼壓升高、軟腦膜血管瘤中的兩項1)。增強深度OCT和MRI對脈絡膜血管瘤的評估有幫助。頭部CT顯示腦皮質內鈣化。
青光眼的監測需要定期進行眼壓測量、視神經評估和視野檢查。嬰幼兒可能需要在麻醉下進行裂隙燈檢查、眼底檢查和眼壓測量。
VHL的診斷
Section titled “VHL的診斷”基因檢測幾乎100%能檢測出VHL突變,是目前確診的主流方法。建議從1歲起每年進行一次散瞳眼底檢查。周邊部橙紅色球形腫瘤伴擴張迂曲血管是特徵性表現。螢光眼底造影有助於發現小的周邊部血管母細胞瘤,OCT用於評估小病變。
臨床診斷中,共濟失調、球結膜毛細血管擴張和眼球運動異常三聯徵很重要。實驗室檢查可見血清AFP升高、CA125升高和ATM蛋白缺失(Western blot)。球結膜毛細血管擴張是本病的特徵性表現(pathognomonic)。MRI顯示後顱窩瀰漫性小腦萎縮,尤其是蚓部和半球1)。
5. 標準治療方法
Section titled “5. 標準治療方法”NF1的眼部相關治療
Section titled “NF1的眼部相關治療”- Lisch結節:無症狀的錯構瘤,無需治療。
- 視神經膠質瘤:進行性病例考慮手術切除,但視功能喪失且術後併發症多。視交叉浸潤病例適用化學治療。
- 蔓狀神經纖維瘤:手術完全切除困難且易復發。進行病例可能需要眼眶內容物剜除術。不可切除病例可使用司美替尼(MEK抑制劑)作為新療法1)。
- 青光眼:按照常規青光眼治療進行管理。
NF2的治療
Section titled “NF2的治療”前庭神經鞘瘤以手術切除為基本治療,小於3cm的腫瘤中65%可保留聽力1)。暴露性角膜炎使用人工淚液、角膜保護眼鏡,必要時行瞼板縫合處理。
結節性硬化症(TSC)的眼部相關治療
Section titled “結節性硬化症(TSC)的眼部相關治療”- 視網膜星形細胞過誤瘤:通常無增大趨勢,無需治療。
- 視網膜血管異常(動脈瘤樣擴張、動靜脈畸形):因有玻璃體出血和視網膜剝離的風險,需進行預防性光凝治療。若發生玻璃體出血或視網膜剝離,考慮玻璃體手術。
- 癲癇:嬰兒局部性發作和嬰兒點頭痙攣的首選治療為氨己烯酸1)。SEGA(室管膜下巨細胞星形細胞瘤)需神經外科手術切除1)。
SWS的眼部治療
Section titled “SWS的眼部治療”青光眼的治療根據發病年齡而有所不同。
- 先天性青光眼(早發型):必須手術治療。選擇小樑切開術或隅角切開術。需注意脈絡膜剝離和出血,由於鞏膜上靜脈壓升高,併發症風險高於常規。對藥物治療往往有抗藥性。
- 晚期發病型:首先進行藥物治療,無效時考慮手術。
脈絡膜血管瘤的治療根據有無滲出性變化從以下選擇。
- 出現滲出性變化時→光凝固
- 光凝固無效或滲出性視網膜剝離→放射治療(總劑量約20戈瑞)。可期待大皰性視網膜剝離復位和血管瘤縮小。
- 難治病例→玻璃體手術
- 光動力療法(PDT)和外照射放射治療也可能是選擇3)。
VHL的眼部治療
Section titled “VHL的眼部治療”早期治療是原則。
- 光凝固(首選):使用氬雷射或染料雷射,先緻密凝固血管瘤周圍的視網膜和營養血管,然後直接凝固瘤體。對於大於2個視盤直徑的腫瘤,先凝固流入動脈和周圍視網膜,再直接凝固腫瘤。
- 冷凍凝固:當眼底周邊部或巨大血管瘤導致光凝固困難時,經鞏膜施行。
- 玻璃體切除術:當滲出性變化嚴重、發生視網膜剝離或出現增殖性變化時考慮。
- 末期病例:需要管理新生血管性青光眼。
- 如有家族史,應對所有家庭成員進行眼底檢查,早期治療可望獲得良好預後。
結膜毛細血管擴張沒有特異性治療。對於免疫缺陷,進行預防性抗生素和靜脈注射免疫球蛋白(IVIg)治療1)。共濟失調以對症治療為主。
對於VHL,建議從1歲開始每年進行一次散瞳眼底檢查。已確認VHL基因突變的患者的所有家庭成員也應接受眼底檢查,早期治療有望獲得良好的視功能預後。
6. 病理生理學與詳細發病機制
Section titled “6. 病理生理學與詳細發病機制”各疾病的分子層級發病機制如下所示。
VHL(HIF路徑)
pVHL:E3泛素連接酶複合體(elongin B/C、Cullin 2、RBX1)的組成部分。在正常氧氣條件下,脯氨醯羥化酶將HIF-α羥化→pVHL辨識→泛素化→蛋白酶體降解。
VHL突變:持續出現假性缺氧狀態→HIF-α累積→與HIF-1β形成異二聚體→VEGF、紅血球生成、代謝和細胞增殖相關基因的轉錄活化→血管腫瘤形成2)。
- NF2(merlin):腫瘤抑制蛋白,在許旺細胞和軟腦膜細胞中表現。突變導致許旺瘤、腦膜瘤和室管膜瘤。
- SWS(GNAQ體細胞嵌合突變):G蛋白相關跨膜訊息傳導異常。胚胎中突變的時間和位置導致三叉神經區域、顱內和眼部的表現模式不同1)。GNAQ也是SWS、KTS和PPV的共同分子基礎3)。
- AT(ATM激酶):參與DNA雙股斷裂修復和基因組穩定性維持的腫瘤抑制因子。突變→DNA修復障礙→癌症易感性、放射敏感性顯著增加和免疫缺陷1)。
Chevalier等人(2021)研究了母斑症與內分泌腫瘤的關聯,報告指出NF1、TSC和VHL的訊息傳導路徑(RAS-PI3K-Akt-mTOR路徑、HIF路徑)共同參與多發性內分泌腫瘤的發生2)。
母斑症共同的病理生理基礎是神經嵴細胞的形成、遷移和分化異常。神經嵴細胞來源於外胚層,產生許旺細胞、黑色素細胞等多種細胞,因此病變會波及神經、皮膚、眼睛等多個器官。此外,RAS-mTOR路徑和VHL-HIF路徑等共同訊息傳導路徑的突變促進了跨器官的腫瘤發生。
7. 最新研究與未來展望(研究階段報告)
Section titled “7. 最新研究與未來展望(研究階段報告)”司美替尼(MEK抑制劑)
Section titled “司美替尼(MEK抑制劑)”一種獲得FDA核准用於不可切除的叢狀神經纖維瘤的分子標靶藥物。它靶向NF1中MAPK路徑的過度活化1)。
布格替尼(ALK抑制劑衍生物)
Section titled “布格替尼(ALK抑制劑衍生物)”針對NF2相關許旺氏瘤和進展性腫瘤的臨床試驗由INTUITT-NF2聯盟進行,已報告有希望的結果1)。
HIF-2α抑制劑(VHL相關腫瘤)
Section titled “HIF-2α抑制劑(VHL相關腫瘤)”針對VHL相關透明細胞腎細胞癌和胰臟神經內分泌腫瘤的第二期試驗正在進行中。
Chevalier等人(2021)的MK6482試驗中,64%的胰臟神經內分泌腫瘤達到客觀緩解,12個月無惡化存活率為98.3% 2)。
mTOR抑制劑everolimus(TSC相關腫瘤)
Section titled “mTOR抑制劑everolimus(TSC相關腫瘤)”針對TSC相關腎血管平滑肌脂肪瘤和SEGA的EXIST試驗證實了形態學緩解,其在內分泌腫瘤中的應用也備受期待 2)。
PPV、SWS和KTS重疊症候群
Section titled “PPV、SWS和KTS重疊症候群”GNAQ基因突變已被確定為SWS、克利佩爾-特雷諾內症候群(KTS)和色素血管性母斑症(PPV)的共同分子基礎 3)。這些重疊病例有脈絡膜黑色素瘤的風險,因此建議每年進行1-2次散瞳眼底檢查 3)。
8. 參考文獻
Section titled “8. 參考文獻”- Gama SM, Tamanini JVG, Moraes MPM, et al. A diagnostic approach to neurocutaneous syndromes. Arq Neuro-Psiquiatr. 2025;83(7):s00451809664.
- Chevalier B, Dupuis H, Jannin A, et al. Phakomatoses and endocrine gland tumors: noteworthy and (not so) rare associations. Front Endocrinol. 2021;12:678869.
- Senthilkumar VA, Kohli P, Mishra C, et al. Ocular features in a patient presenting with a rare combination of multiple phakomatoses. BMJ Case Rep. 2022;15:e252746.
