NF1与TSC(mTOR通路)

斑痣性错构瘤病的眼部症状
一目了然的要点
Section titled “一目了然的要点”1. 什么是斑痣性错构瘤病的眼部症状?
Section titled “1. 什么是斑痣性错构瘤病的眼部症状?”斑痣性错构瘤病是一组以皮肤、中枢神经系统和眼睛的错构瘤性病变为特征的先天性疾病的总称。也称为神经皮肤综合征。
该命名由荷兰眼科医生Van der Hoeve提出,源自希腊语“phakos”(透镜或斑点)。最初包括神经纤维瘤病、结节性硬化症和冯·希佩尔-林道病,随后加入了斯特奇-韦伯综合征和毛细血管扩张性共济失调。目前已有超过60种综合征被描述。
共同的病理基础是神经嵴细胞的形成、迁移和分化异常。由于神经嵴细胞来源于外胚层,产生施万细胞、黑素细胞等多种细胞,因此神经、皮肤和眼睛等多个器官会出现病变。已知涉及的信号通路包括RAS、MAPK/MEK、mTOR、PI3K/AKT、GNAQ和VHL-HIF通路。
六大主要疾病的发病率如下。
| 疾病 | 发病率(每X人中1例) |
|---|---|
| NF1(神经纤维瘤病1型) | 3,000~5,000 |
| 结节性硬化症(TSC) | 6,000~10,000 |
| SWS(斯特奇-韦伯综合征) | 20,000~50,000 |
| VHL(冯·希佩尔-林道病) | 36,000 |
| NF2(神经纤维瘤病2型) | 25,000~100,000 |
| 毛细血管扩张性共济失调症(AT) | 88,000至100,000以下 |
2. 主要症状和临床所见
Section titled “2. 主要症状和临床所见”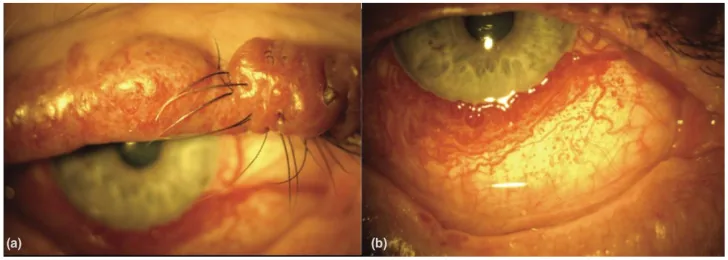
各疾病的眼部并发症类型不同,自觉症状也多种多样。
- NF1:视路肿瘤(视神经胶质瘤)进展时,会出现视力下降、色觉丧失和视野缺损。丛状神经纤维瘤可能导致眼球突出。
- 结节性硬化症:视网膜星形细胞错构瘤通常无症状。当累及黄斑或视盘时,会导致视力障碍。
- SWS:伴有先天性青光眼时,会出现角膜混浊、流泪和畏光。迟发性青光眼导致无痛性进行性视野缺损。
- VHL:早期无症状。视网膜毛细血管瘤进展时出现渗出性改变、黄斑水肿、环状白斑,导致视力下降。
- AT:视力通常保持正常。主要表现为眼球运动障碍(眼球震颤、眼球运动失用)。
NF1(神经纤维瘤病1型)的眼部表现
Section titled “NF1(神经纤维瘤病1型)的眼部表现”- Lisch结节:NF1最常见的眼部表现。虹膜上多发淡褐色、边界清晰、圆顶状的小结节(<1–2 mm)。年龄别患病率:<3岁5%,3–4岁42%,5–6岁55%,≥21岁100%,随年龄增长而增加,并纳入NF1诊断标准(≥2个)。日本人虹膜颜色偏棕,因此裂隙灯下仔细检查很重要。
- 视路肿瘤(视神经胶质瘤):约15–25%的NF1患者合并。多为低级别毛细胞星形细胞瘤,常无症状。进展时可导致视神经萎缩、视力障碍和视野缺损。可能侵犯视交叉。
- 丛状神经纤维瘤:发生于不到10%的NF1患者。特征为眼睑的“S形变形”,触诊时有“虫袋”样感觉。可导致眼球突出、斜视、弱视和先天性青光眼。
- 蝶骨翼发育不全:眼眶骨壁的先天性缺损,可能引起搏动性眼球突出。
- 青光眼:发生于1-2%的NF1患者。有先天性(单眼)和迟发性两种类型。
- 其他:角膜有髓神经纤维明显、脉络膜增厚、视网膜有髓神经纤维。
NF2(神经纤维瘤病2型)的眼部表现
Section titled “NF2(神经纤维瘤病2型)的眼部表现”- 视神经鞘脑膜瘤:NF2的特征性表现。与NF1的视路胶质瘤形成对比的肿瘤类型。
- 白内障:可见青年性白内障。
- 视网膜/RPE错构瘤、视网膜前膜:可能合并出现。
- 暴露性角膜炎:双侧听神经瘤导致第V、第VII脑神经功能障碍,引起面部麻木、复视、兔眼,继发暴露性角膜炎。
- Lisch结节罕见。
结节性硬化症(TSC)的眼部表现
Section titled “结节性硬化症(TSC)的眼部表现”- 视网膜星形细胞错构瘤:约50%合并出现。分为三型:(i) 扁平、半透明、非钙化型;(ii) 隆起、多结节、钙化型(桑葚样外观);(iii) 过渡型。通常在后极部可见多个。
- 视网膜脱色素病变:呈“打孔状”外观。
- 视网膜血管异常:可出现动脉瘤样扩张和动静脉畸形,可能导致玻璃体出血、增生性玻璃体视网膜病变和视网膜脱离。
- 其他:眼睑血管纤维瘤、虹膜脱色素斑、非典型脉络膜缺损。
SWS(斯特奇-韦伯综合征)的眼部表现
Section titled “SWS(斯特奇-韦伯综合征)的眼部表现”三大主要特征为:(1)三叉神经分布区的面部血管瘤,(2)同侧颅内血管瘤,(3)同侧青光眼或脉络膜血管瘤。
- 青光眼:SWS最重要的眼部表现。发生率30%~70%。先天性青光眼(出生至4岁)约占60%,导致牛眼、角膜混浊和大角膜。病因被认为涉及房角发育异常、巩膜上静脉压升高和脉络膜血管瘤。在眼睑血管瘤存在时发生频率高。
- 脉络膜血管瘤:约20-70%的患者发生。弥漫性、边界不清,常规眼底检查难以识别。眼底呈“番茄酱样”外观。通常无增大趋势,但可引起渗出性改变和渗出性视网膜脱离。
- 其他:结膜、上巩膜和虹膜的血管扩张迂曲。
VHL(冯·希佩尔-林道病)的眼部表现
Section titled “VHL(冯·希佩尔-林道病)的眼部表现”- 视网膜毛细血管瘤(血管母细胞瘤):43-85%的VHL患者发生(国内报告约60%)。约1/3为双眼性、多发性。好发于视网膜颞侧周边部,表现为伴有扩张迂曲的输入和输出血管的橙红色结节。平均发病年龄为25岁,通常在30岁前出现。
- 进展可引起渗出性改变、视网膜出血、黄斑水肿、环状白斑和视力下降。
- 进一步进展可导致玻璃体出血、牵拉性视网膜脱离、新生血管性青光眼和失明。
- 荧光眼底造影显示染料流入输入动脉→输出静脉灌注,肿瘤区域早期出现明显染料渗漏。
AT(毛细血管扩张性共济失调症)的眼部表现
Section titled “AT(毛细血管扩张性共济失调症)的眼部表现”3. 病因与风险因素
Section titled “3. 病因与风险因素”各疾病的遗传方式、致病基因和染色体位点如下所示。
| 疾病 | 遗传方式 | 致病基因 | 染色体位点 |
|---|---|---|---|
| NF1 | 常染色体显性 | NF1 | 17q11.2 |
| NF2 | 常染色体显性 | NF2 | 22q11.1-q13.1 |
| TSC | 常染色体显性 | TSC1/TSC2 | 9q34/16p13 |
| VHL | 常染色体显性 | VHL | 3p25-26 |
| SWS | 散发性(体细胞嵌合) | GNAQ | 9q21 |
| AT | 常染色体隐性 | ATM | 11q22 |
各疾病的遗传特征如下。
- NF1:约50%为新发突变。几乎完全外显,但表现型多样。神经纤维蛋白作为RAS-GAP发挥作用,将GTP-RAS转化为GDP-RAS2)。
- NF2:梅林蛋白功能丧失。主要表达于施万细胞和脑膜细胞的肿瘤抑制因子,其缺失导致施万瘤、脑膜瘤和室管膜瘤。
- TSC:散发病例约占2/3。TSC2突变占散发病例的75-80%,且比TSC1突变表现更严重的表型1)。错构蛋白/结节蛋白直接抑制mTOR通路2)。
- SWS:散发性,由GNAQ基因体细胞嵌合突变引起1)。累及三叉神经第一支(V1)整个区域的葡萄酒色斑(PWB)具有较高的眼部和神经系统并发症风险。
- VHL:外显率几乎100%,约20%为新发突变。pVHL参与HIF-α的泛素化和蛋白酶体降解2)。1型(无嗜铬细胞瘤)约占80%,2型(有嗜铬细胞瘤)约占20%2)。
- AT:常染色体隐性遗传,ATM激酶参与DNA双链断裂修复和基因组稳定性维持1)。恶性肿瘤(淋巴系统)风险和放射敏感性显著增高。
4. 诊断与检查方法
Section titled “4. 诊断与检查方法”NF1的诊断与眼科检查
Section titled “NF1的诊断与眼科检查”NF1的诊断标准(NIH标准、日本皮肤科学会2008年)要求满足以下7项中的2项或以上方可确诊。
- 6个或更多咖啡牛奶斑(青春期前:最大直径≥5mm;青春期后:≥15mm)
- 2个或更多神经纤维瘤或1个弥漫性神经纤维瘤
- 腋窝或腹股沟区雀斑样色素沉着
- 视神经胶质瘤
- 2个或更多Lisch虹膜结节
- 特征性骨病变(如蝶骨发育不良)
- 一级亲属患有相同疾病
眼科检查的作用如下。
- 裂隙灯显微镜:检测Lisch结节(在年轻患者中可能困难)。
- 眼前节OCT和超声生物显微镜:有助于辅助检测Lisch结节。
- MRI:视路肿瘤的最佳诊断方法。对视交叉和视束的评估至关重要。
- 视野检查:视路肿瘤筛查(在幼儿中难以实施)。
- 光学相干断层扫描(OCT):评估视路肿瘤相关的视网膜神经纤维层变薄。
- VEP(视觉诱发电位):早期检测视神经损伤。
- 定期检查间隔:仅有Lisch结节→每年1次。伴有视神经胶质瘤→每3个月1次。
NF2的诊断
Section titled “NF2的诊断”临床标准中,双侧前庭神经鞘瘤是特征性表现。由于皮肤症状不明显,诊断可能比NF1更困难。基因检测可检出90%以上的突变。CT/MRI可确认双侧听神经瘤。
结节性硬化症(TSC)的诊断
Section titled “结节性硬化症(TSC)的诊断”确诊需要满足2项主要特征,或1项主要特征加2项及以上次要特征。TSC1/TSC2致病性变异的鉴定被认可为独立的诊断标准1)。
视网膜星形细胞错构瘤的评估使用眼底检查、荧光眼底造影和OCT。最重要的鉴别诊断是视网膜母细胞瘤。根据儿童期无钙化、营养血管稀少、伴有全身症状的特点可以进行鉴别,但与桑葚状肿瘤的鉴别有时较为困难。
SWS的诊断
Section titled “SWS的诊断”Roach诊断量表要求至少满足面部葡萄酒色斑、眼压升高、软脑膜血管瘤中的两项1)。增强深度OCT和MRI对脉络膜血管瘤的评估有用。头部CT显示脑皮质内钙化。
青光眼的监测需要定期进行眼压测量、视神经评估和视野检查。婴幼儿可能需要在麻醉下进行裂隙灯检查、眼底检查和眼压测量。
VHL的诊断
Section titled “VHL的诊断”基因检测几乎100%能检测出VHL突变,是目前确诊的主流方法。建议从1岁起每年进行一次散瞳眼底检查。周边部橙红色球形肿瘤伴扩张迂曲血管是特征性表现。荧光眼底造影有助于发现小的周边部血管母细胞瘤,OCT用于评估小病变。
临床诊断中,共济失调、球结膜毛细血管扩张和眼球运动异常三联征很重要。实验室检查可见血清AFP升高、CA125升高和ATM蛋白缺失(Western blot)。球结膜毛细血管扩张是本病的特征性表现(pathognomonic)。MRI显示后颅窝弥漫性小脑萎缩,尤其是蚓部和半球1)。
5. 标准治疗方法
Section titled “5. 标准治疗方法”NF1的眼部相关治疗
Section titled “NF1的眼部相关治疗”- Lisch结节:无症状的错构瘤,无需治疗。
- 视神经胶质瘤:对于进展性病例考虑手术切除,但视功能丧失且术后并发症多。视交叉浸润病例适用化疗。
- 蔓状神经纤维瘤:手术完全切除困难且易复发。进展病例可能需要眼眶内容物剜除术。不可切除病例可使用司美替尼(MEK抑制剂)作为新疗法1)。
- 青光眼:按照常规青光眼治疗进行管理。
NF2的治疗
Section titled “NF2的治疗”前庭神经鞘瘤以手术切除为基本治疗,小于3cm的肿瘤中65%可保留听力1)。暴露性角膜炎使用人工泪液、角膜保护眼镜,必要时行睑板缝合处理。
结节性硬化症(TSC)的眼部相关治疗
Section titled “结节性硬化症(TSC)的眼部相关治疗”- 视网膜星形细胞错构瘤:通常无增大趋势,无需治疗。
- 视网膜血管异常(动脉瘤样扩张、动静脉畸形):因存在玻璃体出血和视网膜脱离的风险,需进行预防性光凝治疗。若发生玻璃体出血或视网膜脱离,考虑玻璃体手术。
- 癫痫:婴儿局灶性发作和婴儿痉挛症的首选治疗为氨己烯酸1)。SEGA(室管膜下巨细胞星形细胞瘤)需神经外科手术切除1)。
SWS的眼部治疗
Section titled “SWS的眼部治疗”青光眼的治疗根据发病年龄而有所不同。
- 先天性青光眼(早发型):必须手术治疗。选择小梁切开术或房角切开术。需注意脉络膜脱离和出血,由于巩膜上静脉压升高,并发症风险高于常规。对药物治疗往往耐药。
- 晚期发病型:首先进行药物治疗,无效时考虑手术。
脉络膜血管瘤的治疗根据有无渗出性变化从以下选择。
- 出现渗出性变化时→光凝
- 光凝无效或渗出性视网膜脱离→放射治疗(总剂量约20戈瑞)。可期待大疱性视网膜脱离复位和血管瘤缩小。
- 难治病例→玻璃体手术
- 光动力疗法(PDT)和外照射放射治疗也可能是选择3)。
VHL的眼部治疗
Section titled “VHL的眼部治疗”早期治疗是原则。
- 光凝(首选):使用氩激光或染料激光,先致密凝固血管瘤周围的视网膜和滋养血管,然后直接凝固瘤体。对于大于2个视盘直径的肿瘤,先凝固流入动脉和周围视网膜,再直接凝固肿瘤。
- 冷冻凝固:当眼底周边部或巨大血管瘤导致光凝困难时,经巩膜施行。
- 玻璃体切除术:当渗出性改变严重、发生视网膜脱离或出现增殖性改变时考虑。
- 终末期病例:需要管理新生血管性青光眼。
- 如有家族史,应对所有家庭成员进行眼底检查,早期治疗可望获得良好预后。
结膜毛细血管扩张没有特异性治疗。对于免疫缺陷,进行预防性抗生素和静脉注射免疫球蛋白(IVIg)治疗1)。共济失调以对症治疗为主。
对于VHL,建议从1岁开始每年进行一次散瞳眼底检查。已确认VHL基因突变的患者的所有家庭成员也应接受眼底检查,早期治疗有望获得良好的视功能预后。
6. 病理生理学与详细发病机制
Section titled “6. 病理生理学与详细发病机制”各疾病的分子水平发病机制如下所示。
VHL(HIF通路)
pVHL:E3泛素连接酶复合体(elongin B/C、Cullin 2、RBX1)的组成部分。在正常氧条件下,脯氨酰羟化酶将HIF-α羟化→pVHL识别→泛素化→蛋白酶体降解。
VHL突变:持续出现假性缺氧状态→HIF-α积累→与HIF-1β形成异二聚体→VEGF、红细胞生成、代谢和细胞增殖相关基因的转录激活→血管肿瘤形成2)。
- NF2(merlin):肿瘤抑制蛋白,在施万细胞和软脑膜细胞中表达。突变导致施万瘤、脑膜瘤和室管膜瘤。
- SWS(GNAQ体细胞嵌合突变):G蛋白相关跨膜信号传导异常。胚胎中突变的时间和位置导致三叉神经区域、颅内和眼部的表达模式不同1)。GNAQ也是SWS、KTS和PPV的共同分子基础3)。
- AT(ATM激酶):参与DNA双链断裂修复和基因组稳定性维持的肿瘤抑制因子。突变→DNA修复障碍→癌症易感性、放射敏感性显著增加和免疫缺陷1)。
Chevalier等人(2021)研究了母斑病与内分泌肿瘤的关联,报告称NF1、TSC和VHL的信号通路(RAS-PI3K-Akt-mTOR通路、HIF通路)共同参与多发性内分泌肿瘤的发生2)。
母斑病的共同病理基础是神经嵴细胞的形成、迁移和分化异常。神经嵴细胞来源于外胚层,产生施万细胞、黑色素细胞等多种细胞,因此病变累及神经、皮肤、眼等多个器官。此外,RAS-mTOR通路和VHL-HIF通路等共同信号通路的突变促进了跨器官的肿瘤发生。
7. 最新研究与未来展望(研究阶段报告)
Section titled “7. 最新研究与未来展望(研究阶段报告)”司美替尼(MEK抑制剂)
Section titled “司美替尼(MEK抑制剂)”一种获得FDA批准用于不可切除的丛状神经纤维瘤的分子靶向药物。它靶向NF1中MAPK通路的过度激活1)。
布格替尼(ALK抑制剂衍生物)
Section titled “布格替尼(ALK抑制剂衍生物)”针对NF2相关施万瘤和进展性肿瘤的临床试验由INTUITT-NF2联盟进行,已报告有希望的结果1)。
HIF-2α抑制剂(VHL相关肿瘤)
Section titled “HIF-2α抑制剂(VHL相关肿瘤)”针对VHL相关透明细胞肾细胞癌和胰腺神经内分泌肿瘤的2期试验正在进行中。
Chevalier等人(2021)的MK6482试验中,64%的胰腺神经内分泌肿瘤获得客观缓解,12个月无进展生存率为98.3% 2)。
mTOR抑制剂依维莫司(TSC相关肿瘤)
Section titled “mTOR抑制剂依维莫司(TSC相关肿瘤)”针对TSC相关肾血管平滑肌脂肪瘤和SEGA的EXIST试验证实了形态学缓解,其在内分泌肿瘤中的应用也值得期待 2)。
PPV、SWS和KTS重叠综合征
Section titled “PPV、SWS和KTS重叠综合征”GNAQ基因突变已被确定为SWS、克利佩尔-特雷诺内综合征(KTS)和色素血管性斑痣性错构瘤病(PPV)的共同分子基础 3)。这些重叠病例存在脉络膜黑色素瘤的风险,因此建议每年进行1-2次散瞳眼底检查 3)。
8. 参考文献
Section titled “8. 参考文献”- Gama SM, Tamanini JVG, Moraes MPM, et al. A diagnostic approach to neurocutaneous syndromes. Arq Neuro-Psiquiatr. 2025;83(7):s00451809664.
- Chevalier B, Dupuis H, Jannin A, et al. Phakomatoses and endocrine gland tumors: noteworthy and (not so) rare associations. Front Endocrinol. 2021;12:678869.
- Senthilkumar VA, Kohli P, Mishra C, et al. Ocular features in a patient presenting with a rare combination of multiple phakomatoses. BMJ Case Rep. 2022;15:e252746.
