眶内视神经局限型
最常见的发生形式。主要症状为单眼视力下降和眼球突出。
局限于眶内视神经,基本处理为观察。 合并NF1的病例有自然缩小的报道。

视神经胶质瘤(optic nerve glioma / optic pathway glioma)是发生在视神经的一种胶质瘤。狭义上指发生于视交叉之前的视神经的胶质瘤。广义上包括发生于视交叉后方整个视路的胶质瘤(optic pathway glioma)。
组织学上,多数为良性的毛细胞星形细胞瘤(WHO I级)。但也有少数恶性病例的报道。约70%发生于儿童期,是一种罕见的疾病,约占儿童脑肿瘤的0.5%~5%。
与神经纤维瘤病1型(NF1,von Recklinghausen病)密切相关,约20%~30%的视神经胶质瘤病例合并NF1。反之,NF1患者的眼眶病变中最常见的是视神经胶质瘤。
眶内视神经局限型
最常见的发生形式。主要症状为单眼视力下降和眼球突出。
局限于眶内视神经,基本处理为观察。 合并NF1的病例有自然缩小的报道。
视交叉浸润型
浸润至视交叉的类型。
引起双眼视力障碍,管理复杂。 多见于低龄发病,需评估向丘脑下部的进展。
视路-丘脑下部型
从视交叉后方进展至丘脑下部的类型。
可能合并内分泌异常(生长障碍、性早熟等)。 治疗上需要神经外科和内分泌科的协作。
根据遗传背景分类,有NF1合并型(约占30%)和散发型(约占70%)。 NF1合并型可见双侧发生。
低龄儿童不会主动诉说视力下降。因此,家长或周围人常注意到斜视(尤其是内斜视),并首次就诊于眼科。
无斜视的单眼视力下降更容易被延迟发现。有时初诊时已出现视神经萎缩。
双眼视神经胶质瘤多见于低龄发病者。常因视线异常或“看不见”的行为而被首次发现,视力障碍可能严重。
眼球突出不明显,也无疼痛。
视神经胶质瘤中,低龄儿童无法自觉或诉说视力下降,因此斜视(尤其是内斜视)常作为首发症状成为眼科就诊的契机。对于诊断为斜视的儿童,尤其是单眼斜视,应考虑视神经胶质瘤的可能性,并进行包括视力、眼底和影像检查在内的全面评估。
眼底检查常可见以下所见:
合并NF1(神经纤维瘤病1型)的病例伴有以下全身所见:
CT表现:
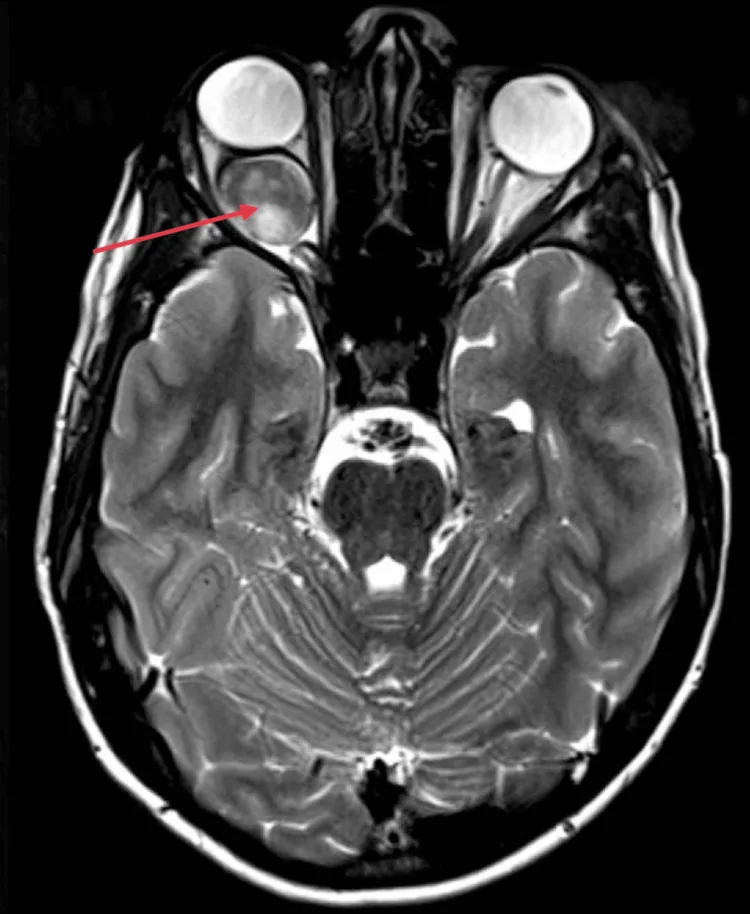
MRI表现(需详细检查):
NF1患者发生视神经胶质瘤的风险显著增高,所有视神经胶质瘤病例的20-30%合并NF11)。确诊NF1后,建议定期进行眼科随访作为视神经胶质瘤的筛查。反之,当发现儿童视神经胶质瘤时,应检查所有病例是否符合NF1的诊断标准。
NF1(神经纤维瘤病1型)的诊断标准主要项目如下所示2)。
| 表现 | 标准 |
|---|---|
| 咖啡斑 | ≥6个(儿童:长径≥5mm;青春期后:长径≥15mm) |
| 神经纤维瘤 | ≥2个(任何类型)或≥1个丛状神经纤维瘤 |
| 虹膜Lisch结节 | ≥2个 |
| 特征性骨病变 | 蝶骨翼发育不良或长骨皮质变薄 |
| 视神经胶质瘤 | ≥1个 |
| 腋窝或腹股沟雀斑 | 存在 |
| 一级亲属 | 确诊NF1者 |
确诊NF1需满足上述标准中的至少2项。
MRI在评估肿瘤扩展范围方面优于CT,是精查必需的检查。
| 表现 | 详细 |
|---|---|
| T1加权像 | 呈低信号 |
| Gd-DTPA增强效果 | 均匀增粗并呈明显强化 |
| 向下弯曲 | NF1合并病例的特征性表现(视神经向下弯曲) |
| 颅内扩展评估 | 确认通过视神经管向颅内扩展,以及视交叉、下丘脑是否存在肿瘤 |
视神经鞘脑膜瘤
最重要的鉴别诊断。
多见于成年女性,可合并NF2。 CT/MRI显示特征性的电车轨道征,有助于与视神经胶质瘤鉴别。
视神经炎
常急性起病,伴有眼球运动痛。
MRI显示视神经强化,但肿大轻微。 通常对类固醇治疗反应良好。
其他鉴别诊断:
视神经胶质瘤表现为均匀增粗和向下弯曲(downward kinking),可与视神经鞘脑膜瘤的**轨道征(tram-track sign)**明确区分。
视神经胶质瘤是儿童常见的良性肿瘤(毛细胞星形细胞瘤),常合并NF1。CT/MRI表现为视神经均匀增粗和向下弯曲。视神经鞘脑膜瘤多见于成年女性,有时合并NF2,CT/MRI表现为轨道征(沿视神经鞘的钙化或强化),以此鉴别。
由于肿瘤为良性且多见于儿童,如果局限于眶内视神经,原则上不进行手术切除或放射治疗。以定期影像学检查(MRI:每3-6个月)为中心的谨慎观察是基本方针。
过去曾进行手术,但由于导致不可逆失明的风险很高,目前倾向于避免手术切除。合并NF1的病例有自然缩小的报道,因此尤其需要谨慎观察。
当出现视力下降或肿瘤进展时,卡铂联合长春新碱(CV方案)的联合化疗被用作标准一线治疗3)4)。
标准CV方案(如COG A9952等):
CV方案的客观有效率(部分缓解+稳定)据报道为60-80%4)。
二线治疗选择:
考虑用于化疗耐药的进展期病例。 但在儿童中,由于担心继发性癌症风险、内分泌功能障碍(下丘脑附近照射)和认知功能影响,倾向于尽可能避免。
目前倾向于避免积极的手术切除。
考虑手术适应症的情况:
视神经胶质瘤的组织病理学表现为良性的毛细胞星形细胞瘤(WHO I级)。 与胶质母细胞瘤(WHO IV级)等高恶性度胶质瘤本质不同。
肿瘤细胞呈双极细胞突起的特征性形态,并含有Rosenthal纤维。 起源于视神经的胶质细胞(星形胶质细胞),从内部压迫并取代视神经。
与神经纤维瘤病1型(NF1)相关的视神经胶质瘤是由**NF1基因(染色体17q11.2)**的突变引起的。
在散发性(非NF1)毛细胞星形细胞瘤中,BRAF-KIAA1549融合基因常见。 该融合基因也激活MAPK通路,促进肿瘤生长。
部分病例携带BRAF V600E突变,具有该突变的病例恶性程度往往较高6)。
大多数视神经胶质瘤是低级别的,生长缓慢。 肿瘤从内部使视神经肿大,并在眼眶内导致视神经屈曲(向下屈曲)。 MRI上均匀肿大和向下屈曲是影像诊断的关键点。
局限于眼眶的病例:
视交叉/下丘脑浸润病例:
生命预后:
功能预后:
视力预后并非一致,进展型和稳定型并存,因此除了肿瘤大小外,还需要纵向评估视功能。有些病例尽管MRI表现稳定,但视功能恶化;相反,NF1合并病例可能显示自然缩小。1, 8, 9)
已有报道MEK抑制剂对NF1相关低级别胶质瘤的有效性。
在SPRINT试验(II期)中,司美替尼对NF1相关进展性低级别胶质瘤(丛状神经纤维瘤)的客观缓解率为66% 7)。其应用于包括视神经胶质瘤在内的NF1相关低级别胶质瘤正在研究中。
对于携带BRAF V600E突变的儿童低级别胶质瘤,达拉非尼+曲美替尼联合疗法正在临床试验中评估 6)。在BRAF-KIAA1549融合阳性病例中,BRAF抑制剂的疗效有限。
随着MEK抑制剂和BRAF抑制剂的出现,治疗正从传统化疗(CV方案)转向基于分子谱的个体化治疗 8)。未来,基于基因突变谱(BRAF融合、BRAF V600E、NF1突变等)的治疗选择可能成为标准。
Listernick R, Charrow J, Greenwald M, Mets M. Natural history of optic pathway tumors in children with neurofibromatosis type 1: a longitudinal study. J Pediatr. 1994;125(1):63-66.
Ferner RE, Huson SM, Thomas N, et al. Guidelines for the diagnosis and management of individuals with neurofibromatosis 1. J Med Genet. 2007;44(2):81-88.
Gnekow AK, Walker DA, Kandels D, et al. A European randomised controlled trial of the addition of etoposide to standard vincristine and carboplatin induction as part of an 18-month treatment programme for childhood (≤16 years) low grade glioma - A final report. Eur J Cancer. 2017;81:206-225.
Ater JL, Zhou T, Holmes E, et al. Randomized study of two chemotherapy regimens for treatment of low-grade glioma in young children: a report from the Children’s Oncology Group. J Clin Oncol. 2012;30(21):2641-2647.
Lassaletta A, Scheinemann K, Zelcer SM, et al. Phase II weekly vinblastine for chemotherapy-naive children with progressive low-grade glioma: a Canadian Pediatric Brain Tumor Consortium study. J Clin Oncol. 2016;34(29):3537-3543.
Fangusaro J, Onar-Thomas A, Young Poussaint T, et al. Selumetinib in paediatric patients with BRAF-aberrant or neurofibromatosis type 1-associated recurrent, refractory, or progressive low-grade glioma: a multicentre, phase 2 trial. Lancet Oncol. 2019;20(7):1011-1022.
Banerjee A, Jakacki RI, Onar-Thomas A, et al. A phase I trial of the MEK inhibitor selumetinib (AZD6244) in pediatric patients with recurrent or refractory low-grade gliomas: a Pediatric Brain Tumor Consortium (PBTC) study. Neuro Oncol. 2017;19(8):1135-1144.
de Blank PMK, Orne-Ibekwe E, Packer R. International consensus recommendations for visual surveillance in optic pathway gliomas associated with neurofibromatosis type 1. J Neurooncol. 2020;148(3):571-578.
Listernick R, Louis DN, Packer RJ, Gutmann DH. Optic pathway gliomas in children with neurofibromatosis 1: consensus statement from the NF1 Optic Pathway Glioma Task Force. Ann Neurol. 1997;41(2):143-149.