ชนิดจำกัดเฉพาะในเบ้าตาของเส้นประสาทตา
รูปแบบที่พบบ่อยที่สุด อาการหลักคือการมองเห็นลดลงข้างเดียวและตาโปน
จำกัดเฉพาะเส้นประสาทตาภายในเบ้าตา การติดตามผลเป็นพื้นฐาน ในกรณีที่มี NF1 มีรายงานการหดตัวเองได้

ไกลโอมาของเส้นประสาทตา (optic nerve glioma / optic pathway glioma) เป็นไกลโอมาชนิดหนึ่งที่เกิดจากเส้นประสาทตา ในความหมายแคบ หมายถึงไกลโอมาที่เกิดจากเส้นประสาทตาก่อนถึงออปติกไคแอสมาของเส้นประสาทตา ในความหมายกว้าง หมายถึงไกลโอมาที่เกิดจากทางเดินสายตาทั้งหมดรวมถึงส่วนหลังออปติกไคแอสมาของเส้นประสาทตา (optic pathway glioma)
ทางจุลกายวิภาค ส่วนใหญ่เป็นพิโลไซติกแอสโตรไซโตมาที่ไม่ร้ายแรง (pilocytic astrocytoma, WHO Grade I) อย่างไรก็ตาม มีรายงานบางกรณีที่ร้ายแรง ประมาณ 70% เกิดในวัยเด็ก และเป็นโรคที่พบได้ยาก คิดเป็นประมาณ 0.5-5% ของเนื้องอกสมองในเด็ก
มีความสัมพันธ์อย่างมากกับนิวโรไฟโบรมาทิซิสชนิดที่ 1 (NF1, โรคฟอน เรคลิงเฮาเซน) และประมาณ 20-30% ของผู้ป่วยไกลโอมาของเส้นประสาทตามี NF1 ร่วมด้วย ในทางกลับกัน ไกลโอมาของเส้นประสาทตาเป็นเนื้องอกที่พบบ่อยที่สุดในรอยโรคเบ้าตาของผู้ป่วย NF1
ชนิดจำกัดเฉพาะในเบ้าตาของเส้นประสาทตา
รูปแบบที่พบบ่อยที่สุด อาการหลักคือการมองเห็นลดลงข้างเดียวและตาโปน
จำกัดเฉพาะเส้นประสาทตาภายในเบ้าตา การติดตามผลเป็นพื้นฐาน ในกรณีที่มี NF1 มีรายงานการหดตัวเองได้
ชนิดแทรกซึมเข้าสู่จุดตัดประสาทตา
ชนิดที่แทรกซึมเข้าสู่จุดตัดประสาทตา
ทำให้เกิดความบกพร่องทางการมองเห็นทั้งสองข้าง และการจัดการมีความซับซ้อน มักเกิดในอายุน้อย และต้องประเมินการลุกลามไปยังไฮโปทาลามัส
ชนิดทางเดินประสาทตา-ไฮโปทาลามัส
ชนิดที่ขยายจากด้านหลังจุดตัดประสาทตาไปยังไฮโปทาลามัส
อาจมีภาวะผิดปกติของต่อมไร้ท่อร่วมด้วย (เช่น ความผิดปกติของการเจริญเติบโต วัยแรกรุ่นก่อนวัย) การรักษาต้องอาศัยความร่วมมือกับศัลยกรรมประสาทและต่อมไร้ท่อ
ตามการจำแนกทางพันธุกรรม มี ชนิดที่สัมพันธ์กับ NF1 (ประมาณ 30%) และ ชนิดประปราย (ประมาณ 70%) ในชนิดที่สัมพันธ์กับ NF1 อาจเกิดได้ทั้งสองข้าง
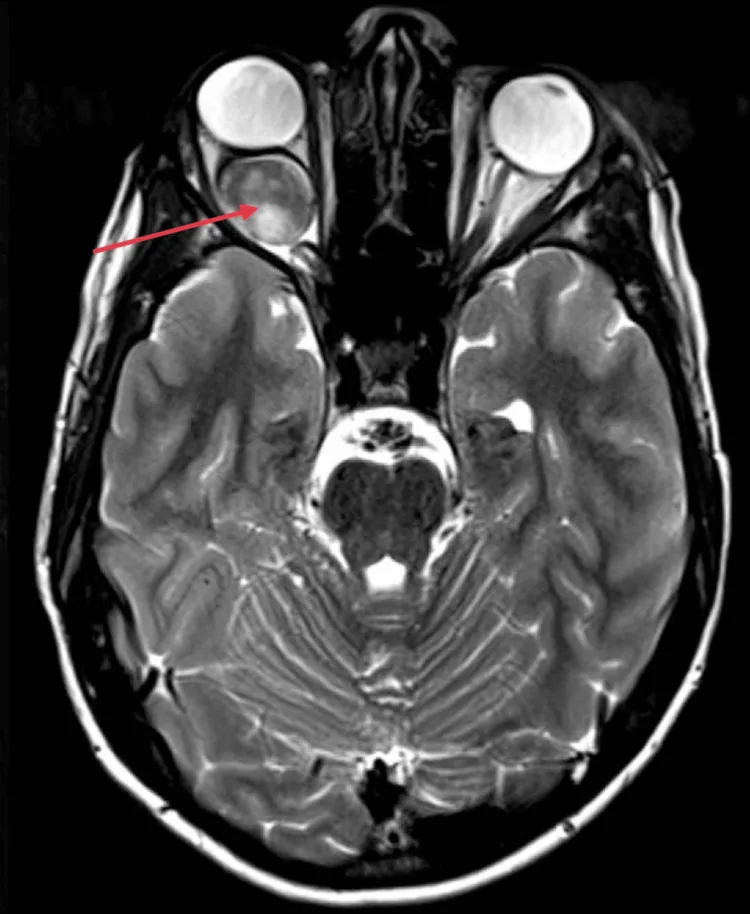
เด็กเล็กไม่สามารถบอกอาการตามัวได้เอง ดังนั้น ผู้ปกครองหรือคนรอบข้างมักสังเกตเห็นตาเหล่ (โดยเฉพาะตาเหล่เข้า) และพามาพบจักษุแพทย์เป็นครั้งแรก
การมองเห็นลดลงข้างเดียวโดยไม่มีตาเหล่จะยิ่งตรวจพบได้ช้า บางครั้งอาจมีฝ่อของเส้นประสาทตาเกิดขึ้นแล้วเมื่อมาพบแพทย์ครั้งแรก
เนื้องอกแก้วนำแสงชนิดสองข้างพบได้บ่อยในผู้ป่วยที่เริ่มมีอาการตั้งแต่อายุน้อย มักสังเกตพบครั้งแรกจากความผิดปกติของการจ้องมองหรือ “พฤติกรรมที่มองไม่เห็น” และความบกพร่องทางการมองเห็นอาจรุนแรง
ตาโปนไม่ชัดเจน และไม่มีอาการปวด
ในเนื้องอกแก้วนำแสง เด็กเล็กไม่สามารถรับรู้หรือบอกอาการตามัวได้ ดังนั้น ตาเหล่ (โดยเฉพาะตาเหล่เข้า) มักเป็นอาการเริ่มแรกที่นำไปสู่การพบจักษุแพทย์ สิ่งสำคัญคือต้องพิจารณาการตรวจอย่างละเอียดรวมถึงการวัดสายตา การตรวจอวัยวะภายในตา และการถ่ายภาพในเด็กที่ได้รับการวินิจฉัยว่าตาเหล่ โดยเฉพาะตาเหล่ข้างเดียว โดยคำนึงถึงความเป็นไปได้ของเนื้องอกแก้วนำแสง
การตรวจอวัยวะภายในตามักพบผลดังต่อไปนี้
ในผู้ป่วยร่วมกับ NF1 (นิวโรไฟโบรมาโตซิสชนิดที่ 1) จะมีอาการทางระบบดังต่อไปนี้
ผลการตรวจ CT:
ผลการตรวจ MRI (จำเป็นสำหรับการตรวจละเอียด):
ผู้ป่วย NF1 มีความเสี่ยงสูงอย่างมีนัยสำคัญในการเกิด optic glioma โดย 20–30% ของผู้ป่วย optic glioma ทั้งหมดเกี่ยวข้องกับ NF11) หลังการวินิจฉัย NF1 แนะนำให้ติดตามตรวจตาเป็นระยะเพื่อคัดกรอง optic glioma ในทางกลับกัน หากตรวจพบ optic glioma ในเด็ก ควรตรวจสอบว่าเข้าเกณฑ์การวินิจฉัย NF1 หรือไม่ในทุกราย
รายการหลักของเกณฑ์การวินิจฉัย NF1 (neurofibromatosis type 1) แสดงไว้ด้านล่าง2)
| ลักษณะที่พบ | เกณฑ์ |
|---|---|
| รอยด่างสีน้ำนมกาแฟ | ≥6 จุด (เด็ก: เส้นผ่านศูนย์กลาง ≥5 มม. หลังวัยเจริญพันธุ์: เส้นผ่านศูนย์กลาง ≥15 มม.) |
| เนื้องอกเส้นประสาท | ≥2 ก้อน (ชนิดใดก็ได้) หรือ ≥1 ก้อนแบบ plexiform |
| ก้อน Lisch ที่ม่านตา | ≥2 ก้อน |
| รอยโรคกระดูกที่มีลักษณะเฉพาะ | กระดูกปีกผีเสื้อเจริญผิดปกติ หรือกระดูกยาวส่วนคอร์เทกซ์บางลง |
| เนื้องอกไกลโอมาของเส้นประสาทตา | ≥1 ก้อน |
| กระที่รักแร้หรือขาหนีบ | มี |
| ญาติสายตรงลำดับที่หนึ่ง | ผู้ที่ได้รับการวินิจฉัยแน่นอนว่าเป็น NF1 |
การวินิจฉัย NF1 อย่างแน่นอนต้องมีเกณฑ์ข้างต้นอย่างน้อย 2 ข้อขึ้นไป
MRI เหนือกว่า CT ในการประเมินขอบเขตการแพร่กระจายของเนื้องอก และเป็นการตรวจที่จำเป็นสำหรับการประเมินอย่างละเอียด
| ผลการตรวจ | รายละเอียด |
|---|---|
| ภาพน้ำหนัก T1 | แสดงสัญญาณต่ำ |
| ผลการเพิ่มความคมชัดด้วย Gd-DTPA | แสดงการขยายใหญ่สม่ำเสมอพร้อมการเพิ่มความคมชัดอย่างมาก |
| การโค้งลงด้านล่าง | ลักษณะเฉพาะในผู้ป่วย NF1 (การโค้งลงของเส้นประสาทตา) |
| การประเมินการลุกลามเข้าสู่กะโหลกศีรษะ | ยืนยันการลุกลามจากภายในคลองประสาทตาเข้าสู่กะโหลกศีรษะ ออปติกไคแอสมา และไฮโปทาลามัส |
เยื่อหุ้มเส้นประสาทตาอักเสบชนิดเมนินจิโอมา
โรคที่สำคัญที่สุดในการวินิจฉัยแยกโรค.
พบบ่อยในหญิงวัยผู้ใหญ่ อาจพบร่วมกับ NF2 CT/MRI แสดง tram-track sign (ลักษณะคล้ายรางรถไฟ) ซึ่งเป็นลักษณะเฉพาะ ช่วยแยกจาก optic glioma
เส้นประสาทตาอักเสบ
มักมีอาการเฉียบพลันและปวดเมื่อขยับลูกตา
MRI พบการเพิ่มความเข้มของเส้นประสาทตา แต่การบวมมักไม่รุนแรง มักตอบสนองต่อการรักษาด้วยสเตียรอยด์
โรคอื่นๆ ที่ต้องวินิจฉัยแยก:
เนื้องอกไกลโอมาของเส้นประสาทตา (Optic glioma) แสดง การขยายตัวที่สม่ำเสมอและการโค้งลง (downward kinking) และสามารถแยกความแตกต่างได้อย่างชัดเจนจาก เครื่องหมายรางรถราง (tram-track sign) ของเนื้องอกเยื่อหุ้มเส้นประสาทตา (Optic nerve sheath meningioma)
เนื้องอกไกลโอมาของเส้นประสาทตาเป็นเนื้องอกชนิดไม่ร้าย (pilocytic astrocytoma) ที่พบบ่อยในเด็ก และอาจเกี่ยวข้องกับ NF1 ในการตรวจ CT/MRI มีลักษณะเฉพาะคือการขยายตัวที่สม่ำเสมอของเส้นประสาทตาและการโค้งลง ส่วนเนื้องอกเยื่อหุ้มเส้นประสาทตาพบมากในผู้หญิงวัยผู้ใหญ่ อาจเกี่ยวข้องกับ NF2 และในการตรวจ CT/MRI จะแสดงเครื่องหมายรางรถราง (การกลายเป็นปูนหรือการเพิ่มความเข้มตามแนวรอบนอกของเส้นประสาทตา) ซึ่งใช้ในการแยกความแตกต่าง
เนื่องจากเนื้องอกเป็นชนิดไม่ร้ายและพบบ่อยในเด็ก จึงไม่ทำการผ่าตัดเอาเนื้องอกออกหรือการฉายรังสีเป็นประจำหากเนื้องอกจำกัดอยู่เฉพาะในเส้นประสาทตาภายในเบ้าตา หลักการพื้นฐานคือการสังเกตอาการอย่างใกล้ชิดด้วยการตรวจ MRI เป็นระยะ (ทุก 3-6 เดือน)
ในอดีตมักมีการผ่าตัด แต่เนื่องจากมีความเสี่ยงสูงต่อการสูญเสียการมองเห็นแบบถาวร ปัจจุบันจึงมีแนวโน้มที่จะหลีกเลี่ยงการผ่าตัดเอาเนื้องอกออก ในกรณีที่เกี่ยวข้องกับ NF1 มีรายงานการหดตัวของเนื้องอกเอง ดังนั้นจึงมีการสังเกตอาการอย่างใกล้ชิดเป็นพิเศษ
ในกรณีที่การมองเห็นลดลงหรือเนื้องอกมีขนาดใหญ่ขึ้น การใช้เคมีบำบัดร่วมกับคาร์โบพลาตินและวินคริสติน (CV) เป็นการรักษามาตรฐานบรรทัดแรก3)4)
สูตรมาตรฐานของ CV (เช่น COG A9952):
อัตราการตอบสนองตามวัตถุประสงค์ (การทุเลาบางส่วน + การคงที่) ของการรักษาด้วย CV รายงานว่าอยู่ที่ 60-80%4)
ทางเลือกการรักษาบรรทัดที่สอง:
พิจารณาในกรณีที่โรคลุกลามและดื้อต่อเคมีบำบัด อย่างไรก็ตาม ในเด็ก มีความกังวลเกี่ยวกับความเสี่ยงของมะเร็งทุติยภูมิ ความผิดปกติของต่อมไร้ท่อ (เนื่องจากการฉายรังสีใกล้ไฮโปทาลามัส) และผลกระทบต่อการทำงานของสมอง ดังนั้นจึงมีแนวโน้มที่จะหลีกเลี่ยงให้มากที่สุด
ปัจจุบันมีแนวโน้มที่จะหลีกเลี่ยงการผ่าตัดตัดก้อนเนื้องอกที่รุกราน
สถานการณ์ที่พิจารณาการผ่าตัด:
ผลการตรวจทางพยาธิวิทยาของออปติกไกลโอมาคือ แอสโตรไซโตมาแบบพิโลไซติกชนิดไม่ร้ายแรง (pilocytic astrocytoma, WHO Grade I) ซึ่งแตกต่างโดยพื้นฐานจากไกลโอมาชนิดร้ายแรงสูง เช่น ไกลโอบลาสโตมา มัลติฟอร์ม (glioblastoma multiforme, WHO Grade IV)
เซลล์เนื้องอกมีลักษณะทางสัณฐานวิทยาที่โดดเด่นด้วยกระบวนการเซลล์แบบสองขั้ว และมีเส้นใยโรเซนธัล เกิดจากเซลล์เกลีย (แอสโตรไซต์) ของเส้นประสาทตา กดทับและแทนที่เส้นประสาทตาจากภายใน
ไกลโอมาของเส้นประสาทตาที่เกี่ยวข้องกับ NF1 (นิวโรไฟโบรมาโทซิสชนิดที่ 1) เกิดจากการกลายพันธุ์ของยีน NF1 (โครโมโซม 17q11.2)
ในแอสโตรไซโตมาแบบพิโลไซติกที่เกิดประปราย (ไม่ร่วมกับ NF1) มักพบ ยีนฟิวชัน BRAF-KIAA1549 ยีนฟิวชันนี้ยังกระตุ้นวิถี MAPK และส่งเสริมการเจริญเติบโตของเนื้องอก
บางกรณีมีการ กลายพันธุ์ BRAF V600E และกรณีเหล่านี้มีแนวโน้มที่จะมีความร้ายแรงสูงกว่า6)
ไกลโอมาของเส้นประสาทตาส่วนใหญ่เป็น ชั้นต่ำ และมีการเจริญเติบโตช้า เนื้องอกทำให้เส้นประสาทตาบวมจากภายใน ทำให้เส้นประสาทตางอ (kinking และ downward kinking) ภายในเบ้าตา การบวมอย่างสม่ำเสมอและการงอลงด้านล่างในการตรวจ MRI เป็นจุดสำคัญในการวินิจฉัยด้วยภาพ
กรณีที่จำกัดอยู่ภายในเบ้าตา:
กรณีที่มีการแทรกซึมของออปติกไคแอส-ไฮโปทาลามัส:
พยากรณ์โรคการรอดชีวิต:
พยากรณ์โรคการทำงาน:
พยากรณ์โรคทางสายตาไม่สม่ำเสมอ เนื่องจากมีทั้งกรณีที่ลุกลามและคงที่ปะปนกัน ดังนั้นจึงจำเป็นต้องประเมินการทำงานของสายตาในระยะยาวนอกเหนือจากขนาดของเนื้องอก การทำงานของสายตาอาจแย่ลงแม้ผล MRI จะคงที่ และในทางกลับกัน กรณีที่ร่วมกับ NF1 อาจแสดงการถดถอยเองตามธรรมชาติ 1, 8, 9)
มีรายงานประสิทธิภาพของสารยับยั้ง MEK ต่อ glioma ระดับต่ำที่เกี่ยวข้องกับ NF1
ในการทดลอง SPRINT (ระยะที่ 2) มีรายงานอัตราการตอบสนองตามวัตถุประสงค์ 66% สำหรับ selumetinib ใน glioma ระดับต่ำที่ลุกลามซึ่งเกี่ยวข้องกับ NF1 (plexiform neurofibroma)7) กำลังพิจารณาการประยุกต์ใช้กับ glioma ระดับต่ำที่เกี่ยวข้องกับ NF1 รวมถึง optic glioma
สำหรับ glioma ระดับต่ำในเด็กที่มีการกลายพันธุ์ BRAF V600E การรักษาแบบผสมผสาน dabrafenib + trametinib กำลังถูกประเมินในการทดลองทางคลินิก6) ในกรณีที่ผลบวกต่อ BRAF-KIAA1549 fusion ประสิทธิภาพของสารยับยั้ง BRAF มีจำกัด
ด้วยการเกิดขึ้นของสารยับยั้ง MEK และ BRAF มีการเปลี่ยนแปลงจากการให้เคมีบำบัดแบบดั้งเดิม (สูตร CV) ไปสู่ การรักษาเฉพาะบุคคลตามโปรไฟล์โมเลกุล8) ในอนาคต การเลือกการรักษาตามโปรไฟล์การกลายพันธุ์ของยีน (BRAF fusion, BRAF V600E, การกลายพันธุ์ NF1 ฯลฯ) อาจกลายเป็นมาตรฐาน
Listernick R, Charrow J, Greenwald M, Mets M. Natural history of optic pathway tumors in children with neurofibromatosis type 1: a longitudinal study. J Pediatr. 1994;125(1):63-66.
Ferner RE, Huson SM, Thomas N, et al. Guidelines for the diagnosis and management of individuals with neurofibromatosis 1. J Med Genet. 2007;44(2):81-88.
Gnekow AK, Walker DA, Kandels D, et al. A European randomised controlled trial of the addition of etoposide to standard vincristine and carboplatin induction as part of an 18-month treatment programme for childhood (≤16 years) low grade glioma - A final report. Eur J Cancer. 2017;81:206-225.
Ater JL, Zhou T, Holmes E, et al. Randomized study of two chemotherapy regimens for treatment of low-grade glioma in young children: a report from the Children’s Oncology Group. J Clin Oncol. 2012;30(21):2641-2647.
Lassaletta A, Scheinemann K, Zelcer SM, et al. Phase II weekly vinblastine for chemotherapy-naive children with progressive low-grade glioma: a Canadian Pediatric Brain Tumor Consortium study. J Clin Oncol. 2016;34(29):3537-3543.
Fangusaro J, Onar-Thomas A, Young Poussaint T, et al. Selumetinib in paediatric patients with BRAF-aberrant or neurofibromatosis type 1-associated recurrent, refractory, or progressive low-grade glioma: a multicentre, phase 2 trial. Lancet Oncol. 2019;20(7):1011-1022.
Banerjee A, Jakacki RI, Onar-Thomas A, et al. A phase I trial of the MEK inhibitor selumetinib (AZD6244) in pediatric patients with recurrent or refractory low-grade gliomas: a Pediatric Brain Tumor Consortium (PBTC) study. Neuro Oncol. 2017;19(8):1135-1144.
de Blank PMK, Orne-Ibekwe E, Packer R. International consensus recommendations for visual surveillance in optic pathway gliomas associated with neurofibromatosis type 1. J Neurooncol. 2020;148(3):571-578.
Listernick R, Louis DN, Packer RJ, Gutmann DH. Optic pathway gliomas in children with neurofibromatosis 1: consensus statement from the NF1 Optic Pathway Glioma Task Force. Ann Neurol. 1997;41(2):143-149.