안와 내 시신경 국한형
가장 흔한 발생 형태입니다. 단안 시력 저하와 안구 돌출이 주요 증상입니다.
안와 내 시신경에 국한되며, 경과 관찰이 기본입니다. NF1 동반 예에서는 자연 소실 보고도 있습니다.

시신경교종(optic nerve glioma / optic pathway glioma)은 시신경에 발생하는 신경아교종의 일종입니다. 좁은 의미로는 시교차 전방의 시신경에 생긴 신경아교종을 가리킵니다. 넓은 의미로는 시교차 후방을 포함한 전체 시로(optic pathway)에 생긴 신경아교종(optic pathway glioma)을 의미합니다.
조직학적으로 대부분이 양성인 모세포성 성상세포종(WHO Grade I)입니다. 다만 일부 악성 예도 보고되었습니다. 약 70%가 소아기에 발병하며, 소아 뇌종양의 약 0.5~5%를 차지하는 드문 질환입니다.
신경섬유종증 1형(NF1, von Recklinghausen병)과의 관련성이 강하며, 시신경교종 환자의 약 20~30%에서 NF1이 동반됩니다. 반대로 NF1 환자의 안와 병변으로는 시신경교종이 가장 흔합니다.
안와 내 시신경 국한형
가장 흔한 발생 형태입니다. 단안 시력 저하와 안구 돌출이 주요 증상입니다.
안와 내 시신경에 국한되며, 경과 관찰이 기본입니다. NF1 동반 예에서는 자연 소실 보고도 있습니다.
시교차 침윤형
시교차까지 침윤하는 형입니다.
양안성 시력 장애를 초래하며 관리가 복잡합니다. 저연령 발병에 많으며, 시상하부로의 진행을 평가합니다.
시로-시상하부형
시교차 후방에서 시상하부까지 진행하는 형입니다.
내분비 이상(성장 장애, 성조숙증 등)을 동반할 수 있습니다. 치료상 신경외과, 내분비내과와의 협력이 필요합니다.
유전적 배경에 따른 분류로 NF1 동반형(전체의 약 30%)과 고립형(약 70%)이 있습니다. NF1 동반형에서는 양측성 발생도 보입니다.
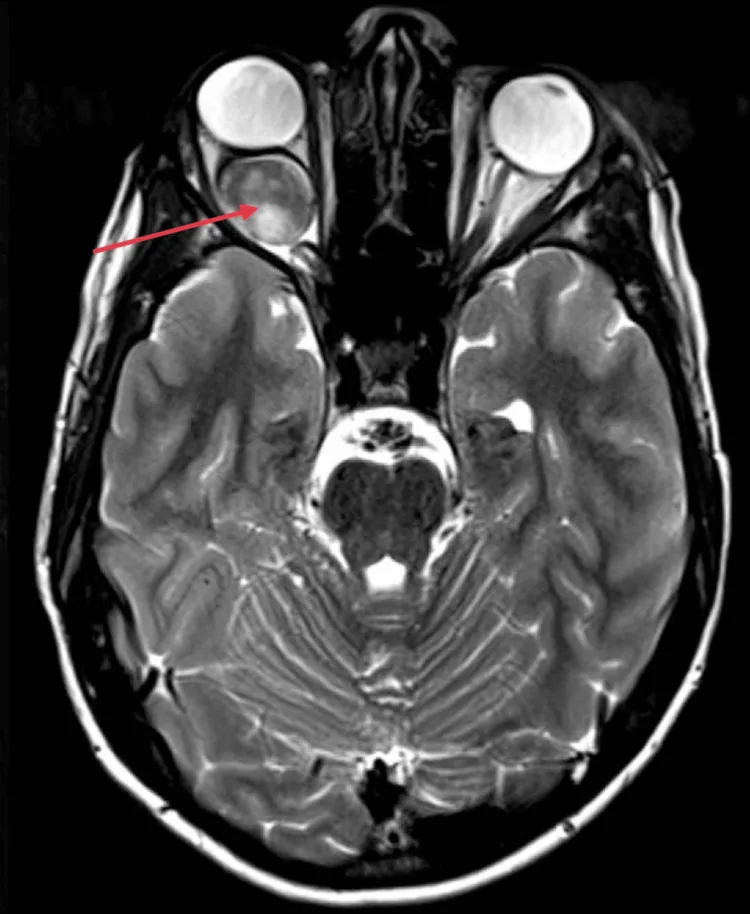
어린 소아는 스스로 시력 저하를 호소하지 않습니다. 따라서 부모나 주변 사람이 **사시(특히 내사시)**를 발견하고 안과를 처음 방문하는 경우가 많습니다.
사시가 없는 단안성 시력 저하는 더욱 발견이 늦어지기 쉽습니다. 첫 진료 시 이미 시신경 위축이 나타난 경우도 있습니다.
양안성 시신경 교종은 어린 연령에서 발병한 경우에 많습니다. 시선의 이상이나 ‘보지 못하는 행동’으로 처음 발견되며, 시력 장애가 심각할 수 있습니다.
안구 돌출은 명확하지 않으며 통증도 없습니다.
안저 검사에서는 다음 소견이 자주 관찰됩니다.
NF1(신경섬유종증 1형) 동반 예에서는 다음과 같은 전신 소견을 동반합니다.
CT 소견:
MRI 소견(정밀 검사 필요):
NF1 환자에서는 시신경교종의 위험이 현저히 높으며, 전체 시신경교종 증례의 20~30%가 NF1 동반 사례입니다1). NF1 진단 후에는 시신경교종 선별검사로서 정기적인 안과 추적 관찰이 권장됩니다. 반대로, 소아에서 시신경교종이 발견된 경우 모든 사례에서 NF1 진단 기준을 충족하는지 확인하는 것이 중요합니다.
NF1(신경섬유종증 1형)의 진단 기준 주요 항목은 다음과 같습니다2).
| 소견 | 기준 |
|---|---|
| 카페오레 반점 | ≥6개 (소아: 장경 ≥5mm, 사춘기 이후: 장경 ≥15mm) |
| 신경섬유종 | ≥2개 (모든 유형) 또는 ≥1개의 총상 신경섬유종 |
| 홍채 Lisch 결절 | ≥2개 |
| 특징적 골 병변 | 접형골 날개 형성 이상 또는 장관골 피질 비박 |
| 시신경교종 | ≥1개 |
| 액와 또는 서혜부 주근깨 | 존재함 |
| 일차 친족 | NF1 확진자 |
NF1 확진을 위해서는 위 기준 중 2개 이상을 충족해야 합니다.
MRI는 CT보다 종양의 범위 평가에 우수하며 정밀 검사에 필수적이다.
| 소견 | 상세 |
|---|---|
| T1 강조 영상 | 저신호 강도를 보인다 |
| Gd-DTPA 조영 증강 | 균일한 비대와 강한 조영 증강을 보인다 |
| 하향 꺾임 | NF1 동반 예에서 특징적 (시신경 하향 굴곡) |
| 두개내 진행 평가 | 시신경관을 통한 두개내 진행, 시교차 및 시상하부 종양 존재 확인 |
시신경초 수막종
가장 중요한 감별 질환.
성인 여성에 많고, NF2 동반 예가 있음. CT/MRI에서 tram-track sign (전차 선로 모양 소견)이 특징적이며, 시신경교종과의 감별에 유용.
시신경염
급성 발병, 안구 운동 시 통증을 동반하는 경우가 많음.
MRI에서 시신경 조영 증강을 보이나, 종대는 경미함. 스테로이드 치료로 호전되는 경우가 많음.
기타 감별 질환:
시신경교종은 **균일한 비대와 하방 꺾임(downward kinking)**을 보이며, 시신경초수막종의 tram-track sign과 명확히 구별됩니다.
시신경교종은 소아에 흔한 양성 종양(모세포성 성상세포종)으로, NF1 동반이 있습니다. CT/MRI에서 시신경의 균일한 비대와 하방 꺾임이 특징적입니다. 시신경초수막종은 성인 여성에 많고, NF2 동반 예도 있으며, CT/MRI에서 tram-track sign(시신경초를 따라 달리는 석회화 또는 조영 증강)을 나타내는 점에서 감별됩니다.
종양은 양성이며 소아에 많기 때문에, 안와 내 시신경에 국한되어 있는 경우 외과적 절제나 방사선 조사는 원칙적으로 시행하지 않습니다. 정기적인 영상 검사(MRI: 3~6개월마다)를 중심으로 한 신중한 경과 관찰이 기본 방침입니다.
과거에는 수술이 이루어졌지만, 비가역적 실명에 이르는 위험이 높기 때문에 현재는 외과적 절제를 피하는 경향입니다. NF1 동반 예에서는 자연 퇴축(regression) 보고도 있으므로, 특히 신중한 경과 관찰이 이루어집니다.
시력 저하·종양 증대가 진행되는 경우, 카보플라틴 + 빈크리스틴(CV 요법) 병용 화학 요법이 표준 일차 치료로 사용됩니다3)4).
표준 CV 요법 레지멘(COG A9952 등):
CV 요법의 객관적 반응률(부분 관해 + 안정화)은 60~80%로 보고됩니다4).
이차 치료 선택지:
항암화학요법에 저항하는 진행성 사례에서 고려됩니다. 그러나 소아에서는 이차 암 위험, 내분비 기능 장애(시상하부 근처 조사), 인지 기능에 미치는 영향이 우려되므로 가능한 한 피하는 경향이 있습니다.
현재는 적극적인 수술적 절제를 피하는 경향이 있습니다.
수술 적응증이 고려되는 상황:
시신경 교종의 병리조직학적 소견은 양성의 **모세포성 성상세포종 (pilocytic astrocytoma, WHO Grade I)**입니다. 교모세포종 (glioblastoma multiforme, WHO Grade IV) 등 고악성도 교종과는 본질적으로 다릅니다.
종양 세포는 양극성 세포 돌기를 가진 특징적인 형태를 보이며, Rosenthal 섬유를 포함합니다. 시신경의 신경아교세포(별아교세포)에서 발생하여 시신경을 내부에서 압박하고 대체합니다.
신경섬유종증 1형(NF1) 관련 시신경교종은 **NF1 유전자(염색체 17q11.2)**의 돌연변이로 인해 발생합니다.
산발성(NF1 비동반) 모세포성 별아교세포종에서는 BRAF-KIAA1549 융합 유전자가 높은 빈도로 관찰됩니다. 이 융합 유전자도 MAPK 경로를 활성화하여 종양 증식을 촉진합니다.
일부 증례는 BRAF V600E 돌연변이를 가지며, 이를 가진 증례는 악성도가 높은 경향이 있습니다6).
시신경교종의 대부분은 저등급이며, 완만한 증식을 보입니다. 종양은 시신경을 내부에서 종대시키고, 안와 내에서 시신경을 구부러지게(kinking, downward kinking) 만듭니다. MRI에서 균일한 종대와 하방 굴곡이 영상 진단의 핵심 포인트입니다.
안와 내 국한 증례:
시교차/시상하부 침윤 예:
생명 예후:
기능 예후:
시력 예후는 균일하지 않으며 진행형과 안정형이 혼재하므로 종양 크기뿐만 아니라 시 기능의 종적 평가가 필요합니다. MRI 소견이 안정적이어도 시 기능이 악화되는 증례가 있으며, 반대로 NF1 동반 예에서는 자연 퇴축을 보이기도 합니다. 1, 8, 9)
NF1 관련 저등급 신경교종에 대한 MEK 억제제의 유효성이 보고되었습니다.
SPRINT 시험(2상)에서 셀루메티닙은 NF1 관련 진행성 저등급 신경교종(총상 신경섬유종)에 대해 객관적 반응률 66%를 보였습니다 7). 시신경 신경교종을 포함한 NF1 관련 저등급 신경교종으로의 적용이 검토되고 있습니다.
BRAF V600E 돌연변이를 가진 소아 저등급 신경교종에 대해 다브라페닙 + 트라메티닙 병용 요법이 임상 시험에서 평가되고 있습니다 6). BRAF-KIAA1549 융합 양성 사례에서는 BRAF 억제제의 유효성이 제한적입니다.
MEK 억제제와 BRAF 억제제의 등장으로 기존 화학요법(CV 요법)에서 분자 프로파일에 기반한 개인 맞춤 치료로의 전환이 진행되고 있습니다 8). 향후 유전자 돌연변이 프로파일(BRAF 융합, BRAF V600E, NF1 돌연변이 등)에 기반한 치료 선택이 표준화될 가능성이 있습니다.
Listernick R, Charrow J, Greenwald M, Mets M. Natural history of optic pathway tumors in children with neurofibromatosis type 1: a longitudinal study. J Pediatr. 1994;125(1):63-66.
Ferner RE, Huson SM, Thomas N, et al. Guidelines for the diagnosis and management of individuals with neurofibromatosis 1. J Med Genet. 2007;44(2):81-88.
Gnekow AK, Walker DA, Kandels D, et al. A European randomised controlled trial of the addition of etoposide to standard vincristine and carboplatin induction as part of an 18-month treatment programme for childhood (≤16 years) low grade glioma - A final report. Eur J Cancer. 2017;81:206-225.
Ater JL, Zhou T, Holmes E, et al. Randomized study of two chemotherapy regimens for treatment of low-grade glioma in young children: a report from the Children’s Oncology Group. J Clin Oncol. 2012;30(21):2641-2647.
Lassaletta A, Scheinemann K, Zelcer SM, et al. Phase II weekly vinblastine for chemotherapy-naive children with progressive low-grade glioma: a Canadian Pediatric Brain Tumor Consortium study. J Clin Oncol. 2016;34(29):3537-3543.
Fangusaro J, Onar-Thomas A, Young Poussaint T, et al. Selumetinib in paediatric patients with BRAF-aberrant or neurofibromatosis type 1-associated recurrent, refractory, or progressive low-grade glioma: a multicentre, phase 2 trial. Lancet Oncol. 2019;20(7):1011-1022.
Banerjee A, Jakacki RI, Onar-Thomas A, et al. A phase I trial of the MEK inhibitor selumetinib (AZD6244) in pediatric patients with recurrent or refractory low-grade gliomas: a Pediatric Brain Tumor Consortium (PBTC) study. Neuro Oncol. 2017;19(8):1135-1144.
de Blank PMK, Orne-Ibekwe E, Packer R. International consensus recommendations for visual surveillance in optic pathway gliomas associated with neurofibromatosis type 1. J Neurooncol. 2020;148(3):571-578.
Listernick R, Louis DN, Packer RJ, Gutmann DH. Optic pathway gliomas in children with neurofibromatosis 1: consensus statement from the NF1 Optic Pathway Glioma Task Force. Ann Neurol. 1997;41(2):143-149.