نوع محدود به داخل حدقه
شایعترین شکل بروز. کاهش بینایی یک طرفه و بیرونزدگی چشم از علائم اصلی هستند.
محدود به عصب بینایی داخل حدقه است و اساساً تحت نظر گرفته میشود. در موارد همراه با NF1، مواردی از کوچک شدن خودبهخودی نیز گزارش شده است.

گلیوم عصب بینایی (optic nerve glioma / optic pathway glioma) نوعی گلیوما است که از عصب بینایی منشأ میگیرد. به معنای محدود، به گلیومای ایجاد شده در عصب بینایی قبل از کیاسمای بینایی اطلاق میشود. به معنای گسترده، شامل گلیومای کل مسیر بینایی (optic pathway glioma) از جمله نواحی پشت کیاسما نیز میشود.
از نظر بافتشناسی، اکثر موارد آستروسیتوم پیلوسیتیک خوشخیم (درجه I WHO) هستند. با این حال، موارد بدخیم نیز گزارش شده است. حدود 70 درصد موارد در دوران کودکی رخ میدهد و این بیماری نادر حدود 0.5 تا 5 درصد تومورهای مغزی کودکان را تشکیل میدهد.
ارتباط قوی با نوروفیبروماتوز نوع 1 (NF1، بیماری فون رکلینگهاوزن) وجود دارد و حدود 20 تا 30 درصد موارد گلیوم عصب بینایی با NF1 همراه هستند. برعکس، شایعترین ضایعه چشمی در بیماران NF1 گلیوم عصب بینایی است.
نوع محدود به داخل حدقه
شایعترین شکل بروز. کاهش بینایی یک طرفه و بیرونزدگی چشم از علائم اصلی هستند.
محدود به عصب بینایی داخل حدقه است و اساساً تحت نظر گرفته میشود. در موارد همراه با NF1، مواردی از کوچک شدن خودبهخودی نیز گزارش شده است.
نوع تهاجم به کیاسمای بینایی
نوعی که تا کیاسمای بینایی نفوذ میکند.
باعث اختلال بینایی دوطرفه میشود و مدیریت آن پیچیده است. در سنین پایین شایعتر است و گسترش به هیپوتالاموس ارزیابی میشود.
نوع مسیر بینایی-هیپوتالاموسی
نوعی که از پشت کیاسما تا هیپوتالاموس گسترش مییابد.
ممکن است با ناهنجاریهای غدد درونریز (مانند اختلال رشد، بلوغ زودرس) همراه باشد. درمان نیاز به همکاری جراحی مغز و اعصاب و غدد درونریز دارد.
بر اساس زمینه ژنتیکی، دو نوع همراه با NF1 (حدود 30٪ موارد) و تک گیر (حدود 70٪) وجود دارد. در نوع همراه با NF1، بروز دوطرفه نیز دیده میشود.
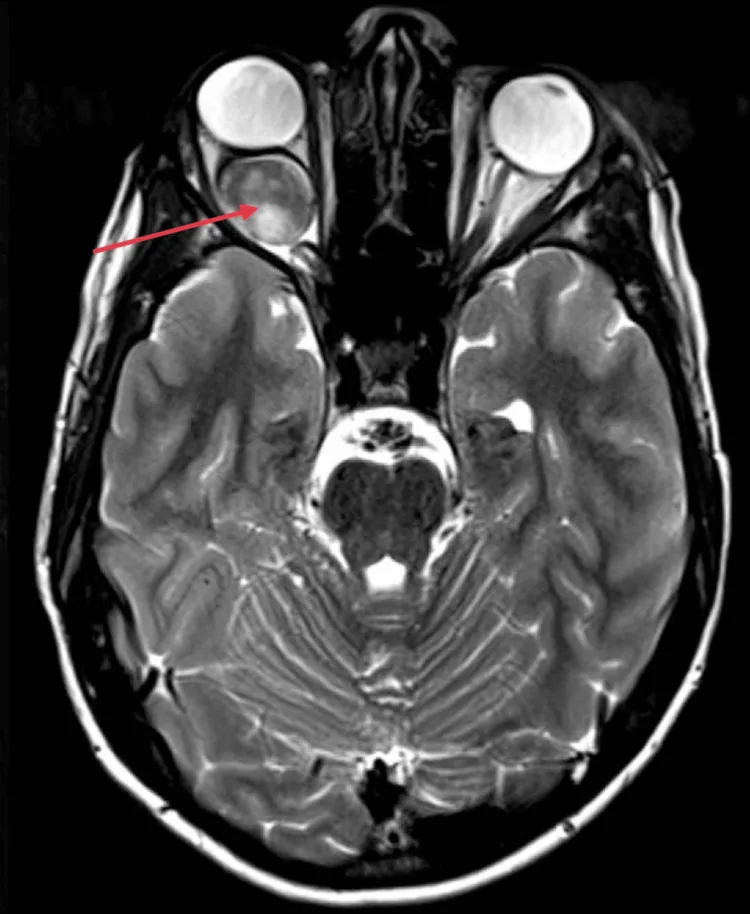
کودکان کمسن و سال خودشان از کاهش بینایی شکایت نمیکنند. بنابراین، والدین یا اطرافیان معمولاً متوجه انحراف چشم (بهویژه انحراف به داخل) میشوند و برای اولین بار به چشمپزشک مراجعه میکنند.
کاهش بینایی یکطرفه بدون انحراف چشم حتی دیرتر کشف میشود. ممکن است در اولین مراجعه، آتروفی عصب بینایی ایجاد شده باشد.
گلیوم عصب بینایی دوطرفه در موارد با شروع در سنین پایین شایعتر است. ابتدا با ناهنجاری در نگاه یا رفتارهای «ندیدن» تشخیص داده میشود و اختلال بینایی ممکن است شدید باشد.
برجستگی چشم واضح نیست و دردی وجود ندارد.
در گلیوم عصب بینایی، کودکان کمسن و سال نمیتوانند کاهش بینایی را درک یا ابراز کنند، بنابراین انحراف چشم (بهویژه انحراف به داخل) اغلب بهعنوان اولین علامت منجر به مراجعه به چشمپزشک میشود. در کودکانی که انحراف چشم تشخیص داده میشود، بهویژه انحراف یکطرفه، مهم است که گلیوم عصب بینایی را در نظر گرفته و معاینات کامل شامل بینایی، فوندوس و تصویربرداری انجام شود.
در معاینه فوندوس معمولاً یافتههای زیر دیده میشود:
در موارد همراه با NF1 (نوروفیبروماتوز نوع 1)، یافتههای سیستمیک زیر وجود دارد:
یافتههای CT:
یافتههای MRI (برای بررسی دقیق):
در بیماران NF1، خطر گلیوم عصب بینایی به طور قابل توجهی افزایش مییابد و 20 تا 30٪ از کل موارد گلیوم عصب بینایی با NF1 همراه هستند 1). پس از تشخیص NF1، پیگیری منظم چشمی به عنوان غربالگری گلیوم عصب بینایی توصیه میشود. برعکس، در صورت تشخیص گلیوم عصب بینایی در کودکان، بررسی اینکه آیا معیارهای تشخیصی NF1 را دارند یا خیر در همه موارد مهم است.
موارد اصلی معیارهای تشخیصی NF1 (نوروفیبروماتوز نوع 1) در زیر آورده شده است 2).
| یافته | معیار |
|---|---|
| لکههای کافهاو له | ≥6 عدد (در کودکان: قطر ≥5 میلیمتر، پس از بلوغ: قطر ≥15 میلیمتر) |
| نوروفیبروم | ≥2 عدد (از هر نوع) یا یک یا چند نوروفیبروم پلکسیفرم |
| ندولهای لیش عنبیه | ≥2 عدد |
| ضایعات استخوانی مشخصه | دیسپلازی بال پروانهای یا نازک شدن قشر استخوانهای بلند |
| گلیوم عصب بینایی | ≥1 عدد |
| ککمک در زیربغل و کشاله ران | وجود دارد |
| خویشاوند درجه یک | فرد با تشخیص قطعی NF1 |
برای تشخیص قطعی NF1، حداقل دو مورد از معیارهای فوق باید وجود داشته باشد.
MRI نسبت به CT در ارزیابی گسترش تومور برتر است و برای بررسی دقیق ضروری است.
| یافته | جزئیات |
|---|---|
| تصویر T1-weighted | سیگنال پایین نشان میدهد |
| افکت کنتراست Gd-DTPA | بزرگ شدن یکنواخت و کنتراست قوی را نشان میدهد |
| خمیدگی رو به پایین | ویژگی در موارد همراه با NF1 (خمیدگی رو به پایین عصب بینایی) |
| ارزیابی گسترش داخل جمجمهای | تأیید گسترش از کانال عصب بینایی به داخل جمجمه، وجود تومور در کیاسمای بینایی و هیپوتالاموس |
مننژیوم غلاف عصب بینایی
مهمترین بیماری برای تشخیص افتراقی.
بیشتر در زنان بالغ دیده میشود و موارد همراه با NF2 وجود دارد. در CT/MRI، علامت tram-track (ظاهر ریل قطار) مشخصه است و برای افتراق از گلیوم عصب بینایی مفید میباشد.
نوریت بینایی
اغلب با شروع حاد و درد هنگام حرکت چشم همراه است.
در MRI، افزایش کنتراست عصب بینایی دیده میشود، اما تورم خفیف است. معمولاً با درمان استروئیدی بهبود مییابد.
سایر بیماریهای افتراقی:
گلیوم عصب بینایی باعث بزرگ شدن یکنواخت و خمیدگی رو به پایین (downward kinking) میشود و به وضوح از علامت ترام-تراک (tram-track sign) در مننژیوم غلاف عصب بینایی قابل تشخیص است.
گلیوم عصب بینایی یک تومور خوشخیم شایع در کودکان (آستروسیتوم پیلوسیتیک) است و با NF1 همراهی دارد. در CT/MRI، بزرگ شدن یکنواخت عصب بینایی و خمیدگی رو به پایین مشخصه آن است. مننژیوم غلاف عصب بینایی بیشتر در زنان بالغ دیده میشود، موارد همراه با NF2 نیز وجود دارد، و در CT/MRI علامت ترام-تراک (کلسیفیکاسیون یا افزایش کنتراست در اطراف عصب بینایی) را نشان میدهد که از این طریق افتراق داده میشود.
از آنجایی که تومور خوشخیم است و بیشتر در کودکان دیده میشود، در صورت محدود بودن به عصب بینایی داخل کاسه چشم، اصولاً جراحی برداشتن یا پرتودرمانی انجام نمیشود. پیگیری دقیق با تصویربرداری دورهای (MRI هر ۳ تا ۶ ماه) اساس درمان است.
در گذشته جراحی انجام میشد، اما به دلیل خطر بالای نابینایی غیرقابل برگشت، امروزه تمایل به اجتناب از برداشتن جراحی وجود دارد. در موارد همراه با NF1، گزارشهایی از پسرفت خودبهخودی (regression) وجود دارد، بنابراین پیگیری با دقت بیشتری انجام میشود.
در صورت پیشرفت کاهش بینایی یا افزایش اندازه تومور، شیمیدرمانی ترکیبی با کربوپلاتین و وینکریستین (رژیم CV) به عنوان درمان خط اول استاندارد استفاده میشود 3)4).
رژیم استاندارد CV (مانند COG A9952):
نرخ پاسخ عینی (بهبودی نسبی + تثبیت) در رژیم CV ۶۰ تا ۸۰٪ گزارش شده است 4).
گزینههای درمان خط دوم:
در موارد پیشرفته مقاوم به شیمیدرمانی در نظر گرفته میشود. با این حال، در کودکان به دلیل خطر سرطان ثانویه، اختلال عملکرد غدد درونریز (به دلیل تابش نزدیک هیپوتالاموس) و تأثیر بر عملکرد شناختی، تا حد امکان از آن اجتناب میشود.
در حال حاضر تمایل به اجتناب از جراحی تهاجمی برداشتن تومور وجود دارد.
شرایطی که در آن جراحی در نظر گرفته میشود:
یافتههای پاتولوژی بافتی گلیوم عصب بینایی، آستروسیتوم پیلوسیتیک خوشخیم (pilocytic astrocytoma, WHO Grade I) است. این تومور اساساً با گلیومهای با درجه بدخیمی بالا مانند گلیوبلاستوم مولتی فرم (WHO Grade IV) متفاوت است.
سلولهای تومور شکل مشخصی با زوائد سلولی دوقطبی دارند و حاوی الیاف روزنتال هستند. آنها از سلولهای گلیال (آستروسیتهای) عصب بینایی منشأ گرفته و عصب بینایی را از داخل فشرده و جایگزین میکنند.
گلیوم عصب بینایی مرتبط با NF1 (نوروفیبروماتوز نوع 1) ناشی از جهش در ژن NF1 (کروموزوم 17q11.2) است.
در آستروسیتوم پیلوسیتیک پراکنده (بدون NF1)، ژن همجوشی BRAF-KIAA1549 با فراوانی بالا دیده میشود. این ژن همجوشی نیز مسیر MAPK را فعال کرده و رشد تومور را تسریع میکند.
برخی موارد دارای جهش BRAF V600E هستند که با درجه بدخیمی بالاتر همراه است6).
اکثر گلیومهای عصب بینایی از نوع درجه پایین (low-grade) بوده و رشد آهسته دارند. تومور عصب بینایی را از داخل متورم کرده و باعث خمیدگی (kinking و downward kinking) عصب در داخل حدقه میشود. تورم یکنواخت و خمیدگی رو به پایین در MRI نکات کلیدی تشخیص تصویربرداری هستند.
موارد محدود به حدقه:
موارد با نفوذ به کیاسمای بینایی و هیپوتالاموس:
پیشآگهی حیاتی:
پیشآگهی عملکردی:
پیشآگهی بینایی یکسان نیست و موارد پیشرونده و پایدار با هم مخلوط میشوند، بنابراین ارزیابی طولی عملکرد بینایی علاوه بر اندازه تومور ضروری است. در برخی موارد، یافتههای MRI پایدار است اما عملکرد بینایی بدتر میشود، و برعکس، در موارد همراه با NF1 ممکن است پسرفت خودبهخودی رخ دهد.1, 8, 9)
اثربخشی مهارکنندههای MEK برای گلیومهای با درجه پایین مرتبط با NF1 گزارش شده است.
در کارآزمایی SPRINT (فاز II)، نرخ پاسخ عینی 66٪ برای سلمتینیب در گلیومهای پیشرونده با درجه پایین مرتبط با NF1 (نوروفیبروم پلکسیفرم) گزارش شد7). کاربرد آن برای گلیومهای با درجه پایین مرتبط با NF1 از جمله گلیومهای عصب بینایی در حال بررسی است.
برای گلیومهای با درجه پایین کودکان با جهش BRAF V600E، درمان ترکیبی داورافنیب + ترامتینیب در کارآزماییهای بالینی ارزیابی شده است6). در موارد مثبت از نظر همجوشی BRAF-KIAA1549، اثربخشی مهارکنندههای BRAF محدود است.
با ظهور مهارکنندههای MEK و BRAF، تغییر از شیمیدرمانی سنتی (رژیم CV) به درمان فردی بر اساس پروفایل مولکولی در حال انجام است8). در آینده، انتخاب درمان بر اساس پروفایل جهشهای ژنتیکی (همجوشی BRAF، BRAF V600E، جهش NF1 و غیره) ممکن است استاندارد شود.
Listernick R, Charrow J, Greenwald M, Mets M. Natural history of optic pathway tumors in children with neurofibromatosis type 1: a longitudinal study. J Pediatr. 1994;125(1):63-66.
Ferner RE, Huson SM, Thomas N, et al. Guidelines for the diagnosis and management of individuals with neurofibromatosis 1. J Med Genet. 2007;44(2):81-88.
Gnekow AK, Walker DA, Kandels D, et al. A European randomised controlled trial of the addition of etoposide to standard vincristine and carboplatin induction as part of an 18-month treatment programme for childhood (≤16 years) low grade glioma - A final report. Eur J Cancer. 2017;81:206-225.
Ater JL, Zhou T, Holmes E, et al. Randomized study of two chemotherapy regimens for treatment of low-grade glioma in young children: a report from the Children’s Oncology Group. J Clin Oncol. 2012;30(21):2641-2647.
Lassaletta A, Scheinemann K, Zelcer SM, et al. Phase II weekly vinblastine for chemotherapy-naive children with progressive low-grade glioma: a Canadian Pediatric Brain Tumor Consortium study. J Clin Oncol. 2016;34(29):3537-3543.
Fangusaro J, Onar-Thomas A, Young Poussaint T, et al. Selumetinib in paediatric patients with BRAF-aberrant or neurofibromatosis type 1-associated recurrent, refractory, or progressive low-grade glioma: a multicentre, phase 2 trial. Lancet Oncol. 2019;20(7):1011-1022.
Banerjee A, Jakacki RI, Onar-Thomas A, et al. A phase I trial of the MEK inhibitor selumetinib (AZD6244) in pediatric patients with recurrent or refractory low-grade gliomas: a Pediatric Brain Tumor Consortium (PBTC) study. Neuro Oncol. 2017;19(8):1135-1144.
de Blank PMK, Orne-Ibekwe E, Packer R. International consensus recommendations for visual surveillance in optic pathway gliomas associated with neurofibromatosis type 1. J Neurooncol. 2020;148(3):571-578.
Listernick R, Louis DN, Packer RJ, Gutmann DH. Optic pathway gliomas in children with neurofibromatosis 1: consensus statement from the NF1 Optic Pathway Glioma Task Force. Ann Neurol. 1997;41(2):143-149.