رادیوتراپی استریوتاکتیک فرکشن (fSRT)
پرتو درمانی فرکشن (رادیوتراپی استریوتاکتیک فرکشن): مزیت کاهش آسیب به عصب بینایی را دارد.
دوز: 50 تا 54 گری در 25 تا 30 جلسه استاندارد است. نرخ تثبیت و بهبود میدان بینایی 83 تا 100٪ گزارش شده است.3)5)

مننژیوم غلاف عصب بینایی (ONSM) توموری است که از مننژ (پوشش) اطراف عصب بینایی منشأ میگیرد. در میان تومورهای حدقه نسبتاً نادر است و حدود 1-2% از کل مننژیومها، 10% از تومورهای حدقه و 33% از تومورهای عصب بینایی را تشکیل میدهد. بیشتر در بزرگسالان، به ویژه زنان میانسال رخ میدهد.
دو الگوی اصلی بروز وجود دارد: نوع اولیه داخل حدقهای که مستقیماً از غلاف عصب بینایی در حدقه منشأ میگیرد، و نوع گسترش داخل جمجمهای که در آن مننژیوم داخل جمجمه از طریق کانال عصب بینایی به حدقه گسترش مییابد. تمایز این دو نوع برای تعیین استراتژی مدیریت مهم است.
انواع بافتی متعددی وجود دارد که به سه نوع اصلی تقسیم میشوند:
گزارش شده است که حدود 20% موارد دارای ویژگیهای بدخیم (آتیپی سلولی، افزایش میتوز، نکروز و غیره) هستند. در طبقهبندی WHO، اکثر موارد درجه I (خوشخیم) هستند، اما درجه II (آتیپیک) و درجه III (بدخیم) نیز وجود دارند.
بیشتر آنها خوشخیم (WHO Grade I) هستند، اما گزارش شده است که حدود 20٪ ویژگیهای بدخیم نشان میدهند. به ندرت، ویژگیهای تهاجمی و بدخیم ظاهر میشوند و میزان عود بالاتر میرود. در کودکان، خطر بدخیمی و گسترش داخل جمجمهای نسبت به بزرگسالان بیشتر است.
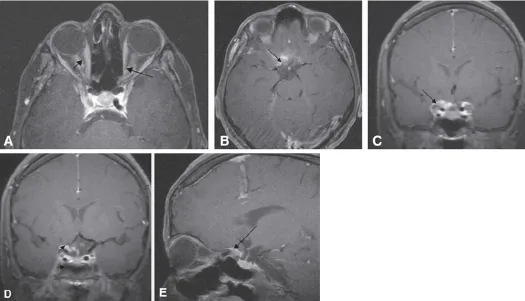
بارزترین ویژگی کاهش تدریجی بینایی یک طرفه است که طی چند ماه تا چند سال سیر مزمن دارد. معمولاً با درد همراه نیست.
با رشد تومور، یافتههای فوندوسکوپی به شرح زیر تغییر میکنند.
عروق شانت اپتو-سیلیاری (optociliary shunt vessels): عروق جانبی در اطراف پاپی که در نتیجه جبرانی برای فشار مزمن ورید مرکزی شبکیه توسط تومور ایجاد میشوند. این یکی از یافتههای مشخص فوندوسکوپی در ONSM است.
نقص نسبی آوران مردمک (RAPD) اغلب مثبت است. ممکن است با کاهش دید رنگی همراه باشد.
تصویربرداری برای تأیید ONSM بسیار مهم است و الگوهای زیر شناخته شدهاند.
الگوهای اصلی تصویربرداری در CT/MRI با کنتراست:
| الگو | ویژگی |
|---|---|
| نوع لولهای (علامت tram-track) | بزرگ شدن استوانهای در تمام طول عصب بینایی و کنتراست دوخطی |
| نوع کروی | شبیه سیبی که به تیر خورده، اطراف عصب بینایی را به صورت کروی احاطه میکند |
| نوع غیرمرکزی | بزرگ شدن آنوریسممانند به یک طرف عصب بینایی |
بخشی از تومور ممکن است کلسیفیکاسیون داشته باشد (CT در تشخیص آن بهتر است). در MRI با کنتراست، تومور افزایش سیگنال یکنواخت و قوی نشان میدهد.
علامت tram-track یک یافته تصویربرداری مشخص است که در آن تومور در دو طرف عصب بینایی به صورت دو خط (مانند ریل قطار) در CT یا MRI با کنتراست در نمای محوری دیده میشود. این به دلیل رشد تومور در اطراف عصب بینایی در حالی که خود عصب داخلی حفظ شده است، ایجاد میشود. این علامت اختصاصیت بالایی برای ONSM دارد و در موارد معمولی، تشخیص تصویربرداری بدون بیوپسی امکانپذیر است.
ONSM در میان تومورهای حدقه نسبتاً نادر است.
همراهی با نوروفیبروماتوز نوع 2 (NF2): NF2 به عنوان یک بیماری ارثی مرتبط با ONSM شناخته میشود. ژن NF2 در بازوی بلند کروموزوم 22 (22q12) قرار دارد و پروتئین مرلین را کد میکند. تصور میشود که از دست دادن عملکرد مرلین در ایجاد تومور نقش دارد. در موارد ONSM کودکان، میزان همراهی با NF2 بالاست و باید به خطر مننژیوم دوطرفه و چندگانه توجه کرد.
علاوه بر این، قرار گرفتن در معرض پرتوهای یونیزان به عنوان یک عامل خطر برای مننژیوم به طور کلی گزارش شده است.
MRI با کنتراست (انتخاب اول): MRI اربیت با ترکیب ماده حاجب گادولینیوم و تکنیک سرکوب چربی مفیدترین روش است.
CT: CT در تشخیص کلسیفیکاسیون برتر است. علامت tram-track نیز در CT قابل مشاهده است. در صورت گسترش ضایعه به کانال بینایی، گشاد شدن کانال بینایی دیده میشود.
معاینه فوندوس، تست میدان بینایی و OCT: برای ارزیابی مورفولوژی دیسک بینایی، عروق شانت اپتو-سیلیاری و ضخامت لایه فیبرهای عصبی شبکیه (RNFL) استفاده میشود. تست میدان بینایی الگوی آسیب را مشخص میکند.
تشخیص افتراقی از بیماریهای زیر مهم است:
| بیماری | نکات افتراقی |
|---|---|
| گلیوم عصب بینایی | شایع در کودکان و همراه با NF1. در T2 سیگنال بالا، بزرگ شدن یکنواخت و پیچخوردگی عصب بینایی (downward kinking) مشخصه است. اثر کنتراست خفیف تا متغیر |
| نوریت بینایی | کاهش بینایی حاد یا تحت حاد. همراه با درد (درد هنگام حرکت چشم). در MRI با کنتراست، افزایش سیگنال داخل عصب بینایی دیده میشود |
| شبهتومور اربیت (التهاب اربیت مرتبط با IgG4 و غیره) | پاسخ به استروئید. در موارد مرتبط با IgG4، اغلب التهاب غده اشکی و بافت نرم اربیت همراه است |
| پرینوریت اپتیک | سیر حاد یا تحت حاد. ضخیم شدن التهابی غلاف عصب بینایی |
| لنفوم | نفوذ لنفوم سیستمیک به اربیت نیز باید در نظر گرفته شود. تشخیص با بررسی بافتشناسی قطعی میشود |
در صورت مشکوک بودن به NF2، بررسی برای شوانوم آکوستیک دوطرفه و مننژیوم متعدد انجام شود.
اصل بیوپسی: در صورت وجود یافتههای تصویربرداری معمول (مانند tram-track sign)، معمولاً بیوپسی ضروری نیست. عصب بینایی و غلاف آن (ONSM) جریان خون نرمشامهای مشترک دارند و اقدامات جراحی از جمله بیوپسی خطر آسیب به عصب بینایی را به همراه دارد. در صورت باقی ماندن دید مفید، باید از مداخله جراحی خودداری کرد. 6)
گلیوم عصب بینایی بیشتر در کودکان دیده میشود و همراهی با NF1 (نوروفیبروماتوز نوع 1) مشخصه آن است، در حالی که مننژیوم غلاف عصب بینایی در زنان میانسال شایعتر است و با NF2 مرتبط شناخته میشود. در تصویربرداری، گلیوم باعث بزرگ شدن یکنواخت عصب بینایی و پیچخوردگی (downward kinking) میشود و در تصاویر T2-weighted سیگنال بالا نشان میدهد. در مقابل، مننژیوم غلاف عصب بینایی باعث کنتراستگیری غلاف (محیطی) و ایجاد tram-track sign میشود و آکسونهای عصب بینایی در داخل حفظ میشوند که نکته تمایز مهمی است.
استراتژی درمان ONSM بر اساس وضعیت عملکرد بینایی و میزان پیشرفت تومور تعیین میشود.
در صورت کاهش آهسته یا خفیف عملکرد بینایی، پیگیری دقیق با معاینات منظم انتخاب میشود.
در صورت پیشرفت کاهش عملکرد بینایی یا گسترش تومور به داخل جمجمه، رادیوتراپی استریوتاکتیک خط اول درمان است. انتظار میرود که عملکرد بینایی حفظ شده و از رشد تومور جلوگیری شود.2)3)
رادیوتراپی استریوتاکتیک فرکشن (fSRT)
پرتو درمانی فرکشن (رادیوتراپی استریوتاکتیک فرکشن): مزیت کاهش آسیب به عصب بینایی را دارد.
دوز: 50 تا 54 گری در 25 تا 30 جلسه استاندارد است. نرخ تثبیت و بهبود میدان بینایی 83 تا 100٪ گزارش شده است.3)5)
گاما نایف (GKRS)
جراحی رادیواکتیو استریوتاکتیک: امکان کاهش شدید دوز در یک جلسه وجود دارد.
نرخ کنترل تومور بیش از 90٪ گزارش شده است. تمرکز دوز در تومورهای خارجی مزیت محسوب میشود.1)
سایبر نایف
پرتو درمانی استریوتاکتیک رباتیک: میتواند تومورهایی با اشکال پیچیده را نیز درمان کند.
نرخ کنترل تومور مشابه گاما نایف گزارش شده است.4)
نرخ حفظ عملکرد بینایی پس از رادیوتراپی 70 تا 95٪ و نرخ کنترل تومور بیش از 90٪ است.2)3) هرچه حدت بینایی قبل از درمان بهتر باشد، پیشآگهی بهتر است.
عوارض جانبی اصلی پرتودرمانی:
در صورت باقی ماندن بینایی مفید، برداشت جراحی اصولاً توصیه نمیشود. تومور و عصب بینایی جریان خون مشترکی از پیا ماتر دارند و خطر از دست دادن بینایی ناشی از برداشت بسیار بالاست.
مواردی که جراحی در نظر گرفته میشود:
در موارد گسترش داخل جمجمهای، با همکاری جراحی مغز و اعصاب، ترکیب کرانیوتومی و پرتودرمانی بررسی میشود.
ONSM از مننژهای تشکیلدهنده غلاف عصب بینایی (به ویژه سلولهای کلاهک عنکبوتیه) منشأ میگیرد. عصب بینایی از پشت کره چشم از طریق کانال بینایی به داخل جمجمه ادامه مییابد و در تمام طول خود توسط غلافی متشکل از دورا ماتر، عنکبوتیه و پیا ماتر احاطه میشود. تومور از سلولهای این غلاف منشأ گرفته و به صورت دایرهای و هممرکز عصب بینایی را احاطه کرده و تکثیر مییابد.
تومور در امتداد غلاف عصب بینایی گسترش یافته و عصب بینایی را از خارج فشرده میکند. این امر از طریق مسیرهای زیر منجر به اختلال بینایی میشود.
اگر تومور محدود به حفره چشم باشد، پیشآگهی حیاتی خوب است، اما در صورت گسترش به کانال عصب بینایی و داخل جمجمه، بر مسیر بینایی طرف مقابل و کیاسم تأثیر گذاشته و پیشآگهی بدتر میشود.
ONSM یک تومور خوشخیم است و سیر طبیعی آن با پیشرفت آهسته طی چندین سال تا چندین دهه مشخص میشود.
پس از درمان، با انجام منظم MRI، آزمایش میدان بینایی و بینایی، وجود یا عدم وجود رشد مجدد پایش میشود.
پرتودرمانی پروتونی (proton beam radiotherapy): دوز پراکندگی کم بوده و انتظار میرود سمیت دیررس کاهش یابد. به ویژه در کودکان، از نظر کاهش خطر سرطان ثانویه ممکن است به عنوان یک گزینه در نظر گرفته شود. 7)
تصویربرداری گیرنده سوماتواستاتین (Ga-68 PET/CT): مننژیوم گیرنده سوماتواستاتین (SSTR2A) را به میزان بالایی بیان میکند. کاربرد آن در ارزیابی فعالیت تومور با تصویربرداری عملکردی در حال تحقیق است.
میفپریستون (داروی ضد پروژسترون): به عنوان درمان دارویی با تمرکز بر مثبت بودن PR در مننژیوم، در موارد مقاوم به درمان مورد تحقیق قرار گرفته است، اما به عنوان درمان استاندارد تثبیت نشده است. 4)