靜脈阻塞引起的原因

上鞏膜靜脈壓升高相關青光眼
1. 什麼是與上鞏膜靜脈壓升高相關的青光眼
Section titled “1. 什麼是與上鞏膜靜脈壓升高相關的青光眼”上鞏膜靜脈壓(EVP)升高是由於房水流出通路下游靜脈壓異常升高導致眼壓升高,從而引起續發性開放隅角青光眼的病理狀態3)。在青光眼分類中,它被歸類為續發性開放隅角青光眼,其主要房水流出阻力位於Schlemm管後方4)。隅角基本上呈開放狀態。
EVP的正常值和Goldmann公式
Section titled “EVP的正常值和Goldmann公式”EVP的正常值約為8~11.5 mmHg,並隨體位變化。臨床上沒有測量EVP的儀器,通常透過臨床發現和影像學檢查間接推斷EVP升高。根據Goldmann公式,眼壓由以下關係式表示:
IOP = (F / C) + EVP
其中F是房水生成率(μL/min),C是房水流出易度(μL/min/mmHg),EVP是上鞏膜靜脈壓(mmHg)。從該公式可以明顯看出,EVP升高直接導致眼壓升高。實測數據顯示,EVP每升高1 mmHg,IOP約升高0.83±0.21 mmHg,兩者呈線性關係。正常眼中EVP的正常值因文獻而異,從「8~10 mmHg」到「8~11.5 mmHg」不等,但無論如何,EVP作為房水流出通路的下游壓力,在決定眼壓方面扮演重要角色。
房水流出通路的解剖
Section titled “房水流出通路的解剖”在房水的傳統流出通路中,房水從Schlemm管經集合管、深層鞏膜靜脈叢、鞏膜內靜脈叢和上鞏膜靜脈叢匯入上眼靜脈。上眼靜脈流入海綿竇,再經頸內靜脈和上腔靜脈到達右心房。該通路中任何部位的阻塞或壓力升高都可能導致EVP升高3)。
當眼壓高於8 mmHg(相當於上鞏膜靜脈壓)時,房水流入Schlemm管的量隨眼壓線性增加。
仰臥位與EVP
Section titled “仰臥位與EVP”夜間睡眠仰臥位時,EVP升高。這是睡眠時眼壓升高的主要機制之一。從坐位變為仰臥位時,頭部靜脈回流減少,上鞏膜靜脈壓升高。即使在正常人,臥位時眼壓也會升高1~6 mmHg,但在有EVP升高基礎疾病的患者中,這種波動會進一步放大。體位變化引起的眼壓波動也可作為EVP升高的輔助診斷手段。
特發性EVP升高(Radius-Maumenee症候群)
Section titled “特發性EVP升高(Radius-Maumenee症候群)”當排除所有其他原因後,診斷為特發性(Radius-Maumenee症候群)1)。該病於1968年由Minas和Podos首次描述,1978年Radius和Maumenee報告了4例,因此得名1)。文獻報導約60例,極為罕見1)。
根據Goldmann公式,眼壓由房水生成量、流出阻力以及上鞏膜靜脈壓(EVP)決定。房水從Schlemm管經集合管和上鞏膜靜脈排入體循環。當這條流出通路下游的靜脈壓升高時,房水從Schlemm管流出的阻力增加。結果,房水在眼內積聚,導致眼壓升高。存在線性關係:EVP每升高1 mmHg,眼壓約升高0.83 mmHg。
2. 主要症狀和臨床所見
Section titled “2. 主要症狀和臨床所見”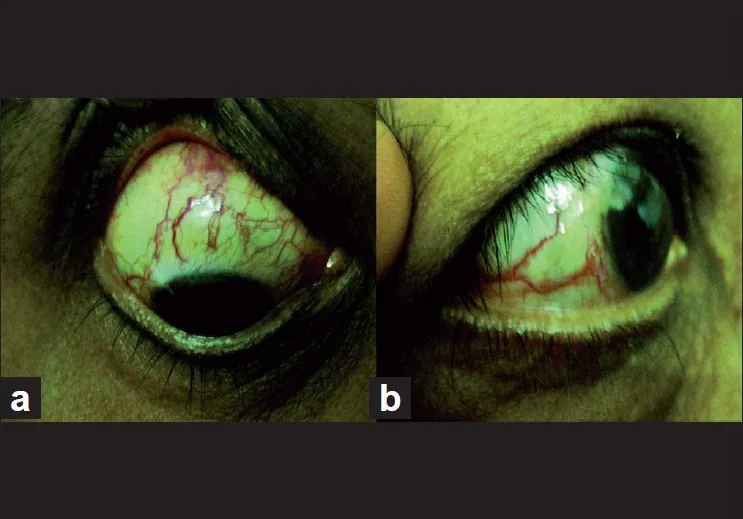
EVP升高的患者常因常規治療無效的慢性眼充血就診。常被誤診為慢性結膜炎3)。通常很少有疼痛或刺激感的主訴。
急性病例(如頸動脈海綿靜脈竇瘻)可能出現眼刺激症狀和眼痛3)。CCF患者可自覺顱內與脈搏同步的雜音(bruit)。也可能伴有因眼球運動障礙引起的複視。
臨床所見(醫師檢查確認的所見)
Section titled “臨床所見(醫師檢查確認的所見)”| 所見 | 特徵 |
|---|---|
| 上鞏膜血管 | 螺旋狀(開瓶器樣)非炎性擴張 |
| 隅角鏡 | 開角 + Schlemm管血液逆流 |
| 眼壓 | 慢性病例中持續升高 |
| 眼球突出 | CCF中呈搏動性 |
| 體位變化 | 臥位時EVP升高→眼壓升高 |
特徵性表現是無發炎的螺旋狀鞏膜表層血管擴張,隅角鏡檢查可見開放隅角和Schlemm管血液逆流1, 2)。慢性病例中也可能出現Schlemm管壁玻璃樣變性。
CCF的臨床所見
Section titled “CCF的臨床所見”CCF的三主徵如下:
- 搏動性眼球突出:由於海綿竇至眼窩的動脈血流所致
- 血管雜音:聽診器在眼眶上或顳部可聽見
- 結膜充血水腫:迂曲怒張的結膜血管稱為「梅杜莎頭」
其他表現包括眼運動神經(動眼、外展、滑車神經)麻痺導致的眼球運動障礙和複視、視網膜出血、靜脈迂曲擴張、脈絡膜剝離、眼痛、頭痛和耳鳴。
- 直接型CCF:內頸動脈主幹直接流入海綿竇。分流量大,症狀嚴重。75%由頭部外傷引起,但近年有報告指出特發性比例增加。
- 硬腦膜頸動脈海綿竇瘻管(硬腦膜瘻管):血液從內頸動脈或外頸動脈的硬腦膜穿通支流入海綿竇。先天性動靜脈畸形、高血壓和糖尿病可能是誘因。分流血量少,病程慢性。在主要引流至下岩竇且上眼靜脈逆流少的病例中,可能不出現特徵性眼部症狀,需注意。
海綿竇血栓症的臨床特徵
Section titled “海綿竇血栓症的臨床特徵”繼發於臉部、眼眶、咽部或鼻竇的感染。最常見的致病菌是葡萄球菌。急性發作,出現發燒、眼瞼明顯腫脹、眼球突出、外眼肌麻痺導致的複視。結膜血管怒張迂曲、視力下降,視乳頭水腫是其特點。可進展至對側而呈雙側性。必須迅速使用抗生素治療,延誤會導致嚴重併發症。
Sturge-Weber症候群的臨床所見
Section titled “Sturge-Weber症候群的臨床所見”以臉部血管瘤(葡萄酒色斑)、同側軟腦膜血管瘤和青光眼三聯徵為特徵的局限性母斑症。多為散發病例,病因被認為是胚胎期交感神經功能障礙導致的血管發育異常。出生時在三叉神經第1、2支分佈區可見特徵性火焰狀母斑(通常單側)。
眼部所見中青光眼最為重要,伴有以下所見:
- 結膜和上鞏膜血管擴張迂曲:反映EVP升高
- 脈絡膜血管瘤:眼底呈瀰漫性紅色。螢光眼底造影早期顯示大型脈絡膜血管模式,晚期腫瘤整體呈過螢光。
- 視網膜血管迂曲:反映脈絡膜血管瘤相關的循環障礙
- 滲出性視網膜剝離:脈絡膜血管瘤增大時可能發生
同側軟腦膜血管瘤導致大腦皮質萎縮和鈣化進展,3歲前常出現癲癇發作(多為難治性)。可合併精神發育遲緩、偏癱和同向偏盲。
甲狀腺眼病的臨床所見
Section titled “甲狀腺眼病的臨床所見”眼瞼症狀如上眼瞼腫脹和上眼瞼退縮早期出現。可見眼球突出、複視和視力障礙。外眼肌肥大導致眼眶內壓升高,引起靜脈淤滯,這是EVP升高的機轉。常伴有甲狀腺功能亢進,但也可作為甲狀腺功能正常眼病發生。
Radius-Maumenee症候群的臨床所見
Section titled “Radius-Maumenee症候群的臨床所見”常單側或雙側不對稱發病1, 2)。一例38歲女性患者,主訴右眼充血持續3年以上,可見瀰漫性上鞏膜血管怒張,眼壓22 mmHg(使用噻嗎洛爾),眼底所見正常1)。
3. 原因與風險因素
Section titled “3. 原因與風險因素”EVP升高的原因大致分為三類:靜脈阻塞、動靜脈異常和特發性3)。
| 分類 | 主要疾病 |
|---|---|
| 靜脈阻塞 | 上腔靜脈症候群、海綿竇血栓症、頸靜脈阻塞 |
| 動靜脈異常 | CCF(直接/硬腦膜)、硬腦膜瘻管、Sturge-Weber症候群 |
| 特發性 | Radius-Maumenee症候群 |
動靜脈異常與特發性
頸動脈海綿竇瘻管(CCF):直接型為內頸動脈主幹直接分流,分流量大,症狀嚴重。硬腦膜型為硬腦膜穿通支分流,病程慢性。
硬腦膜瘻管:低流量動靜脈分流3)
Sturge-Weber症候群:胚胎期交感神經功能障礙導致的血管發育異常。眼瞼有血管瘤時,30%~70%會發展為青光眼4)。
眼眶靜脈曲張:特徵為Valsalva動作時眼球突出加重。
Radius-Maumenee症候群:排除性診斷。約報告60例1)。
EGS對EVP升高的病因進行了更詳細的分類3)。
- 眼眶/鞏膜表層疾病:化學燒傷或放射線導致的鞏膜表層靜脈障礙、Sturge-Weber症候群、太田母斑、內分泌性眼眶疾病(甲狀腺眼病)、眼眶腫瘤/假瘤、眼眶靜脈炎。
- 神經系統疾病:硬腦膜分流、海綿竇血栓形成。
- 全身性原因:上腔靜脈阻塞、頸靜脈阻塞(頸部廓清術後)、肺靜脈阻塞。
- 特發性
在CCF中,持續的眼缺血可導致虹膜和隅角新生血管形成,有發生新生血管性青光眼的風險。若不處理,血液可能逆流至腦靜脈系統,導致海綿竇破裂、腦出血或蜘蛛膜下腔出血,直接型CCF尤其需要注意。可能直接危及生命。
在鞏膜炎或鞏膜表層炎中,炎症波及鞏膜表層靜脈可導致房水流出受阻,引起眼壓升高10)。
Sturge-Weber症候群的發病時間與病因
Section titled “Sturge-Weber症候群的發病時間與病因”- 早發型(出生後至4歲):約佔60%。主要原因為隅角發育異常。
- 晚發型(幼兒期以後):涉及EVP升高和脈絡膜血管瘤
大致分為三組:靜脈閉塞(上腔靜脈症候群、海綿竇血栓形成、甲狀腺眼病、眼眶腫瘤)、動靜脈異常(頸動脈海綿竇瘻、硬腦膜瘻、Sturge-Weber症候群、眼眶靜脈曲張)和特發性(Radius-Maumenee症候群)。CCF分為直接型和硬腦膜型;直接型分流量大,症狀嚴重。Radius-Maumenee症候群是排除性診斷,需通過影像學檢查排除所有繼發性原因後才能診斷。
4. 診斷與檢查方法
Section titled “4. 診斷與檢查方法”EVP升高的診斷中,確定病因最為重要。
確認開放隅角和Schlemm管血液逆流1)。這是提示EVP升高最簡單的發現。
- CT/MRI:評估海綿竇擴大、眼上靜脈擴張、眼外肌肥大。輕度CCF時CT/MRI可能無明顯發現1)
- MRI特有表現:正常海綿竇在MRI上顯示強化,但CCF因血流速度快,表現為流空(無信號區)
- MRA:有助於顯示眼上靜脈擴張、海綿竇及異常血管
- 確診:需要腦血管造影(確認頸內動脈和頸外動脈的動靜脈短路)。硬腦膜型CCF需行雙側頸內動脈和頸外動脈的四血管造影
- CT血管造影:有助於評估眼眶和顱內的血管異常
- 眼眶都卜勒超音波:用於非侵入性確認上眼靜脈擴張
EVP測量方法
Section titled “EVP測量方法”存在直接穿刺法(最準確)和間接法(靜脈壓力計、空氣噴射等),但尚未用於日常臨床常規2)。臨床上沒有測量EVP的設備。
甲狀腺功能檢查
Section titled “甲狀腺功能檢查”所有EVP升高的病例都應進行1)。當TSH受體抗體(TRAb、TSAb)、抗TG抗體(TgAb)或抗TPO抗體(TPOAb)中任何一項陽性時,診斷為甲狀腺眼病。
Sturge-Weber症候群的診斷
Section titled “Sturge-Weber症候群的診斷”根據皮膚表現+癲癇發作+頭部CT顯示腦皮質鈣化來診斷。即使在鈣化出現之前,也可以通過增強MRI和SPECT檢測到腦病變。兒童必須在全身麻醉下進行精確的眼壓測量、前節、隅角和眼底檢查。螢光眼底血管攝影對診斷脈絡膜血管瘤有用,早期顯示大的脈絡膜血管模式,晚期整個腫瘤呈強螢光。
與表現為慢性眼充血的疾病進行鑑別很重要。
- 上鞏膜炎/鞏膜炎:炎症性血管擴張,壓迫時褪色。常伴有疼痛10)
- 慢性結膜炎:結膜瀰漫性充血。與EVP升高的螺旋狀血管擴張分布不同
- 急性閉角型青光眼:伴有隅角關閉,與EVP升高的病理生理不同
- 酒渣鼻:伴有面部潮紅和毛細血管擴張
- 真性紅血球增多症:伴有結膜血管怒張,但背景是全身性紅血球增多
在Radius-Maumenee症候群病例中,據報導顱內MRI血管攝影、甲狀腺功能檢查和腦血管攝影均正常1)。只有當這些檢查未發現異常時,才診斷為特發性。
5. 標準治療方法
Section titled “5. 標準治療方法”治療的基礎是原發疾病的治療,需要與神經外科等其他科室協作3)。通過治療原發疾病使EVP正常化後,眼壓會改善,但有些病例在原發疾病治療後高眼壓仍持續存在。採用類似於原發性開放角型青光眼的藥物治療,但僅通過藥物治療即可控制眼壓而無需手術的情況也很多。
房水生成抑制劑(第一線用藥)
Rho激酶抑制劑及其他
奈他舒地爾0.02%:增加小樑網流出 + 降低EVP作用。眼壓下降率20~25%。點眼後EVP平均降低0.79 mmHg3)
利帕舒地爾0.4%:增加小樑網流出。眼壓下降率約20%。點眼8小時後鞏膜表層靜脈房水柱寬度顯著增加3)
前列腺素相關藥物:由於擴張整個鞏膜表層血管,效果有限。通過促進旁路流出有一定效果
在6隻Sturge-Weber症候群相關青光眼眼中,添加奈他舒地爾後報告有顯著眼壓降低。
按病因的特殊治療
Section titled “按病因的特殊治療”- 海綿竇血栓形成:抗生素治療是核心
- CCF:分流量小則觀察(數月內可能自行閉合)。手術適應症包括分流量大、持續性眼壓升高、視力下降、複視、有腦出血或蜘蛛膜下腔出血風險、以及預期不能自行閉合的情況。外科治療由神經外科進行血管內手術(以閉合瘻口)
- 甲狀腺眼病變:矯正甲狀腺功能是基本。有時需要眼眶減壓手術。
- 鞏膜炎/上鞏膜炎:透過治療原發病(如自體免疫疾病)控制發炎。
- 小樑切除術:合適的手術選擇,但在眼表靜脈壓升高的眼中,脈絡膜滲出的風險很高。建議使用可調式縫線以防止術中眼壓快速下降 2)。
- 青光眼引流裝置(GDD):Ahmed瓣膜或Baerveldt植入物用於難治性病例。五年結果顯示,在再次手術病例中GDD優於小樑切除術 2)。
- XEN45凝膠支架:微創替代方案。可保留結膜組織 2)。
- 雷射小樑成形術:對眼表靜脈壓升高的證據有限 2)。
在Radius-Maumenee症候群的三例長期追蹤中,進行了小樑切除術、XEN45、Ahmed瓣膜、Baerveldt植入物和睫狀體光凝術 2)。所有病例至少有一隻眼接受了小樑切除術,但常需要再次手術,兩例發生脈絡膜滲出(無低眼壓)2)。病例1中,XEN45在73個月的長期追蹤中提供了良好的眼壓控制 2)。
Sturge-Weber症候群的年齡特異性治療演算法
Section titled “Sturge-Weber症候群的年齡特異性治療演算法”- 先天性/嬰兒期發病:適用小樑切開術或隅角切開術 4, 6, 7)。
- 年長兒童(以眼表靜脈壓升高為主):藥物治療是首選 4)。如果藥物治療或流出道重建失敗,考慮小樑切除術或帶板的引流管分流手術 4, 8)。
- 手術併發症:如果存在同側脈絡膜血管瘤,有發生脈絡膜上腔出血或視網膜剝離等嚴重併發症的風險 4, 5)。
- 如果脈絡膜血管瘤增大並引起滲出性視網膜剝離,則適用冷凍療法。
6. 病理生理學與詳細發病機轉
Section titled “6. 病理生理學與詳細發病機轉”房水流出通道與眼壓調節
Section titled “房水流出通道與眼壓調節”房水通過兩條途徑排出眼外:主通道(佔總流出量的80-95%)和副通道(5-20%)9)。主通道中,房水依次流經小梁網→Schlemm管→集合管→房水靜脈→上鞏膜靜脈→眼上靜脈→海綿竇→頸內靜脈→上腔靜脈。
主通道的房水流出是眼壓依賴性的,隨著眼壓升高而增加。然而,在EVP升高的情況下,僅靠這種代償機制不足以使眼壓恢復正常。
EVP升高的病理狀態
Section titled “EVP升高的病理狀態”當上鞏膜吻合口下游的靜脈壓升高時,房水從Schlemm管流向上鞏膜靜脈的阻力增加3)。慢性病例中,血液反流入Schlemm管,導致通過小梁網的房水流出減少。結果,眼壓慢性升高,導致青光眼性視神經病變3)。
副通道(葡萄膜鞏膜途徑)的流出是非眼壓依賴性的,受EVP升高的影響較小。這一特性為前列腺素相關藥物通過副通道促進流出具有一定效果提供了依據。
CCF的眼缺血與新生血管性青光眼
Section titled “CCF的眼缺血與新生血管性青光眼”在CCF中,長期EVP升高損害眼部血流,導致眼缺血。由於動脈血分流至海綿竇,眼動脈系統的灌注壓降低。慢性眼缺血持續存在,通過視網膜缺血誘導血管內皮生長因子(VEGF)產生,導致虹膜和房角新生血管形成,從而發生新生血管性青光眼。一旦發展到這一階段,開角被阻塞,治療變得更加困難。CCF的治療(瘻口閉合)可改善眼缺血,有望使新生血管消退,但進展期病例可能留下不可逆的房角損傷。
Sturge-Weber症候群的眼壓升高:多因素機轉
Section titled “Sturge-Weber症候群的眼壓升高:多因素機轉”Sturge-Weber症候群的眼壓升高並非單一機轉,而是涉及多種因素4)。
- 原發性房角發育異常:早發型的主要原因
- Schlemm管萎縮:房水流出通道的結構性障礙
- 上鞏膜靜脈壓升高:由上鞏膜血管瘤引起
- 周邊虹膜前粘連(PAS)形成:隅角的慢性變化
- 脈絡膜血管瘤相關的通透性增加:從變薄的血管壁滲漏
由於這些多因子複合,Sturge-Weber症候群的青光眼比發育性青光眼更難治療。然而,如果早期達成良好的眼壓控制,可以保留視力。
Sturge-Weber症候群的眼壓升高並非單一機制,而是由原發性隅角發育異常、Schlemm管萎縮、EVP升高、PAS形成和脈絡膜血管瘤相關的通透性增加這五個因素共同作用所致。因此,僅靠藥物治療往往難以控制眼壓。此外,手術治療也存在同側脈絡膜血管瘤引起的脈絡膜上腔出血和視網膜剝離的風險,需要謹慎選擇治療方案。
7. 最新研究與未來展望
Section titled “7. 最新研究與未來展望”Rho激酶抑制劑對上鞏膜靜脈流出的影響
Section titled “Rho激酶抑制劑對上鞏膜靜脈流出的影響”一項使用自動靜脈壓計的研究報告稱,滴用奈他舒地爾0.02%後,EVP平均降低0.79 mmHg。紅血球媒介血管造影也證實上鞏膜靜脈流出顯著增加。對於利帕舒地爾,滴眼8小時後上鞏膜靜脈內的房水柱寬度顯著增加,提示上鞏膜靜脈流出增強。
前房內貝美前列素植入物
Section titled “前房內貝美前列素植入物”前房內給予的貝美前列素選擇性擴張上鞏膜靜脈系統並增強流出。與局部滴眼的前列腺素類似物擴張整個上鞏膜血管不同,前房內給藥僅作用於靜脈系統。
QLS-111
Section titled “QLS-111”一種新型局部點眼藥,選擇性靶向上鞏膜血管並降低EVP。具有經由ATP敏感性鉀離子通道調節的血管擴張作用。目前正在開發中,初步數據顯示顯著的眼壓下降且無嚴重副作用。
Radius-Maumenee症候群的長期手術結果
Section titled “Radius-Maumenee症候群的長期手術結果”Elksne等人(2023)報告了3例患者的長期追蹤。病例1左眼植入XEN45凝膠支架,73個月的長期追蹤中眼壓控制良好。術後脈絡膜滲出和囊樣黃斑水腫等併發症的管理仍是挑戰2)。
8. 參考文獻
Section titled “8. 參考文獻”
- Estacia CT, Gameiro Filho AR, da Silveira IBE, et al. Radius-Maumenee syndrome (idiopathic dilated episcleral vessels). GMS Ophthalmol Cases. 2024;14:Doc15.
- Elksne E, Steiner V, Hohensinn M, et al. Radius-Maumenee syndrome: A case series with a long-term follow-up. Clin Case Rep. 2023;11:e06918.
- European Glaucoma Society. European Glaucoma Society Terminology and Guidelines for Glaucoma, 5th Edition. Br J Ophthalmol. 2021.
- 日本緑内障学会. 緑内障診療ガイドライン(第5版). 日眼会誌. 2022;126(2):85-177.
- Addison PK, et al. Serous retinal detachment induced by topical bimatoprost in a patient with Sturge-Weber syndrome. Eye (Lond). 2011;31:124-125.
- Olsen KE, et al. The efficacy of goniotomy/trabeculotomy in early-onset glaucoma associated with the Sturge-Weber syndrome. J AAPOS. 1998;2:365-368.
- Iwach AG, et al. Analysis of surgical and medical management of glaucoma in Sturge-Weber syndrome. Ophthalmology. 1990;97:904-909.
- Budenz DL, et al. Two-staged Baerveldt glaucoma implant for childhood glaucoma associated with Sturge-Weber syndrome. Ophthalmology. 2000;107(11):2105-2110.
- Acott TS, et al. Normal and glaucomatous outflow regulation. Prog Retin Eye Res. 2014;44:46-84.
- Bodh SA, et al. Inflammatory glaucoma. Oman J Ophthalmol. 2011;4(1):3-9.
