①解剖與生理因素

淺前房(Shallow Anterior Chamber)
1. 淺前房定義
Section titled “1. 淺前房定義”淺前房(shallow anterior chamber)是指角膜內皮與虹膜、水晶體前面之間的前房深度(ACD)較正常淺的狀態。一般以中心前房深度 < 2.5 mm 為參考,但眼軸較短的高齡遠視眼在正常範圍內也可能相對較淺。
原發閉塞隅角疾病(PACD)的眼睛具有淺前房、短眼軸、位置偏前的較厚水晶體等特徵性解剖結構。淺前房並非單一疾病,而是閉塞隅角疾病等多種病態的臨床表徵。多數情況下以PACS → PAC → PACG的連續體進行診療。
流行病學與風險因子
Section titled “流行病學與風險因子”全球40歲以上人口中約0.7%患有閉角型青光眼(PACG),估計患者人數約2020萬人,其中亞洲人約佔1550萬人2)。隨著年齡增長,水晶體增厚並向前移動,前房自然有變淺的趨勢。
| 風險因子 | 詳細說明 |
|---|---|
| 性別與年齡 | 多見於老年女性 |
| 屈光與眼球形狀 | 遠視、短眼軸長、小角膜直徑、水晶體增厚 |
| 家族史 | 一親等親屬有閉角型青光眼病史 |
| 種族 | 亞洲人(中國、日本)、因紐特人患病率較高2) |
| 藥物 | 抗膽鹼藥、散瞳藥、三環抗憂鬱藥、SSRI、鼻充血消除劑 |
| 誘發情況 | 長時間低頭姿勢、夜間自然散瞳 |
淺前房階段(PACS)多數無症狀,不一定需要立即治療。但預防性雷射虹膜切開術(LI)據報告可降低6年47%、14年70%的PAC發生風險2)。從PACS進展到PAC/急性發作在6年約4%、14年約12%,相對罕見,但應考慮家族史、散瞳藥使用頻率、就醫困難環境等,與眼科醫師討論後決定方針。
2. 主要症狀與臨床表現
Section titled “2. 主要症狀與臨床表現”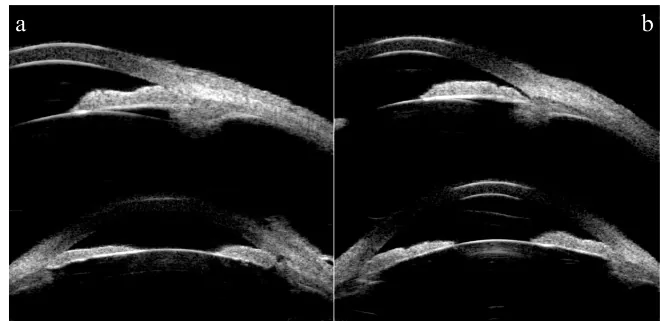
淺前房的症狀依原因與病程可分為急性型與慢性型。
急性淺前房(急性青光眼發作時)
Section titled “急性淺前房(急性青光眼發作時)”急性原發性閉鎖隅角(APACA)發作時,眼壓急遽且高度上升至40~80 mmHg,需以眼科急症處理。
自覺症狀:
- 急劇的眼痛、眼眶周圍疼痛(可能被誤診為消化道疾病或偏頭痛)
- 頭痛、噁心、嘔吐(迷走神經反射)
- 霧視、視力急遽下降(因角膜水腫所致)
- 虹視症(光源周圍看到彩虹色光環)
他覺所見:
- 嚴重淺前房(發作時前房深度約1.4毫米,角膜與虹膜可能接觸)
- 角膜水腫、結膜及睫狀體充血
- 中度瞳孔散大、固定(反映虹膜缺血)
- 光反射減弱或消失
- 前房內發炎(flare、cell、虹彩炎樣色素飛散)
- Glaucomflecken(水晶體前囊下局部白色點狀混濁:虹膜缺血後遺症)2)
慢性淺前房(PACS、PAC、CACG)
Section titled “慢性淺前房(PACS、PAC、CACG)”慢性淺前房通常無症狀,常在發現20–30 mmHg的中度眼壓升高或視野變化時才被察覺。以裂隙燈顯微鏡確認周邊前房變淺,並使用van Herick法及隅角鏡檢查進行篩檢。
3. 原因與風險因素
Section titled “3. 原因與風險因素”淺前房的原因可分為五大類。
②瞳孔阻塞
機轉: 後房→前房的房水流出受阻,導致虹膜向前膨隆
相對性瞳孔阻滯:虹膜背面與晶狀體前面接觸→後房壓力升高→小梁網阻塞。
包括急性/慢性原發性閉角型青光眼(APACG/CACG)、虹膜高褶、晶狀體膨脹1)。
③睫狀體·脈絡膜病變
④術後·外傷性
⑤發炎性
機轉: 水腫、發炎導致後眼部組織向前移位
原田病(Vogt-小柳-原田病):脈絡膜水腫、睫狀體水腫導致房角閉塞。雙眼性,伴隨全身症狀(頭痛、耳鳴、皮膚症狀)。
葡萄膜炎相關的續發性青光眼也可能出現淺前房。
閉塞隅角的4種機轉
Section titled “閉塞隅角的4種機轉”閉塞隅角青光眼的發病涉及多種機制的共同作用1)。
- 相對性瞳孔阻滯:最常見的機制。虹膜-晶狀體接觸面後房壓力升高→虹膜向前膨隆→小梁網阻塞
- 高原虹膜:睫狀突向前移位導致虹膜根部向前彎曲。散瞳時直接阻塞房角。雷射虹膜切開術後眼壓仍持續升高
- 晶狀體因素:晶狀體向前移位或年齡相關性增厚導致房角狹窄
- 晶狀體後方因素(睫狀體因素):睫狀體向前移位或玻璃體壓力升高導致房角阻塞
繼發性閉塞隅角的原因包括膨脹性白內障、晶狀體脫位、托吡酯或磺胺類藥物(誘發睫狀體水腫)、鞏膜扣帶術後、全視網膜光凝術後等2)。
具有散瞳作用或誘發睫狀體水腫的藥物具有風險。包括抗膽鹼藥物(丁基東莨菪鹼、東莨菪鹼、抗組織胺藥、抗精神病藥)、交感神經興奮劑(鼻充血消除藥)、三環抗憂鬱藥、選擇性血清素再吸收抑制劑、托吡酯、磺胺類藥物2)3)。瞳孔處於中度散大狀態(4~6 mm)時瞳孔阻滯最嚴重,因此散瞳可能成為誘因。若已診斷為淺前房或閉塞隅角,使用這些藥物前應諮詢眼科醫師。
4. 診斷與檢查方法
Section titled “4. 診斷與檢查方法”淺前房及閉塞隅角的診斷需結合多種檢查。
van Herick 法(篩檢)
Section titled “van Herick 法(篩檢)”這是一種僅使用裂隙燈顯微鏡的非接觸式篩檢檢查。保持受檢眼正視,以斜向60度角將細窄的裂隙光照射於顳側角膜緣,評估周邊前房深度(ACD)與周邊角膜厚度(CT)的比值。此方法無需隅角鏡或特殊設備,廣泛用於閉塞隅角的篩檢。
| 分級 | ACD/CT 比值 | 隅角閉塞可能性 |
|---|---|---|
| 4 | ≥ 1 | 幾乎無 |
| 3 | 1/4至小於1 | 少 |
| 2 | = 1/4 | 可能(需進一步檢查) |
| 1 | < 1/4 | 高 |
| 0 | 0(接觸) | 閉塞 |
Grade 2以下(ACD/CT ≤ 1/4)可能有隅角閉塞,應進行隅角鏡檢查。但對於虹彩高坪(plateau iris),因中央前房較深,篩檢時可能被忽略,需特別注意。
隅角鏡檢查(確診的黃金標準)
Section titled “隅角鏡檢查(確診的黃金標準)”隅角評估的臨床標準。在暗室中使用細裂隙光,注意照明避免光線通過瞳孔,評估四個象限。
- 靜態隅角鏡檢查:使用Shaffer-Kanski分類、Scheie分類、Spaeth分類評估隅角開放程度
- 動態/壓迫式隅角鏡檢查:鑑別appositional(接觸性)閉塞與synechial(虹膜前粘連=PAS)2)
- 若ITC達180度以上且涉及2個象限以上,則診斷為閉塞隅角
前眼部OCT(AS-OCT)
Section titled “前眼部OCT(AS-OCT)”非接觸式可同時掃描4個象限。可由技術人員操作,適合在暗室及明室條件下評估動態隅角變化。
定量評估指標(皆仍在建立中)2):
- 隅角開放距離(AOD)
- 小樑虹膜空間面積(TISA)
- ITC指數(虹膜小樑接觸面積)
- 前晶體拱高(ALV)
雖然與隅角鏡檢查結果可能不一致,但對於追蹤隨時間的變化很有用2)。無法評估顏色資訊、新生血管及隅角結節,因此不能取代隅角鏡檢查。
超音波生物顯微鏡(UBM)
Section titled “超音波生物顯微鏡(UBM)”是唯一能評估睫狀體及虹膜背面的檢查方法。對於診斷平板虹膜及惡性青光眼不可或缺。
平板虹膜的特徵性UBM所見:
- 前房中央相對較深,虹膜中央部平坦
- 虹膜根部較厚且向前彎曲,隅角底部狹窄
- 睫狀體向前偏移及睫狀溝消失
- 「雙峰徵」:周邊由睫狀突引起的隆起(周邊峰)與中央由水晶體引起的隆起2)
約有1/3的雷射虹彩切開術後仍持續有ITC的病例與平板狀虹膜有關2)。相較於AS-OCT,UBM在識別平板狀虹膜方面更具優勢2)。
閉塞隅角疾病的分期
Section titled “閉塞隅角疾病的分期”| 分期 | ITC ≥ 180° | 眼壓升高 或 PAS | 青光眼性視神經病變(GON) |
|---|---|---|---|
| PACS(原發性閉塞隅角疑似) | 有 | 無 | 無 |
| PAC(原發性閉塞隅角症) | 有 | 有 | 無 |
| PACG(原發性閉塞隅角青光眼) | 有 | 有 | 有 |
ITC:虹膜小梁接觸。以隅角鏡或AS-OCT評估2)。
鑑別診斷要點:
- 惡性青光眼:LI後仍持續淺前房及高眼壓。UBM顯示房水異常流入玻璃體腔
- 脈絡膜出血:術後急性發作。B超確認。眼壓可能偏低或正常
- 原田病:特徵為雙眼性、全身症狀(頭痛、耳鳴、皮膚白斑)、睫狀體水腫
- 水晶體半脫位:單眼深前房合併開放隅角時需懷疑3)
5. 標準治療方法
Section titled “5. 標準治療方法”淺前房的治療需根據原因、病期及緊急程度選擇。
急性青光眼發作(APACA)的緊急處理
Section titled “急性青光眼發作(APACA)的緊急處理”急性發作屬於眼科急症,應盡快降低眼壓。
藥物治療(發作後立即)
Section titled “藥物治療(發作後立即)”| 藥物 | 用法與劑量 | 注意事項 |
|---|---|---|
| 20%甘露醇溶液 | 1.0~2.0 g/kg,靜脈滴注30~60分鐘 | 心衰竭或腎功能障礙者禁用或慎用 |
| 甘油 | 300~500 mL,靜脈滴注45~90分鐘 | 糖尿病患者需注意高血糖 |
| 1~2%鹽酸毛果芸香鹼 | 每20~30分鐘點眼一次(每小時2~3次) | 高眼壓導致括約肌麻痺時無效。睫狀肌向前移動可能反而加重瞳孔阻滯1) |
| 乙醯唑胺 | 10 mg/kg 靜脈注射或口服 | 注意代謝性酸中毒及電解質異常 |
| 皮質類固醇眼藥水 | 常規濃度適量使用 | 目的為抑制發炎 |
若因高眼壓導致虹膜括約肌麻痺,頻繁投予毛果芸香鹼無效,且可能因睫狀肌前移而加重瞳孔阻塞,需注意此點1)。
替代性快速降眼壓方法
Section titled “替代性快速降眼壓方法”當藥物治療效果不佳或需要緊急使角膜透明時,選擇此方法。
- 前房穿刺(ACP):使用30G針進行前房穿刺。可立即將眼壓恢復至12至15 mmHg的正常範圍3)。
- 氬雷射周邊虹膜成形術(ALPI):對周邊虹膜進行收縮性雷射照射,以機械方式打開隅角。隨機對照試驗證實,可在15至30分鐘內將眼壓降至安全水平3)。
- 雷射瞳孔成形術(LPP):使用532 nm雷射使瞳孔邊緣的虹膜收縮並外翻,以解除瞳孔阻滯3)。
雷射虹膜切開術(LI)
Section titled “雷射虹膜切開術(LI)”這是解除瞳孔阻滯的根本治療,在青光眼診療指引第5版中建議等級為1A1)。
- 待角膜充分透明後再進行
- 若角膜混濁,則考慮手術性周邊虹膜切除術
- 使用雷射:Nd:YAG雷射(單獨或合併氬氣+YAG)
- 術前術後使用阿普拉可尼定鹽酸鹽眼藥水(預防暫時性眼壓升高)
- 單獨使用氬氣雷射有角膜內皮損傷的風險,通常應避免
水晶體摘除術(急性期)
Section titled “水晶體摘除術(急性期)”將水晶體更換為人工水晶體可增加前房深度,從根本上解除瞳孔阻滯(建議等級1A)1)。急性期手術併發症風險較高,建議由經驗豐富的醫師執行(建議等級1B)1)。
PACS(隅角閉鎖疑似)的管理
Section titled “PACS(隅角閉鎖疑似)的管理”- 對PACS進行預防性LI可在6年內降低47%的PAC發生風險,14年內降低70%2)
- 然而,PACS進展為PAC/急性發作的機率在6年內約為4%,14年內約為12%,相對罕見2)
- 根據個別情況(家族史、散瞳藥使用頻率、就醫困難的環境)來判斷預防性雷射虹膜切開術的適應症1)2)
慢性原發性隅角閉鎖/原發性隅角閉鎖性青光眼的管理
Section titled “慢性原發性隅角閉鎖/原發性隅角閉鎖性青光眼的管理”若雷射虹膜切開術解除瞳孔阻滯後仍持續有高眼壓,則視為殘餘青光眼,需追加藥物或手術治療1)。
EAGLE試驗(Lancet 2016):針對原發性隅角閉鎖(眼壓 ≥ 30 mmHg)及原發性隅角閉鎖性青光眼(眼壓 ≥ 21 mmHg),比較早期水晶體摘除(超音波乳化術合併人工水晶體植入)與雷射虹膜切開術的多中心隨機對照試驗。3年時,早期水晶體摘除組在無藥物眼壓控制率上約為雷射虹膜切開術組的10倍,生活品質指標也顯著較佳4)。基於此結果,急性原發性隅角閉鎖患者被推薦以水晶體重建手術作為首選治療1)。
房水流出通道重建手術(隅角沾黏分離術、小樑切開術、微創青光眼手術)適用於周邊虹膜前沾黏廣泛的病例1)。
虹膜高坪的治療
Section titled “虹膜高坪的治療”- 雷射隅角成形術(LGP):第一線選擇。以氬雷射、光斑大小500 μm、時間0.2~0.5秒、功率200 mW為基準,根據虹膜反應調整功率,對周邊虹膜進行半周至全周照射,每象限約15發。
- 縮瞳藥(如匹羅卡品):牽拉周邊虹膜以開放隅角1)
- 水晶體摘除術:期望透過睫狀突後退達到隅角開放效果1)
將老化水晶體(厚度約5 mm)更換為較薄的眼內透鏡(約0.5~1 mm),可使前房深度平均增加1~2 mm。此外,在閉塞隅角眼中,水晶體摘除後睫狀突向後移動,進一步開放隅角。此雙重機制可解除瞳孔阻滯,使前房深度正常化並開放房水流出通道。EAGLE試驗透過大規模隨機對照試驗證實,此效果遠優於單獨進行雷射周邊虹膜切開術4)。
6. 病理生理學與詳細發病機制
Section titled “6. 病理生理學與詳細發病機制”瞳孔阻滯機制
Section titled “瞳孔阻滯機制”相對性瞳孔阻滯是閉塞隅角疾病最常見的病理狀態。
- 虹膜背面與水晶體前面的接觸面,阻斷了房水從後房經瞳孔流向前房的流動
- 後房壓力上升,虹膜向前膨隆(iris bombe)
- 周邊虹膜幾乎完全覆蓋小梁網,導致房角閉塞
- 惡性循環:水晶體前移→虹膜-水晶體接觸面積增大→瞳孔阻斷增強→虹膜進一步膨隆
- 瞳孔中度散大(直徑4-6 mm)時,虹膜-水晶體接觸面最大,最易發生瞳孔阻斷2)
這是散瞳藥、抗膽鹼藥、夜間暗處成為急性發作誘因的病理生理學依據。
平板虹膜的病理
Section titled “平板虹膜的病理”平板虹膜是指睫狀突向前移位導致虹膜根部向前彎曲的狀態。
- 瞳孔放大時,虹膜根部摺疊直接阻塞隅角底部(散瞳時直接阻塞)
- 前房中央相對較深,使用 van Herick 法容易遺漏
- UBM 顯示「雙峰徵」:周邊由睫狀突引起的隆起(周邊峰)與中央由水晶體引起的隆起2)
- 雷射虹膜切開術後仍持續有虹膜-水晶體接觸的病例中,約三分之一與平板虹膜有關2)
- 重要的是,即使完成雷射虹膜切開術,散瞳時仍可能引發急性發作
惡性青光眼(aqueous misdirection)
Section titled “惡性青光眼(aqueous misdirection)”- 房水異常流入睫狀體後方(玻璃體腔)
- 玻璃體向前偏移,將水晶體-虹膜隔整體向前推擠
- 導致全周性極淺前房及高眼壓
- 特徵為對LI無反應(鑑別重點)
- 治療:首選阿托品(1%)+去氧腎上腺素點眼2)
- 無效時進行前部玻璃體切除術(建立玻璃體腔至前房的旁路)
- 好發於濾過手術後,閉角型眼睛的發病風險較高
脈絡膜膨脹與閉角
Section titled “脈絡膜膨脹與閉角”脈絡膜的動態變化可能參與閉角型青光眼的急性發作。影像研究報告指出,眼壓升高時脈絡膜膨脹導致後方壓力上升,將水晶體-虹膜隔向前推,從而觸發房角關閉3)。這被認為是急性發作好發於夜間(暗處)及俯臥姿勢(脈絡膜充血)的背景之一。
白內障手術對前房深度的影響
Section titled “白內障手術對前房深度的影響”白內障手術將增厚的晶狀體更換為薄的人工晶狀體,不僅增加前房深度,在閉角型眼中,摘除晶狀體後睫狀突向後移動,進一步開大房角。這種雙重機制支持了EAGLE試驗中早期晶狀體摘除的高有效性4)。
7. 最新研究與未來展望
Section titled “7. 最新研究與未來展望”- 早期晶狀體摘除的適應症擴大:基於EAGLE試驗的成果,正在探討進一步擴大輕症PAC/PACG早期晶狀體摘除的適應標準4)。APACG共識指出,APACA後單獨行LI最多有58%進展為CACG,因此建議急性發作後1~3個月進行早期晶狀體摘除3)
- 與MIGS的聯合手術:正在研究晶狀體摘除聯合房角粘連分離術(GSL)、房角切開術、小梁微旁路支架、內鏡下睫狀體光凝術(ECP)的組合。對於PACG,phaco+goniotomy相比phaco+trabeculectomy併發症更少且生活品質更佳2)
- AI用於PACD篩查:基於AS-OCT影像的機器學習自動檢測閉角及風險分層處於研究階段
- 藥物誘發性閉角型青光眼的流行病學:SSRI及鼻充血消除劑導致閉角型青光眼風險的數據正在累積3)
8. 參考文獻
Section titled “8. 參考文獻”- 日本緑内障学会緑内障診療ガイドライン改訂委員会. 緑内障診療ガイドライン(第5版). 日眼会誌. 2022;126(2):85-177.
- Gedde SJ, Chopra V, Vinod K, et al. Primary Angle-Closure Disease Preferred Practice Pattern®. Ophthalmology. 2026;133(2):P154-P200.
- Chan PP, Zhang X, Aung T, et al. Controversies, consensuses, and guidelines for acute primary angle closure attack (APACA) by the Asia-Pacific Glaucoma Society (APGS) and the Academy of Asia-Pacific Professors of Ophthalmology (AAPPO). Prog Retin Eye Res. 2025;105:101327.
- Azuara-Blanco A, Burr J, Ramsay C, et al; EAGLE Study Group. Effectiveness of early lens extraction for the treatment of primary angle-closure glaucoma (EAGLE): a randomised controlled trial. Lancet. 2016;388(10052):1389-1397.
