手術相關因子

術後脈絡膜剝離(脈絡膜滲出)
1. 什麼是術後脈絡膜剝離?
Section titled “1. 什麼是術後脈絡膜剝離?”脈絡膜滲出是指脈絡膜毛細血管的漿液成分異常積聚在脈絡膜上腔(脈絡膜外腔)的病理狀態。當睫狀體與脈絡膜與鞏膜分離,液體在此間隙積聚並向玻璃體腔側隆起時,稱為脈絡膜剝離。若發生較大血管破裂,則成為出血性脈絡膜剝離,甚至可能導致驅逐性出血。
脈絡膜滲出、睫狀體脈絡膜滲出和漿液性脈絡膜剝離幾乎同義使用。脈絡膜剝離是一個更廣泛的概念,也包括出血性類型。脈絡膜剝離的整體分類包括特發性脈絡膜剝離、續發性脈絡膜剝離和葡萄膜滲漏症候群三組。術後脈絡膜剝離屬於續發性。續發性脈絡膜剝離的原因包括低眼壓、脈絡膜循環障礙、脈絡膜發炎、惡性腫瘤等多種疾病。
漿液性與出血性的分類
Section titled “漿液性與出血性的分類”| 分類 | 內容物 | 主要發病機轉 |
|---|---|---|
| 漿液性 | 漿液性液體 | 低眼壓引起的靜水壓差 |
| 出血性 | 血液 | 後睫狀動脈破裂 |
青光眼手術是脈絡膜剝離最常見的原因。根據日本青光眼指引(第5版),小樑切除術後早期主要併發症的發生率包括淺前房(0.9–13%)、脈絡膜剝離(5–14%)、前房積血(2.7–11%)和結膜傷口滲漏(3.4–14%)1)。在TVT(導管 vs 小樑切除術)研究中,小樑切除術後脈絡膜滲出的發生率為19%,青光眼引流植入物術後為16%4)。出血性脈絡膜剝離在引流管植入手術中為1.2–2.7%,在小樑切除術中為0.6–1.4%。XEN45凝膠支架植入後也有0–15%的脈絡膜滲出報導2)。
白內障手術中也會發生術中脈絡膜滲出。在無縫線微切口白內障手術中,由於眼壓降低時間短,發生率約為0.05%。危險因子包括高齡、高血壓/動脈硬化、高眼壓/青光眼、高度近視、小眼球和Sturge-Weber症候群。
可能導致術後視功能損害的低眼壓黃斑病變的發生率為0.9–5%,濾過泡相關感染的發生率為0.97–5%1)。
小的周邊脈絡膜滲出通常無症狀,可自行消退。但大的滲出可能導致視力下降和前房變淺。多數病例透過散瞳藥和類固醇的保守治療改善,但前房消失的重症病例或接吻性脈絡膜滲出需要外科引流。詳情請參閱「標準治療方法」一節。
2. 主要症狀和臨床所見
Section titled “2. 主要症狀和臨床所見”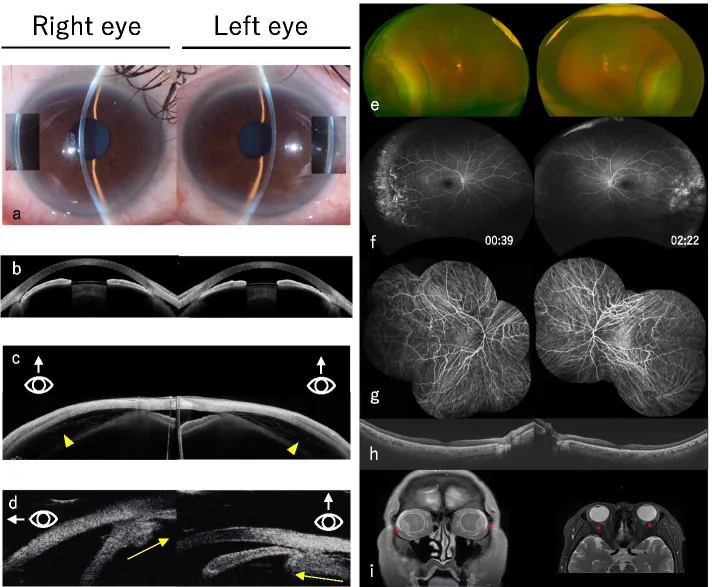
漿液性脈絡膜滲出:術後2~5天最常見。小的周邊滲出通常無症狀。大的滲出出現以下症狀:
- 視力下降:由脈絡膜隆起引起的屈光改變所致
- 周邊視野狹窄:隆起的脈絡膜壓迫視網膜
- 近視化:由於水晶體虹膜隔前移
出血性脈絡膜剝離:術後數日內出現急劇眼痛、噁心、視力下降時懷疑1)。表現為突然的劇烈搏動性疼痛和即時視力喪失。睫狀神經牽引引起的疼痛可伴有噁心、嘔吐。
術中發病(白內障手術時):伴有淺前房的急劇玻璃體壓力升高是發病徵兆。隨著後囊升高,有後囊破裂的風險;當前房極度變淺時,手術難以繼續。若眼底可見,可觀察到脈絡膜皺襞。
臨床所見(醫師檢查確認的所見)
Section titled “臨床所見(醫師檢查確認的所見)”漿液性和出血性的臨床所見比較如下。
| 所見 | 漿液性 | 出血性 |
|---|---|---|
| 眼壓 | 通常較低 | 通常較高 |
| 透照(Hagen徵) | 陽性 | 陰性 |
| B型超音波 | 無回音 | 高回音 |
眼底所見:檢眼鏡下,脈絡膜剝離呈現茶褐色、表面平滑的凸透鏡樣硬性隆起。初期或輕度時,表現為睫狀體扁平部與周邊部脈絡膜的隆起,無需壓迫鞏膜即可輕易觀察鋸齒緣。大的脈絡膜剝離呈現由渦靜脈附著部分隔、最多4個多房性氣球樣隆起。
前房所見:前房深度可正常、變淺或消失。脈絡膜剝離導致水晶體前移,引起淺前房。
合併低眼壓黃斑病變時的所見:持續低眼壓導致眼軸長縮短,出現脈絡膜皺襞、黃斑部皺襞、視網膜血管迂曲及視乳頭水腫1)。若持續存在,可能導致永久性視力障礙。
續發性青光眼:續發性脈絡膜剝離可引起急性青光眼發作。這是由於水晶體虹彩隔前移導致隅角閉塞,眼壓急遽上升的病理狀態。
3. 原因與風險因素
Section titled “3. 原因與風險因素”漿液性脈絡膜滲出的成因
Section titled “漿液性脈絡膜滲出的成因”術後低眼壓是最常見的原因。根據Starling公式,眼壓降低(間質壓降低)導致微血管壓相對升高,引起脈絡膜上腔液體蓄積。發炎引起的脈絡膜微血管通透性增加也扮演角色6)。
脈絡膜上腔的液體蓄積形成以下惡性循環:
- 術後低眼壓→脈絡膜上腔液體蓄積
- 睫狀體功能下降→房水生成減少→進一步低眼壓
- 水晶體前移→前房變淺→脈絡膜剝離加重
- 房水流入葡萄膜鞏膜流出通道→濾過泡形成不良
- 房水中蛋白濃度升高→促進濾過泡疤痕化
白內障術中發病被認為是因為高齡導致的動脈硬化以及術中眼壓急劇下降,導致短後睫狀動脈迅速滲出漿液成分所致。
出血性脈絡膜剝離的成因
Section titled “出血性脈絡膜剝離的成因”後睫狀動脈分支破裂導致血液迅速在脈絡膜上腔蓄積。眼球突然減壓,特別是從高眼壓狀態開始手術時風險較高。使用抗代謝藥物(絲裂黴素C、5-FU)也會促進低眼壓並有貢獻1)。
患者相關因素
4. 診斷與檢查方法
Section titled “4. 診斷與檢查方法”脈絡膜剝離表現為茶褐色、表面平滑、凸透鏡狀的硬性隆起。其特徵是無需壓迫即可輕易觀察到鋸齒緣。大的脈絡膜剝離表現為由渦靜脈附著處分隔的多房性隆起。
B型超音波檢查
Section titled “B型超音波檢查”此檢查對於鑑別漿液性與出血性脈絡膜剝離至關重要。
- 漿液性:無回音、光滑、厚實的半球形隆起
- 出血性:高回音隆起
它還可以檢測臨床上不明顯的微小脈絡膜上腔積液 5)。
超音波生物顯微鏡(UBM)
Section titled “超音波生物顯微鏡(UBM)”可以觀察睫狀體與鞏膜的分離,用於顯示睫狀體的前旋。對眼前節的詳細評估很有用。
不僅可以測量脈絡膜厚度,還可以測量鞏膜厚度,對診斷小眼球也有用。
需要與術後出現前房變淺、眼壓異常的疾病進行鑑別。
- 視網膜剝離:脈絡膜剝離通過其前部位置、向鋸齒緣延伸、以及由渦靜脈附著處分隔的多房性隆起與視網膜剝離區別。與裂孔源性視網膜剝離不同,脈絡膜剝離不會隨眼球運動而明顯移動。
- 驅逐性出血:術中急性發作,導致前房消失。脈絡膜皺襞的有無有助於與脈絡膜滲漏鑑別。驅逐性出血常伴有眼內容物的急劇脫出,預後不良。
- 灌注迷流症候群(IMS):白內障術中發生的玻璃體壓力升高,但眼底無脈絡膜皺襞,可與脈絡膜滲漏區分。
- 惡性青光眼(房水迷流):存在淺前房,但無相應的低眼壓、脈絡膜剝離或睫狀體上腔出血時需懷疑。房水流入玻璃體腔導致前房變淺,治療選擇包括散瞳藥、房水生成抑制劑和玻璃體手術。
- 後鞏膜炎:B型超音波顯示後鞏膜和脈絡膜增厚,球後組織水腫呈T徵為特徵。多見於中年女性,常為單眼,伴有眼痛和視力下降,常合併前鞏膜炎或葡萄膜炎。
5. 標準治療方法
Section titled “5. 標準治療方法”預防的基本原則是盡量減少術中和術後低眼壓1)。
- 小樑切除術:在鞏膜瓣上放置多根縫線,術後通過雷射縫線鬆解(LSL)管理眼壓。術中多縫線以減少過度濾過是常見的管理方法1)。
- 雷射縫線鬆解的時機:至少延遲1週。避免早期雷射縫線鬆解。
- 前房穩定:使用黏彈劑或前房維持器。
- 無瓣青光眼引流裝置:需要用可吸收縫線結紮引流管。
- 術後管理:停用局部和全身的房水生成抑制劑1)。
許多脈絡膜滲出通過保守治療可消退。部分病例因結膜下和鞏膜瓣周圍組織瘢痕化而自然改善1)。
- 散瞳藥(硫酸阿托品水合物):使水晶體虹膜隔向後旋轉,加深前房。
- 局部皮質類固醇:抑制發炎(推薦等級1B)1)。
- 加壓眼罩:準確壓迫鞏膜瓣可改善過度濾過1)。
- 重症病例:合併口服prednisolone(1 mg/kg,逐漸減量)5)
- 前房消失時:向前房內注入空氣或黏彈性物質以重建前房
白內障術中的處理:若能透過向前房內注入Healon V®(高黏度玻尿酸鈉)形成前房,則可繼續手術。在微切口白內障手術中,隨著眼壓升高,傷口自然閉合,因此等待20-30分鐘前房可能加深,手術可繼續進行。若Healon V®被從傷口推出,則應中止手術;若無法形成前房,則於次日或之後重新手術。
此外,若單眼發生術中脈絡膜滲出,對側眼同樣具有高風險,因此對側眼手術最好在全身麻醉下進行,或考慮轉診至可行全身麻醉的機構。
外科引流的適應症如下5):
- 前房消失伴持續性水晶體角膜接觸:角膜內皮損傷風險高
- 接吻型脈絡膜剝離:脈絡膜從視神經到水晶體均接觸的嚴重脈絡膜剝離
- 併發漿液性視網膜剝離:RPE幫浦機制失代償導致的繼發性視網膜剝離
- 持續性濾過泡滲漏伴低眼壓
- 保守治療無效的持續性脈絡膜滲出
操作:在距角膜緣3.5-4.5 mm後方做全層鞏膜切口,排出脈絡膜上腔液體。術中在引流的同時向前房內注入灌注液或黏彈性物質以重建前房5)。
出血性脈絡膜剝離的引流:出血可能自行吸收,但若需引流,最好等待7-10天至血液液化1)。
針對過度濾過的額外介入
Section titled “針對過度濾過的額外介入”對於過度濾過相關的低眼壓,逐步考慮以下介入措施1):
- 經結膜鞏膜瓣縫合:透過結膜直接使用尼龍線縫合鞏膜瓣的方法,作為低眼壓黃斑部病變的治療,長期有效性已被證實1)
- 自體血注射:有報告指出將自體血注射至濾過泡內及周圍可改善低眼壓黃斑部病變。但可能導致眼壓急劇升高1)
- 開放性鞏膜瓣縫合:若上述方法無效,則重新打開結膜,在直視下縫合鞏膜瓣1)
- 鞏膜開窗術:當出現明顯的脈絡膜剝離時,引流積聚在脈絡膜上腔的液體1)
許多漿液性脈絡膜滲出會隨著術後傷口癒合和結膜下組織疤痕化而消退。大多數病例透過散瞳藥和類固醇眼藥水等保守治療即可改善。但大的或持續的脈絡膜滲出需要外科引流。出血性脈絡膜剝離比漿液性更嚴重,需要更積極的介入。
Kissing choroidal(接觸型脈絡膜剝離)是指對側的脈絡膜剝離隆起至從視神經到水晶體相互接觸的狀態。伴有前房消失,視網膜血流障礙和角膜內皮損傷的風險高,是外科引流的絕對適應症。
6. 病理生理學·詳細發病機轉
Section titled “6. 病理生理學·詳細發病機轉”脈絡膜的解剖特徵
Section titled “脈絡膜的解剖特徵”脈絡膜組織學上從外向內分為上脈絡膜、血管層、脈絡膜微血管層和Bruch膜四層。脈絡膜在視神經和後睫狀動脈進入眼球以及渦靜脈離開眼球的部位與鞏膜牢固結合。上脈絡膜與鞏膜的連接前方較鬆,後方較緊。這些連接部位決定了脈絡膜剝離的多房形態。
鞏膜與脈絡膜之間的間隙稱為脈絡膜外腔,上脈絡膜(一層薄的有色結締組織膜)存在於該間隙中。由於上脈絡膜與鞏膜前方的連接較鬆,早期脈絡膜剝離表現為睫狀體平坦部和周邊脈絡膜的隆起。
Starling公式與脈絡膜滲出
Section titled “Starling公式與脈絡膜滲出”在正常的脈絡膜微血管中,靜水壓保持平衡。當各種原因導致這種平衡被破壞時,血液中的白蛋白會漏出微血管,滲出液積聚在脈絡膜上腔6)。
低眼壓導致間質壓(≈眼壓)降低,微血管壓相對升高,液體在脈絡膜上腔積聚。一旦形成脈絡膜滲出,含有蛋白質的血清在脈絡膜上腔積聚,膠體滲透壓的平衡限制了葡萄膜的再吸收。在脈絡膜循環障礙中,脈絡膜微血管的漏出增加;在脈絡膜發炎中,微血管通透性增加,血液的液體成分漏出到血管外。
出血性脈絡膜剝離的發病機制
Section titled “出血性脈絡膜剝離的發病機制”後睫狀動脈(短後睫狀動脈)的分支因眼球突然減壓而破裂,血液迅速在脈絡膜上腔積聚。從高眼壓狀態突然降低眼壓是最大的風險。伴有動脈硬化的老年人血管壁脆弱,破裂閾值降低。如果發生在術中,可能導致驅逐性出血,這是一種嚴重的併發症,導致眼內容物脫出。
RPE幫浦衰竭與漿液性視網膜剝離
Section titled “RPE幫浦衰竭與漿液性視網膜剝離”如果脈絡膜剝離持續較長時間,視網膜色素上皮(RPE)的屏障機制失代償,導致視網膜下液積聚,發生非裂孔源性視網膜剝離。如果伴隨的非裂孔源性視網膜剝離長期存在,且中心凹下的視網膜色素上皮受損,即使手術獲得解剖學改善,視力改善也很困難。
小眼球與葡萄膜滲漏症候群
Section titled “小眼球與葡萄膜滲漏症候群”在小眼球中,鞏膜異常(增厚)壓迫渦靜脈,阻礙渦靜脈引流,導致視網膜下液積聚。有報導稱鞏膜增厚是由於膠原纖維排列異常所致。
在葡萄膜滲漏症候群中,鞏膜異常阻礙了富含蛋白質的液體從脈絡膜血管外經鞏膜向外移動6)。富含蛋白質的滲出液在脈絡膜上腔積聚,膠體滲透壓差導致液體持續滯留。本病緩解與復發交替,遷延不癒,長期脈絡膜剝離逐漸導致脈絡膜視網膜萎縮和視網膜色素上皮功能下降,引起視力障礙。
Gass於1983年報告鞏膜部分切除術和鞏膜開窗術對葡萄膜滲漏症候群有效,1990年報告約56%的病例視力改善兩行以上。但若非裂孔源性視網膜剝離長期存在,即使手術獲得解剖學改善,視力恢復也有限。
此外,像Hunter症候群這樣的黏多醣代謝異常也可導致鞏膜增厚,繼發性脈絡膜剝離。
7. 最新研究與未來展望
Section titled “7. 最新研究與未來展望”微創青光眼手術與脈絡膜滲出
Section titled “微創青光眼手術與脈絡膜滲出”微創青光眼手術相較於傳統濾過手術,脈絡膜滲出的風險較低。然而,儘管XEN45凝膠支架的小內腔(約45 μm)理論上可避免術後早期低眼壓,但仍有脈絡膜滲出的報告2)。
Cassottana等人(2023)報告了一名84歲男性在XEN45植入術後發生雙側脈絡膜滲出的病例。右眼使用散瞳藥和類固醇後一個月內改善,但左眼對保守治療無效,兩個月後需要經鞏膜引流。高齡、術前多種藥物使用、術後一週內眼壓低於10 mmHg被確定為主要風險因子2)。
術後24至48小時內眼壓低於10 mmHg被認為是預後不良因子2)。
單眼發病與對側眼風險
Section titled “單眼發病與對側眼風險”單眼脈絡膜滲出可能是對側眼相同手術的風險因子2)。在白內障手術中,如果一隻眼發生術中脈絡膜滲出,對側眼的風險也很高,因此可考慮在全身麻醉下手術或轉送至具備全身麻醉條件的機構。
藥物誘發的脈絡膜滲出
Section titled “藥物誘發的脈絡膜滲出”Shaheen等人(2023)報告了一例局部使用多佐胺引起的急性漿液性和出血性脈絡膜滲出病例。一名78歲男性在開始使用多佐胺-噻嗎洛爾複方眼藥水兩天後出現左眼脈絡膜滲出,停用多佐胺並使用1%潑尼松龍和1%阿托品眼藥水後四天內完全消退。十年前也有類似發作,證實了特異體質反應的再現性3)。
在人工水晶體眼中,由於缺乏水晶體屏障,藥物向玻璃體的滲透增加,可能增加發病風險3)。口服碳酸酐酶抑制劑(乙醯唑胺、醋甲唑胺)未引起脈絡膜滲出的病例也有報告,提示局部和全身用藥的病理生理可能不同3)。
葡萄膜滲漏症候群的鞏膜手術
Section titled “葡萄膜滲漏症候群的鞏膜手術”對於葡萄膜滲漏症候群,部分鞏膜切除術和鞏膜開窗術的有效性已有報告。Gass報告約56%的病例視力改善兩行或以上。然而,如果伴隨的非裂孔源性視網膜剝離持續時間長,中心凹下視網膜色素上皮受損,即使手術獲得解剖學改善,視力改善也可能困難。
- 影像診斷的進步:期待OCTA和廣角OCT對術後脈絡膜滲出的早期檢測和定量評估的標準化。傳統B超難以檢測的微小滲出評估正成為可能。
- 按手術方式的管理指引:隨著微創青光眼手術的普及,需要建立每種手術方式特有的脈絡膜滲出發生率和處理指引。
- 對側眼風險評估:單眼發病後對側眼風險預測的生物標記探索是未來的研究課題。
- 藥物誘發機制的闡明:碳酸酐酶抑制劑的局部給藥和全身給藥可能具有不同的病理生理學,有報告指出口服乙醯唑胺未發生脈絡膜滲出的病例3)。有望提高藥物選擇的安全性。
微創青光眼手術相比傳統濾過手術風險較低,但即使採用XEN凝膠支架等術式,也有0-15%的病例報告發生脈絡膜滲出。高齡、術前使用多種青光眼藥物、術後早期眼壓降至10 mmHg以下時風險較高。詳情請參見「原因與風險因素」一節。
8. 參考文獻
Section titled “8. 參考文獻”- 日本緑内障学会. 緑内障診療ガイドライン(第5版). 日眼会誌. 2022;126(2):85-177.
- Cassottana P, Toma C, Maltese C, et al. A Case of Bilateral Choroidal Effusion after XEN Gel Stent Implantation. Gels. 2023;9(4):276.
- Shaheen A, Schultis S, Magraner M, et al. Acute serous and hemorrhagic choroidal effusion associated with topical dorzolamide therapy. Am J Ophthalmol Case Rep. 2023;31:101866.
- Gedde SJ, Herndon LW, Brandt JD, et al. Postoperative complications in the Tube Versus Trabeculectomy (TVT) study during five years of follow-up. Am J Ophthalmol. 2012;153(5):804-814.e1. doi:10.1016/j.ajo.2011.10.024. PMID: 22244522.
- Schrieber C, Liu Y. Choroidal effusions after glaucoma surgery. Curr Opin Ophthalmol. 2015;26(2):134-142. doi:10.1097/ICU.0000000000000131. PMID: 25643198.
- Brubaker RF, Pederson JE. Ciliochoroidal detachment. Surv Ophthalmol. 1983;27(5):281-289. doi:10.1016/0039-6257(83)90228-X. PMID: 6407132.
