第I期(濾過泡炎)

濾過泡相關感染
一目瞭然的要點
Section titled “一目瞭然的要點”1. 什麼是濾過泡相關感染?
Section titled “1. 什麼是濾過泡相關感染?”濾過泡相關感染(BRI)是青光眼濾過手術(如小樑切除術)後,細菌經由濾過泡侵入引起的感染性併發症。感染侷限於濾過泡內稱為濾過泡炎,感染波及眼內稱為濾過泡相關眼內炎(BAE),臨床上將這兩種情況分開處理。
- 濾過泡炎(blebitis):感染侷限於濾過泡內或周圍。可伴有輕度至中度前房反應。
- 濾過泡相關眼內炎(BAE):感染波及玻璃體。視力預後極差。
臨床分期如下 1)。
- 第I期:濾過泡局部發炎(濾過泡炎)
- 第II期:前房內細胞、閃輝、前房蓄膿
- 第IIIa期:玻璃體波及。眼底可透見
- 第IIIb期:玻璃體嚴重混濁,眼底無法透見
與其他內眼手術不同,濾過手術不僅在術後早期,而且在長期內都有濾過泡感染的風險。一項關於絲裂黴素C合併小樑切除術的多中心前瞻性研究(Collaborative Bleb-Related Infection Incidence and Treatment Study)報告,術後5年濾過泡感染的累積發生率為2.2%,其中濾過泡相關性眼內炎(BAE)為1.1% 5)。該研究由日本青光眼學會實施,是一項全國性的前瞻性調查,數據可靠性高。術後1個月後濾過泡相關性感染的發生率據報導為0.97%~5% 4),高於其他內眼手術的遲發性感染發生率。青光眼術後濾過泡感染常在術後數年發生,發生率高於白內障術後。
根據發病時間,濾過泡相關性感染大致分為早發型(術後1個月內)和遲發型(術後1個月後)1)。早發型多由低毒力菌(凝固酶陰性葡萄球菌)引起,遲發型多由高毒力菌(鏈球菌屬、流感嗜血桿菌)引起,預後往往不良1)。術後早期濾過泡感染的發生率為0.1%~0.2%,低於遲發型4)。對於接受濾過手術的患者,應充分告知遲發性感染的風險,並指示一旦出現充血、流淚、視力模糊、眼痛等提示感染的症狀,應立即就醫4)。
濾過泡炎是指感染侷限於濾過泡內的情況,透過適當的局部治療可望獲得良好的視力預後。而濾過泡相關性眼內炎(BAE)是指感染已波及玻璃體的情況,即使積極治療,視力預後也往往不良。如果存在前房蓄膿和明顯的濾過泡感染,除非能證明其他原因,否則應作為眼內炎處理1)。
2. 主要症狀與臨床所見
Section titled “2. 主要症狀與臨床所見”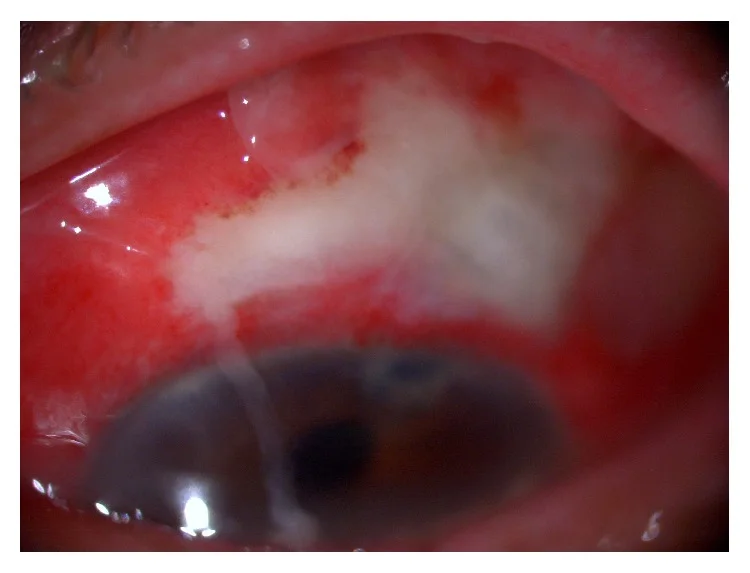
- 眼痛:急性發作。BAE時更劇烈
- 充血:從濾過泡周圍擴展到整個結膜
- 視力下降:濾過泡炎時輕度,BAE時顯著
- 畏光(刺眼):與前房發炎相關
- 眼分泌物和流淚:可能伴有膿性分泌物
- 前驅症狀:35%的患者在發病前數天至數週出現眼瞼炎、眉部疼痛、頭痛和外眼發炎1)
第II-III期(BAE)
當前房蓄膿和明顯的濾過泡感染同時存在時,除非有其他原因證明,否則應作為眼內炎處理1)。常可觀察到濾過泡滲漏,但發炎碎片可能暫時堵塞滲漏部位。
濾過泡外觀評估(5項)
Section titled “濾過泡外觀評估(5項)”為了預測濾過手術後的濾過功能以及早期發現併發症,每次就診時都需要仔細檢查濾過泡。使用裂隙燈顯微鏡檢查以下5個項目。
- 範圍(擴散):瀰漫性濾過泡比侷限性濾過泡降眼壓效果更好。向角膜側下垂的overhanging bleb可能妨礙視力。
- 高度:低平濾過泡提示濾過功能下降。
- 壁厚:使用抗代謝藥物時,濾過泡壁變薄的頻率較高。薄壁濾過泡通常降眼壓效果良好,但容易發生房水滲漏。濾過泡內腔被厚膜包裹的包裹性濾過泡(encapsulated bleb)通常降眼壓效果不佳。
- 血管分布:無血管的缺血性濾過泡房水滲漏風險高。
- Seidel試驗:用螢光素試紙染色濾過泡表面,檢查有無房水滲漏。詳見「診斷和檢查方法」一節。
3. 原因和風險因素
Section titled “3. 原因和風險因素”主要風險因素
Section titled “主要風險因素”- 濾過泡滲漏(最大風險因素):使感染風險增加26倍1)。濾過泡房水滲漏是主要風險因素4)7),晚期滲漏比早期滲漏風險更高1)。如果是滲出的oozing,可在注意感染的同時觀察,但明確的滲漏原則上需要處理。
- 使用抗代謝藥物(MMC、5-FU):導致杯狀細胞減少,黏蛋白產生下降,結膜防禦屏障減弱。促進濾過泡壁整體變薄和無血管化,使用絲裂黴素C後5年滲漏風險達15%11)。
- 濾過泡壁變薄、無血管化:在聯合抗代謝藥物的小樑切除術中常見。壁變薄的濾過泡容易發生房水滲漏,滲漏是濾過泡感染的風險因素。
- 下方濾過泡:由於暴露於淚液積聚和缺乏上眼瞼保護,感染率升高。上方為1.3%/患者·年,而下方為7.8%/患者·年1)。
- 以角膜緣為基底的結膜切口(limbus-based):比以穹窿為基底的切口感染率高(8% vs 0%)1)。無血管濾過泡更容易發生在以角膜緣為基底的切口技術中。
- 其他:結膜炎、眼瞼炎、上呼吸道感染、年輕、軸性近視、慢性使用抗菌藥物。
致病菌因發病時間而異。文獻中已報告超過100種致病微生物1)。
| 發病時間 | 主要致病菌 | 特點 |
|---|---|---|
| 早期發病 | 凝固酶陰性葡萄球菌 | 低毒性,預後相對良好 |
| 晚期發病 | 鏈球菌、流感嗜血桿菌 | 高毒性,預後不良 |
革蘭氏陽性球菌最常見,其中鏈球菌屬(約385株)和葡萄球菌屬(約296株)是主要菌種。革蘭氏陰性菌中,莫拉菌屬(約79例)和嗜血桿菌屬(約63例)較多1)。罕見情況下,也有報告人畜共通感染如犬咬二氧化碳嗜纖維菌2)。瑞典的一項回顧性研究報告,小樑切除術後眼內炎和嚴重濾過泡炎的發生率為每1000例手術7.2例12)。
濾過泡的房水滲漏是最大風險因子,使感染風險增加26倍1)。使用抗代謝藥物導致濾過泡壁變薄、無血管化,增加滲漏風險。尤其是壁薄、血管分佈少的缺血性濾過泡更容易發生滲漏。每次檢查時透過Seidel試驗確認有無滲漏非常重要。
4. 診斷與檢查方法
Section titled “4. 診斷與檢查方法”裂隙燈顯微鏡檢查
Section titled “裂隙燈顯微鏡檢查”觀察濾過泡外觀是基本,需確認上述5個項目(範圍、高度、壁厚、血管分佈、Seidel試驗)。
Seidel試驗
Section titled “Seidel試驗”這是確認濾過泡房水滲漏的基本檢查。
- 將浸有表面麻醉藥的螢光素試紙輕輕塗抹在濾過泡表面。
- 在藍色濾光片下觀察整個濾過泡。
- 如果有房水滲漏,可看到被房水稀釋的螢光素流動(Seidel試驗陽性)。
- 讓患者閉眼,然後睜眼後立即觀察整個濾過泡數秒,更容易判斷。
- 確認滲漏的位置和範圍也很重要。
濾過泡分類系統
Section titled “濾過泡分類系統”以下是基於外觀的代表性濾過泡分類方法。
- Moorfields bleb grading system(MBGS):一種標準化評估濾過泡形態的分類方法8)
- Indiana bleb appearance grading scale(IBAGS):一種系統化對濾過泡外觀進行分級的分類方法9)
兩者均有助於評估濾過功能和預測感染風險。合併使用前段OCT可以更客觀地評估濾過泡的內部結構和泡壁厚度10)。
微生物學檢查
Section titled “微生物學檢查”- 結膜拭子及培養:從膿性分泌物中採集檢體,接種於血瓊脂、巧克力瓊脂、硫乙醇酸鹽培養基等1)
- 前房水及玻璃體穿刺:II期及以上必須進行。培養同時進行玻璃體內抗生素注射。
- PCR:由於培養陰性率高達21-86%,PCR作為補充非常有用。有報告指出檢出率從47.6%提高到95.3%1)。
- B超:當IIIb期眼底無法透見時,確認玻璃體混濁和脈絡膜增厚1)。
- 前段OCT:用於評估濾過泡內部結構。可觀察鞏膜瓣開口、濾過泡腔、微囊等10)。
- 白內障術後眼內炎:發病時間和手術方式不同。白內障術後眼內炎通常發生在術後早期(約1週),而濾過泡相關感染常發生在術後數年。透過有無濾過泡感染徵象進行鑑別。
- 急性前葡萄膜炎:濾過泡混濁及周圍明顯充血(white-on-red)的有無是鑑別的關鍵。非感染性葡萄膜炎不伴有濾過泡本身的白濁。
- 包裹性濾過泡(encapsulated bleb):術後數週發生的非感染性併發症。濾過泡腔被厚膜包圍,導致眼壓下降不良,但缺乏感染徵象(white-on-red)。
5. 標準治療方法
Section titled “5. 標準治療方法”濾過泡炎(Stage I~II)的治療
Section titled “濾過泡炎(Stage I~II)的治療”若無玻璃體波及,應積極進行局部抗菌藥物治療。若感染侷限於濾過泡及前房,可透過局部及全身抗菌藥物處理。
- 強化眼藥水療程:萬古黴素(25~50 mg/mL)或頭孢唑林(50 mg/mL)與妥布黴素(14 mg/mL)每30分鐘交替點眼。48小時後依改善情況逐漸減量。
- 替代療程:第四代氟喹諾酮類(如莫西沙星)每小時一次。
- 結膜下注射:依濾過泡感染分期,可進行結膜下或前房內抗菌藥物注射。
臨床改善24小時後可考慮加入局部類固醇,但需謹慎判斷,因為有預後惡化的報告。根據培養結果調整抗菌藥物,並密切監測治療反應。確認感染已控制後再開始使用類固醇。
濾過泡相關眼內炎(BAE)的治療
Section titled “濾過泡相關眼內炎(BAE)的治療”在玻璃體穿刺取樣的同時,進行玻璃體內抗菌藥物注射。
| 藥物 | 劑量 | 備註 |
|---|---|---|
| 萬古黴素 | 1 mg/0.1 mL | 涵蓋革蘭氏陽性菌 |
| 頭孢他啶 | 2.25 mg/0.1 mL | 涵蓋革蘭氏陰性菌 |
| 地塞米松 | 0.4mg/0.1mL | 輔助(抗發炎) |
當感染擴散到玻璃體腔時,通常需要玻璃體切除術。有報告指出玻璃體切除術(PPV)比穿刺注射法的視力預後更好,但近年也有數據顯示兩者的視力預後相當。一旦感染波及玻璃體腔,視力預後極差,因此需要迅速處理。需要注意的是,眼內炎玻璃體切除研究(EVS)針對的是白內障術後眼內炎,與BRI/BAE的患者背景、致病菌和發病機制不同,因此不能直接套用EVS的結果。特別是BAE常為遲發性且涉及高毒性菌,應考慮更積極的玻璃體切除術。
術後感染預防
Section titled “術後感染預防”青光眼診療指引(第5版)CQ6中,關於小樑切除術後抗菌藥物的使用建議如下4)。
術後早期抗菌藥物使用
Section titled “術後早期抗菌藥物使用”建議預防性使用抗菌藥物,但對於藥物、方法和療程尚未達成共識4)。參與研究的專家通常在術後13個月內持續點用抗菌藥物,在此期間未發生術後感染,因此強烈建議術後持續使用抗菌藥物13個月(建議強度:強烈建議實施;證據強度:C)4)。
術後長期抗菌藥物使用
Section titled “術後長期抗菌藥物使用”全國規模的濾過泡感染調查(104眼)比較了長期使用抗菌藥物組和未使用組,結果顯示抗菌藥物可顯著延遲濾過泡感染的發生6)。
- 未使用組:感染發生中位時間 3.9年
- 長期使用組:感染發生中位時間 6.4年
- 眼藥膏組:感染發生中位時間 10.5年
如果濾過泡壁薄,上眼瞼抬起時有房水滲出,或起床時淚液積聚等自覺症狀,應積極考慮睡前使用新喹諾酮類抗菌眼藥膏4)。
長期使用組26眼中9眼檢出抗藥菌,但其中6眼為表皮葡萄球菌,不易導致重症眼內炎4)。從醫療經濟角度也應避免濫用抗菌藥物。
濾過胞滲漏的管理
Section titled “濾過胞滲漏的管理”如果發現滲漏(濾過胞感染的最大風險因子),需要進行適當的管理。
- 保守治療:繃帶式隱形眼鏡、壓迫縫合、氰基丙烯酸酯組織膠、加壓眼罩
- 自體血注射:將自體血注射到濾過胞內及周圍。可能引起眼壓急劇升高。
- 手術治療:結膜前徙術(成功率100%)、羊膜移植(成功率45%)。如果感染風險高或低眼壓無法恢復,則適合採用遊離結膜瓣或上方帶蒂結膜瓣進行濾過胞重建。長期需要同時重新評估濾過胞形態和眼壓管理 11)
青光眼診療指南(第5版)強烈建議術後1-3個月繼續使用抗生素(證據強度C)4)。之後根據感染風險(如濾過胞滲漏的有無),考慮長期睡前使用新喹諾酮類眼膏。有報告稱,長期使用可將感染發生的中位時間從非使用組的3.9年顯著延遲至眼膏組的10.5年 6)。但應避免盲目使用,需與主治醫師協商後決定是否繼續。
6. 病理生理學與詳細發病機制
Section titled “6. 病理生理學與詳細發病機制”濾過胞相關性感染的病理源於青光眼濾過手術形成的濾過胞成為感染的入口。
感染建立的機制
Section titled “感染建立的機制”在小樑切除術中,房水從鞏膜瓣下被引導至結膜下形成濾過泡。如果濾過泡壁變薄或滲漏,淚液或眼周常在菌可能進入眼內。
抗代謝藥物(MMC、5-FU)的使用透過以下複合機制增加感染風險:
- 減少結膜杯狀細胞數量,降低黏蛋白產生,削弱淚液防禦功能
- 促進結膜整體變薄和無血管化,減弱濾過泡壁的機械強度
- 削弱物理和免疫防禦屏障,使細菌易於從結膜表面侵入眼內
- 抑制纖維母細胞增殖,延遲傷口癒合,降低結膜上皮修復能力
抗代謝藥物在當前小樑切除術中對抑制疤痕形成至關重要,但必須始終牢記其使用伴隨的長期感染風險增加。
濾過泡壁變薄與滲漏
Section titled “濾過泡壁變薄與滲漏”濾過泡的形態隨時間變化。小樑切除術後,傷口癒合過程中結膜下組織形成疤痕。合併使用絲裂黴素C(MMC)可抑制早期過度組織反應,提高長期維持濾過泡的可能性,但在術後最初幾個月疤痕形成迅速進展時,鞏膜瓣的流出阻力和濾過泡形態會迅速變化。如果在此期間管理不當,濾過泡壁變薄容易進展。
無血管的缺血性濾過泡房水滲漏風險特別高。無血管濾過泡更容易發生在以角膜緣為基底的結膜切開術中,這也與以角膜緣為基底的切口感染率較高(8% vs. 以穹窿為基底的0%)1)有關。房水滲漏(oozing或明顯滲漏)和濾過泡感染(細菌進入濾過泡)是需要關注的長期併發症。對於滲出現象,可在注意感染的同時進行觀察,但明顯滲漏需要介入處理。
致病菌與病程階段的關係
Section titled “致病菌與病程階段的關係”致病菌的毒力與發病時間相關1)。早期發病型主要由低毒力菌(凝固酶陰性葡萄球菌)引起,與白內障術後眼內炎相似,來源於淚液和眼瞼的正常菌群。這些細菌不產生外毒素,適當治療預後良好。
相反,晚期發病型涉及毒力更強的細菌,如鏈球菌屬(肺炎鏈球菌、草綠色鏈球菌群)、流感嗜血桿菌和沙雷菌屬1)。這些細菌具有高外毒素產生能力和組織侵襲性,導致臨床病程快速進展和視力預後不良。
Kandarakis等人(2022年)全面回顧了文獻中報告的BRI致病菌,鑑定出100多種微生物。在革蘭氏陽性球菌中,鏈球菌屬(約385株)和葡萄球菌屬(約296株)占絕對優勢,而在革蘭氏陰性菌中,莫拉菌屬(約79例)和嗜血桿菌屬(約63例)是主要菌種1)。
Yang等人(2021年)報告了一名81歲男性,在小樑切除術後10年發生由犬咬二氧化碳嗜纖維菌引起的濾過泡炎。患者的臉部經常被其寵物狗舔舐,推測狗的口腔常駐菌通過濾過泡感染。通過小樑切除術修復獲得了良好的視力預後(20/70)2)。
7. 最新研究與未來展望(研究階段報告)
Section titled “7. 最新研究與未來展望(研究階段報告)”分子診斷技術的進步
Section titled “分子診斷技術的進步”Kandarakis等人(2022年)的綜述指出,傳統培養的陰性率高達21%至86%。即時PCR可將細菌檢出率從47.6%提高到95.3%。此外,通過宏基因組學(高通量DNA測序)進行全面的微生物鑑定有望成為下一代診斷方法1)。
微創青光眼手術(MIGS)降低感染風險
Section titled “微創青光眼手術(MIGS)降低感染風險”MIGS的綜述指出,與傳統濾過手術相比,它有望減少創傷並降低嚴重術後併發症。但某些術式使用形成濾過泡的裝置,因此需要根據手術類型評估感染風險3)。
罕見病原體的應對
Section titled “罕見病原體的應對”Yang等人(2021年)關於犬咬二氧化碳嗜纖維菌濾過泡炎的報導表明,與寵物動物的接觸可能成為有濾過手術史眼睛的新感染風險因素。DNA測序使得以前難以培養的病原體得以鑑定2)。
術後抗菌藥物使用的未來挑戰
Section titled “術後抗菌藥物使用的未來挑戰”青光眼診療指南(第5版)指出,雖然術後長期使用抗菌藥物可顯著延遲感染發生,但關於給藥藥物、方法和持續時間尚未達成共識,期待高證據水準的研究4)。隨著結膜菌群變化和耐藥菌出現,長期隨機對照試驗的實施是未來的重要課題。
8. 參考文獻
Section titled “8. 參考文獻”- Kandarakis SA, Doumazos L, Mitsopoulou D, et al. A Review on Pathogens and Necessary Diagnostic Work for Bleb-Related Infections (BRIs). Diagnostics. 2022;12(9):2075.
- Yang MC, Ling J, Mosaed S. Capnocytophaga canimorsus blebitis: case report and review of literature. BMC Ophthalmol. 2021;21:59.
- Balas M, Mathew DJ, Bicket AK. Minimally Invasive Glaucoma Surgery: A Review of the Literature. Vision (Basel). 2023;7(3):54. doi:10.3390/vision7030054. PMID: 37606500.
- 日本緑内障学会. 緑内障診療ガイドライン(第5版). 日眼会誌. 2022;126(2):85-177.
- Yamamoto T, Sawada A, Mayama C, et al. The 5-year incidence of bleb-related infection and its risk factors after filtering surgeries with adjunctive mitomycin C: collaborative bleb-related infection incidence and treatment study 2. Ophthalmology. 2014;121:1001-1006. doi:10.1016/j.ophtha.2013.11.001. PMID: 24491639.
- Sagara H, Yamamoto T, Imaizumi K, Sekiryu T. Impact of topically administered steroids, antibiotics, and sodium hyaluronate on bleb-related infection onset: the Japan Glaucoma Society survey of bleb-related infection report 4. J Ophthalmol. 2017;2017:7062565. doi:10.1155/2017/7062565. PMID: 29138694. PMCID: PMC5613473.
- Yamamoto T, Kuwayama Y, Kano K, et al. Clinical features of bleb-related infection: a 5-year survey in Japan. Acta Ophthalmol. 2013;91(7):619-624. doi:10.1111/j.1755-3768.2012.02480.x. PMID: 22883301.
- Wells AP, Ashraff NN, Hall RC, et al. Comparison of two clinical bleb grading systems. Ophthalmology. 2006;113(1):77-83. doi:10.1016/j.ophtha.2005.06.037. PMID: 16389104.
- Cantor LB, Mantravadi AV, WuDunn D, et al. Indiana Bleb Appearance Grading Scale. J Glaucoma. 2003;12(5):266-271. doi:10.1097/00134372-200310000-00012. PMID: 14520142.
- Kojima S, Inoue T, Kawaji T, Tanihara H. Filtration bleb revision guided by 3-dimensional anterior segment optical coherence tomography. J Glaucoma. 2014;23(5):312-315. doi:10.1097/IJG.0b013e3182741ee6. PMID: 23377583.
- Kim EA, Law SK, Coleman AL, et al. Long-Term Bleb-Related Infections After Trabeculectomy: Incidence, Risk Factors, and Influence of Bleb Revision. Am J Ophthalmol. 2015;159(6):1082-1091. doi:10.1016/j.ajo.2015.03.001. PMID: 25748577.
- Wallin Ö, Al-ahramy AM, Lundström M, Montan P. Endophthalmitis and severe blebitis following trabeculectomy: epidemiology and risk factors; a single-centre retrospective study. Acta Ophthalmol. 2014;92(5):426-431. doi:10.1111/aos.12257. PMID: 24020653.
